沪教版九年级化学-杨艳-第五章第1节金属与金属矿物-第二课时.doc(江苏省扬州市高邮市)
文档属性
| 名称 | 沪教版九年级化学-杨艳-第五章第1节金属与金属矿物-第二课时.doc(江苏省扬州市高邮市) |

|
|
| 格式 | rar | ||
| 文件大小 | 35.4KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2009-05-08 00:00:00 | ||
图片预览

文档简介
立德 践行 慎教 善导
学 科:化学 班 级: 日 期: 11.4 教 者:杨艳
课 题:金属与金属矿物2 课时数:1 教案类型: 新 授
教学目标
知识与技能:复习金属的物理性质,巩固钨金属的化学性质,掌握实验室制氢气的原理和方法
过程与方法:通过对氧气与二氧化碳的实验室制取方法的复习,进一步巩固气体制备的方法;培养学生科学探究的意识,
情感态度价值观:培养学生学会分析问题的一般方法
教学重点 氢气的实验室制法
教学难点 实验室制氢气的装置的选择
教学方法
问题情景→实验探究→得出结论→练习巩固→联系实际。
【复习】1、金属的一般的物理性质
2、金属的化学性质(完成下列反应方程式)
3、复习氧气,二氧化碳的实验室制法
请按要求回答下列有关问题。
(1)选择实验室制取和收集氧气、二氧化碳气体的仪器装置图。(填“√”)
序号 A B C D E
仪器装置图 气体名称
氧气
二氧化碳
(2)请说明你所选择的实验室制取和收集氢气装置的依据是 。
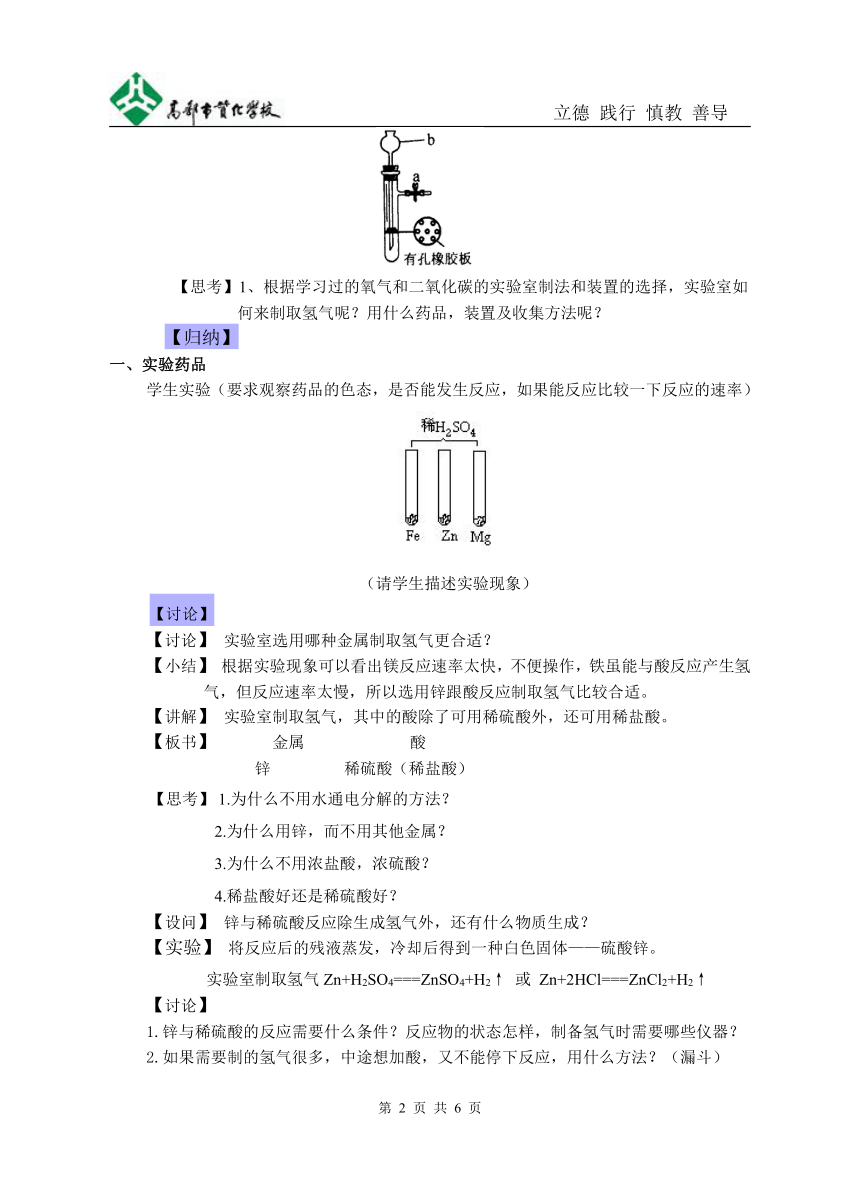
(3)某同学将B装置做了如下图所示的改进,使用时把固体反应物放在有孔橡胶板上,由长颈漏斗加入液体反应物,打开弹簧夹,使液体和固体反应物接触而发生反应,产生的气体从导气管放出。不用时关闭,反应物固体与液体脱离接触,反应自行停止。使用该装置制取气体可起到节约药品和取用方便的效果。
请写出检验此装置气密性的方法: 。
【思考】1、根据学习过的氧气和二氧化碳的实验室制法和装置的选择,实验室如何来制取氢气呢?用什么药品,装置及收集方法呢?
【归纳】
一、实验药品
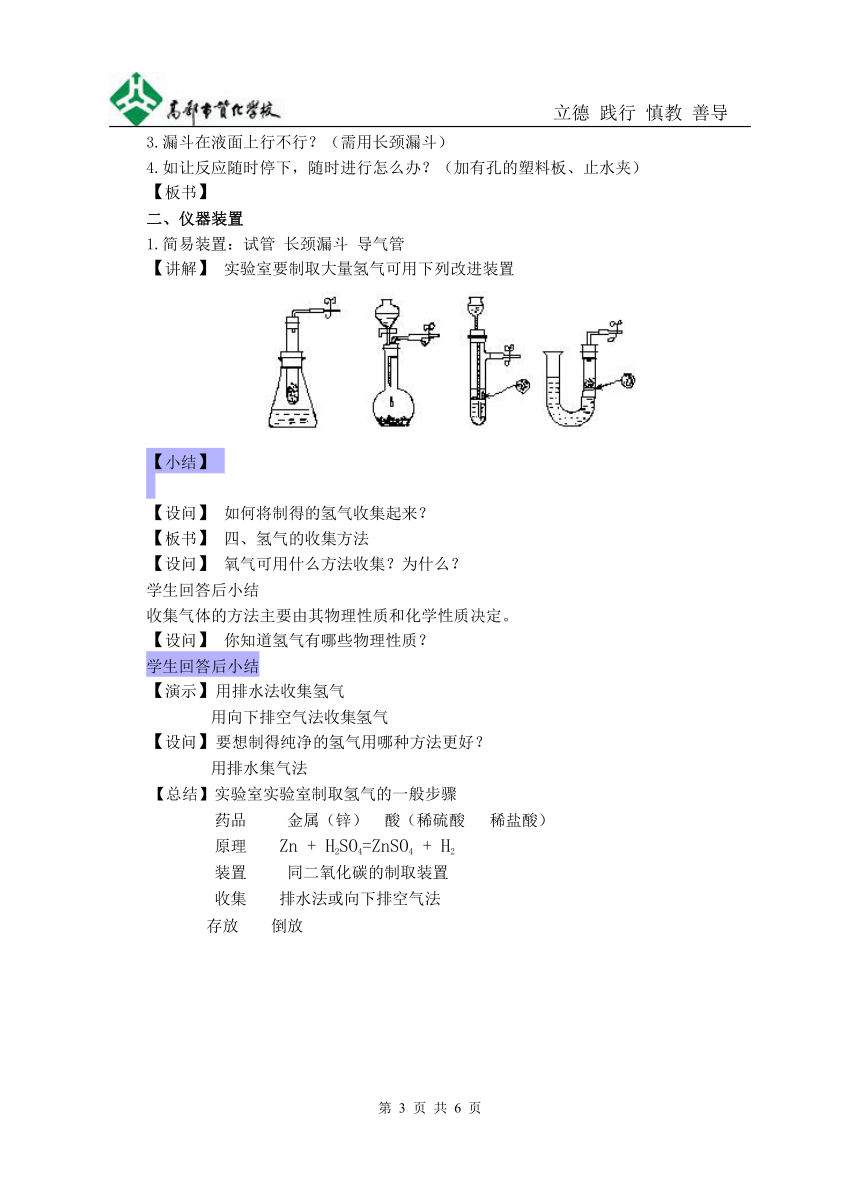
学生实验(要求观察药品的色态,是否能发生反应,如果能反应比较一下反应的速率)
(请学生描述实验现象)
【讨论】
【讨论】 实验室选用哪种金属制取氢气更合适?
【小结】 根据实验现象可以看出镁反应速率太快,不便操作,铁虽能与酸反应产生氢气,但反应速率太慢,所以选用锌跟酸反应制取氢气比较合适。
【讲解】 实验室制取氢气,其中的酸除了可用稀硫酸外,还可用稀盐酸。
【板书】 金属 酸
锌 稀硫酸(稀盐酸)
【思考】 1.为什么不用水通电分解的方法?
2.为什么用锌,而不用其他金属?
3.为什么不用浓盐酸,浓硫酸?
4.稀盐酸好还是稀硫酸好?
【设问】 锌与稀硫酸反应除生成氢气外,还有什么物质生成?
【实验】 将反应后的残液蒸发,冷却后得到一种白色固体——硫酸锌。
实验室制取氢气Zn+H2SO4===ZnSO4+H2↑ 或 Zn+2HCl===ZnCl2+H2↑
【讨论】
1.锌与稀硫酸的反应需要什么条件?反应物的状态怎样,制备氢气时需要哪些仪器?
2.如果需要制的氢气很多,中途想加酸,又不能停下反应,用什么方法?(漏斗)
3.漏斗在液面上行不行?(需用长颈漏斗)
4.如让反应随时停下,随时进行怎么办?(加有孔的塑料板、止水夹)
【板书】
二、仪器装置
1.简易装置:试管 长颈漏斗 导气管
【讲解】 实验室要制取大量氢气可用下列改进装置
【小结】
【设问】 如何将制得的氢气收集起来?
【板书】 四、氢气的收集方法
【设问】 氧气可用什么方法收集?为什么?
学生回答后小结
收集气体的方法主要由其物理性质和化学性质决定。
【设问】 你知道氢气有哪些物理性质?
学生回答后小结
【演示】用排水法收集氢气
用向下排空气法收集氢气
【设问】要想制得纯净的氢气用哪种方法更好?
用排水集气法
【总结】实验室实验室制取氢气的一般步骤
药品 金属(锌) 酸(稀硫酸 稀盐酸)
原理 Zn + H2SO4=ZnSO4 + H2
装置 同二氧化碳的制取装置
收集 排水法或向下排空气法
存放 倒放
课后练习:
一、选择题:(每小题只有一个选项符合题意)
1. 下列物质,不能和锌反应产生氢气的为( )
A.稀硫酸 B.稀盐酸 C.稀醋酸 D.氯化钠溶液
2. 把铁片放入下列溶液中充分反应后,溶液的质量比反应前减轻的是
A.稀H2SO4 B.稀HCl C.CuSO4溶液 D.FeSO4溶液
3. 铁在纯氧中燃烧,其生成物是( )
A.FeO B.Fe2O3 C.FeO和Fe2O3 D.Fe3O4
4. 遇稀盐酸不产生气体的是( )
A.铁片 B.铜片 C.铝片 D.石灰片
5. 下列对铁的性质的描述中,属于化学性质的是( )
A.铁容易传热导电 B.纯铁是银白色的金属
C.铁在潮湿的空气中易生锈 D.铁有良好的延展性
6. 收藏家收藏的清末铝制艺术品,至今保存完好,该艺术品未被锈蚀的主要原因是 ( )
A.铝不易被氧化 B.铝的氧化物容易发生还原反应
C.铝不易发生化学反应 D.铝表面的氧化铝具有保护作用
7. 废旧计算机的某些部件含有Zn、Fe、Cu、Ag、Pt(铂)、Au(金)等金属,经物理方法初步处理后,与足量稀盐酸充分反应,然后过滤。剩余的固体中不应有的金属是 ( )
A.Cu、Ag B.Fe、Zn C.Pt、Cu D.Ag、Au
8. 金属钛(Ti)是航空、宇航、军工、电子等方面的必须原料。在生产钛的过程中可用镁在加热条件下与TiCl4反应制得金属钛,反应的化学方程式为:
TiCl4+2 MgTi+2 MgCl2。该反应属于 ( )
A.化合反应 B.分解反应 C.置换反应 D.无法确定
9. 下列说法错误的是 ( )
A.铝制容器可贮运浓硝酸
B.导电性Ag>Cu>Al
C.铁、铝、铜都能与氧气发生反应
D.金属都不与冷水发生反应
10.把一定质量的锌和镁分别投入足量的稀盐酸中,充分反应后,生成氢气的质量关系如图5-1所示(图中m表示氢气的质量,t表示反应时间),则投入的锌和镁的质量比是 ( )
A.1:1 B.24:65
C.65:24 D.无法确定
二、填空题
11.写出下列反应的化学方程式,并指明所属反应类型:
(1)铝与稀盐酸反应 ,属于 反应。
(2)“曾青得铁化为铜” ,属于 反应。
(3)铝和氧化铁高温下反应制得铁水用于野外铁轨焊接 ,属于 反应。
12.锌与铁的化学性质相似都较 (填“活泼”或“不活泼”)能与 、 、 等几类物质发生化学反应。写出锌与以上几类物质反应的化学方程式: 、
、 。13.金属钠能与水发生化学反应生成氢氧化钠和氢气。写出该反应的化学方程式
,该反应的反应类型是 反应。
14.铅笔笔芯的主要成份是 而不是 ,该成分 (填“属于”、“不属于”)金属,可用 对比实验加以验证。
15.如果人体血液中缺乏亚铁离子,就会造成“贫血”。市场出售的某种麦片中含有微量的颗粒很细的还原铁粉。这种铁粉在人体胃液(主要成份为稀盐酸)中转化为亚铁盐的化学方程式是 ;
16.常见的铁矿石有:磁铁矿(主要成分是Fe304)、赤铁矿(主要成分是Fe2O3)、褐铁矿(主要成分是Fe2O3·3H2O)、菱铁矿(主要成分是FeCO3)、黄铁矿(主要成分是FeS2)。其中理论上最适宜炼铁的两种矿石为 , 理由为 。
17.黄金是一种贵重金属。在人类漫长的历史中,素有“沙里淘金”、“真金不怕火炼"之说。这说明黄金在自然界中主要以 形式存在,也说明黄金的化学性质在自然条件下非常 。
【思维拓展】
三、实验题:
18.实验室有一包混有铁粉的铜粉,请你用以下两种方法除去铜粉中的铁粉(简述操作过程)。
(1)物理方法:
(2)化学方法:
19.某学习小组为探究金属的性质,将一根铝条放入盛有稀盐酸的试管中,实验现象记录如下:
反应时间/min 1 5 8 1O 16 18
实验现象 少量气泡 较多气泡 大量气泡 反应剧烈 少量气泡 反应停止,铝条剩余
试解释上述实验过程中,产生一系列现象的原因:
【能力创新】
四、计算题:
20.一定质量的铁粉和铜粉的混合物,将其分为两等份,一份与足量的稀盐酸充分反应,产生氢气0.4 g;另一份与足量的硫酸铜充分反应,经过滤、烘干,得固体25.6 g。求混合物中铁的质量分数。
【教学后记】
学生刚学习这部分的内容时,做此处的作业可能暂时有困难,但是成绩较好的学生还是可以很容易地想出答案,中游学生可能就有问题,教学时我采用了介入法取得了较好的效果。
图5-1
第 1 页 共 6 页
学 科:化学 班 级: 日 期: 11.4 教 者:杨艳
课 题:金属与金属矿物2 课时数:1 教案类型: 新 授
教学目标
知识与技能:复习金属的物理性质,巩固钨金属的化学性质,掌握实验室制氢气的原理和方法
过程与方法:通过对氧气与二氧化碳的实验室制取方法的复习,进一步巩固气体制备的方法;培养学生科学探究的意识,
情感态度价值观:培养学生学会分析问题的一般方法
教学重点 氢气的实验室制法
教学难点 实验室制氢气的装置的选择
教学方法
问题情景→实验探究→得出结论→练习巩固→联系实际。
【复习】1、金属的一般的物理性质
2、金属的化学性质(完成下列反应方程式)
3、复习氧气,二氧化碳的实验室制法
请按要求回答下列有关问题。
(1)选择实验室制取和收集氧气、二氧化碳气体的仪器装置图。(填“√”)
序号 A B C D E
仪器装置图 气体名称
氧气
二氧化碳
(2)请说明你所选择的实验室制取和收集氢气装置的依据是 。
(3)某同学将B装置做了如下图所示的改进,使用时把固体反应物放在有孔橡胶板上,由长颈漏斗加入液体反应物,打开弹簧夹,使液体和固体反应物接触而发生反应,产生的气体从导气管放出。不用时关闭,反应物固体与液体脱离接触,反应自行停止。使用该装置制取气体可起到节约药品和取用方便的效果。
请写出检验此装置气密性的方法: 。
【思考】1、根据学习过的氧气和二氧化碳的实验室制法和装置的选择,实验室如何来制取氢气呢?用什么药品,装置及收集方法呢?
【归纳】
一、实验药品
学生实验(要求观察药品的色态,是否能发生反应,如果能反应比较一下反应的速率)
(请学生描述实验现象)
【讨论】
【讨论】 实验室选用哪种金属制取氢气更合适?
【小结】 根据实验现象可以看出镁反应速率太快,不便操作,铁虽能与酸反应产生氢气,但反应速率太慢,所以选用锌跟酸反应制取氢气比较合适。
【讲解】 实验室制取氢气,其中的酸除了可用稀硫酸外,还可用稀盐酸。
【板书】 金属 酸
锌 稀硫酸(稀盐酸)
【思考】 1.为什么不用水通电分解的方法?
2.为什么用锌,而不用其他金属?
3.为什么不用浓盐酸,浓硫酸?
4.稀盐酸好还是稀硫酸好?
【设问】 锌与稀硫酸反应除生成氢气外,还有什么物质生成?
【实验】 将反应后的残液蒸发,冷却后得到一种白色固体——硫酸锌。
实验室制取氢气Zn+H2SO4===ZnSO4+H2↑ 或 Zn+2HCl===ZnCl2+H2↑
【讨论】
1.锌与稀硫酸的反应需要什么条件?反应物的状态怎样,制备氢气时需要哪些仪器?
2.如果需要制的氢气很多,中途想加酸,又不能停下反应,用什么方法?(漏斗)
3.漏斗在液面上行不行?(需用长颈漏斗)
4.如让反应随时停下,随时进行怎么办?(加有孔的塑料板、止水夹)
【板书】
二、仪器装置
1.简易装置:试管 长颈漏斗 导气管
【讲解】 实验室要制取大量氢气可用下列改进装置
【小结】
【设问】 如何将制得的氢气收集起来?
【板书】 四、氢气的收集方法
【设问】 氧气可用什么方法收集?为什么?
学生回答后小结
收集气体的方法主要由其物理性质和化学性质决定。
【设问】 你知道氢气有哪些物理性质?
学生回答后小结
【演示】用排水法收集氢气
用向下排空气法收集氢气
【设问】要想制得纯净的氢气用哪种方法更好?
用排水集气法
【总结】实验室实验室制取氢气的一般步骤
药品 金属(锌) 酸(稀硫酸 稀盐酸)
原理 Zn + H2SO4=ZnSO4 + H2
装置 同二氧化碳的制取装置
收集 排水法或向下排空气法
存放 倒放
课后练习:
一、选择题:(每小题只有一个选项符合题意)
1. 下列物质,不能和锌反应产生氢气的为( )
A.稀硫酸 B.稀盐酸 C.稀醋酸 D.氯化钠溶液
2. 把铁片放入下列溶液中充分反应后,溶液的质量比反应前减轻的是
A.稀H2SO4 B.稀HCl C.CuSO4溶液 D.FeSO4溶液
3. 铁在纯氧中燃烧,其生成物是( )
A.FeO B.Fe2O3 C.FeO和Fe2O3 D.Fe3O4
4. 遇稀盐酸不产生气体的是( )
A.铁片 B.铜片 C.铝片 D.石灰片
5. 下列对铁的性质的描述中,属于化学性质的是( )
A.铁容易传热导电 B.纯铁是银白色的金属
C.铁在潮湿的空气中易生锈 D.铁有良好的延展性
6. 收藏家收藏的清末铝制艺术品,至今保存完好,该艺术品未被锈蚀的主要原因是 ( )
A.铝不易被氧化 B.铝的氧化物容易发生还原反应
C.铝不易发生化学反应 D.铝表面的氧化铝具有保护作用
7. 废旧计算机的某些部件含有Zn、Fe、Cu、Ag、Pt(铂)、Au(金)等金属,经物理方法初步处理后,与足量稀盐酸充分反应,然后过滤。剩余的固体中不应有的金属是 ( )
A.Cu、Ag B.Fe、Zn C.Pt、Cu D.Ag、Au
8. 金属钛(Ti)是航空、宇航、军工、电子等方面的必须原料。在生产钛的过程中可用镁在加热条件下与TiCl4反应制得金属钛,反应的化学方程式为:
TiCl4+2 MgTi+2 MgCl2。该反应属于 ( )
A.化合反应 B.分解反应 C.置换反应 D.无法确定
9. 下列说法错误的是 ( )
A.铝制容器可贮运浓硝酸
B.导电性Ag>Cu>Al
C.铁、铝、铜都能与氧气发生反应
D.金属都不与冷水发生反应
10.把一定质量的锌和镁分别投入足量的稀盐酸中,充分反应后,生成氢气的质量关系如图5-1所示(图中m表示氢气的质量,t表示反应时间),则投入的锌和镁的质量比是 ( )
A.1:1 B.24:65
C.65:24 D.无法确定
二、填空题
11.写出下列反应的化学方程式,并指明所属反应类型:
(1)铝与稀盐酸反应 ,属于 反应。
(2)“曾青得铁化为铜” ,属于 反应。
(3)铝和氧化铁高温下反应制得铁水用于野外铁轨焊接 ,属于 反应。
12.锌与铁的化学性质相似都较 (填“活泼”或“不活泼”)能与 、 、 等几类物质发生化学反应。写出锌与以上几类物质反应的化学方程式: 、
、 。13.金属钠能与水发生化学反应生成氢氧化钠和氢气。写出该反应的化学方程式
,该反应的反应类型是 反应。
14.铅笔笔芯的主要成份是 而不是 ,该成分 (填“属于”、“不属于”)金属,可用 对比实验加以验证。
15.如果人体血液中缺乏亚铁离子,就会造成“贫血”。市场出售的某种麦片中含有微量的颗粒很细的还原铁粉。这种铁粉在人体胃液(主要成份为稀盐酸)中转化为亚铁盐的化学方程式是 ;
16.常见的铁矿石有:磁铁矿(主要成分是Fe304)、赤铁矿(主要成分是Fe2O3)、褐铁矿(主要成分是Fe2O3·3H2O)、菱铁矿(主要成分是FeCO3)、黄铁矿(主要成分是FeS2)。其中理论上最适宜炼铁的两种矿石为 , 理由为 。
17.黄金是一种贵重金属。在人类漫长的历史中,素有“沙里淘金”、“真金不怕火炼"之说。这说明黄金在自然界中主要以 形式存在,也说明黄金的化学性质在自然条件下非常 。
【思维拓展】
三、实验题:
18.实验室有一包混有铁粉的铜粉,请你用以下两种方法除去铜粉中的铁粉(简述操作过程)。
(1)物理方法:
(2)化学方法:
19.某学习小组为探究金属的性质,将一根铝条放入盛有稀盐酸的试管中,实验现象记录如下:
反应时间/min 1 5 8 1O 16 18
实验现象 少量气泡 较多气泡 大量气泡 反应剧烈 少量气泡 反应停止,铝条剩余
试解释上述实验过程中,产生一系列现象的原因:
【能力创新】
四、计算题:
20.一定质量的铁粉和铜粉的混合物,将其分为两等份,一份与足量的稀盐酸充分反应,产生氢气0.4 g;另一份与足量的硫酸铜充分反应,经过滤、烘干,得固体25.6 g。求混合物中铁的质量分数。
【教学后记】
学生刚学习这部分的内容时,做此处的作业可能暂时有困难,但是成绩较好的学生还是可以很容易地想出答案,中游学生可能就有问题,教学时我采用了介入法取得了较好的效果。
图5-1
第 1 页 共 6 页
同课章节目录
- 第1章 开启化学之门
- 第1节 化学给我们带来什么
- 第2节 化学研究些什么
- 第3节 怎样学习和研究化学
- 第2章 身边的化学物质
- 第1节 性质活泼的氧气
- 第2节 奇妙的二氧化碳
- 第3节 自然界中的水
- 基础实验1 氧气的制取与性质
- 基础实验2 二氧化碳的制取与性质
- 第3章 物质构成的奥秘
- 第1节 构成物质的基本微粒
- 第2节 组成物质的化学元素
- 第3节 物质的组成
- 第4章 认识化学变化
- 第1节 常见的化学反应——燃烧
- 第2节 化学反应中的质量关系
- 第3节 化学方程式的书写与运用
- 基础实验3 物质燃烧的条件
- 第5章 金属的冶炼与利用
- 第1节 金属的性质和利用
- 第2节 金属矿物 铁的冶炼
- 第3节 金属防护和废金属回收
- 基础实验4 常见金属的性质
