第一课时 物质的分类与转化(浙江省温州市龙湾区)
文档属性
| 名称 | 第一课时 物质的分类与转化(浙江省温州市龙湾区) |
|
|
| 格式 | rar | ||
| 文件大小 | 1.3MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2009-05-29 00:00:00 | ||
图片预览











文档简介
课件37张PPT。专题1:化学家眼中的物质世界物质的分类和转化商场大超市有成千上万种商品,为什么你能够迅速挑出你所需要的商品?图书馆图书馆里有许许多多的书籍,
为什么你能够很快找到你所需要的书籍?网络中的信息分类复杂的道理往往蕴涵在平凡的生活中,学习也要注意分类!目前已知的化合物已达数千万种,近来每年化学家创造的化合物就达100万种以上。物质的分类与转化同一类物质在组成和性能方面往往
具有一定的相似性。分类有利于更好的研究物质,能实现“掌握一种物质”向“贯通一类物质”转变,提高效率。物质的分类及转化 在我们的日常生活中,常会接触到下列物质:
空气、乙醇、硫酸铵、铜、碘酒、碘、氢气、石墨、食盐水。
P3交流与讨论请将上述物质进行分类,并说明分类的依据。气态:
液态:
固态:易溶:
微溶:
难溶: 导体为:
半导体:
绝缘体: 空气、氢气
乙醇、食盐水、碘酒
硫酸铵、铜、碘、石墨乙醇、食盐水、硫酸铵
碘
空气、氢气、铜、石墨铜、石墨、食盐水
空气、乙醇、碘、氢气、碘酒4.根据物质的组成分单质:铜、碘、氢气、石墨
化合物:乙醇、硫酸铵混合物:空气、食盐水、碘酒
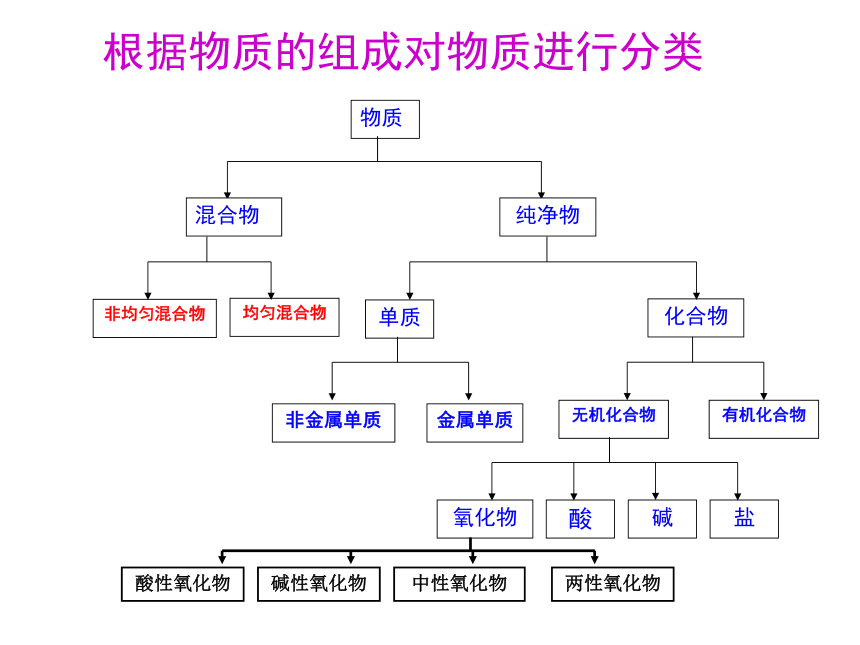
纯净物:物质分类标准不同,分类结果也不同物质根据物质的组成对物质进行分类同一类物质在组成和某些性质
方面往往具有一定的相似性P4问题解决KOH属于碱,CO2和SO2是非金属氧化
物。请写出足量KOH溶液分别与
CO2、SO2 反应的化学方程式。若是少量KOH溶液呢?KOH足量:2KOH + CO2 = K2CO3 +H2O
2KOH + SO2 = K2SO3 +H2O
若CO2 、SO2足量:KOH + CO2+H2O=KHCO3
KOH + SO2+H2O=KHSO3酸性氧化物:
CO2、SO2等能与碱反应生成盐和水的氧化物碱性氧化物:
CaO、Na2O等能与酸反应生成盐和水的氧化物氧化物定义中性氧化物:CO、NO等即不能与酸反应,又不能与碱反应生成盐和水的氧化物两性氧化物: Al2O3、ZnO等即能与酸反应,又能与碱反应生成盐和水的氧化物问题解决:1、实验室中有下列物质,根据物质组成对下列物质进行分类
钠(Na) 、氯气(Cl2) 、氯化铁(FeCl3)溶液、 硫酸(H2SO4) 、碳酸钙(CaCO3) 、氧化钙(CaO) 、氢氧化钠(NaOH) 、甲烷、牛奶、
一氧化碳、海水、石灰乳、硝酸钾、汞物质的分类 纯净物混合物 单质 化合物非均匀混合物:如:泥浆、牛奶、石灰乳、均匀混合物: 氯化铁溶液(硫酸溶液) 、海水无机化合物 有机化合物 :甲烷氧化物:氧化钙 、一氧化碳酸 :硫酸 碱:氢氧化钠 盐:碳酸钙 、硝酸钾其它 金属单质:钠、汞非金属单质:氯气 它是酸性还是碱性氧化物???物质物质转化规律P4交流与讨论1、在初中阶段,我们已经学习了一些物质转化的知识。请举例
说明下表中所列物质的转化类型,并将你所知道的其他转化类型
补充到列表中。
物质关系图解读CaO+H2O==Ca(OH)2H2SO4 + 2NaOH ==Na2SO4+2H2OCO2+H2O==H2CO32NaOH + CO2 ==Na2CO3+H2OFe+CuSO4==FeSO4+Cu思维点拨:本题是对分类方法巩固,同时要注意有序思维方式的养成CaCO3CaOCa(OH)2CaCl2CaCO2CO2或Na2CO3 H2OO2 H2O HCl HCl HClHCl或Cl2 NaOH不同类别的含钙物质的相互转化 电解交流与讨论方程式:1.2Ca+O2==2CaO3.CaO+CO2==CaCO34.CaO+H2O==Ca(OH)27.Ca(OH)2+2HCl== CaCl2+2 H2O5.CaO+ 2HCl== CaCl2+2 H2O人们常根据
物质在转化过程中所表现出的特点,
将化学反应分成不同地类型。化学反应的分类
(1)根据反应物和生成物的类别以及反应前后物质种类的多少可分为:化合反应分解反应置换反应复分解反应H2SO4 +2NaOH====Na2SO4 +2H2O
P5整理与归纳
(2)一种金属与另一种金属的盐溶液发生 的置换反应
活动性强的金属置换活动性弱的金属。金属活动性的强弱,可根据“常见金属活动性顺序”进行判断。整理与归纳CaAgNaMgAlZnFeSnPbHCuHg(1)酸、碱、盐之间发生的复分解反应;
是否有沉淀、气体或 水生成P6整理与归纳判断反应类型: Fe2O3+3CO Fe+2CO2高温是四种基本反应吗?回忆初中氧化反应和还原反应的定义 得到氧的反应叫氧化反应——得氧
氧化物里的氧被夺取的反应叫还原反应——失氧
其实氧化还原反应是同时出现的
请分析下面这条方程式中化合价的变化情况: 0 +2 0 +2定义深化:
有元素化合价变化的反应称为氧化还原反应
化学反应可分为:氧化还原反应和非氧化还原反应
化合价升高被氧化,叫氧化反应,
化合价降低被还原,叫还原反应
还原剂被氧化, 氧化剂被还原, 3、转化类型:基本类型元素价态是否变化 四种基本类型的反应与氧化还原反应之间有什么关系呢?Fe+CuSO4==FeSO4+Cu CaCl2+Na2CO3=CaCO3 +2NaCl
2NaOH+H2SO4 =Na2SO4 +H2O MnO22KClO3==2KCl+3O2Cu(OH)2==CuO+H2OHCl+NH3==NH4Cl不一定不一定不一定不一定一定一定一定不是一定不是氧化还原反应四种基本反应类型与氧化还原反应之间的关系历史上曾经认为有机化合物只能由生物的细胞在一种特殊力量――生命力的作用下才能产生,人工合成有机物是不可能。1828年,德国化学家维勒通过蒸发氰酸铵(NH4CNO,一种无机化合物,由氯化铵和氰酸银反应制得)水溶液得到尿素[CO(NH2)2]。尿素的人工合成,揭开了人工合成有机物的序幕。化学史话例2、下列物质属于纯净物的是( )
A、洁净的空气 B、食盐水
C、浮有冰块的水 D、纯净的盐酸
E、含氮35%的硝酸铵化肥 F、生石灰
C F例1、今有下列三组物质,每组中都有一种物质跟其他三种属于不同的种类。将此种物质(写化学式)和分类依据(选出的物质与其他物质不同之处)写在下面相应的表格内。三组物质分别为:(1)O2、F2、S、N2;(2)Fe、Na、Al、Si;(3)NO、CO2、SO2、P2O5。
?
?
?
?
S固体,其余是气体Si非金属,其余是金属NO难溶氧化物(不成盐氧化物),其余是易溶于水的成盐氧化物中的酸性氧化物。练习下列反应中,属于氧化还原反应的是( )A CaCO3+2HCl=CaCl2+CO2↑+H2O
B CaO+H2O=Ca(OH)2
C 2KMnO4===K2MnO4 +MnO2 +3O2↑
D CaCO3===CaO + CO2↑
E N2 + 3H2 ===2NH3
F 6NO + 4NH3 ==5N2 + 6NO2、有一些不法分子以铜锌合金假冒黄金进行诈骗。
请你至少设计2个实验方案,证明某黄色金属是真金还是黄铜。课堂练兵3、有钠、氢、氧、硫四种元素,试关于它们填写下列空白:
(1)用其中的一种或几种元素写出符合下列要求的化学式:
单质 ,氧化物 ,酸 ,
碱 ,盐 。
(2)写出上述物质间相互发生反应的化学方程式:
单质与酸 ;
酸与氧化物 ;
碱与氧化物 ;
酸与碱 ;
单质与单质 。
(3)又知潜水艇中需要配备氧气再生装置,利用过氧化钠(O2)
与二氧化碳反应生成碳酸钠和氧气,该反应的化学方程式为 。 【课堂练习】1、同学们吃的零食的包装袋中经常有一个小纸袋,上面写着“干燥剂”,其主要成分是生石灰(CaO)。
(1)生石灰属于哪种类别的物质?
(2)生石灰可做干燥剂的理由是什么?(用化学方程式表示)
(3)生石灰还可以跟哪些类别的物质发生化学反应?列举两例,并写出化学方程式
(4)小纸袋中的物质能否长期持续地做干燥剂?为什么?
(5)在你所认识的化学物质中,还有哪些可以用作干燥剂?列举一例。课堂练兵1、现有下列物质:①碳酸钠 ②氧化钠 ③二氧化硅 ④铁 ⑤氧气
⑥氢氧化钙 ⑦硫酸请将上述物质按下列要求分类,并将其序号填
入空白处:
(1)按组成分类,属于单质的是 ,属于氧化物的
是 ,属于酸的是 ,属于碱的是 ,
属于盐的是 。
(2)按溶解性分类,属于易溶物的是 ,属于难
溶物的是 属于微溶物的是 。
(3)按常温状态分类,属于固态的是 ,属于液态的
是 ,属于气态的是 。
为什么你能够很快找到你所需要的书籍?网络中的信息分类复杂的道理往往蕴涵在平凡的生活中,学习也要注意分类!目前已知的化合物已达数千万种,近来每年化学家创造的化合物就达100万种以上。物质的分类与转化同一类物质在组成和性能方面往往
具有一定的相似性。分类有利于更好的研究物质,能实现“掌握一种物质”向“贯通一类物质”转变,提高效率。物质的分类及转化 在我们的日常生活中,常会接触到下列物质:
空气、乙醇、硫酸铵、铜、碘酒、碘、氢气、石墨、食盐水。
P3交流与讨论请将上述物质进行分类,并说明分类的依据。气态:
液态:
固态:易溶:
微溶:
难溶: 导体为:
半导体:
绝缘体: 空气、氢气
乙醇、食盐水、碘酒
硫酸铵、铜、碘、石墨乙醇、食盐水、硫酸铵
碘
空气、氢气、铜、石墨铜、石墨、食盐水
空气、乙醇、碘、氢气、碘酒4.根据物质的组成分单质:铜、碘、氢气、石墨
化合物:乙醇、硫酸铵混合物:空气、食盐水、碘酒
纯净物:物质分类标准不同,分类结果也不同物质根据物质的组成对物质进行分类同一类物质在组成和某些性质
方面往往具有一定的相似性P4问题解决KOH属于碱,CO2和SO2是非金属氧化
物。请写出足量KOH溶液分别与
CO2、SO2 反应的化学方程式。若是少量KOH溶液呢?KOH足量:2KOH + CO2 = K2CO3 +H2O
2KOH + SO2 = K2SO3 +H2O
若CO2 、SO2足量:KOH + CO2+H2O=KHCO3
KOH + SO2+H2O=KHSO3酸性氧化物:
CO2、SO2等能与碱反应生成盐和水的氧化物碱性氧化物:
CaO、Na2O等能与酸反应生成盐和水的氧化物氧化物定义中性氧化物:CO、NO等即不能与酸反应,又不能与碱反应生成盐和水的氧化物两性氧化物: Al2O3、ZnO等即能与酸反应,又能与碱反应生成盐和水的氧化物问题解决:1、实验室中有下列物质,根据物质组成对下列物质进行分类
钠(Na) 、氯气(Cl2) 、氯化铁(FeCl3)溶液、 硫酸(H2SO4) 、碳酸钙(CaCO3) 、氧化钙(CaO) 、氢氧化钠(NaOH) 、甲烷、牛奶、
一氧化碳、海水、石灰乳、硝酸钾、汞物质的分类 纯净物混合物 单质 化合物非均匀混合物:如:泥浆、牛奶、石灰乳、均匀混合物: 氯化铁溶液(硫酸溶液) 、海水无机化合物 有机化合物 :甲烷氧化物:氧化钙 、一氧化碳酸 :硫酸 碱:氢氧化钠 盐:碳酸钙 、硝酸钾其它 金属单质:钠、汞非金属单质:氯气 它是酸性还是碱性氧化物???物质物质转化规律P4交流与讨论1、在初中阶段,我们已经学习了一些物质转化的知识。请举例
说明下表中所列物质的转化类型,并将你所知道的其他转化类型
补充到列表中。
物质关系图解读CaO+H2O==Ca(OH)2H2SO4 + 2NaOH ==Na2SO4+2H2OCO2+H2O==H2CO32NaOH + CO2 ==Na2CO3+H2OFe+CuSO4==FeSO4+Cu思维点拨:本题是对分类方法巩固,同时要注意有序思维方式的养成CaCO3CaOCa(OH)2CaCl2CaCO2CO2或Na2CO3 H2OO2 H2O HCl HCl HClHCl或Cl2 NaOH不同类别的含钙物质的相互转化 电解交流与讨论方程式:1.2Ca+O2==2CaO3.CaO+CO2==CaCO34.CaO+H2O==Ca(OH)27.Ca(OH)2+2HCl== CaCl2+2 H2O5.CaO+ 2HCl== CaCl2+2 H2O人们常根据
物质在转化过程中所表现出的特点,
将化学反应分成不同地类型。化学反应的分类
(1)根据反应物和生成物的类别以及反应前后物质种类的多少可分为:化合反应分解反应置换反应复分解反应H2SO4 +2NaOH====Na2SO4 +2H2O
P5整理与归纳
(2)一种金属与另一种金属的盐溶液发生 的置换反应
活动性强的金属置换活动性弱的金属。金属活动性的强弱,可根据“常见金属活动性顺序”进行判断。整理与归纳CaAgNaMgAlZnFeSnPbHCuHg(1)酸、碱、盐之间发生的复分解反应;
是否有沉淀、气体或 水生成P6整理与归纳判断反应类型: Fe2O3+3CO Fe+2CO2高温是四种基本反应吗?回忆初中氧化反应和还原反应的定义 得到氧的反应叫氧化反应——得氧
氧化物里的氧被夺取的反应叫还原反应——失氧
其实氧化还原反应是同时出现的
请分析下面这条方程式中化合价的变化情况: 0 +2 0 +2定义深化:
有元素化合价变化的反应称为氧化还原反应
化学反应可分为:氧化还原反应和非氧化还原反应
化合价升高被氧化,叫氧化反应,
化合价降低被还原,叫还原反应
还原剂被氧化, 氧化剂被还原, 3、转化类型:基本类型元素价态是否变化 四种基本类型的反应与氧化还原反应之间有什么关系呢?Fe+CuSO4==FeSO4+Cu CaCl2+Na2CO3=CaCO3 +2NaCl
2NaOH+H2SO4 =Na2SO4 +H2O MnO22KClO3==2KCl+3O2Cu(OH)2==CuO+H2OHCl+NH3==NH4Cl不一定不一定不一定不一定一定一定一定不是一定不是氧化还原反应四种基本反应类型与氧化还原反应之间的关系历史上曾经认为有机化合物只能由生物的细胞在一种特殊力量――生命力的作用下才能产生,人工合成有机物是不可能。1828年,德国化学家维勒通过蒸发氰酸铵(NH4CNO,一种无机化合物,由氯化铵和氰酸银反应制得)水溶液得到尿素[CO(NH2)2]。尿素的人工合成,揭开了人工合成有机物的序幕。化学史话例2、下列物质属于纯净物的是( )
A、洁净的空气 B、食盐水
C、浮有冰块的水 D、纯净的盐酸
E、含氮35%的硝酸铵化肥 F、生石灰
C F例1、今有下列三组物质,每组中都有一种物质跟其他三种属于不同的种类。将此种物质(写化学式)和分类依据(选出的物质与其他物质不同之处)写在下面相应的表格内。三组物质分别为:(1)O2、F2、S、N2;(2)Fe、Na、Al、Si;(3)NO、CO2、SO2、P2O5。
?
?
?
?
S固体,其余是气体Si非金属,其余是金属NO难溶氧化物(不成盐氧化物),其余是易溶于水的成盐氧化物中的酸性氧化物。练习下列反应中,属于氧化还原反应的是( )A CaCO3+2HCl=CaCl2+CO2↑+H2O
B CaO+H2O=Ca(OH)2
C 2KMnO4===K2MnO4 +MnO2 +3O2↑
D CaCO3===CaO + CO2↑
E N2 + 3H2 ===2NH3
F 6NO + 4NH3 ==5N2 + 6NO2、有一些不法分子以铜锌合金假冒黄金进行诈骗。
请你至少设计2个实验方案,证明某黄色金属是真金还是黄铜。课堂练兵3、有钠、氢、氧、硫四种元素,试关于它们填写下列空白:
(1)用其中的一种或几种元素写出符合下列要求的化学式:
单质 ,氧化物 ,酸 ,
碱 ,盐 。
(2)写出上述物质间相互发生反应的化学方程式:
单质与酸 ;
酸与氧化物 ;
碱与氧化物 ;
酸与碱 ;
单质与单质 。
(3)又知潜水艇中需要配备氧气再生装置,利用过氧化钠(O2)
与二氧化碳反应生成碳酸钠和氧气,该反应的化学方程式为 。 【课堂练习】1、同学们吃的零食的包装袋中经常有一个小纸袋,上面写着“干燥剂”,其主要成分是生石灰(CaO)。
(1)生石灰属于哪种类别的物质?
(2)生石灰可做干燥剂的理由是什么?(用化学方程式表示)
(3)生石灰还可以跟哪些类别的物质发生化学反应?列举两例,并写出化学方程式
(4)小纸袋中的物质能否长期持续地做干燥剂?为什么?
(5)在你所认识的化学物质中,还有哪些可以用作干燥剂?列举一例。课堂练兵1、现有下列物质:①碳酸钠 ②氧化钠 ③二氧化硅 ④铁 ⑤氧气
⑥氢氧化钙 ⑦硫酸请将上述物质按下列要求分类,并将其序号填
入空白处:
(1)按组成分类,属于单质的是 ,属于氧化物的
是 ,属于酸的是 ,属于碱的是 ,
属于盐的是 。
(2)按溶解性分类,属于易溶物的是 ,属于难
溶物的是 属于微溶物的是 。
(3)按常温状态分类,属于固态的是 ,属于液态的
是 ,属于气态的是 。
