食醋总酸含量的测定(浙江省绍兴市越城区)
图片预览







文档简介
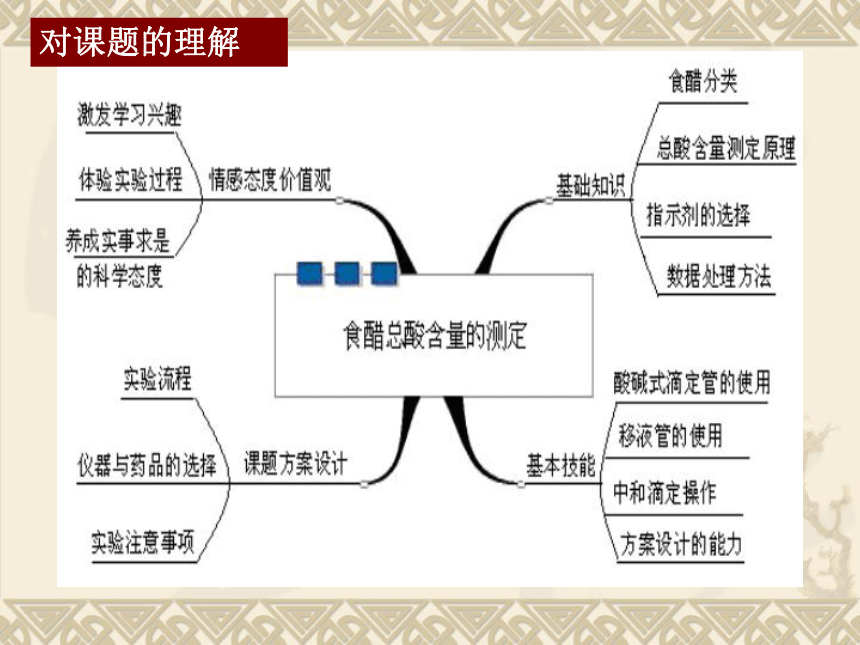
课件29张PPT。 食醋总酸含量的测定对课题的理解酿造醋:以粮食、糖类等为原料,发酵而成。一、食醋的分类配制醋:以酿造醋为主体,加以冰醋酸调和二、食醋的总酸含量以及测定1、定义:食醋的总酸含量是指每100mL食醋中含酸(以醋酸计)的质量,也称食醋的酸度。
2、标准:国家标准规定酿造食醋总酸含量不得低于3.5g/100mL.问:如何测定食醋的总酸含量? 利用滴定分析法,用已知浓度的氢氧化钠溶液
滴定待测食醋样品溶液3、实验原理:
CH3COOH+NaOH = CH3COONa + H2O4、测定方法:酸碱中和滴定
(1).概念
利用已知浓度的酸(或碱)去滴定一定体积未知浓度的碱(或酸),通过测定反应完全时消耗已知浓度的酸(或碱)的体积,从而推算出未知浓度的碱(或酸)的浓度的方法
(2).操作步骤
检漏、润洗、注液、赶气泡、调液、取液、滴定、
记录、计算
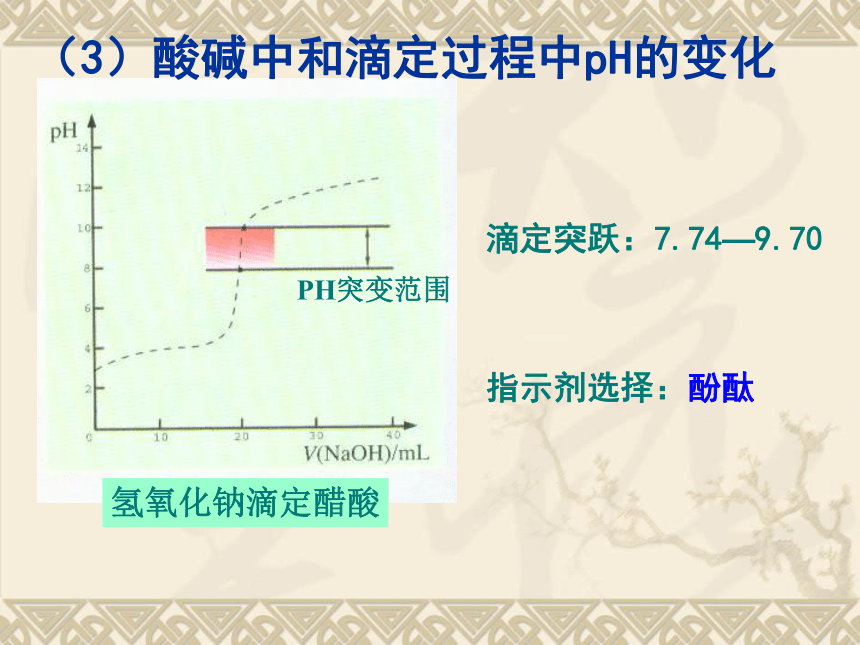
滴定突跃:7.74—9.70指示剂选择:酚酞(3)酸碱中和滴定过程中pH的变化指示剂的选择A、强酸滴定强碱
B、强酸滴定弱碱
C、强碱滴定弱酸酚酞溶液、甲基橙两者正好完全反应,生成强酸弱碱盐,溶液呈酸性,选用甲基橙作指示剂两者正好完全反应,生成强碱弱酸盐,溶液呈碱性,选用酚酞作指示剂(4)、准确的判断滴定的终点指示剂问:当用盐酸滴定氨水时,应选择什么作为指示剂?(二)、实验样品与仪器
待测样品:市售食醋
仪器:移液管、容量瓶、碱式滴定管、酸式滴定管、锥形瓶、铁架台、滴定管夹、洗耳球、玻璃棒
试剂:0.100mol·L-1NaOH标准溶液、0.1%酚酞溶液、蒸馏水三、课题方案设计(一)、实验原理1、标注:温度和容量无分刻度移液管 分刻度移液管(三)实验中移液管的操作 2、用途:
准确移取一定体积的液体洗涤、润洗、移液、洗涤干净4、注意事项:
A.使用前应用少量移取液润洗2-3次
B.移取液体时,管尖应插入液面以下约1cm左右,并随着液面下降而下移。插入太浅可能吸入气泡,太深则移液管外壁粘液过多,影响移取液体体积的精确度。用洗耳球抽吸液体至刻度线上2—3cm处时,迅速用食指按住上口,用中指和拇指配合,保持移液管垂直状态,并左右旋动同时稍松食指,使液面缓慢下降至所需刻度(凹液面最低点与标线水平相切)。若管尖有液滴,可使其与容器壁接触让液滴落下。
C.放液时,务必将移液管下端伸入接受容器内,容器倾斜,移液管垂直,使管尖处与接受容器内壁接触。残留在管尖内的液滴不能用外力(如洗耳球吹)使其移入接受容器中,3、操作:(三)实验中容量瓶的操作 1、常见规格:100mL、250mL、500mL、1000mL
2、操作步骤:
洗涤、检漏、称量、溶解、转移、洗涤、稀释、定容、摇匀3、注意事项:
A.向容量瓶里转移溶液或加入蒸馏水,都要用玻璃棒引流,并且玻璃棒的下端要靠在容量瓶刻度线以下的瓶颈内壁上,棒身要在瓶口的中央位置。
B.用胶头滴管向容量瓶里加蒸馏水时,要逐滴慢加,水滴要落在瓶内液面的中央位置,滴管的尖嘴要在瓶口以上1—2cm处。
C.读取容量瓶内液体的体积时,要使眼睛的视线与容量瓶的刻度线平行,当液体凹液面与容量瓶的刻度线恰好相切时,立即停止滴加蒸馏水。
D.容量瓶使用完毕,应洗净、晾干,1、常见规格:25mL,50mL
2、滴定管的选择:
等于或大于溶液体积的预定值
酸式滴定管:中性、酸性
碱式滴定管:碱性
(三)实验中滴定管的操作(1)、使用前的处理
滴定管在使用前要洗净,还要检查是否漏水,酸式滴定管的活塞是否转动灵活、碱式滴定管的橡胶管是否老化失去弹性等。只有经检查合格的滴定管才能使用。
(2)检漏的方法:
A:酸式滴定管:将滴定管用滴定管夹固定在滴定台上,关闭活塞,向滴定管内加蒸馏水,使液面处在“0”刻度线附近,观察1-2min的时间,看玻璃活塞处是否有水渗出,玻璃尖嘴里是否有水流出。若无水渗出或流出,将玻璃活塞转动180度后再观察1-2min的时间。若仍无水渗出或流出,滴定管活塞的密封性合格。
B:碱式滴定管:检查的部位是滴定管的橡胶管处和尖嘴处,检查方法同上。
(3)使用前还要用待测体积的溶液润洗2—3次,以避免溶液被滴定管内壁上附着的蒸馏水稀释而导致浓度变小。
(4)液体体积测量
调整液面:向滴定管内注入溶液,使液面在“0”刻度线以上2—3cm处,将滴定管垂直夹持在滴定管上。以快速放液的方法赶走滴定管尖嘴内的气泡。调整液面到“0”刻度或“0”刻度以下。
从滴定管放出液体,要用左手操作滴定管。
(5)读数时,眼睛应与液面保持平行。3、注意事项:4.滴定中误差分析(1)仪器润洗不当
A.标准液滴定管不润洗
B.移取待测液的滴定管或移液管不润洗
C.锥形瓶用待测液润洗
(2)读数方式有误
A.滴定前仰视、滴定后俯视
B.滴定前俯视、滴定后仰视
(3)操作出现问题
A.盛标准液的移液管漏液
B.盛标准液的移液管滴定前有气泡,后无
C.振荡锥形瓶时,不小心将待测液溅出
D.将标准液滴到锥形瓶外面
E.移液时将尖嘴部分吹入锥形瓶
F.指示剂变色后立刻读数
(4)指示剂选择不当
A.强酸滴定弱碱用酚酞
B.强碱滴定弱酸用甲基橙
(5)终点判断不准
A.强酸滴定弱碱,甲基橙由黄变红就停止
B.终点有一滴悬而未滴
(6)用固体配制标准液时,样品还有杂质
A.含有氧化钠的氢氧化钠固体配制标准液滴定醋酸
B. 含有碳酸钠的氢氧化钠固体配制标准液滴定醋酸1、将食醋溶液稀释10倍
2、把滴定样品溶液装入酸式滴定管
3、把标准NaOH溶液装入碱式滴定管
4、取待测食醋溶液25mL左右
5、用NaOH标准溶液滴定待测食醋溶液
6、记录数据
7、数据处理(四)实验步骤:数据处理与结论
m(CH3COOH) = c(NaOH)·V(NaOH)·M(CH3COOH)
100mL食醋中所含醋酸的质量为:
m′(CH3COOH) = c(NaOH)·V(NaOH)·
M(CH3COOH)× ×
根据3次接近的平行测定值,可计算食醋中总酸含量的平均值。(五)、实验数据的处理:随堂检测1、酸碱恰好完全中和时 ( )
A、酸和碱的物质的量一定相等
B、溶液呈中性
C、酸和碱的物质的量浓度相等
D、酸所能提供的H+与碱所能提供的OH-的
物质的量相等D随堂检测2、进行中和滴定时,下列仪器事先不应用所盛
溶液洗涤的是 ( )
A、酸式滴定管 B、碱式滴定管
C、锥形瓶 D、移液管C随堂检测3、下列说法正确的是( )
A、滴定管下端带有玻璃活塞的是碱式滴定管
B、滴定操作时,左手摇动锥形瓶,右手控制
滴定管
C、滴定管在滴定前都要先排除尖嘴部分的空
气泡
D、滴定时两眼应注视滴定管中液面的变化,
以免滴定过量AC4、下列操作会导致待测食醋总酸量偏低的是
A、酸式滴定管用蒸馏水洗过后,未用食醋溶液润洗
B、配制碱液时,称量后固体吸湿
C、碱式滴定管滴定前平视,滴定后仰视
D、滴定过程中不慎将锥形瓶中的少量食醋液体摇出
E、酸式滴定管取样前有气泡,取样后气泡消失
AD5、用中和滴定法测定某烧碱的纯度。
⑴配制待测液:将1.7g含有少量杂质(不与盐酸反应)的固体烧碱样品配制成200mL溶液,所用的主要仪器有________________________________________。
⑵滴定:①盛装0.20mol/L盐酸标准液应该用_______式滴定管,滴定管洗涤干净的标准是_______________ _________________________________________。
②滴定时,应先向锥形瓶中加酚酞作为指示剂;滴定过程中两眼应该注视__________________,滴定终点时,锥形瓶中的溶液的颜色变化是(选序号)________。
A、由黄色变为红色 B、由黄色变为橙色 C、由浅红色变为无色 D、由无色变为红色
烧杯、200mL容量瓶、玻璃棒、药匙、滴管酸 滴定管内壁上
的水均匀了,既不聚成水滴也不成股流下 锥形瓶内溶液的颜色变化 C⑶纯度计算:NaOH溶液的浓度为______________mol/L,
烧碱样品的纯度为____________。0.2094.6%⑷对几种假定情况的讨论:(填无影响、偏高、偏低)
①若用蒸馏水冲洗锥形瓶,则会使测定的结果_________________。
②若在滴定过程中不慎将数滴酸液滴在锥形瓶外,则会使测定结果_________。
③若刚见到指示剂局部的颜色有变化就停止滴定,则会使测定结果_________。
④读数时,若滴定前仰视,滴定后俯视,则会使测定结果_________________。无影响 偏高偏低偏低课堂练习1.下列仪器中,没有“0”刻度的是
A. 量筒; B. 温度计; C. 酸式滴定管; D. 托盘天平游码刻度尺;
2.欲量取25.0 mL氢氧化钠溶液置于锥形瓶中,可选用的量器是
A. 刻度烧杯; B. 25 mL移液管; C. 25 mL容量瓶; D. 100 mL量筒;
3.要准确量取25.00 mL高锰酸钾溶液,应选的仪器是
A. 50 mL的量筒; B. 25 mL量筒; C. 50 mL酸式滴定管;D. 25 mL碱式滴定管;ABC4.对于容积为25 mL的量筒和酸式滴定管的刻度,说法正确的是
A. 最上方刻度都是25;B. 量筒最下方刻度是0;
C. 酸式滴定管最下方刻度是25;D. 量筒最上方刻度是25
5.欲量取25.0 0mL氢氧化钠溶液置于锥形瓶中,可选用的量器是
A. 刻度烧杯; B. 25 mL移液管; C. 25 mL容量瓶; D. 100 mL量筒;CB
2、标准:国家标准规定酿造食醋总酸含量不得低于3.5g/100mL.问:如何测定食醋的总酸含量? 利用滴定分析法,用已知浓度的氢氧化钠溶液
滴定待测食醋样品溶液3、实验原理:
CH3COOH+NaOH = CH3COONa + H2O4、测定方法:酸碱中和滴定
(1).概念
利用已知浓度的酸(或碱)去滴定一定体积未知浓度的碱(或酸),通过测定反应完全时消耗已知浓度的酸(或碱)的体积,从而推算出未知浓度的碱(或酸)的浓度的方法
(2).操作步骤
检漏、润洗、注液、赶气泡、调液、取液、滴定、
记录、计算
滴定突跃:7.74—9.70指示剂选择:酚酞(3)酸碱中和滴定过程中pH的变化指示剂的选择A、强酸滴定强碱
B、强酸滴定弱碱
C、强碱滴定弱酸酚酞溶液、甲基橙两者正好完全反应,生成强酸弱碱盐,溶液呈酸性,选用甲基橙作指示剂两者正好完全反应,生成强碱弱酸盐,溶液呈碱性,选用酚酞作指示剂(4)、准确的判断滴定的终点指示剂问:当用盐酸滴定氨水时,应选择什么作为指示剂?(二)、实验样品与仪器
待测样品:市售食醋
仪器:移液管、容量瓶、碱式滴定管、酸式滴定管、锥形瓶、铁架台、滴定管夹、洗耳球、玻璃棒
试剂:0.100mol·L-1NaOH标准溶液、0.1%酚酞溶液、蒸馏水三、课题方案设计(一)、实验原理1、标注:温度和容量无分刻度移液管 分刻度移液管(三)实验中移液管的操作 2、用途:
准确移取一定体积的液体洗涤、润洗、移液、洗涤干净4、注意事项:
A.使用前应用少量移取液润洗2-3次
B.移取液体时,管尖应插入液面以下约1cm左右,并随着液面下降而下移。插入太浅可能吸入气泡,太深则移液管外壁粘液过多,影响移取液体体积的精确度。用洗耳球抽吸液体至刻度线上2—3cm处时,迅速用食指按住上口,用中指和拇指配合,保持移液管垂直状态,并左右旋动同时稍松食指,使液面缓慢下降至所需刻度(凹液面最低点与标线水平相切)。若管尖有液滴,可使其与容器壁接触让液滴落下。
C.放液时,务必将移液管下端伸入接受容器内,容器倾斜,移液管垂直,使管尖处与接受容器内壁接触。残留在管尖内的液滴不能用外力(如洗耳球吹)使其移入接受容器中,3、操作:(三)实验中容量瓶的操作 1、常见规格:100mL、250mL、500mL、1000mL
2、操作步骤:
洗涤、检漏、称量、溶解、转移、洗涤、稀释、定容、摇匀3、注意事项:
A.向容量瓶里转移溶液或加入蒸馏水,都要用玻璃棒引流,并且玻璃棒的下端要靠在容量瓶刻度线以下的瓶颈内壁上,棒身要在瓶口的中央位置。
B.用胶头滴管向容量瓶里加蒸馏水时,要逐滴慢加,水滴要落在瓶内液面的中央位置,滴管的尖嘴要在瓶口以上1—2cm处。
C.读取容量瓶内液体的体积时,要使眼睛的视线与容量瓶的刻度线平行,当液体凹液面与容量瓶的刻度线恰好相切时,立即停止滴加蒸馏水。
D.容量瓶使用完毕,应洗净、晾干,1、常见规格:25mL,50mL
2、滴定管的选择:
等于或大于溶液体积的预定值
酸式滴定管:中性、酸性
碱式滴定管:碱性
(三)实验中滴定管的操作(1)、使用前的处理
滴定管在使用前要洗净,还要检查是否漏水,酸式滴定管的活塞是否转动灵活、碱式滴定管的橡胶管是否老化失去弹性等。只有经检查合格的滴定管才能使用。
(2)检漏的方法:
A:酸式滴定管:将滴定管用滴定管夹固定在滴定台上,关闭活塞,向滴定管内加蒸馏水,使液面处在“0”刻度线附近,观察1-2min的时间,看玻璃活塞处是否有水渗出,玻璃尖嘴里是否有水流出。若无水渗出或流出,将玻璃活塞转动180度后再观察1-2min的时间。若仍无水渗出或流出,滴定管活塞的密封性合格。
B:碱式滴定管:检查的部位是滴定管的橡胶管处和尖嘴处,检查方法同上。
(3)使用前还要用待测体积的溶液润洗2—3次,以避免溶液被滴定管内壁上附着的蒸馏水稀释而导致浓度变小。
(4)液体体积测量
调整液面:向滴定管内注入溶液,使液面在“0”刻度线以上2—3cm处,将滴定管垂直夹持在滴定管上。以快速放液的方法赶走滴定管尖嘴内的气泡。调整液面到“0”刻度或“0”刻度以下。
从滴定管放出液体,要用左手操作滴定管。
(5)读数时,眼睛应与液面保持平行。3、注意事项:4.滴定中误差分析(1)仪器润洗不当
A.标准液滴定管不润洗
B.移取待测液的滴定管或移液管不润洗
C.锥形瓶用待测液润洗
(2)读数方式有误
A.滴定前仰视、滴定后俯视
B.滴定前俯视、滴定后仰视
(3)操作出现问题
A.盛标准液的移液管漏液
B.盛标准液的移液管滴定前有气泡,后无
C.振荡锥形瓶时,不小心将待测液溅出
D.将标准液滴到锥形瓶外面
E.移液时将尖嘴部分吹入锥形瓶
F.指示剂变色后立刻读数
(4)指示剂选择不当
A.强酸滴定弱碱用酚酞
B.强碱滴定弱酸用甲基橙
(5)终点判断不准
A.强酸滴定弱碱,甲基橙由黄变红就停止
B.终点有一滴悬而未滴
(6)用固体配制标准液时,样品还有杂质
A.含有氧化钠的氢氧化钠固体配制标准液滴定醋酸
B. 含有碳酸钠的氢氧化钠固体配制标准液滴定醋酸1、将食醋溶液稀释10倍
2、把滴定样品溶液装入酸式滴定管
3、把标准NaOH溶液装入碱式滴定管
4、取待测食醋溶液25mL左右
5、用NaOH标准溶液滴定待测食醋溶液
6、记录数据
7、数据处理(四)实验步骤:数据处理与结论
m(CH3COOH) = c(NaOH)·V(NaOH)·M(CH3COOH)
100mL食醋中所含醋酸的质量为:
m′(CH3COOH) = c(NaOH)·V(NaOH)·
M(CH3COOH)× ×
根据3次接近的平行测定值,可计算食醋中总酸含量的平均值。(五)、实验数据的处理:随堂检测1、酸碱恰好完全中和时 ( )
A、酸和碱的物质的量一定相等
B、溶液呈中性
C、酸和碱的物质的量浓度相等
D、酸所能提供的H+与碱所能提供的OH-的
物质的量相等D随堂检测2、进行中和滴定时,下列仪器事先不应用所盛
溶液洗涤的是 ( )
A、酸式滴定管 B、碱式滴定管
C、锥形瓶 D、移液管C随堂检测3、下列说法正确的是( )
A、滴定管下端带有玻璃活塞的是碱式滴定管
B、滴定操作时,左手摇动锥形瓶,右手控制
滴定管
C、滴定管在滴定前都要先排除尖嘴部分的空
气泡
D、滴定时两眼应注视滴定管中液面的变化,
以免滴定过量AC4、下列操作会导致待测食醋总酸量偏低的是
A、酸式滴定管用蒸馏水洗过后,未用食醋溶液润洗
B、配制碱液时,称量后固体吸湿
C、碱式滴定管滴定前平视,滴定后仰视
D、滴定过程中不慎将锥形瓶中的少量食醋液体摇出
E、酸式滴定管取样前有气泡,取样后气泡消失
AD5、用中和滴定法测定某烧碱的纯度。
⑴配制待测液:将1.7g含有少量杂质(不与盐酸反应)的固体烧碱样品配制成200mL溶液,所用的主要仪器有________________________________________。
⑵滴定:①盛装0.20mol/L盐酸标准液应该用_______式滴定管,滴定管洗涤干净的标准是_______________ _________________________________________。
②滴定时,应先向锥形瓶中加酚酞作为指示剂;滴定过程中两眼应该注视__________________,滴定终点时,锥形瓶中的溶液的颜色变化是(选序号)________。
A、由黄色变为红色 B、由黄色变为橙色 C、由浅红色变为无色 D、由无色变为红色
烧杯、200mL容量瓶、玻璃棒、药匙、滴管酸 滴定管内壁上
的水均匀了,既不聚成水滴也不成股流下 锥形瓶内溶液的颜色变化 C⑶纯度计算:NaOH溶液的浓度为______________mol/L,
烧碱样品的纯度为____________。0.2094.6%⑷对几种假定情况的讨论:(填无影响、偏高、偏低)
①若用蒸馏水冲洗锥形瓶,则会使测定的结果_________________。
②若在滴定过程中不慎将数滴酸液滴在锥形瓶外,则会使测定结果_________。
③若刚见到指示剂局部的颜色有变化就停止滴定,则会使测定结果_________。
④读数时,若滴定前仰视,滴定后俯视,则会使测定结果_________________。无影响 偏高偏低偏低课堂练习1.下列仪器中,没有“0”刻度的是
A. 量筒; B. 温度计; C. 酸式滴定管; D. 托盘天平游码刻度尺;
2.欲量取25.0 mL氢氧化钠溶液置于锥形瓶中,可选用的量器是
A. 刻度烧杯; B. 25 mL移液管; C. 25 mL容量瓶; D. 100 mL量筒;
3.要准确量取25.00 mL高锰酸钾溶液,应选的仪器是
A. 50 mL的量筒; B. 25 mL量筒; C. 50 mL酸式滴定管;D. 25 mL碱式滴定管;ABC4.对于容积为25 mL的量筒和酸式滴定管的刻度,说法正确的是
A. 最上方刻度都是25;B. 量筒最下方刻度是0;
C. 酸式滴定管最下方刻度是25;D. 量筒最上方刻度是25
5.欲量取25.0 0mL氢氧化钠溶液置于锥形瓶中,可选用的量器是
A. 刻度烧杯; B. 25 mL移液管; C. 25 mL容量瓶; D. 100 mL量筒;CB
同课章节目录
- 专题一 物质的分离与提纯
- 课题1 海带中碘元素的分离及检验
- 拓展课题1-1 茶叶中某些元素的鉴定
- 课题2 用纸层析法分离铁离子和铜离子
- 拓展课题1-2 菠菜的叶绿体中色素的提取和分离
- 拓展课题1-3 用粉笔进行层析分离
- 课题3 硝酸钾晶体的制备
- 拓展课题1-4 粗盐提纯
- 专题二 物质性质的研究
- 课题1 铝及其化合物的性质
- 拓展课题2-1 铝热反应
- 课题2 乙醇和苯酚的性质
- 拓展课题2-2 苯酚与甲醛的反应
- 专题三 物质的检验与鉴别
- 课题1 牙膏和火柴中某些成分的检验
- 拓展课题3-1 新装修居室内空气中甲醛浓度的检测
- 拓展课题3-2 汽车尾气成分的检验
- 课题2 亚硝酸钠和食盐的鉴别
- 拓展课题3-3 真假碘盐的鉴别
- 专题四 化学反应条件的控制
- 课题1 硫代硫酸钠与酸反应速率的影响因素
- 拓展课题4-1 “蓝瓶子”实验
- 课题2 催化剂对过氧化氢分解反应速率的影响
- 拓展课题4-2 过氧化氢酶的催化作用
- 拓展课题4-3 蔗糖的燃烧
- 课题3 反应条件对化学平衡的影响
- 拓展课题4-4 淀粉与碘显色现象的探究
- 拓展课题4-5 压强对化学平衡的影响
- 专题五 电化学问题研究
- 课题1 原电池
- 拓展课题5-1 干电池模拟实验
- 课题2 电解与电镀
- 拓展课题5-2 阿伏加德罗常数的测定
- 专题六 物质的定量分析
- 课题1 食醋总酸含量的测定
- 拓展课题6-1 配制并标定氢氧化钠溶液
- 课题2 镀锌铁皮锌镀层厚度的测定
- 拓展课题6-2 水果中维生素C含量的测定
- 专题七 物质的制备与合成
- 课题1 硫酸亚铁铵的制备
- 拓展课题7-1 用制氢废液制备硫酸锌晶体
- 课题2 阿司匹林的合成
- 拓展课题7-2 对氨基苯磺酸的合成
