苏教版必修1专题二 第一单元1氯气的生产原理课件
文档属性
| 名称 | 苏教版必修1专题二 第一单元1氯气的生产原理课件 |

|
|
| 格式 | rar | ||
| 文件大小 | 787.6KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2009-06-15 00:00:00 | ||
图片预览









文档简介
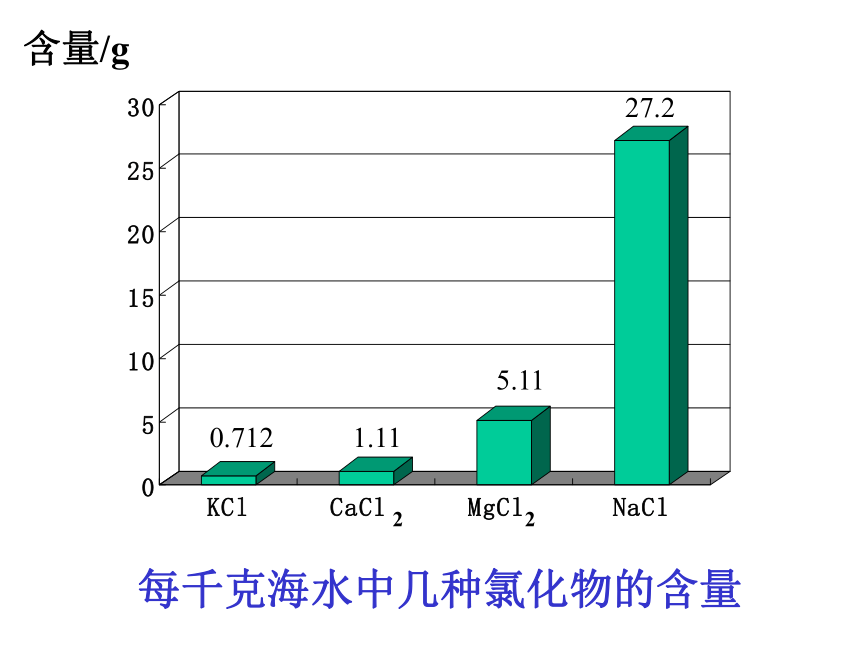
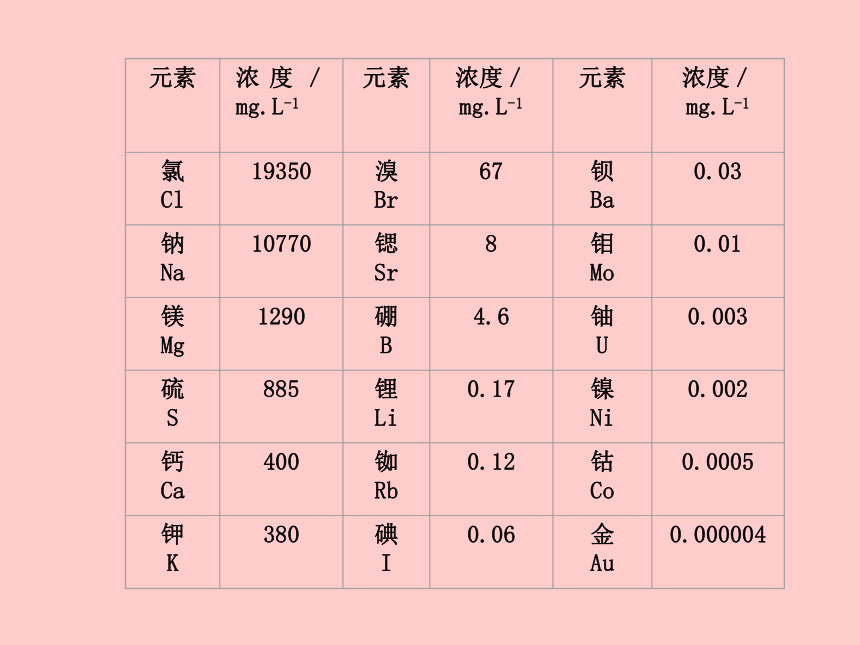
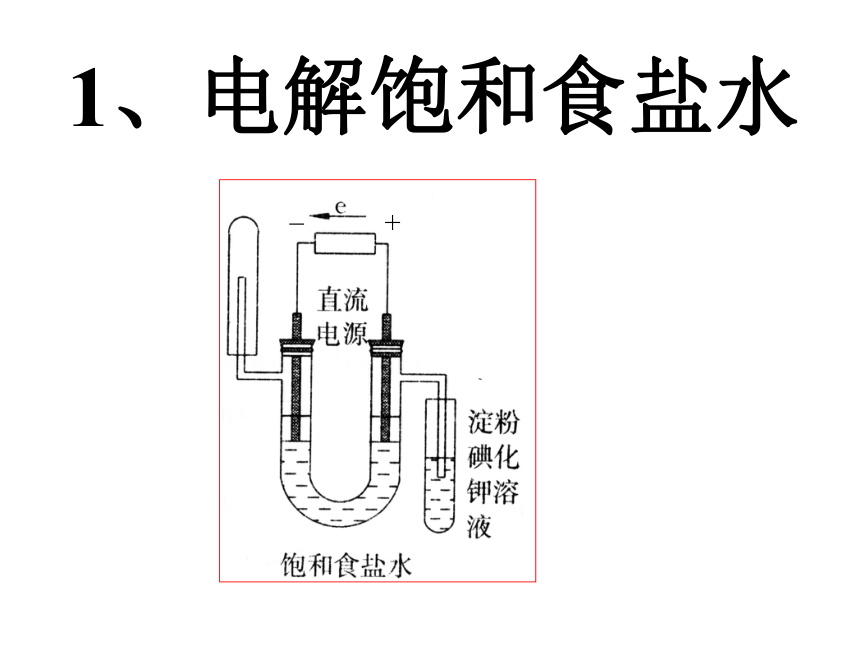
课件42张PPT。从海水中获得的化学物质专题 2 你知道浩瀚的大海中究竟蕴藏着哪些物质吗?请查阅有关资料了解海水中主要含有的物质和各元素的含量。调查研究每千克海水中几种氯化物的含量含量/g0.7121.115.1127.2222查阅有关资料了解人们是如何从海水中获得氯化钠并生产氯气的。调查研究第一单元 氯、溴、碘及其化合物氯气的生产原理(一)氯气的工业制法(二)氯气的实验室制法 电解饱和食盐水(一)氯气的工业制法1、电解饱和食盐水+_两极均产生气泡通电后有新的气体物质生成将铁棒上方收集到的气体靠近火焰,有轻微的爆鸣声有氢气生成黄绿色、刺激性气味的气体产生,湿润的淀粉碘化钾试纸变蓝有氯气生成铁棒周围的颜色变红有碱性物质生成实验原理:氯化钠和水发生电解反应,在阳极生成氯气,在阴极生成氢气和氢氧化钠。2NaCl+2H2O 2NaOH+H2↑+Cl2↑通电电解氯化钠溶液的化学方程式:电极反应式:阳极:2Cl-—2e- = Cl2↑
(氧化反应)阴极 :2H+ + 2e - = H2↑
(还原反应) 氯 气化学式:Cl21774年,瑞典化学家舍勒发现氯气。
1810年,英国化学家戴维将这种元素命名为Chlorine,这个名称来自希腊文,有“绿色”的意思。我国早年译文将其译成“绿气”,后改为氯气。戴维(二)氯气的实验室制法1、主要仪器:分液漏斗、圆底烧瓶、铁架台、石棉网、酒精灯、集气瓶、烧杯、导管、双孔橡皮塞等 2、反应原料:浓盐酸(液体)
与二氧化锰(固体) 3、实验原理:MnO2 + 4HCl(浓) = MnCl2 + Cl2 ↑ + 2H2O强调:MnO2跟浓盐酸在共热的条件下才反应生成Cl2,稀盐酸不与MnO2反应。由于稀盐酸的还原性比浓盐酸弱,不能被MnO2氧化。4、发生装置:固体+液体 气体?实验室制取氯气与制取氧气、氢气的装置相同吗?制Cl2项目装配发生装置的主要仪器收集气体方法发生装置类型Cl2O2H2向上排空集气法(或排饱和食盐水法)排水法(或向上排空集气法排水法(或向下排空集气法固液加热固液不加热固固加热小结选择气体发生装置的原则是反应物的状态和反应条件5、收集装置:向上排空气法
或排饱和食盐水法①氯气的密度大于相同状况下空气密度②氯气能溶于水,但在饱和NaCl溶液中溶
解度很小6、尾气处理:用氢氧化钠溶
液吸收2NaOH + Cl2 = NaCl + NaClO + H2O思考:所得氯气是纯净的吗? 7、除杂干燥: 饱和食盐水(除HCl) 浓硫酸(除水蒸气) 讨论1、使用浓盐酸与足量的MnO2共热制Cl2,实际产生的Cl2总比理论值低,其主要原因是什么?稀盐酸与MnO2不反应,随着反应的进行,浓盐酸的物质的量浓度逐渐变小。讨论2、下图是实验室用来制取干燥、纯净氯气的装置;由于装置和使用药品有错误而未能在D瓶中收集到Cl2,请指出装置中的错误。讨论 3、实验室还可用KMnO4或KClO3代替MnO2与浓盐酸反应制氯气:2KMnO4+16HCl(浓)=2KCl+2MnCl2+8H2O+5Cl2 ↑KClO3+6HCl(浓)=KCl+3H2O+3Cl2 ↑思考上述反应的氧化剂、还原剂分别是何物质?随堂检测1、实验室制氯气时,二氧化锰的作用是 ( )
BDA.催化剂 B.氧化剂
C.还原剂 D.反应物2、实验室用KMnO4制氧气,为除去粘附在试管壁上的MnO2,可用试剂是 ( )
A.汽油 B.水
C.稀盐酸 D.浓盐酸D3、实验室制氯气时有如下操作,操作顺序正确的是 ( ) ①连接好装置,检查气密性 ②缓缓加热,加快反应,使气体均匀逸出 ③在烧瓶中加入二氧化锰粉末 ④往分液漏斗中加入浓盐酸,再缓缓滴入烧瓶中 ⑤用向上排空气法收集氯气,尾气导入吸收剂中
A.①②③④⑤ B.④③①②⑤
C.①③④②⑤ D.①④③②⑤C4、工业上利用电解饱和食盐水的方法制取 、 和 。在电源正极上方收集到的气体能使湿润的 变蓝色,证明是 ;在电源负极上方收集到的气体是 ,在电极附近的水溶液中滴几滴酚酞溶液,则溶液 ,证明有 生成。若电解一段时间后,电源正极上方收集到的气体在标准状况下为4.48L,则在电源负极上方将收集到 g 气体,在溶液中产生 g 。停止通电后,待溶液混合均匀,溶液的pH会 。 Cl2 H2 NaOH 淀粉碘化钾试纸 Cl2 H2 变红 NaOH0.4g H2 16g NaOH升高 5、某学生设计如下实验装置用于制备纯净的氯气。 (1)装置中有六处错误,请指出。
① ,
② ,
③ ,
④ ,
⑤ ,
⑥ 。 烧瓶下面缺石棉网 铁圈下面缺酒精灯 原料使用了稀盐酸 不应使用长颈漏斗 盛浓硫酸的洗气瓶和盛饱和食盐水的洗气瓶位置颠倒了 洗气瓶D的气体入口导管应深插在液面下,而出口导管应靠近瓶塞 再见1.发生装置固、固加热制气固、液不加热制气固、液加热制气1.试管口稍向下倾斜
2.铁夹夹在离管口1/3处
3.加热时先均匀受热,再用外焰在药品底部加热优点:随开随用,
随关随停
适用于制取较多气体洗气瓶:
盛液体试剂干燥管:
盛固体试剂U型管:
盛固体试剂2.气体除杂、干燥装置知识扩展:通过简易装置得到的氯气是不是纯净的,如果不是还含有哪些杂质,应该怎么除去。有HCl气体和水蒸气。用浓H2SO4除去水蒸气,饱和NaCl溶液除HCl气体顺序 :先杂 ,后水气体导管:长 进,短出。向上排空法
(密度比空气大)3.收集装置排水法向下排空法
(密度比空气小)不溶于水,
不和水反应氯气向上排空法或排饱和食盐水法收集4.氯气的收集和尾气处理装置收集
装置Cl2Cl2有毒气体必需
进行尾气处理若气体在吸收剂中溶速快且溶解度极大,易倒吸,选用B;难以吸收的可以点燃处理,选用D。吸收溶解速度不很快,溶解度也不很大的气体用装置A;少量尾气可以集于气球中,选用C;小结:尾气的处理方法
(氧化反应)阴极 :2H+ + 2e - = H2↑
(还原反应) 氯 气化学式:Cl21774年,瑞典化学家舍勒发现氯气。
1810年,英国化学家戴维将这种元素命名为Chlorine,这个名称来自希腊文,有“绿色”的意思。我国早年译文将其译成“绿气”,后改为氯气。戴维(二)氯气的实验室制法1、主要仪器:分液漏斗、圆底烧瓶、铁架台、石棉网、酒精灯、集气瓶、烧杯、导管、双孔橡皮塞等 2、反应原料:浓盐酸(液体)
与二氧化锰(固体) 3、实验原理:MnO2 + 4HCl(浓) = MnCl2 + Cl2 ↑ + 2H2O强调:MnO2跟浓盐酸在共热的条件下才反应生成Cl2,稀盐酸不与MnO2反应。由于稀盐酸的还原性比浓盐酸弱,不能被MnO2氧化。4、发生装置:固体+液体 气体?实验室制取氯气与制取氧气、氢气的装置相同吗?制Cl2项目装配发生装置的主要仪器收集气体方法发生装置类型Cl2O2H2向上排空集气法(或排饱和食盐水法)排水法(或向上排空集气法排水法(或向下排空集气法固液加热固液不加热固固加热小结选择气体发生装置的原则是反应物的状态和反应条件5、收集装置:向上排空气法
或排饱和食盐水法①氯气的密度大于相同状况下空气密度②氯气能溶于水,但在饱和NaCl溶液中溶
解度很小6、尾气处理:用氢氧化钠溶
液吸收2NaOH + Cl2 = NaCl + NaClO + H2O思考:所得氯气是纯净的吗? 7、除杂干燥: 饱和食盐水(除HCl) 浓硫酸(除水蒸气) 讨论1、使用浓盐酸与足量的MnO2共热制Cl2,实际产生的Cl2总比理论值低,其主要原因是什么?稀盐酸与MnO2不反应,随着反应的进行,浓盐酸的物质的量浓度逐渐变小。讨论2、下图是实验室用来制取干燥、纯净氯气的装置;由于装置和使用药品有错误而未能在D瓶中收集到Cl2,请指出装置中的错误。讨论 3、实验室还可用KMnO4或KClO3代替MnO2与浓盐酸反应制氯气:2KMnO4+16HCl(浓)=2KCl+2MnCl2+8H2O+5Cl2 ↑KClO3+6HCl(浓)=KCl+3H2O+3Cl2 ↑思考上述反应的氧化剂、还原剂分别是何物质?随堂检测1、实验室制氯气时,二氧化锰的作用是 ( )
BDA.催化剂 B.氧化剂
C.还原剂 D.反应物2、实验室用KMnO4制氧气,为除去粘附在试管壁上的MnO2,可用试剂是 ( )
A.汽油 B.水
C.稀盐酸 D.浓盐酸D3、实验室制氯气时有如下操作,操作顺序正确的是 ( ) ①连接好装置,检查气密性 ②缓缓加热,加快反应,使气体均匀逸出 ③在烧瓶中加入二氧化锰粉末 ④往分液漏斗中加入浓盐酸,再缓缓滴入烧瓶中 ⑤用向上排空气法收集氯气,尾气导入吸收剂中
A.①②③④⑤ B.④③①②⑤
C.①③④②⑤ D.①④③②⑤C4、工业上利用电解饱和食盐水的方法制取 、 和 。在电源正极上方收集到的气体能使湿润的 变蓝色,证明是 ;在电源负极上方收集到的气体是 ,在电极附近的水溶液中滴几滴酚酞溶液,则溶液 ,证明有 生成。若电解一段时间后,电源正极上方收集到的气体在标准状况下为4.48L,则在电源负极上方将收集到 g 气体,在溶液中产生 g 。停止通电后,待溶液混合均匀,溶液的pH会 。 Cl2 H2 NaOH 淀粉碘化钾试纸 Cl2 H2 变红 NaOH0.4g H2 16g NaOH升高 5、某学生设计如下实验装置用于制备纯净的氯气。 (1)装置中有六处错误,请指出。
① ,
② ,
③ ,
④ ,
⑤ ,
⑥ 。 烧瓶下面缺石棉网 铁圈下面缺酒精灯 原料使用了稀盐酸 不应使用长颈漏斗 盛浓硫酸的洗气瓶和盛饱和食盐水的洗气瓶位置颠倒了 洗气瓶D的气体入口导管应深插在液面下,而出口导管应靠近瓶塞 再见1.发生装置固、固加热制气固、液不加热制气固、液加热制气1.试管口稍向下倾斜
2.铁夹夹在离管口1/3处
3.加热时先均匀受热,再用外焰在药品底部加热优点:随开随用,
随关随停
适用于制取较多气体洗气瓶:
盛液体试剂干燥管:
盛固体试剂U型管:
盛固体试剂2.气体除杂、干燥装置知识扩展:通过简易装置得到的氯气是不是纯净的,如果不是还含有哪些杂质,应该怎么除去。有HCl气体和水蒸气。用浓H2SO4除去水蒸气,饱和NaCl溶液除HCl气体顺序 :先杂 ,后水气体导管:长 进,短出。向上排空法
(密度比空气大)3.收集装置排水法向下排空法
(密度比空气小)不溶于水,
不和水反应氯气向上排空法或排饱和食盐水法收集4.氯气的收集和尾气处理装置收集
装置Cl2Cl2有毒气体必需
进行尾气处理若气体在吸收剂中溶速快且溶解度极大,易倒吸,选用B;难以吸收的可以点燃处理,选用D。吸收溶解速度不很快,溶解度也不很大的气体用装置A;少量尾气可以集于气球中,选用C;小结:尾气的处理方法
