化学必修2乙烯课件(陕西省延安市宝塔区)
文档属性
| 名称 | 化学必修2乙烯课件(陕西省延安市宝塔区) |
|
|
| 格式 | rar | ||
| 文件大小 | 142.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2009-06-17 00:00:00 | ||
图片预览




文档简介
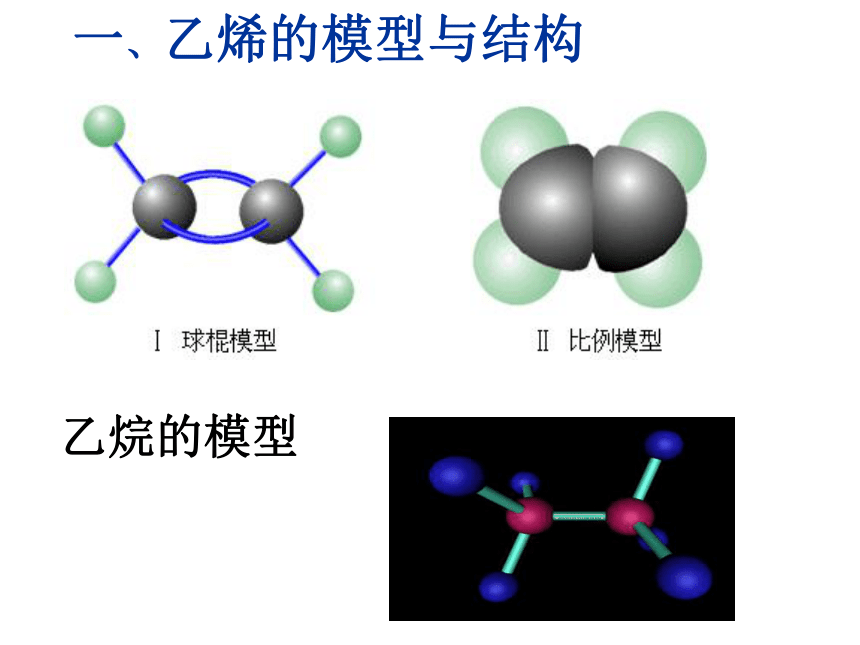
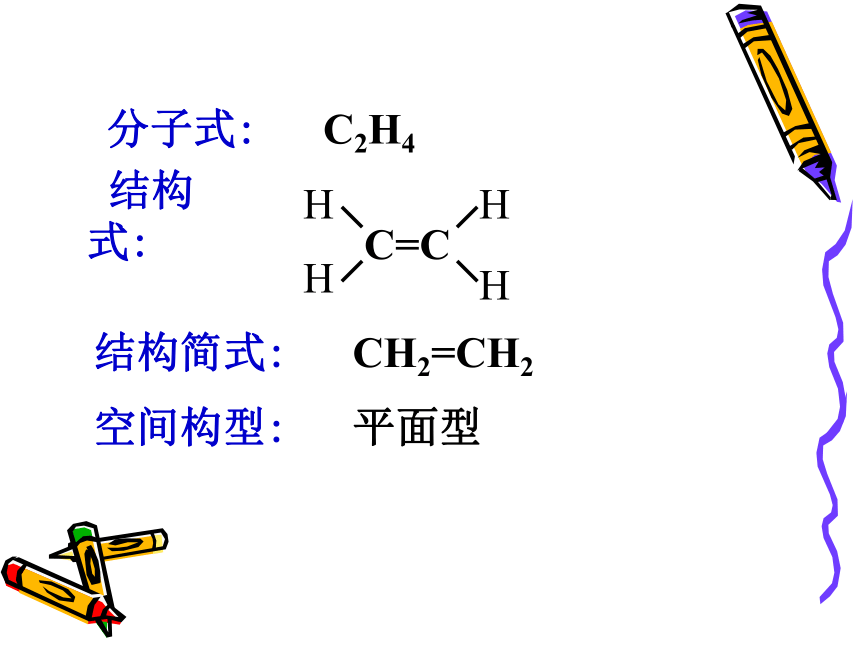
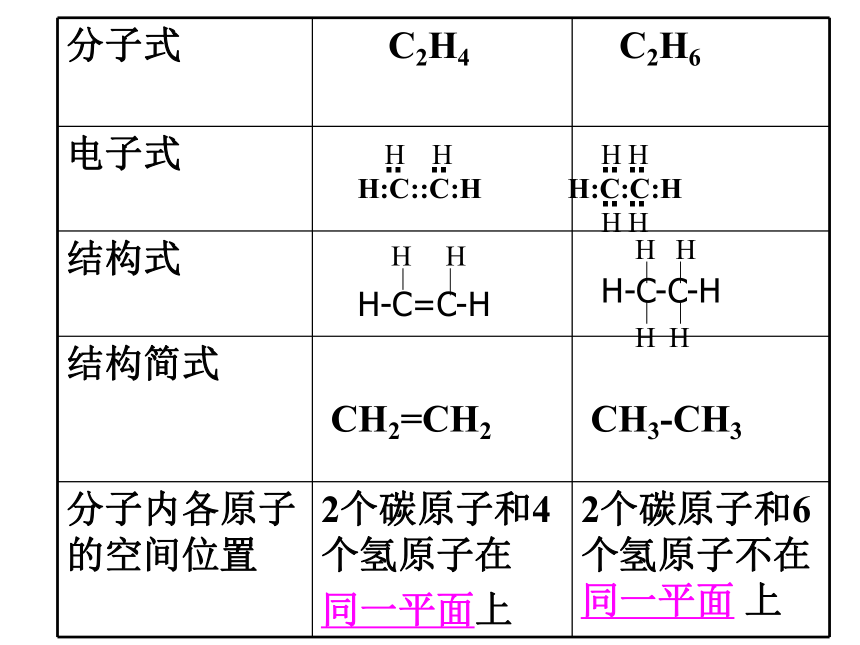
课件17张PPT。乙 烯一、乙烯的模型与结构乙烷的模型分子式: C2H4结构简式: CH2=CH2空间构型: 平面型H:C::C:H H:C:C:H HH............HHHHH-C=C-HHHH-C-C-HHHHH说明:1、C=C的键能和键长并不是C-C的两倍,说明C=C双键中有一个键不稳定,容易断裂,有一个键较稳定。
2、链烃分子里含有碳碳双键的烃称为 烯烃。
3、乙烯是最简单的烯烃。
4、不饱和烃定义:把分子里含有碳碳双键或碳碳三键,碳原子所结合的氢原子少于饱和链烃里的氢原子数,这样的烃叫做不饱和烃。
二、乙烯的性质1.氧化反应
(1)将乙烯气体点燃
化学反应方程式:
(产生黑烟是因为含碳量高,燃烧不充分;火焰明亮是碳微粒受灼热而发光) 乙烯是无色气体,稍有气味,密度是1.25 g/L,比空气略轻(分子量28),难溶于水。乙烯的物理性质:乙烯的化学性质:[活动与探究]观察并记录下列实验现象,实验事实说明乙烯有什么性质?
实验1:把乙烯气体通入酸性高锰酸钾溶液中。
实验2:把乙烯气体通溴的水溶液(即溴水)中。
可使酸性高锰酸钾褪色溴水的红棕色很快褪去可使酸性高锰酸钾褪色---
可以被强氧化剂氧化根据实验1归纳: 表现了酸性高锰酸钾的强氧化性 将乙烯气体通入溴水溶液中,可以看到溴的红棕色很快褪去,说明乙烯与溴发生反应。根据实验2归纳:有机物分子中双键(或三键)两端的碳原子与其他原子或原子团直接结合生成新的化合物的反应,叫做加成反应2、乙烯的加成反应CH2==CH2+H—H →CH2==CH2+H—X→CH2==CH2+H—OH→完成:CH3CH3CH3CH2XCH3CH2OH比较乙烯与甲烷的性质问题解决1、下列分子的所有原子在同一平面的是( )
A、CO2 B、P4 C、CH4 D、C2H4 AD 巩固练习2、下列物质能使溴的四氯化碳溶液褪色的( )
A、SO2 B、CH3CH3 C、C4H10 D、C2H4
AD 4、要获得CH3CH2Cl有两种方法,
方法一:CH3CH3和Cl2取代,
方法二:CH2=CH2和HCl加成,
讨论哪种方法好?为什么?3、用一种试剂鉴别下列一组物质,并说明现象。
乙烷 、 乙烯作业:练习册70页A部分再见
2、链烃分子里含有碳碳双键的烃称为 烯烃。
3、乙烯是最简单的烯烃。
4、不饱和烃定义:把分子里含有碳碳双键或碳碳三键,碳原子所结合的氢原子少于饱和链烃里的氢原子数,这样的烃叫做不饱和烃。
二、乙烯的性质1.氧化反应
(1)将乙烯气体点燃
化学反应方程式:
(产生黑烟是因为含碳量高,燃烧不充分;火焰明亮是碳微粒受灼热而发光) 乙烯是无色气体,稍有气味,密度是1.25 g/L,比空气略轻(分子量28),难溶于水。乙烯的物理性质:乙烯的化学性质:[活动与探究]观察并记录下列实验现象,实验事实说明乙烯有什么性质?
实验1:把乙烯气体通入酸性高锰酸钾溶液中。
实验2:把乙烯气体通溴的水溶液(即溴水)中。
可使酸性高锰酸钾褪色溴水的红棕色很快褪去可使酸性高锰酸钾褪色---
可以被强氧化剂氧化根据实验1归纳: 表现了酸性高锰酸钾的强氧化性 将乙烯气体通入溴水溶液中,可以看到溴的红棕色很快褪去,说明乙烯与溴发生反应。根据实验2归纳:有机物分子中双键(或三键)两端的碳原子与其他原子或原子团直接结合生成新的化合物的反应,叫做加成反应2、乙烯的加成反应CH2==CH2+H—H →CH2==CH2+H—X→CH2==CH2+H—OH→完成:CH3CH3CH3CH2XCH3CH2OH比较乙烯与甲烷的性质问题解决1、下列分子的所有原子在同一平面的是( )
A、CO2 B、P4 C、CH4 D、C2H4 AD 巩固练习2、下列物质能使溴的四氯化碳溶液褪色的( )
A、SO2 B、CH3CH3 C、C4H10 D、C2H4
AD 4、要获得CH3CH2Cl有两种方法,
方法一:CH3CH3和Cl2取代,
方法二:CH2=CH2和HCl加成,
讨论哪种方法好?为什么?3、用一种试剂鉴别下列一组物质,并说明现象。
乙烷 、 乙烯作业:练习册70页A部分再见
