有机化合物的结构特点
图片预览




文档简介
课件47张PPT。第二节有机化合物的结构特点 4、碳原子形成共价键时的杂化方式有:
SP3、SP2、SP 杂化。 3、多个碳原子可以相互结合成链状,也
可以结合成环状,还可以带支链。一、有机化合物中碳原子的成键特点 1、碳原子不仅可以跟其它原子形成4个共
价键,而且碳原子之间也能以共价键相结合。 2、碳原子相互之间不仅可以形成稳定的
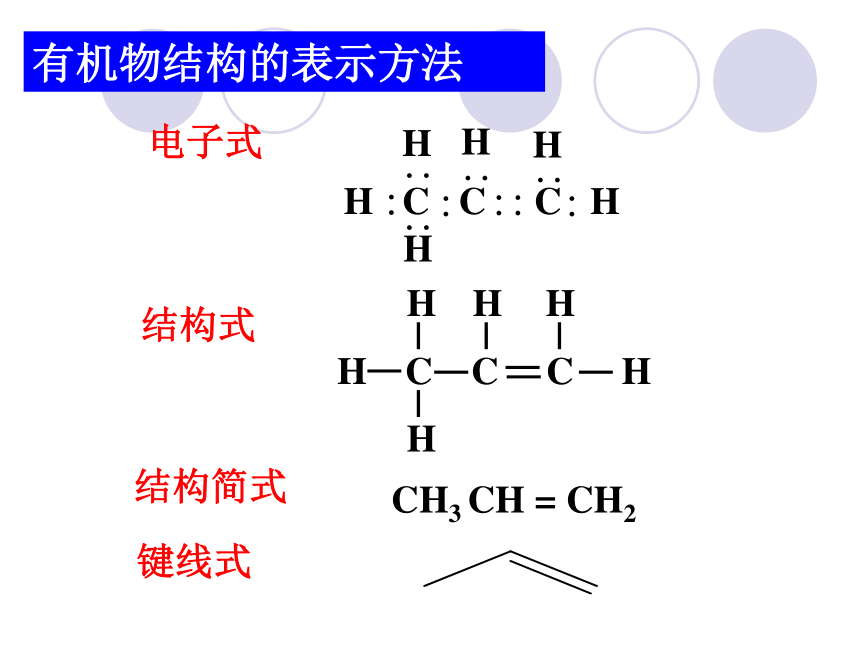
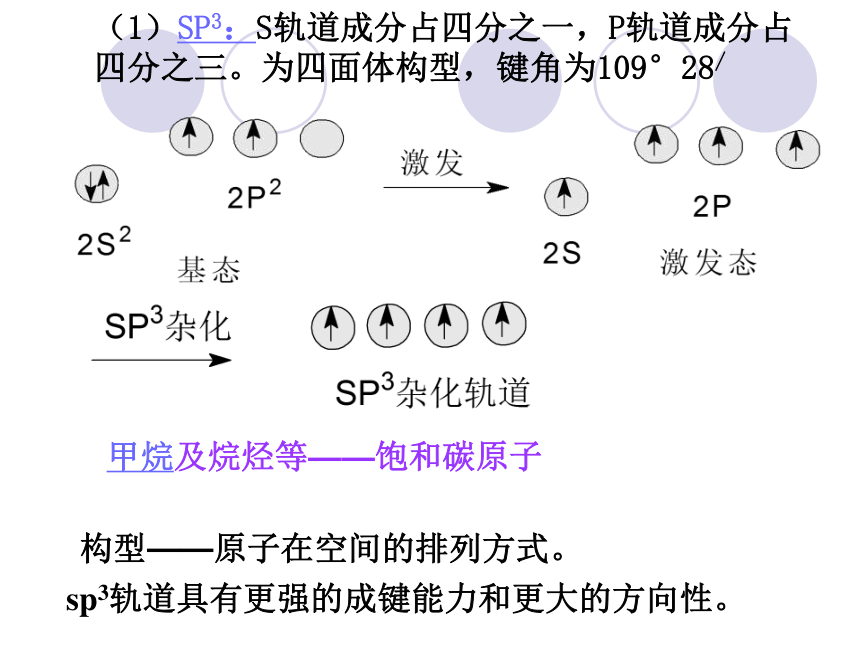
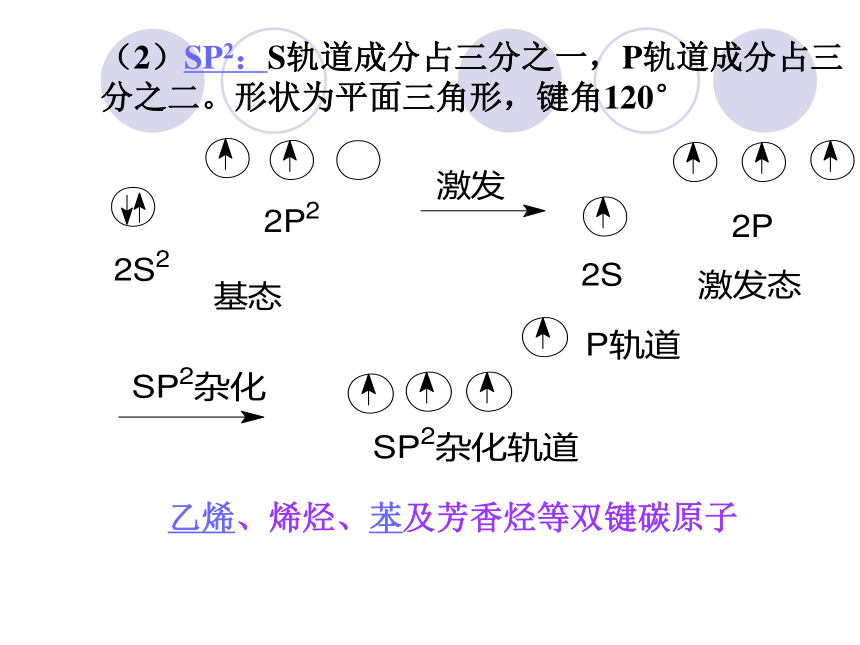
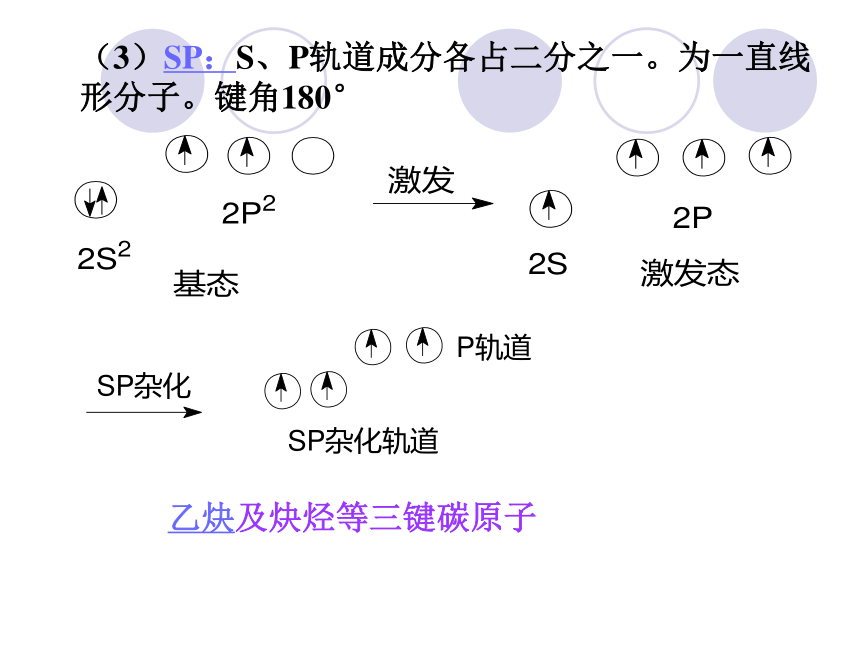
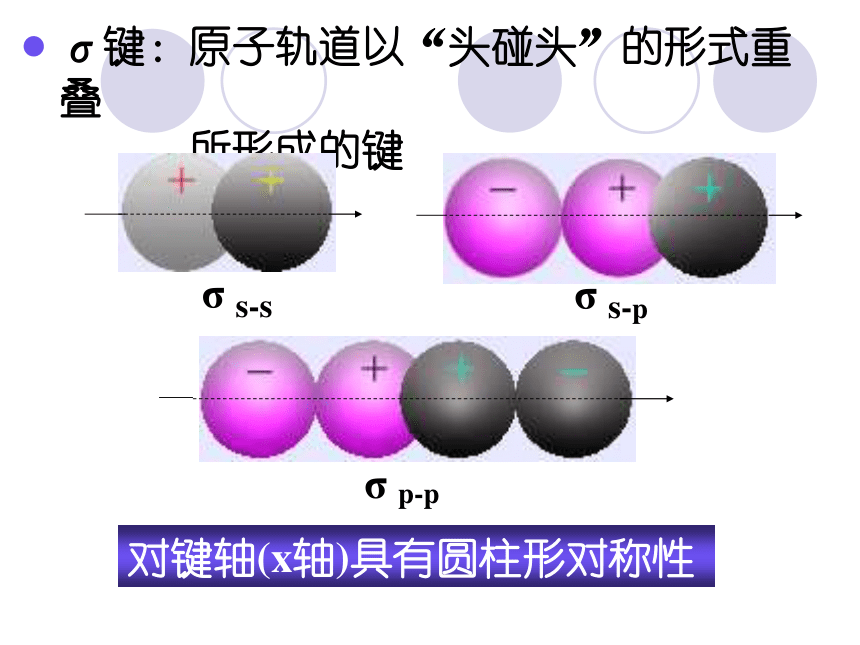
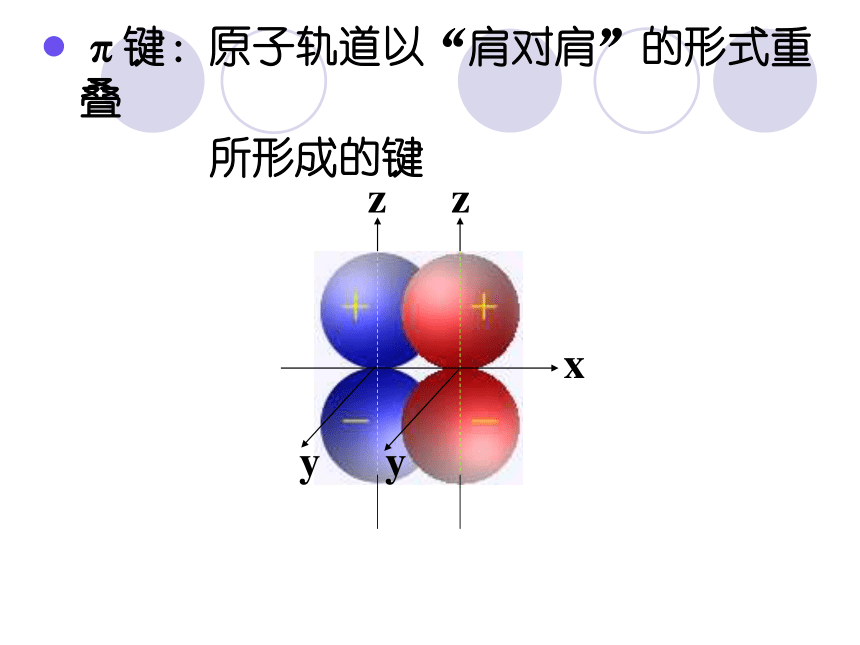
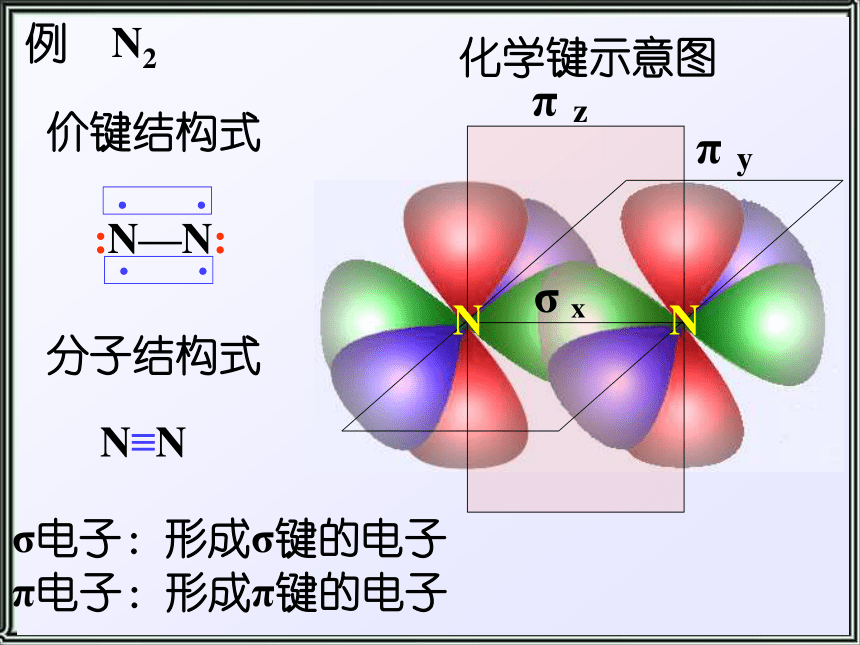
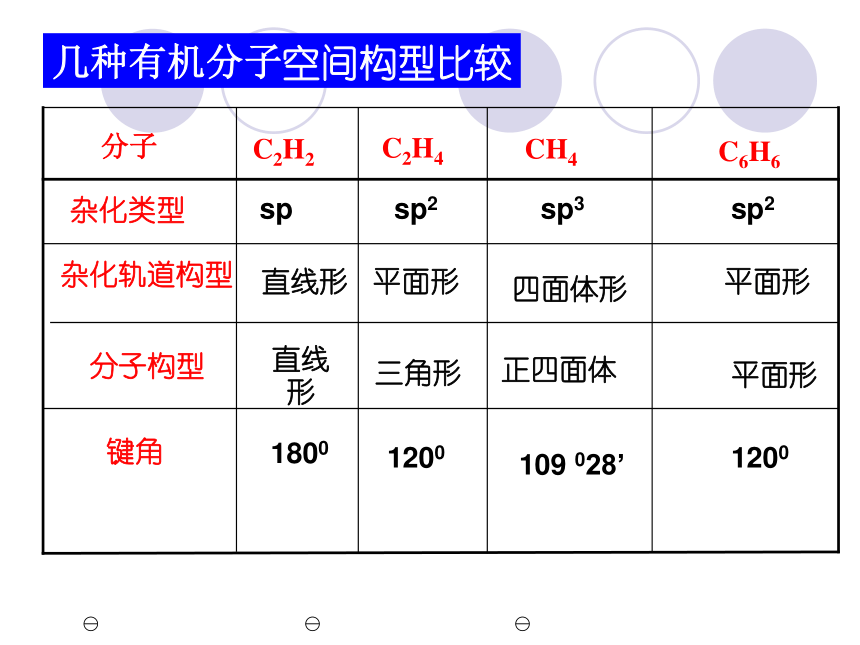
单键,还可以形成稳定的双键或三键。有机物结构的表示方法键线式资料卡片结构——分子中原子间的排列次序,原子相互间的立体位置、化学键的结合状态以及分子中电子的分布状况等各项内容的总和。分子的性质不仅取决于其元素组成,更取决于分子的结构。“结构决定性质,性质反映结构”。构造(结构)——分子中原子间相互连接的顺序叫做分子的构造。 分子式:只能反映分子中原子的种类和个数。 电子式:比较直观,但书写比较麻烦。 结构式:把电子式中的一对共用电子对用一条“-”来表示。 结构简式:把碳原子上所连接的相同原子进行合并,合并以后的个数写在该原子的右下方;省略单键。(1)SP3:S轨道成分占四分之一,P轨道成分占四分之三。为四面体构型,键角为109°28/sp3轨道具有更强的成键能力和更大的方向性。甲烷及烷烃等——饱和碳原子构型——原子在空间的排列方式。(2)SP2:S轨道成分占三分之一,P轨道成分占三分之二。形状为平面三角形,键角120°乙烯、烯烃、苯及芳香烃等双键碳原子(3)SP:S、P轨道成分各占二分之一。为一直线形分子。键角180°乙炔及炔烃等三键碳原子σ键:可以沿键轴旋转。 电子云沿键轴近似于圆柱形对称分布。 成键的两个原子可以围绕键轴旋转,而不影响电子云的分布。π键:不能沿键轴旋转。? 电子云分布在 ? 键所在平面的上下两方,呈块 状分布对键轴(x轴)具有圆柱形对称性 例 N2价键结构式N≡N分子结构式化学键示意图σ电子:形成σ键的电子π电子:形成π键的电子几种有机分子空间构型比较请同学们观察C5H12的球棍模型,完成下表。分子式 相同 C5H12结构不同36.07℃27.9℃9.5℃同分异构体二、有机化合物的同分异构现象 同分异构现象 化合物具有相同的分子式,但结构不同的现象,叫做同分异构现象。 具有同分异构现象的化合物互称为同分异构体。(一)、涵义三个相同:分子组成相同、分子式相同、
相对分子质量相同两个不同:结构不同、性质不同注意(二). 异构类型碳原子数越多,同分异构越多(以烷烃为例)1、碳链异构:分子中碳原子的结合次序不同
而引起的异构现象。2、官能团位置异构:官能团在碳链上位置的不同而引起的异构现象。
酯CnH2nCnH2n-2CnH2n+2OCnH2nOCnH2nO23、常见的官能团类别异构现象氨基酸—硝基烷等;
苯酚的同系物--芳香醇--芳香醚4、顺反异构: 由于双键不能自由旋转,而双键碳上所连接的四个原子或原子团是处在同一平面的,当双键的两个碳原子各连接两个不同的原子或原子团时,就能产生顺反异构体。 Z----顺式E-----反式产生顺反异构体的必要条件: 构成双键的任何一个碳原子上所连的两个基团要不同。乳酸的二个构型5、对映异构:对映异构:是指立体空间构型上互呈镜像对映关系的立体异构现象。就像人的左右手一样
对映异构体之间的物理性质和化学性质基本相同,只
是对平面偏振光的旋转方向(旋光性能)不
同。 练习:指出下列物质哪些属碳链异构、哪些属位置异构、哪些属官能团异构?D、CH3CH2COOH 与 CH3COOCH3F、 CH2=CH-CH=CH2 与 CH3-CH2-C≡CH官能团异构官能团异构碳链异构位置异构碳链异构官能团异构(1)最长碳链C—C—C—C—C—C—CC—C—C—C—C—CC—C—C—C—C—CC7H16的几种同分异构体CH3—CH2—CH2—CH2—CH2—CH2—CH3烷烃分子中支链数与甲基数有何关系?直链烷烃有2个甲基每增加一个支链增加1个甲基在端头脑增加1个双键减少1个甲基 【练习】 1、写出化学式C4H10O的所有可能物质的结构简式 2、 C11H16 的苯的同系物中, 只含有一个支链, 且支链上含有两个“—CH3”的结构有四种, 写出其结构简式.伯碳:与一个C原子直接相连。 仲碳:与二个C原子直接相连。 叔碳:与三个C原子直接相连。 季碳: 与四个C原子直接相连。1、碳原子分类知识扩展①同一碳原子上的氢原子是等效的。
②同一碳原子上所连接甲基上的氢原子是等效的。
③处于同一面对称位置上的氢原子是等效的。2、确定一元取代物的同分异构体的基本方法与技巧(1)等效氢 练习:写出常见一元取代物只有一种的10个碳原子以内的烷烃CH3CH3CH4例如:对称轴
CH3CH2CH2CH2CH3
① ② ③ ② ①② ① ③ ① ②
CH3-CH2-CH-CH2-CH3
① CH2
② CH3 CH3
CH3 – C – CH2- CH3
① CH3 ② ③
aabbbbaa(2)对称技巧练习:进行一氯取代后,只能生成3种沸点不同的产物的烷烃是---------------------------------( )
A、(CH3)2CHCH2CH2CH3
B、(CH3CH2)2CHCH3
C、(CH3)2CHCH(CH3)2
D、(CH3)3CCH2CH3D(3)转换技巧
例、已知化学式为C12H12的物质A的结构简式为:
A苯环上的二溴代物有9种
同分异构体,以此推断A苯
环上的四溴代 物的异构体
数目有 ( )
A.9种 B. 10种
C. 11种 D. 12种A例、式量为43的烷基取代甲苯苯环上的一个氢原子,所得芳香烃产物的数目为 ( )
A.3 B.4 C.5 D.6D— CH2— CH2—CH3— C3H7 顺反异构:下列烯烃中哪些存在顺反异构1、(CH3)2C=CH-CH32、你认为烯烃要存在顺反异构必须满足什么条件?对映异构想一想:有机物中存在什么样的碳原子才能有对映异构?指出下列有机物中具有对映异构现象的中心碳原子。资料卡片结构——分子中原子间的排列次序,原子相互间的立体位置、化学键的结合状态以及分子中电子的分布状况等各项内容的总和。分子的性质不仅取决于其元素组成,更取决于分子的结构。“结构决定性质,性质反映结构”。构造(结构)——分子中原子间相互连接的顺序叫做分子的构造。 分子式:只能反映分子中原子的种类和个数。 电子式:比较直观,但书写比较麻烦。 结构式:把电子式中的一对共用电子对用一条“-”来表示。 结构简式:把碳原子上所连接的相同原子进行合并,合并以后的个数写在该原子的右下方;省略单键。(1)SP3:S轨道成分占四分之一,P轨道成分占四分之三。为四面体构型,键角为109°28/sp3轨道具有更强的成键能力和更大的方向性。甲烷及烷烃等——饱和碳原子构型——原子在空间的排列方式。(2)SP2:S轨道成分占三分之一,P轨道成分占三分之二。形状为平面三角形,键角120°乙烯、烯烃、苯及芳香烃等双键碳原子(3)SP:S、P轨道成分各占二分之一。为一直线形分子。键角180°乙炔及炔烃等三键碳原子σ键:可以沿键轴旋转。 电子云沿键轴近似于圆柱形对称分布。 成键的两个原子可以围绕键轴旋转,而不影响电子云的分布。π键:不能沿键轴旋转。? 电子云分布在 ? 键所在平面的上下两方,呈块 状分布对键轴(x轴)具有圆柱形对称性 例 N2价键结构式N≡N分子结构式化学键示意图σ电子:形成σ键的电子π电子:形成π键的电子四、有机化合物结构与性质的关系 结构决定性质,结构中最关键的是官能团,如何预测物质性质?首先找出官能团,然后从键的极性、碳原子的饱和程度等进一步预测需要注意的是:在推测有机物的性质时还应考虑官能团与相邻基团之间的相互影响
SP3、SP2、SP 杂化。 3、多个碳原子可以相互结合成链状,也
可以结合成环状,还可以带支链。一、有机化合物中碳原子的成键特点 1、碳原子不仅可以跟其它原子形成4个共
价键,而且碳原子之间也能以共价键相结合。 2、碳原子相互之间不仅可以形成稳定的
单键,还可以形成稳定的双键或三键。有机物结构的表示方法键线式资料卡片结构——分子中原子间的排列次序,原子相互间的立体位置、化学键的结合状态以及分子中电子的分布状况等各项内容的总和。分子的性质不仅取决于其元素组成,更取决于分子的结构。“结构决定性质,性质反映结构”。构造(结构)——分子中原子间相互连接的顺序叫做分子的构造。 分子式:只能反映分子中原子的种类和个数。 电子式:比较直观,但书写比较麻烦。 结构式:把电子式中的一对共用电子对用一条“-”来表示。 结构简式:把碳原子上所连接的相同原子进行合并,合并以后的个数写在该原子的右下方;省略单键。(1)SP3:S轨道成分占四分之一,P轨道成分占四分之三。为四面体构型,键角为109°28/sp3轨道具有更强的成键能力和更大的方向性。甲烷及烷烃等——饱和碳原子构型——原子在空间的排列方式。(2)SP2:S轨道成分占三分之一,P轨道成分占三分之二。形状为平面三角形,键角120°乙烯、烯烃、苯及芳香烃等双键碳原子(3)SP:S、P轨道成分各占二分之一。为一直线形分子。键角180°乙炔及炔烃等三键碳原子σ键:可以沿键轴旋转。 电子云沿键轴近似于圆柱形对称分布。 成键的两个原子可以围绕键轴旋转,而不影响电子云的分布。π键:不能沿键轴旋转。? 电子云分布在 ? 键所在平面的上下两方,呈块 状分布对键轴(x轴)具有圆柱形对称性 例 N2价键结构式N≡N分子结构式化学键示意图σ电子:形成σ键的电子π电子:形成π键的电子几种有机分子空间构型比较请同学们观察C5H12的球棍模型,完成下表。分子式 相同 C5H12结构不同36.07℃27.9℃9.5℃同分异构体二、有机化合物的同分异构现象 同分异构现象 化合物具有相同的分子式,但结构不同的现象,叫做同分异构现象。 具有同分异构现象的化合物互称为同分异构体。(一)、涵义三个相同:分子组成相同、分子式相同、
相对分子质量相同两个不同:结构不同、性质不同注意(二). 异构类型碳原子数越多,同分异构越多(以烷烃为例)1、碳链异构:分子中碳原子的结合次序不同
而引起的异构现象。2、官能团位置异构:官能团在碳链上位置的不同而引起的异构现象。
酯CnH2nCnH2n-2CnH2n+2OCnH2nOCnH2nO23、常见的官能团类别异构现象氨基酸—硝基烷等;
苯酚的同系物--芳香醇--芳香醚4、顺反异构: 由于双键不能自由旋转,而双键碳上所连接的四个原子或原子团是处在同一平面的,当双键的两个碳原子各连接两个不同的原子或原子团时,就能产生顺反异构体。 Z----顺式E-----反式产生顺反异构体的必要条件: 构成双键的任何一个碳原子上所连的两个基团要不同。乳酸的二个构型5、对映异构:对映异构:是指立体空间构型上互呈镜像对映关系的立体异构现象。就像人的左右手一样
对映异构体之间的物理性质和化学性质基本相同,只
是对平面偏振光的旋转方向(旋光性能)不
同。 练习:指出下列物质哪些属碳链异构、哪些属位置异构、哪些属官能团异构?D、CH3CH2COOH 与 CH3COOCH3F、 CH2=CH-CH=CH2 与 CH3-CH2-C≡CH官能团异构官能团异构碳链异构位置异构碳链异构官能团异构(1)最长碳链C—C—C—C—C—C—CC—C—C—C—C—CC—C—C—C—C—CC7H16的几种同分异构体CH3—CH2—CH2—CH2—CH2—CH2—CH3烷烃分子中支链数与甲基数有何关系?直链烷烃有2个甲基每增加一个支链增加1个甲基在端头脑增加1个双键减少1个甲基 【练习】 1、写出化学式C4H10O的所有可能物质的结构简式 2、 C11H16 的苯的同系物中, 只含有一个支链, 且支链上含有两个“—CH3”的结构有四种, 写出其结构简式.伯碳:与一个C原子直接相连。 仲碳:与二个C原子直接相连。 叔碳:与三个C原子直接相连。 季碳: 与四个C原子直接相连。1、碳原子分类知识扩展①同一碳原子上的氢原子是等效的。
②同一碳原子上所连接甲基上的氢原子是等效的。
③处于同一面对称位置上的氢原子是等效的。2、确定一元取代物的同分异构体的基本方法与技巧(1)等效氢 练习:写出常见一元取代物只有一种的10个碳原子以内的烷烃CH3CH3CH4例如:对称轴
CH3CH2CH2CH2CH3
① ② ③ ② ①② ① ③ ① ②
CH3-CH2-CH-CH2-CH3
① CH2
② CH3 CH3
CH3 – C – CH2- CH3
① CH3 ② ③
aabbbbaa(2)对称技巧练习:进行一氯取代后,只能生成3种沸点不同的产物的烷烃是---------------------------------( )
A、(CH3)2CHCH2CH2CH3
B、(CH3CH2)2CHCH3
C、(CH3)2CHCH(CH3)2
D、(CH3)3CCH2CH3D(3)转换技巧
例、已知化学式为C12H12的物质A的结构简式为:
A苯环上的二溴代物有9种
同分异构体,以此推断A苯
环上的四溴代 物的异构体
数目有 ( )
A.9种 B. 10种
C. 11种 D. 12种A例、式量为43的烷基取代甲苯苯环上的一个氢原子,所得芳香烃产物的数目为 ( )
A.3 B.4 C.5 D.6D— CH2— CH2—CH3— C3H7 顺反异构:下列烯烃中哪些存在顺反异构1、(CH3)2C=CH-CH32、你认为烯烃要存在顺反异构必须满足什么条件?对映异构想一想:有机物中存在什么样的碳原子才能有对映异构?指出下列有机物中具有对映异构现象的中心碳原子。资料卡片结构——分子中原子间的排列次序,原子相互间的立体位置、化学键的结合状态以及分子中电子的分布状况等各项内容的总和。分子的性质不仅取决于其元素组成,更取决于分子的结构。“结构决定性质,性质反映结构”。构造(结构)——分子中原子间相互连接的顺序叫做分子的构造。 分子式:只能反映分子中原子的种类和个数。 电子式:比较直观,但书写比较麻烦。 结构式:把电子式中的一对共用电子对用一条“-”来表示。 结构简式:把碳原子上所连接的相同原子进行合并,合并以后的个数写在该原子的右下方;省略单键。(1)SP3:S轨道成分占四分之一,P轨道成分占四分之三。为四面体构型,键角为109°28/sp3轨道具有更强的成键能力和更大的方向性。甲烷及烷烃等——饱和碳原子构型——原子在空间的排列方式。(2)SP2:S轨道成分占三分之一,P轨道成分占三分之二。形状为平面三角形,键角120°乙烯、烯烃、苯及芳香烃等双键碳原子(3)SP:S、P轨道成分各占二分之一。为一直线形分子。键角180°乙炔及炔烃等三键碳原子σ键:可以沿键轴旋转。 电子云沿键轴近似于圆柱形对称分布。 成键的两个原子可以围绕键轴旋转,而不影响电子云的分布。π键:不能沿键轴旋转。? 电子云分布在 ? 键所在平面的上下两方,呈块 状分布对键轴(x轴)具有圆柱形对称性 例 N2价键结构式N≡N分子结构式化学键示意图σ电子:形成σ键的电子π电子:形成π键的电子四、有机化合物结构与性质的关系 结构决定性质,结构中最关键的是官能团,如何预测物质性质?首先找出官能团,然后从键的极性、碳原子的饱和程度等进一步预测需要注意的是:在推测有机物的性质时还应考虑官能团与相邻基团之间的相互影响
