氧化还原反应方程式的配平 鲁科版必修1
文档属性
| 名称 | 氧化还原反应方程式的配平 鲁科版必修1 |  | |
| 格式 | rar | ||
| 文件大小 | 378.9KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2009-08-05 12:10:00 | ||
图片预览





文档简介
课件22张PPT。
氧化还原反应方程式的配平一.氧化还原反应的定义1.一种物质被氧化同时另一种被还原的反应。⑴从特征看:有化合价升降的反应。⑵从实质看:有电子的转移的反应。练习一标出下列氧化还原反应的电子转移的
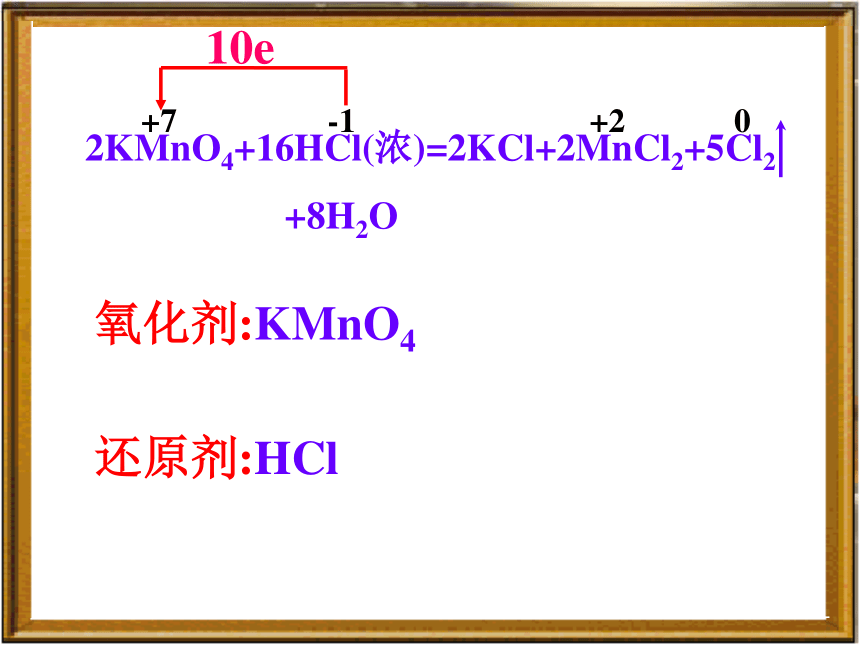
方向和数目,并指出氧化剂和还原剂:氧化剂:KMnO4
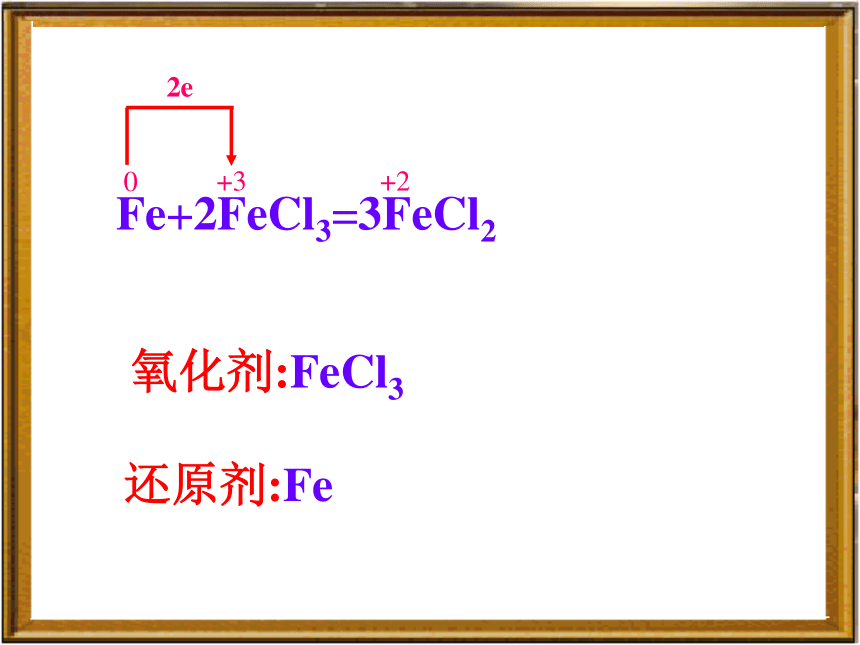
还原剂:HCl +7 -1 +2 0Fe+2FeCl3=3FeCl2氧化剂:FeCl3还原剂:Fe二 配平步骤1.标变价
2.列变化
3.求总数
4.配系数
5.细检查
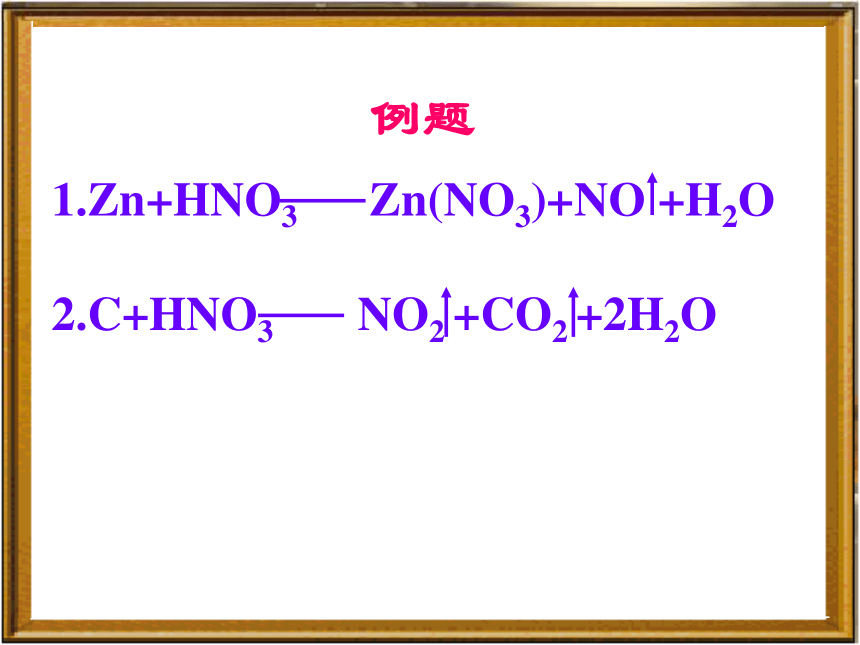
标变价标出反应前后发生改变的化合价,不变不标。0 +5 +2 +2
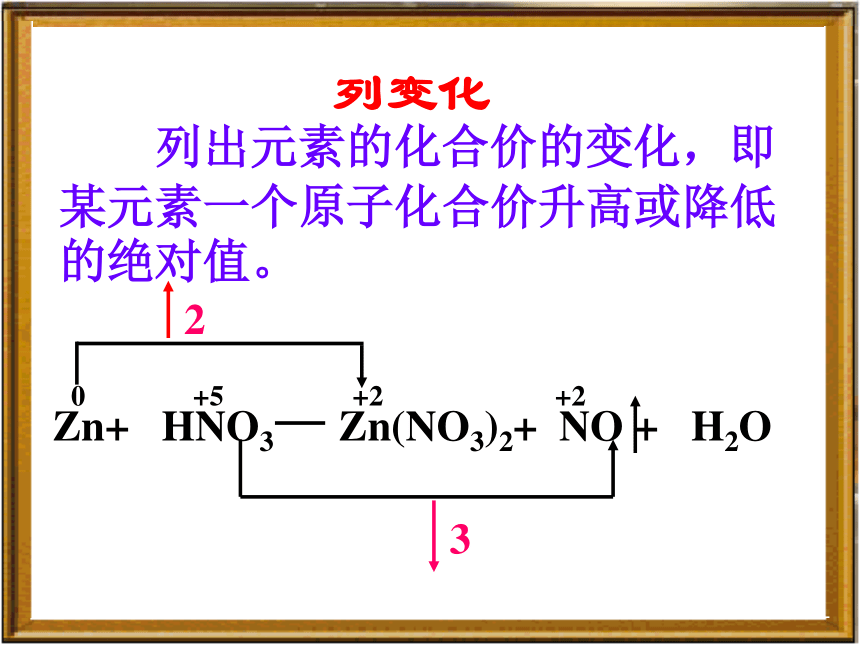
列出元素的化合价的变化,即某元素一个原子化合价升高或降低的绝对值。列变化求总数 求化合价升降的最小公倍数,使化合价升高和降低的总数相等。×3×2配系数 先配变价元素,再用观察法配平其它元素原子的系数。3 3 2 284细检查1.等号两边各种元素的原子总数是否相等。2.离子反应的电荷总数是否相等。 0 +5 +4 +4×1×4 4 42三、配平原则1. 质量守恒原则
即反应前后各元素的原子个数相等
2.电子守恒原则
反应中还原剂失去电子的总数与氧化剂得到的电子总数相等(即化合价升降总数相等)
3.电荷守恒原则
即在离子反应中,反应前后离子所带的正负电荷总数相等练习二用化合价升降法配平下列化学方程式 重点回顾依据:步骤:化合价升降总数相等1.标变价2.列变化3.求总数4.配系数5.细检查
氧化还原反应方程式的配平一.氧化还原反应的定义1.一种物质被氧化同时另一种被还原的反应。⑴从特征看:有化合价升降的反应。⑵从实质看:有电子的转移的反应。练习一标出下列氧化还原反应的电子转移的
方向和数目,并指出氧化剂和还原剂:氧化剂:KMnO4
还原剂:HCl +7 -1 +2 0Fe+2FeCl3=3FeCl2氧化剂:FeCl3还原剂:Fe二 配平步骤1.标变价
2.列变化
3.求总数
4.配系数
5.细检查
标变价标出反应前后发生改变的化合价,不变不标。0 +5 +2 +2
列出元素的化合价的变化,即某元素一个原子化合价升高或降低的绝对值。列变化求总数 求化合价升降的最小公倍数,使化合价升高和降低的总数相等。×3×2配系数 先配变价元素,再用观察法配平其它元素原子的系数。3 3 2 284细检查1.等号两边各种元素的原子总数是否相等。2.离子反应的电荷总数是否相等。 0 +5 +4 +4×1×4 4 42三、配平原则1. 质量守恒原则
即反应前后各元素的原子个数相等
2.电子守恒原则
反应中还原剂失去电子的总数与氧化剂得到的电子总数相等(即化合价升降总数相等)
3.电荷守恒原则
即在离子反应中,反应前后离子所带的正负电荷总数相等练习二用化合价升降法配平下列化学方程式 重点回顾依据:步骤:化合价升降总数相等1.标变价2.列变化3.求总数4.配系数5.细检查
