化学:第七单元 金属复习教案(鲁教版九年级)
文档属性
| 名称 | 化学:第七单元 金属复习教案(鲁教版九年级) |

|
|
| 格式 | rar | ||
| 文件大小 | 33.8KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版(五四学制) | ||
| 科目 | 化学 | ||
| 更新时间 | 2009-08-06 00:00:00 | ||
图片预览

文档简介
本资料来自于资源最齐全的21世纪教育网www.21cnjy.com
第七单元 金属
[主要内容]
1. 了解常见金属的物理性质,知道金属材料在日常生活和工农业生产中的重要用途。
2. 初步建立“混合”能改变物质性质的化学观念。知道在一种金属中熔合进一种或多种其他金属(或非金属)能得到适合人类不同需要的合金。
3. 了解重要的铁矿石和炼铁的基本原理。
4. 知道镁、铝、铁、铜等常见金属与氧气的反应,认识常见金属与盐酸、硫酸及盐溶液的置换反应,并能解释日常生活中的一些现象。能说出常见金属的活动性顺序,了解金属活动性顺序的意义。
5. 了解导致钢铁锈蚀的因素以及减缓钢铁锈蚀的办法,知道废旧金属对环境的污染,认识回收利用废旧金属对环境及金属资源保护的重要性。
二. 知识要点:
(一)常见的金属材料
1. 金属的物理性质
具有金属光泽,密度和硬度较大,熔、沸点较高,具有良好的延展性和导电、导热性能。在室温下除汞外,金属都是固体。
性质的差异决定了金属的用途不同,钨的熔点高,所以被用来制造灯泡中的灯丝,银的导电性优良,故被广泛用于电子制造业。
2. 合金
(1)概念:在金属中加热熔合某些金属或非金属,制得具有金属特征的物质。合金的强度和硬度一般比组成它们的纯金属更高,抗腐蚀性能也更好。
(2)铁的合金:
生铁:含碳量为2%~4.3%
钢:含碳量为0.03%~2%
3. 炼铁的原理
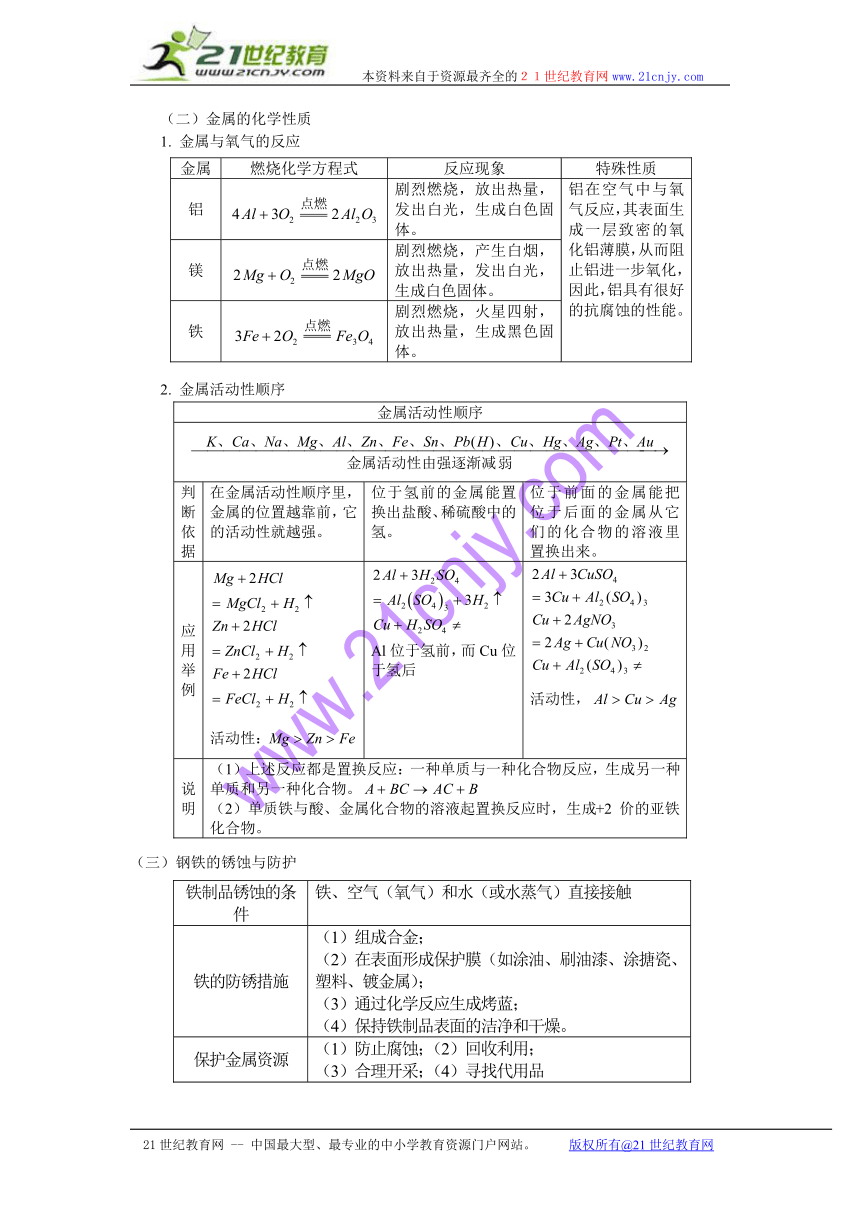
(二)金属的化学性质
1. 金属与氧气的反应
2. 金属活动性顺序
(三)钢铁的锈蚀与防护
【典型例题】
例1. 金属X、Y、Z分别是Fe、Al、Cu、Ag中的一种,其中X能与稀H2SO4反应生成X2(SO4)3,而Y、Z不能与稀H2SO4反应;Y能与AgNO3溶液反应,而Z不能与AgNO3溶液反应,则X、Y、Z依次为( )
A. Fe、Ag、Cu B. Fe、Cu、Ag
C. Al、Cu、Ag D. Al、Ag、Cu
答案:C
例2. 一般情况下,金属越活泼,与酸反应速度越快。为了探究金属Mg、Zn、Fe与酸反应的快慢,某研究性学习小组设计了如下实验(如图所示):
实验步骤:
①取A、B、C三支试管,分别加入2 mL浓度相同的盐酸溶液。
②分别加入足量的、大小相等的Mg、Zn、Fe立即把三个相同的气球分别套在各试管口上。
实验预测与分析:
(1)写出铁与盐酸反应的化学方程式:___________________________。
(2)气球膨胀速度最快的是______________。(填试管编号)
(3)该实验表明,实验室一般用锌而不选用镁、铁制取氢气的主要原因是:_______
_______________________。
(4)步骤②是实验获得成功的关键,你认为在操作过程中小组成员之间应该:________
______________________________。
答案:(1)
(2)A
(3)锌反应速度适中,容易控制
(4)分工合作,团结协作
例3. 下表是某种常见金属的部分性质:
(1)试推断该金属可能的一种用途_______________。
(2)请提出你想要探究的有关该金属化学性质的两个问题:
①____________________________________________;
②____________________________________________。
(3)请自选试剂,设计实验方案对你所提出的两个问题进行探究(简述步骤、现象及结论)。
①_______________________________________________________;
②_______________________________________________________。
答案:(1)做导线
(2)①该金属能否与稀盐酸反应 ②该金属能否与硫酸铜溶液反应
(3)①取少量该金属于试管中,滴入少量稀盐酸,若有气泡产生,则该金属能与稀盐酸反应。
②取少量该金属于试管中,滴入少量硫酸铜溶液,若该金属表面出现红色固体物质,则该金属能与硫酸铜溶液反应。
例4. 将一包含有杂质的铁粉样品分成质量相等的两份(杂质不溶于水,且不参与反应)。若向其中一份中加入足量的稀硫酸,充分反应后得到0.2g不溶物;若向另一份中加入足量的氯化铜溶液,充分反应后得到1.8g不溶物。求该铁粉样品中铁的质量分数。
解:设一份铁粉中含铁的质量为x
铁与氯化铜反应后生成Cu的质量为:
样品中铁的质量分数为:
答:该铁粉样品中铁的质量分数为87.5%。
21世纪教育网 -- 中国最大型、最专业的中小学教育资源门户网站。 版权所有@21世纪教育网
第七单元 金属
[主要内容]
1. 了解常见金属的物理性质,知道金属材料在日常生活和工农业生产中的重要用途。
2. 初步建立“混合”能改变物质性质的化学观念。知道在一种金属中熔合进一种或多种其他金属(或非金属)能得到适合人类不同需要的合金。
3. 了解重要的铁矿石和炼铁的基本原理。
4. 知道镁、铝、铁、铜等常见金属与氧气的反应,认识常见金属与盐酸、硫酸及盐溶液的置换反应,并能解释日常生活中的一些现象。能说出常见金属的活动性顺序,了解金属活动性顺序的意义。
5. 了解导致钢铁锈蚀的因素以及减缓钢铁锈蚀的办法,知道废旧金属对环境的污染,认识回收利用废旧金属对环境及金属资源保护的重要性。
二. 知识要点:
(一)常见的金属材料
1. 金属的物理性质
具有金属光泽,密度和硬度较大,熔、沸点较高,具有良好的延展性和导电、导热性能。在室温下除汞外,金属都是固体。
性质的差异决定了金属的用途不同,钨的熔点高,所以被用来制造灯泡中的灯丝,银的导电性优良,故被广泛用于电子制造业。
2. 合金
(1)概念:在金属中加热熔合某些金属或非金属,制得具有金属特征的物质。合金的强度和硬度一般比组成它们的纯金属更高,抗腐蚀性能也更好。
(2)铁的合金:
生铁:含碳量为2%~4.3%
钢:含碳量为0.03%~2%
3. 炼铁的原理
(二)金属的化学性质
1. 金属与氧气的反应
2. 金属活动性顺序
(三)钢铁的锈蚀与防护
【典型例题】
例1. 金属X、Y、Z分别是Fe、Al、Cu、Ag中的一种,其中X能与稀H2SO4反应生成X2(SO4)3,而Y、Z不能与稀H2SO4反应;Y能与AgNO3溶液反应,而Z不能与AgNO3溶液反应,则X、Y、Z依次为( )
A. Fe、Ag、Cu B. Fe、Cu、Ag
C. Al、Cu、Ag D. Al、Ag、Cu
答案:C
例2. 一般情况下,金属越活泼,与酸反应速度越快。为了探究金属Mg、Zn、Fe与酸反应的快慢,某研究性学习小组设计了如下实验(如图所示):
实验步骤:
①取A、B、C三支试管,分别加入2 mL浓度相同的盐酸溶液。
②分别加入足量的、大小相等的Mg、Zn、Fe立即把三个相同的气球分别套在各试管口上。
实验预测与分析:
(1)写出铁与盐酸反应的化学方程式:___________________________。
(2)气球膨胀速度最快的是______________。(填试管编号)
(3)该实验表明,实验室一般用锌而不选用镁、铁制取氢气的主要原因是:_______
_______________________。
(4)步骤②是实验获得成功的关键,你认为在操作过程中小组成员之间应该:________
______________________________。
答案:(1)
(2)A
(3)锌反应速度适中,容易控制
(4)分工合作,团结协作
例3. 下表是某种常见金属的部分性质:
(1)试推断该金属可能的一种用途_______________。
(2)请提出你想要探究的有关该金属化学性质的两个问题:
①____________________________________________;
②____________________________________________。
(3)请自选试剂,设计实验方案对你所提出的两个问题进行探究(简述步骤、现象及结论)。
①_______________________________________________________;
②_______________________________________________________。
答案:(1)做导线
(2)①该金属能否与稀盐酸反应 ②该金属能否与硫酸铜溶液反应
(3)①取少量该金属于试管中,滴入少量稀盐酸,若有气泡产生,则该金属能与稀盐酸反应。
②取少量该金属于试管中,滴入少量硫酸铜溶液,若该金属表面出现红色固体物质,则该金属能与硫酸铜溶液反应。
例4. 将一包含有杂质的铁粉样品分成质量相等的两份(杂质不溶于水,且不参与反应)。若向其中一份中加入足量的稀硫酸,充分反应后得到0.2g不溶物;若向另一份中加入足量的氯化铜溶液,充分反应后得到1.8g不溶物。求该铁粉样品中铁的质量分数。
解:设一份铁粉中含铁的质量为x
铁与氯化铜反应后生成Cu的质量为:
样品中铁的质量分数为:
答:该铁粉样品中铁的质量分数为87.5%。
21世纪教育网 -- 中国最大型、最专业的中小学教育资源门户网站。 版权所有@21世纪教育网
同课章节目录
- 第一单元 溶液
- 1 溶液的形成
- 2 溶液组成的定量表示
- 3物质的溶解性
- 到实验室去:配制一定溶质质量分数的溶液
- 第二单元 常见的酸和碱
- 1 酸及其性质
- 2 碱及其性质
- 3 溶液的酸碱性
- 4 酸碱中和反应
- 到实验室去:探究酸和碱的化学性质
- 到图书馆去:分子变成离子
- 第三单元 海水中的化学
- 1 海洋化学资源
- 2 海水“晒盐”
- 3 海水“制碱”
- 到实验室去:粗盐中难溶性杂质的去除
- 第四单元 金属
- 1 常见的金属材料
- 2 金属的化学性质
- 3 钢铁的锈蚀与防护
- 到实验室去:探究金属的性质
- 第五单元 化学与健康
- 1 食物中的有机物
- 2 化学元素与人体健康
- 3 远离有毒物质
- 第六单元 化学与社会发展
- 1 化学与能源开发
- 2 化学与材料研制
- 3 化学与农业生产
- 4 化学与环境保护
