第二节 化学计量在化学实验中的应用(2)
文档属性
| 名称 | 第二节 化学计量在化学实验中的应用(2) |

|
|
| 格式 | rar | ||
| 文件大小 | 167.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2009-08-08 00:00:00 | ||
图片预览







文档简介
课件74张PPT。主讲教师:周晓练气体摩尔体积第二节 化学计量在实验中的应用湖南省长沙市一中卫星远程学校1.判断下列说法是否正确
① 物质的量就是物质的质量
② 摩尔为7个基本物理量之一
③ 阿伏加德罗常数是物质的量的单位
④ 摩尔数为4的氢原子课前提问:2. 下列表示不正确的是______ ,错在何处?课前提问:① 3 mol H2SO4 中约有 个H2SO4
分子,溶于水后可以电离出 mol H+。
② 64g O2含有 mol O原子, mol质子。3. 填空课前提问:4. SO2 和 SO3的物质的量相同,下列结论中错误的是
A. 它们的分子数之比为 1 :1
B. 它们所含氧原子数目之比为 2 :3
C. 它们的质量之比为 1 :1
D. 它们所含原子数目之比为 3 :4课前提问:4. SO2 和 SO3的物质的量相同,下列结论中错误的是
A. 它们的分子数之比为 1 :1
B. 它们所含氧原子数目之比为 2 :3
C. 它们的质量之比为 1 :1
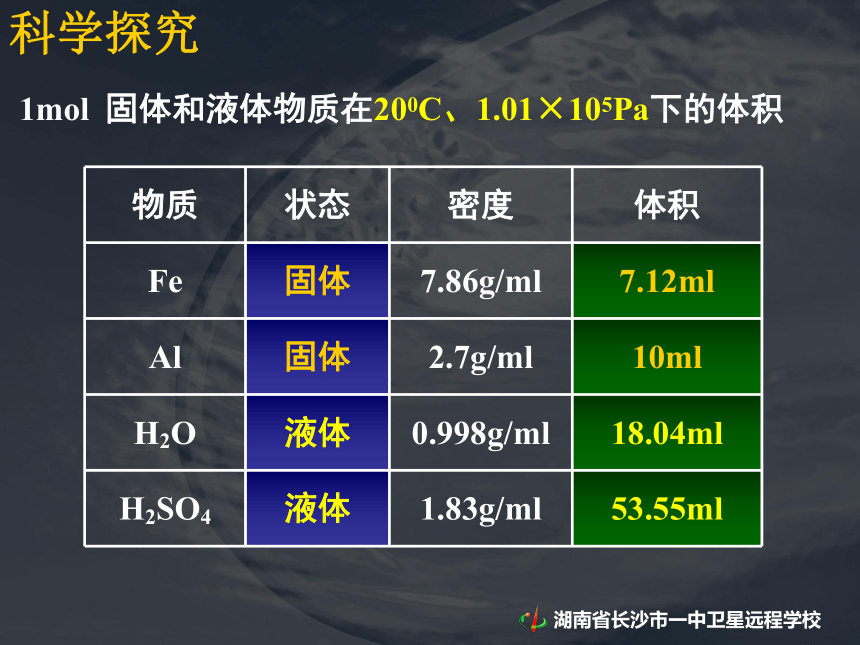
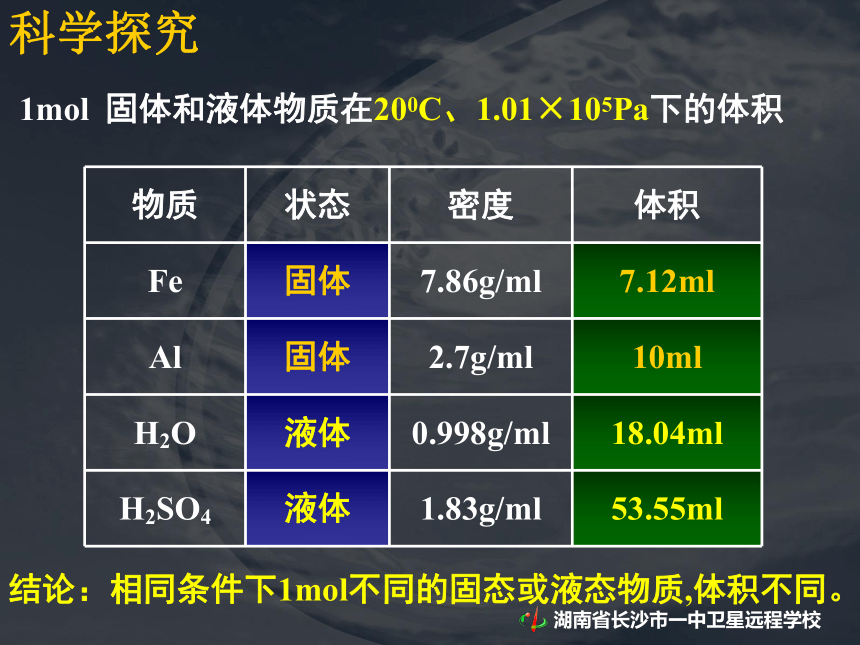
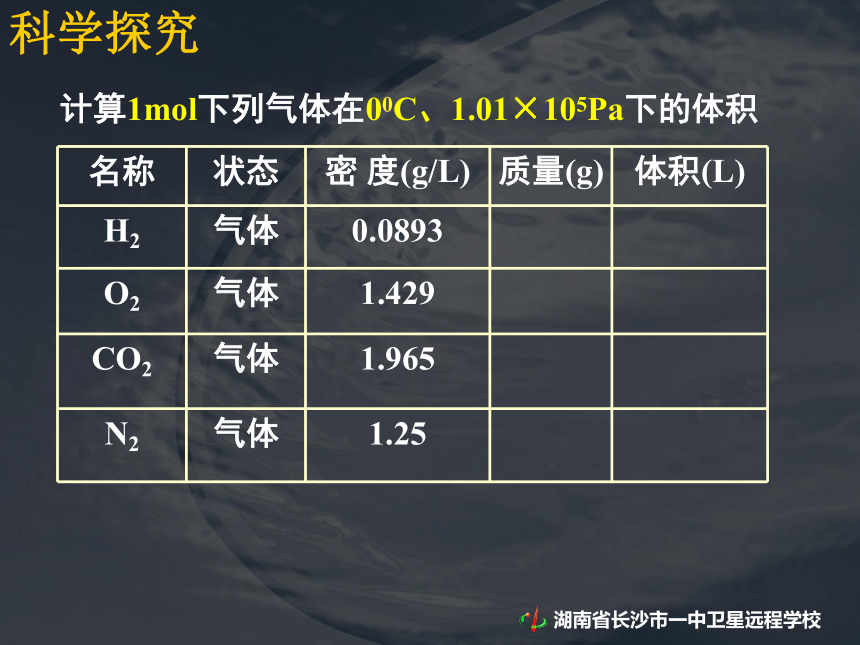
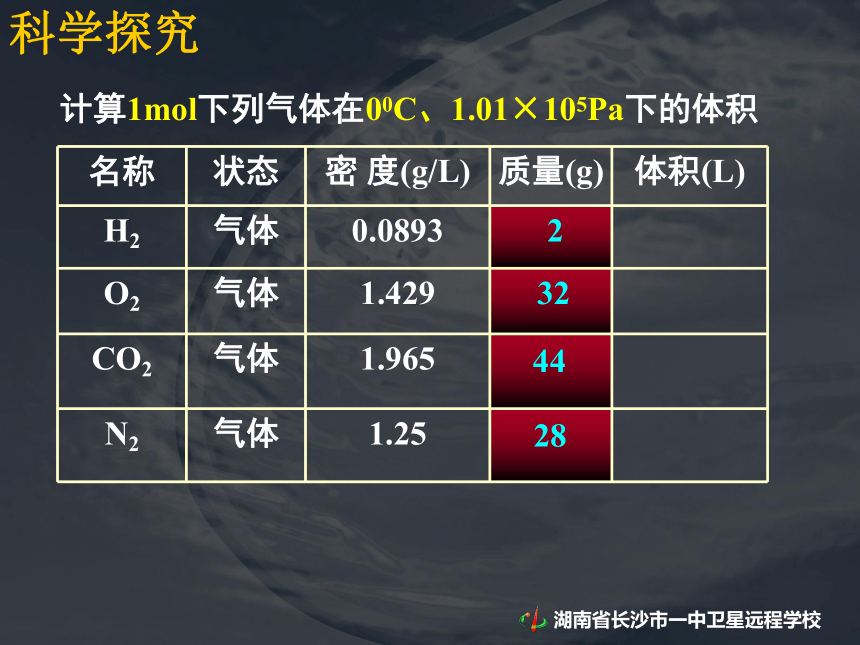
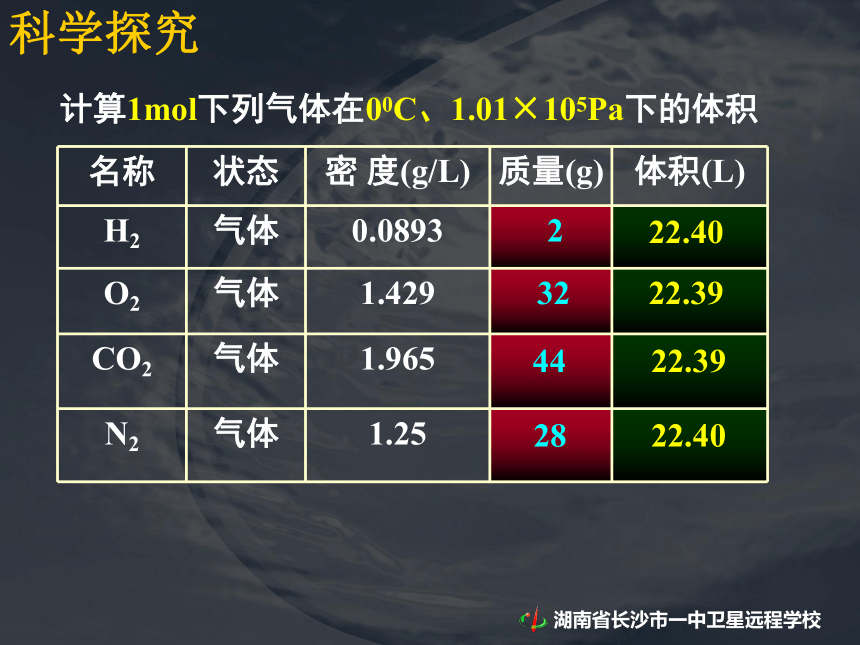
D. 它们所含原子数目之比为 3 :4√课前提问:1mol 固体和液体物质在200C、1.01×105Pa下的体积科学探究1mol 固体和液体物质在200C、1.01×105Pa下的体积科学探究1mol 固体和液体物质在200C、1.01×105Pa下的体积科学探究结论:相同条件下1mol不同的固态或液态物质,体积不同。科学探究计算1mol下列气体在00C、1.01×105Pa下的体积科学探究计算1mol下列气体在00C、1.01×105Pa下的体积2324428科学探究计算1mol下列气体在00C、1.01×105Pa下的体积232442822.4022.3922.3922.40科学探究计算1mol下列气体在00C、1.01×105Pa下的体积232442822.4022.3922.3922.40结论:相同状态下,1mol气体的体积基本相同 [思考]不同状态的物质
的体积大小跟哪些因素
有关? [思考]不同状态的物质
的体积大小跟哪些因素
有关? 例:大家去操场上体育课,需要排
队站在操场上,整个班级的同学
所占据的面积和哪些因素有关?一、影响物质体积的因素固体气体液体一、影响物质体积的因素固体气体液体微粒的数目一、影响物质体积的因素固体气体液体微粒的数目--- 物质的量(n)一、影响物质体积的因素固体气体液体微粒的数目--- 物质的量(n)微粒自身大小一、影响物质体积的因素固体气体液体微粒的数目微粒的数目--- 物质的量(n)微粒自身大小一、影响物质体积的因素固体气体液体微粒的数目微粒的数目--- 物质的量(n)--- 物质的量(n)微粒自身大小一、影响物质体积的因素固体气体液体微粒的数目微粒的数目微粒间距离--- 物质的量(n)--- 物质的量(n)微粒自身大小一、影响物质体积的因素固体气体液体微粒的数目微粒的数目微粒间距离--- 物质的量(n)--- 物质的量(n)微粒自身大小外界条件一、影响物质体积的因素固体气体液体微粒的数目微粒的数目微粒间距离--- 物质的量(n)--- 物质的量(n)微粒自身大小外界条件与气体
种类无关不同气体在一定温度和压强下,分
子间的距离可以看作是相等的,所
以1mol任何气体的体积基本相同。
这里我们就引入了气体摩尔体积。
不同气体在一定温度和压强下,分
子间的距离可以看作是相等的,所
以1mol任何气体的体积基本相同。
这里我们就引入了气体摩尔体积。
结论:相同条件下,1mol 气体的体
积主要决定于分子间的距离。二、气体摩尔体积(Vm)二、气体摩尔体积(Vm)单位物质的量(1 mol)的气体所占的体积1.定义:二、气体摩尔体积(Vm)单位物质的量(1 mol)的气体所占的体积1.定义:2.单位:L/mol (L·mol -1)二、气体摩尔体积(Vm)单位物质的量(1 mol)的气体所占的体积1.定义:2.单位:L/mol (L·mol -1)3.数值:当温度和压强相同的时候,气体摩尔
体积相同。二、气体摩尔体积(Vm)单位物质的量(1 mol)的气体所占的体积1.定义:2.单位:L/mol (L·mol -1)3.数值:当温度和压强相同的时候,气体摩尔
体积相同。可是单一气体,也可是混合气体二、气体摩尔体积(Vm)单位物质的量(1 mol)的气体所占的体积1.定义:2.单位:L/mol (L·mol -1)3.数值:当温度和压强相同的时候,气体摩尔
体积相同。如: 标准状况下,气体摩尔体积是22.4L/mol 。可是单一气体,也可是混合气体4. 气体体积与物质的量的换算4. 气体体积与物质的量的换算V=n×Vm4. 气体体积与物质的量的换算V=n×Vm例:64克氧气中含有多少个O2分子,
其在标准状况下的体积为多少升?
相同条件下与其体积相同的H2的
质量是多少?在20℃, 101KPa的条件下电解水一段时间后,
收集到的H2、O2体积如下表,实验还测得该条件
下两种气体的密度,请填写空格:1.33270.083924.0148.04在20℃, 101KPa的条件下电解水一段时间后,
收集到的H2、O2体积如下表,实验还测得该条件
下两种气体的密度,请填写空格:1.33270.083924.0148.04相同条件下,气体的体积比等于它们物质的量
之比。结论:在20℃, 101KPa的条件下电解水一段时间后,
收集到的H2、O2体积如下表,实验还测得该条件
下两种气体的密度,请填写空格:1.33270.083924.0148.04三、阿伏加德罗定律三、阿伏加德罗定律在相同的温度和压强下,相同体积的任何
气体都含相同数目的分子。三、阿伏加德罗定律在同温同压下:在相同的温度和压强下,相同体积的任何
气体都含相同数目的分子。课堂小结物质的量(n)单位:摩尔(mol)气体体积(V)、质量(m)和微粒数(N)
之间的转化关系气体的体积(V)课堂小结物质的量(n)单位:摩尔(mol)单位:升(L)气体体积(V)、质量(m)和微粒数(N)
之间的转化关系气体的体积(V)×Vm课堂小结物质的量(n)单位:摩尔(mol)单位:升(L)气体体积(V)、质量(m)和微粒数(N)
之间的转化关系气体的体积(V)×Vm÷ Vm课堂小结物质的量(n)单位:摩尔(mol)单位:升(L)气体体积(V)、质量(m)和微粒数(N)
之间的转化关系气体的体积(V)×Vm÷ Vm课堂小结物质的量(n)单位:摩尔(mol)质量(m)单位:克(g)单位:升(L)气体体积(V)、质量(m)和微粒数(N)
之间的转化关系气体的体积(V)×Vm÷ Vm课堂小结物质的量(n)单位:摩尔(mol)质量(m)单位:克(g)× M单位:升(L)气体体积(V)、质量(m)和微粒数(N)
之间的转化关系气体的体积(V)×Vm÷ Vm课堂小结物质的量(n)单位:摩尔(mol)质量(m)单位:克(g)× M÷M单位:升(L)气体体积(V)、质量(m)和微粒数(N)
之间的转化关系气体的体积(V)×Vm÷ Vm课堂小结物质的量(n)单位:摩尔(mol)质量(m)单位:克(g)微粒数(N)单位:(个)× M÷M单位:升(L)气体体积(V)、质量(m)和微粒数(N)
之间的转化关系气体的体积(V)×Vm÷ Vm课堂小结物质的量(n)单位:摩尔(mol)质量(m)单位:克(g)微粒数(N)单位:(个)× NA× M÷M单位:升(L)气体体积(V)、质量(m)和微粒数(N)
之间的转化关系气体的体积(V)×Vm÷ Vm课堂小结物质的量(n)单位:摩尔(mol)质量(m)单位:克(g)微粒数(N)单位:(个)× NA× M÷M÷NA单位:升(L)气体体积(V)、质量(m)和微粒数(N)
之间的转化关系气体的体积(V)×Vm÷ Vm课堂小结物质的量(n)单位:摩尔(mol)质量(m)单位:克(g)微粒数(N)单位:(个)× NA× M÷M÷NA单位:升(L)气体体积(V)、质量(m)和微粒数(N)
之间的转化关系物质的量是联系的纽带,沟通的桥梁1. 下列说法正确的是( )
(A)在标准状况下,1mol水和1molH2的
体积都约是22.4L
(B)2gH2和44gCO2的体积相等
(C)1mol某气体的体积为22.4L,则该气体
一定处于标准状况
(D)在标准状况下,1gH2和11.2LO2的物质
的量相等
(E)标准状况下,1molO2和N2混合气体的
体积约为22.4L课堂练习:1. 下列说法正确的是( )
(A)在标准状况下,1mol水和1molH2的
体积都约是22.4L
(B)2gH2和44gCO2的体积相等
(C)1mol某气体的体积为22.4L,则该气体
一定处于标准状况
(D)在标准状况下,1gH2和11.2LO2的物质
的量相等
(E)标准状况下,1molO2和N2混合气体的
体积约为22.4L[答案] D、E 课堂练习:2. 标准状况下, 112 mL 某气体的质量为 0.14 g , 则其摩尔质量为 ,相对分子质量为 。2. 标准状况下, 112 mL 某气体的质量为 0.14 g , 则其摩尔质量为 ,相对分子质量为 。n =VVm解:2. 标准状况下, 112 mL 某气体的质量为 0.14 g , 则其摩尔质量为 ,相对分子质量为 。n =VVm解:=0 . 112 L22 . 4 L · mol -1 2. 标准状况下, 112 mL 某气体的质量为 0.14 g , 则其摩尔质量为 ,相对分子质量为 。n =VVm解:=0 . 112 L22 . 4 L · mol -1 = 0 . 005 mol 2. 标准状况下, 112 mL 某气体的质量为 0.14 g , 则其摩尔质量为 ,相对分子质量为 。n =VVm解:=0 . 112 L22 . 4 L · mol -1 = 0 . 005 mol n = m / M2. 标准状况下, 112 mL 某气体的质量为 0.14 g , 则其摩尔质量为 ,相对分子质量为 。n =VVm解:=0 . 112 L22 . 4 L · mol -1 = 0 . 005 mol n = m / MM = 0 . 14 g0 . 005 mol 2. 标准状况下, 112 mL 某气体的质量为 0.14 g , 则其摩尔质量为 ,相对分子质量为 。n =VVm解:=0 . 112 L22 . 4 L · mol -1 = 0 . 005 mol n = m / MM = 0 . 14 g0 . 005 mol = 28 g / mol3. 同温同压下,质量相同的N2、CO2、Cl2、
CH4、O 2五种气体所占的体积由大到小的顺序是( )3. 同温同压下,质量相同的N2、CO2、Cl2、
CH4、O 2五种气体所占的体积由大到小的顺序是( )CH4、N2、O2、CO2、Cl23. 同温同压下,质量相同的N2、CO2、Cl2、
CH4、O 2五种气体所占的体积由大到小的顺序是( )CH4、N2、O2、CO2、Cl2求气体
体积的大小3. 同温同压下,质量相同的N2、CO2、Cl2、
CH4、O 2五种气体所占的体积由大到小的顺序是( )CH4、N2、O2、CO2、Cl2求气体
体积的大小求物质的量
大小3. 同温同压下,质量相同的N2、CO2、Cl2、
CH4、O 2五种气体所占的体积由大到小的顺序是( )CH4、N2、O2、CO2、Cl2求气体
体积的大小求物质的量
大小质量相同看
摩尔质量3. 同温同压下,质量相同的N2、CO2、Cl2、
CH4、O 2五种气体所占的体积由大到小的顺序是( )CH4、N2、O2、CO2、Cl2求气体
体积的大小求物质的量
大小质量相同看
摩尔质量等质量的物质其摩尔质量越小,其物质的量越大3. 同温同压下,质量相同的N2、CO2、Cl2、
CH4、O 2五种气体所占的体积由大到小的顺序是( )CH4、N2、O2、CO2、Cl2求气体
体积的大小求物质的量
大小质量相同看
摩尔质量等质量的物质其摩尔质量越小,其物质的量越大等物质的量的以上气体,质量由大到小的顺序是什么?3. 同温同压下,质量相同的N2、CO2、Cl2、
CH4、O 2五种气体所占的体积由大到小的顺序是( )CH4、N2、O2、CO2、Cl2求气体
体积的大小求物质的量
大小质量相同看
摩尔质量等质量的物质其摩尔质量越小,其物质的量越大等物质的量的以上气体,质量由大到小的顺序是什么?相同物质的量的物质,摩尔质量越大质量越大1. 在标准状况下, 6.72升甲烷
和CO的混和气体的质量为6克,
该混和气体中有 mol的
甲烷, 克的CO。拓展提高1. 在标准状况下, 6.72升甲烷
和CO的混和气体的质量为6克,
该混和气体中有 mol的
甲烷, 克的CO。拓展提高0.21. 在标准状况下, 6.72升甲烷
和CO的混和气体的质量为6克,
该混和气体中有 mol的
甲烷, 克的CO。拓展提高0.22.82.(多选)下列两种气体的分子数一定相等的是( )
A. 质量相等、密度不等的N2和C2H4
B. 等体积等密度的CO和C2H4
C. 等温等体积的O2和N2
D. 等压等体积的N2和CO22.(多选)下列两种气体的分子数一定相等的是( )
A. 质量相等、密度不等的N2和C2H4
B. 等体积等密度的CO和C2H4
C. 等温等体积的O2和N2
D. 等压等体积的N2和CO2A B
① 物质的量就是物质的质量
② 摩尔为7个基本物理量之一
③ 阿伏加德罗常数是物质的量的单位
④ 摩尔数为4的氢原子课前提问:2. 下列表示不正确的是______ ,错在何处?课前提问:① 3 mol H2SO4 中约有 个H2SO4
分子,溶于水后可以电离出 mol H+。
② 64g O2含有 mol O原子, mol质子。3. 填空课前提问:4. SO2 和 SO3的物质的量相同,下列结论中错误的是
A. 它们的分子数之比为 1 :1
B. 它们所含氧原子数目之比为 2 :3
C. 它们的质量之比为 1 :1
D. 它们所含原子数目之比为 3 :4课前提问:4. SO2 和 SO3的物质的量相同,下列结论中错误的是
A. 它们的分子数之比为 1 :1
B. 它们所含氧原子数目之比为 2 :3
C. 它们的质量之比为 1 :1
D. 它们所含原子数目之比为 3 :4√课前提问:1mol 固体和液体物质在200C、1.01×105Pa下的体积科学探究1mol 固体和液体物质在200C、1.01×105Pa下的体积科学探究1mol 固体和液体物质在200C、1.01×105Pa下的体积科学探究结论:相同条件下1mol不同的固态或液态物质,体积不同。科学探究计算1mol下列气体在00C、1.01×105Pa下的体积科学探究计算1mol下列气体在00C、1.01×105Pa下的体积2324428科学探究计算1mol下列气体在00C、1.01×105Pa下的体积232442822.4022.3922.3922.40科学探究计算1mol下列气体在00C、1.01×105Pa下的体积232442822.4022.3922.3922.40结论:相同状态下,1mol气体的体积基本相同 [思考]不同状态的物质
的体积大小跟哪些因素
有关? [思考]不同状态的物质
的体积大小跟哪些因素
有关? 例:大家去操场上体育课,需要排
队站在操场上,整个班级的同学
所占据的面积和哪些因素有关?一、影响物质体积的因素固体气体液体一、影响物质体积的因素固体气体液体微粒的数目一、影响物质体积的因素固体气体液体微粒的数目--- 物质的量(n)一、影响物质体积的因素固体气体液体微粒的数目--- 物质的量(n)微粒自身大小一、影响物质体积的因素固体气体液体微粒的数目微粒的数目--- 物质的量(n)微粒自身大小一、影响物质体积的因素固体气体液体微粒的数目微粒的数目--- 物质的量(n)--- 物质的量(n)微粒自身大小一、影响物质体积的因素固体气体液体微粒的数目微粒的数目微粒间距离--- 物质的量(n)--- 物质的量(n)微粒自身大小一、影响物质体积的因素固体气体液体微粒的数目微粒的数目微粒间距离--- 物质的量(n)--- 物质的量(n)微粒自身大小外界条件一、影响物质体积的因素固体气体液体微粒的数目微粒的数目微粒间距离--- 物质的量(n)--- 物质的量(n)微粒自身大小外界条件与气体
种类无关不同气体在一定温度和压强下,分
子间的距离可以看作是相等的,所
以1mol任何气体的体积基本相同。
这里我们就引入了气体摩尔体积。
不同气体在一定温度和压强下,分
子间的距离可以看作是相等的,所
以1mol任何气体的体积基本相同。
这里我们就引入了气体摩尔体积。
结论:相同条件下,1mol 气体的体
积主要决定于分子间的距离。二、气体摩尔体积(Vm)二、气体摩尔体积(Vm)单位物质的量(1 mol)的气体所占的体积1.定义:二、气体摩尔体积(Vm)单位物质的量(1 mol)的气体所占的体积1.定义:2.单位:L/mol (L·mol -1)二、气体摩尔体积(Vm)单位物质的量(1 mol)的气体所占的体积1.定义:2.单位:L/mol (L·mol -1)3.数值:当温度和压强相同的时候,气体摩尔
体积相同。二、气体摩尔体积(Vm)单位物质的量(1 mol)的气体所占的体积1.定义:2.单位:L/mol (L·mol -1)3.数值:当温度和压强相同的时候,气体摩尔
体积相同。可是单一气体,也可是混合气体二、气体摩尔体积(Vm)单位物质的量(1 mol)的气体所占的体积1.定义:2.单位:L/mol (L·mol -1)3.数值:当温度和压强相同的时候,气体摩尔
体积相同。如: 标准状况下,气体摩尔体积是22.4L/mol 。可是单一气体,也可是混合气体4. 气体体积与物质的量的换算4. 气体体积与物质的量的换算V=n×Vm4. 气体体积与物质的量的换算V=n×Vm例:64克氧气中含有多少个O2分子,
其在标准状况下的体积为多少升?
相同条件下与其体积相同的H2的
质量是多少?在20℃, 101KPa的条件下电解水一段时间后,
收集到的H2、O2体积如下表,实验还测得该条件
下两种气体的密度,请填写空格:1.33270.083924.0148.04在20℃, 101KPa的条件下电解水一段时间后,
收集到的H2、O2体积如下表,实验还测得该条件
下两种气体的密度,请填写空格:1.33270.083924.0148.04相同条件下,气体的体积比等于它们物质的量
之比。结论:在20℃, 101KPa的条件下电解水一段时间后,
收集到的H2、O2体积如下表,实验还测得该条件
下两种气体的密度,请填写空格:1.33270.083924.0148.04三、阿伏加德罗定律三、阿伏加德罗定律在相同的温度和压强下,相同体积的任何
气体都含相同数目的分子。三、阿伏加德罗定律在同温同压下:在相同的温度和压强下,相同体积的任何
气体都含相同数目的分子。课堂小结物质的量(n)单位:摩尔(mol)气体体积(V)、质量(m)和微粒数(N)
之间的转化关系气体的体积(V)课堂小结物质的量(n)单位:摩尔(mol)单位:升(L)气体体积(V)、质量(m)和微粒数(N)
之间的转化关系气体的体积(V)×Vm课堂小结物质的量(n)单位:摩尔(mol)单位:升(L)气体体积(V)、质量(m)和微粒数(N)
之间的转化关系气体的体积(V)×Vm÷ Vm课堂小结物质的量(n)单位:摩尔(mol)单位:升(L)气体体积(V)、质量(m)和微粒数(N)
之间的转化关系气体的体积(V)×Vm÷ Vm课堂小结物质的量(n)单位:摩尔(mol)质量(m)单位:克(g)单位:升(L)气体体积(V)、质量(m)和微粒数(N)
之间的转化关系气体的体积(V)×Vm÷ Vm课堂小结物质的量(n)单位:摩尔(mol)质量(m)单位:克(g)× M单位:升(L)气体体积(V)、质量(m)和微粒数(N)
之间的转化关系气体的体积(V)×Vm÷ Vm课堂小结物质的量(n)单位:摩尔(mol)质量(m)单位:克(g)× M÷M单位:升(L)气体体积(V)、质量(m)和微粒数(N)
之间的转化关系气体的体积(V)×Vm÷ Vm课堂小结物质的量(n)单位:摩尔(mol)质量(m)单位:克(g)微粒数(N)单位:(个)× M÷M单位:升(L)气体体积(V)、质量(m)和微粒数(N)
之间的转化关系气体的体积(V)×Vm÷ Vm课堂小结物质的量(n)单位:摩尔(mol)质量(m)单位:克(g)微粒数(N)单位:(个)× NA× M÷M单位:升(L)气体体积(V)、质量(m)和微粒数(N)
之间的转化关系气体的体积(V)×Vm÷ Vm课堂小结物质的量(n)单位:摩尔(mol)质量(m)单位:克(g)微粒数(N)单位:(个)× NA× M÷M÷NA单位:升(L)气体体积(V)、质量(m)和微粒数(N)
之间的转化关系气体的体积(V)×Vm÷ Vm课堂小结物质的量(n)单位:摩尔(mol)质量(m)单位:克(g)微粒数(N)单位:(个)× NA× M÷M÷NA单位:升(L)气体体积(V)、质量(m)和微粒数(N)
之间的转化关系物质的量是联系的纽带,沟通的桥梁1. 下列说法正确的是( )
(A)在标准状况下,1mol水和1molH2的
体积都约是22.4L
(B)2gH2和44gCO2的体积相等
(C)1mol某气体的体积为22.4L,则该气体
一定处于标准状况
(D)在标准状况下,1gH2和11.2LO2的物质
的量相等
(E)标准状况下,1molO2和N2混合气体的
体积约为22.4L课堂练习:1. 下列说法正确的是( )
(A)在标准状况下,1mol水和1molH2的
体积都约是22.4L
(B)2gH2和44gCO2的体积相等
(C)1mol某气体的体积为22.4L,则该气体
一定处于标准状况
(D)在标准状况下,1gH2和11.2LO2的物质
的量相等
(E)标准状况下,1molO2和N2混合气体的
体积约为22.4L[答案] D、E 课堂练习:2. 标准状况下, 112 mL 某气体的质量为 0.14 g , 则其摩尔质量为 ,相对分子质量为 。2. 标准状况下, 112 mL 某气体的质量为 0.14 g , 则其摩尔质量为 ,相对分子质量为 。n =VVm解:2. 标准状况下, 112 mL 某气体的质量为 0.14 g , 则其摩尔质量为 ,相对分子质量为 。n =VVm解:=0 . 112 L22 . 4 L · mol -1 2. 标准状况下, 112 mL 某气体的质量为 0.14 g , 则其摩尔质量为 ,相对分子质量为 。n =VVm解:=0 . 112 L22 . 4 L · mol -1 = 0 . 005 mol 2. 标准状况下, 112 mL 某气体的质量为 0.14 g , 则其摩尔质量为 ,相对分子质量为 。n =VVm解:=0 . 112 L22 . 4 L · mol -1 = 0 . 005 mol n = m / M2. 标准状况下, 112 mL 某气体的质量为 0.14 g , 则其摩尔质量为 ,相对分子质量为 。n =VVm解:=0 . 112 L22 . 4 L · mol -1 = 0 . 005 mol n = m / MM = 0 . 14 g0 . 005 mol 2. 标准状况下, 112 mL 某气体的质量为 0.14 g , 则其摩尔质量为 ,相对分子质量为 。n =VVm解:=0 . 112 L22 . 4 L · mol -1 = 0 . 005 mol n = m / MM = 0 . 14 g0 . 005 mol = 28 g / mol3. 同温同压下,质量相同的N2、CO2、Cl2、
CH4、O 2五种气体所占的体积由大到小的顺序是( )3. 同温同压下,质量相同的N2、CO2、Cl2、
CH4、O 2五种气体所占的体积由大到小的顺序是( )CH4、N2、O2、CO2、Cl23. 同温同压下,质量相同的N2、CO2、Cl2、
CH4、O 2五种气体所占的体积由大到小的顺序是( )CH4、N2、O2、CO2、Cl2求气体
体积的大小3. 同温同压下,质量相同的N2、CO2、Cl2、
CH4、O 2五种气体所占的体积由大到小的顺序是( )CH4、N2、O2、CO2、Cl2求气体
体积的大小求物质的量
大小3. 同温同压下,质量相同的N2、CO2、Cl2、
CH4、O 2五种气体所占的体积由大到小的顺序是( )CH4、N2、O2、CO2、Cl2求气体
体积的大小求物质的量
大小质量相同看
摩尔质量3. 同温同压下,质量相同的N2、CO2、Cl2、
CH4、O 2五种气体所占的体积由大到小的顺序是( )CH4、N2、O2、CO2、Cl2求气体
体积的大小求物质的量
大小质量相同看
摩尔质量等质量的物质其摩尔质量越小,其物质的量越大3. 同温同压下,质量相同的N2、CO2、Cl2、
CH4、O 2五种气体所占的体积由大到小的顺序是( )CH4、N2、O2、CO2、Cl2求气体
体积的大小求物质的量
大小质量相同看
摩尔质量等质量的物质其摩尔质量越小,其物质的量越大等物质的量的以上气体,质量由大到小的顺序是什么?3. 同温同压下,质量相同的N2、CO2、Cl2、
CH4、O 2五种气体所占的体积由大到小的顺序是( )CH4、N2、O2、CO2、Cl2求气体
体积的大小求物质的量
大小质量相同看
摩尔质量等质量的物质其摩尔质量越小,其物质的量越大等物质的量的以上气体,质量由大到小的顺序是什么?相同物质的量的物质,摩尔质量越大质量越大1. 在标准状况下, 6.72升甲烷
和CO的混和气体的质量为6克,
该混和气体中有 mol的
甲烷, 克的CO。拓展提高1. 在标准状况下, 6.72升甲烷
和CO的混和气体的质量为6克,
该混和气体中有 mol的
甲烷, 克的CO。拓展提高0.21. 在标准状况下, 6.72升甲烷
和CO的混和气体的质量为6克,
该混和气体中有 mol的
甲烷, 克的CO。拓展提高0.22.82.(多选)下列两种气体的分子数一定相等的是( )
A. 质量相等、密度不等的N2和C2H4
B. 等体积等密度的CO和C2H4
C. 等温等体积的O2和N2
D. 等压等体积的N2和CO22.(多选)下列两种气体的分子数一定相等的是( )
A. 质量相等、密度不等的N2和C2H4
B. 等体积等密度的CO和C2H4
C. 等温等体积的O2和N2
D. 等压等体积的N2和CO2A B
