1.1.2.2《卤族元素》课件(新人教版必修2)
文档属性
| 名称 | 1.1.2.2《卤族元素》课件(新人教版必修2) |

|
|
| 格式 | rar | ||
| 文件大小 | 126.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2009-08-20 00:00:00 | ||
图片预览




文档简介
课件13张PPT。学习目的:
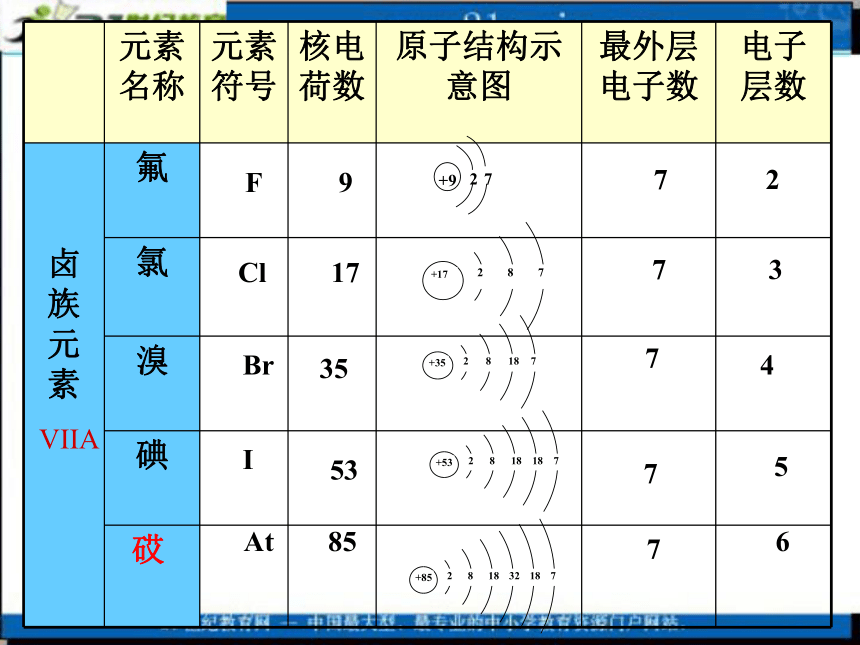
掌握卤族元素的性质与原子结构的关系卤族元素画出周期表的短周期部分H
Li
NaBe
MgB
AlC
SiO
SF
ClHe
Ne
ArIAIIAIIIAIVAVAVIAVIIA0N
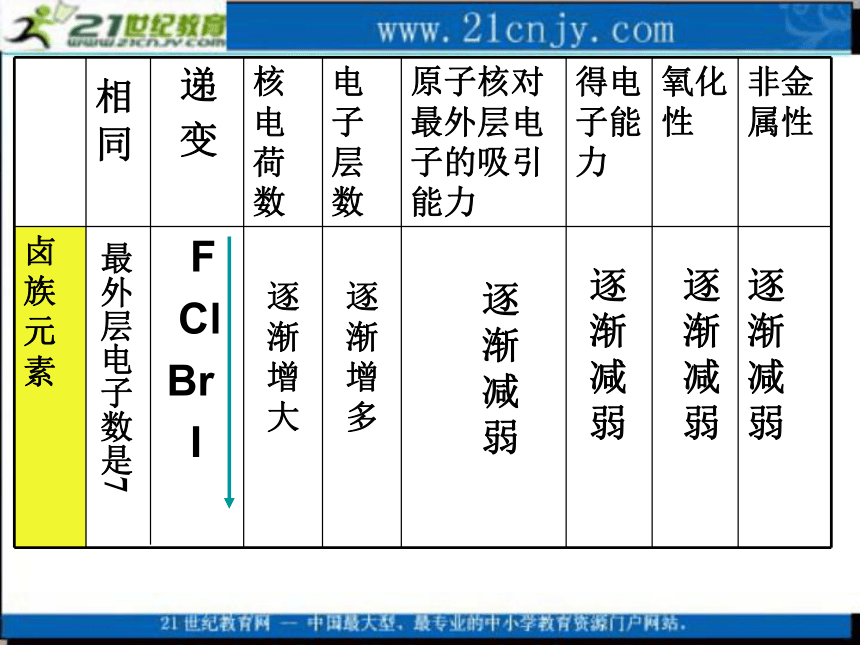
P画出Cl原子结构示意图VIIA卤素单质在物理上的递变性颜色:状态:密度:熔沸点:在水中溶解性:思考根据卤素的原子结构,请你推测氟、氯、溴、碘在化学性质上所表现的相似性和递变性。逐
渐
增
大逐
渐
减
弱逐
渐
减
弱逐
渐
减
弱逐
渐
增
多逐
渐
减
弱相 同最外层电子数是7在我们所学过的知识里氯气能与哪些物质反应?那么F2、Br2、 I2能否与上述物质反应?能反应写出反应方程式。讨论:回忆:1、与金属反应2、与氢气反应3、与水反应4、与碱反应。Cl2 + H2O == HCl + HClO2OH - + Cl2 = ClO -+ Cl - + H2OBr2+ H2O==HBr+HBrO反应越来越难以发生2F2+2H2O==4HF+O2 (特例)Cl2 +H2O==HCl+HClO卤素与水的化学反应方程式通式:X2 + H2O==HX+HXO(X:Cl、Br、I) 冷暗处爆炸 H2+F2==2HF HF很稳定 光照或点燃 H2+Cl2==2HCl HCl稳定高温 H2+Br2==2HBr HBr较不稳定高温、持 H2+I2== 2HI HI很不稳定 续加热
500℃光照 卤素与氢气的反应点燃盛有KI溶液的试
管,CCl4层变深
紫色。盛有NaBr溶液的试管,CCl4层变橙红色。盛有KI溶液的试
管,CCl4层变深
紫色。实验1-1卤素单质间的置换反应F2 + 2NaCl(熔融)= NaF + Cl2Cl2 + 2NaBr= 2NaCl + Br2Cl2 + 2KI = 2KCl + I2Br2 + 2KI = 2KBr + I2讨论:通过以上分析可以得出F2,Cl2,Br2, I2
氧化性逐渐减弱,我们能不能用实
验来证明或有哪些方法能证明物质
的氧化性的强弱关系。
掌握卤族元素的性质与原子结构的关系卤族元素画出周期表的短周期部分H
Li
NaBe
MgB
AlC
SiO
SF
ClHe
Ne
ArIAIIAIIIAIVAVAVIAVIIA0N
P画出Cl原子结构示意图VIIA卤素单质在物理上的递变性颜色:状态:密度:熔沸点:在水中溶解性:思考根据卤素的原子结构,请你推测氟、氯、溴、碘在化学性质上所表现的相似性和递变性。逐
渐
增
大逐
渐
减
弱逐
渐
减
弱逐
渐
减
弱逐
渐
增
多逐
渐
减
弱相 同最外层电子数是7在我们所学过的知识里氯气能与哪些物质反应?那么F2、Br2、 I2能否与上述物质反应?能反应写出反应方程式。讨论:回忆:1、与金属反应2、与氢气反应3、与水反应4、与碱反应。Cl2 + H2O == HCl + HClO2OH - + Cl2 = ClO -+ Cl - + H2OBr2+ H2O==HBr+HBrO反应越来越难以发生2F2+2H2O==4HF+O2 (特例)Cl2 +H2O==HCl+HClO卤素与水的化学反应方程式通式:X2 + H2O==HX+HXO(X:Cl、Br、I) 冷暗处爆炸 H2+F2==2HF HF很稳定 光照或点燃 H2+Cl2==2HCl HCl稳定高温 H2+Br2==2HBr HBr较不稳定高温、持 H2+I2== 2HI HI很不稳定 续加热
500℃光照 卤素与氢气的反应点燃盛有KI溶液的试
管,CCl4层变深
紫色。盛有NaBr溶液的试管,CCl4层变橙红色。盛有KI溶液的试
管,CCl4层变深
紫色。实验1-1卤素单质间的置换反应F2 + 2NaCl(熔融)= NaF + Cl2Cl2 + 2NaBr= 2NaCl + Br2Cl2 + 2KI = 2KCl + I2Br2 + 2KI = 2KBr + I2讨论:通过以上分析可以得出F2,Cl2,Br2, I2
氧化性逐渐减弱,我们能不能用实
验来证明或有哪些方法能证明物质
的氧化性的强弱关系。
