化学:5.1《原电池》课件(3)(苏教版选修6)
文档属性
| 名称 | 化学:5.1《原电池》课件(3)(苏教版选修6) |

|
|
| 格式 | rar | ||
| 文件大小 | 413.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2009-08-27 00:00:00 | ||
图片预览






文档简介
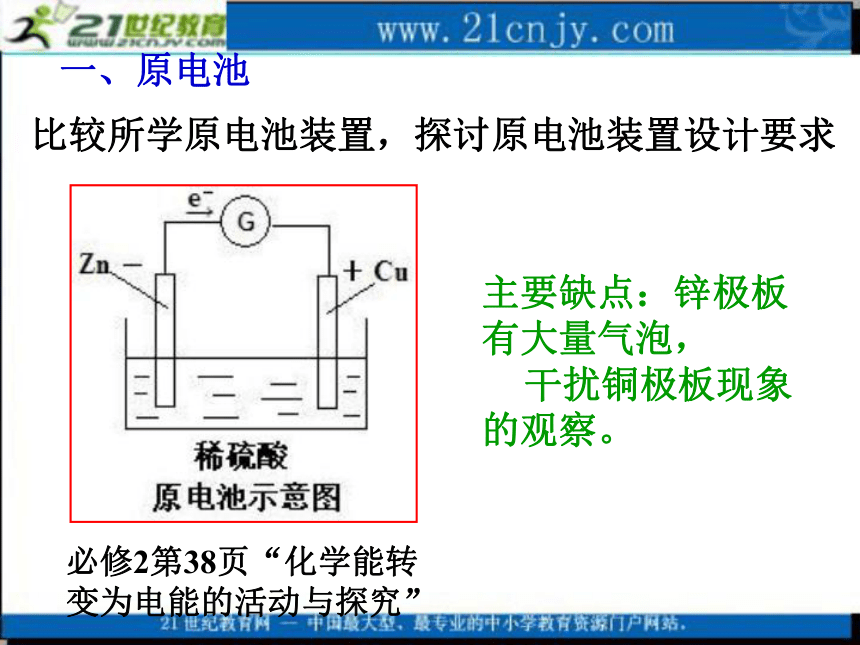
课件18张PPT。专题5 电化学问题研究课题1 原电池一、原电池比较所学原电池装置,探讨原电池装置设计要求必修2第38页“化学能转变为电能的活动与探究” 主要缺点:锌极板有大量气泡,
干扰铜极板现象的观察。一、原电池比较所学原电池装置,探讨原电池装置设计要求选修3第12页“原电池的工作原理活动与探究”优点:克服了锌极板有铜析出的现象;盐桥能说明内电路中离子的迁移 缺点:电流密度依然较小,不足以使小灯泡发亮 总结:原电池装置设计要求提高电池的放电效率;
增大电池的电流密度,
延长电池的工作时间,
。。。。。。。1、影响电池的电流密度的大小的因素:
电极的表面积、极间距、介质等
2、影响电池放电效率、放电时间的因素:
电池的极化作用
弊端:极化作用会使电极的放电反应变得迟钝,充电变得困难,影响电池的工作时间。
措施:加入去极化剂(如高锰酸钾、重铬酸钾和过氧化氢等氧化剂),可有效降低了电极的极化作用,提高了电池的放电效率。
为此设计了如下图的实验装置。检索咨询铜锌原电池 图5-2 Zn - Cu原电池示意图1.装置的组装
取一块锌片(6cm×3.3cm)和一块铜片
(6cm×3.3cm),两者之间放一块海绵(厚度2cm),用橡皮筋固定好,用导线把小灯泡(2.5V 0.3A)和锌片、铜片连接起来,插入放有50ml蒸馏水的100ml小烧杯中,组装这样的装置多个备用。 研究:去极化剂、电极材料、介质对放电效果的影响2.去极化剂的选择 向三个装置中分别加入 10ml 的稀硫酸,编号为甲
乙、丙,观察小灯泡是否发光。
向甲装置中加入 5ml 3% 的双氧水,振荡溶液,
记录小灯泡发光的时间和亮度。
向乙装置中加入 0.5 g 的重铬酸钾晶体,振荡溶液,
记录小灯泡发光的时间和亮度。
向丙装置中加入 0.5 g 的高锰酸钾晶体,振荡溶液,
记录小灯泡发光的时间和亮度。先变亮后变暗2.去极化剂的选择 3.电极材料的选择 电极材料:Zn-C(直径1.1cm),与Zn-Cu对比
溶液介质:稀硫酸
去极化剂:重铬酸钾晶体
电极材料:Al -C (直径1.1cm),与Al-Cu对比
溶液介质:稀盐酸
去极化剂:重铬酸钾晶体
按照上述实验装置和操作方法进行实验,观察现象。 3.电极材料的选择 4.溶液介质的选择 电极材料:Zn - C(直径1.1cm) ,Al - C
溶液介质:加入约 10 g 氢氧化钠固体
去极化剂:重铬酸钾晶体
按照上述实验装置和操作方法进行实验,观察实验
现象。 实验结论:酸溶液优于碱溶液二、燃料电池1、写出氢氧燃料电池在不同介质中(Na2SO4、KOH、H2SO4)的电极反应式2、写出甲烷燃料电池在以KOH溶液为电解质条件下的电极反应式P64 制作氢氧燃料电池三、电化学腐蚀1、析氢腐蚀
条件:
电极反应式:较强酸性介质中2、吸氧腐蚀
条件:
电极反应式:中性、偏碱性或较弱酸性介质中P64 金属电化学腐蚀四、生活中常见电池的化学原理电池反应:
Zn + 2MnO2 + 2NH4+ = Mn2O3 + 2NH3??+ Zn2+ + H2O 1. 普通锌锰干电池四、生活中常见电池的化学原理2、铅蓄电池四、生活中常见电池的化学原理3、镍—镉可充电电池四、生活中常见电池的化学原理4. 银—锌可充电电池电池反应:
Ag2O + Zn + H2O == 2Ag + Zn(OH)2
干扰铜极板现象的观察。一、原电池比较所学原电池装置,探讨原电池装置设计要求选修3第12页“原电池的工作原理活动与探究”优点:克服了锌极板有铜析出的现象;盐桥能说明内电路中离子的迁移 缺点:电流密度依然较小,不足以使小灯泡发亮 总结:原电池装置设计要求提高电池的放电效率;
增大电池的电流密度,
延长电池的工作时间,
。。。。。。。1、影响电池的电流密度的大小的因素:
电极的表面积、极间距、介质等
2、影响电池放电效率、放电时间的因素:
电池的极化作用
弊端:极化作用会使电极的放电反应变得迟钝,充电变得困难,影响电池的工作时间。
措施:加入去极化剂(如高锰酸钾、重铬酸钾和过氧化氢等氧化剂),可有效降低了电极的极化作用,提高了电池的放电效率。
为此设计了如下图的实验装置。检索咨询铜锌原电池 图5-2 Zn - Cu原电池示意图1.装置的组装
取一块锌片(6cm×3.3cm)和一块铜片
(6cm×3.3cm),两者之间放一块海绵(厚度2cm),用橡皮筋固定好,用导线把小灯泡(2.5V 0.3A)和锌片、铜片连接起来,插入放有50ml蒸馏水的100ml小烧杯中,组装这样的装置多个备用。 研究:去极化剂、电极材料、介质对放电效果的影响2.去极化剂的选择 向三个装置中分别加入 10ml 的稀硫酸,编号为甲
乙、丙,观察小灯泡是否发光。
向甲装置中加入 5ml 3% 的双氧水,振荡溶液,
记录小灯泡发光的时间和亮度。
向乙装置中加入 0.5 g 的重铬酸钾晶体,振荡溶液,
记录小灯泡发光的时间和亮度。
向丙装置中加入 0.5 g 的高锰酸钾晶体,振荡溶液,
记录小灯泡发光的时间和亮度。先变亮后变暗2.去极化剂的选择 3.电极材料的选择 电极材料:Zn-C(直径1.1cm),与Zn-Cu对比
溶液介质:稀硫酸
去极化剂:重铬酸钾晶体
电极材料:Al -C (直径1.1cm),与Al-Cu对比
溶液介质:稀盐酸
去极化剂:重铬酸钾晶体
按照上述实验装置和操作方法进行实验,观察现象。 3.电极材料的选择 4.溶液介质的选择 电极材料:Zn - C(直径1.1cm) ,Al - C
溶液介质:加入约 10 g 氢氧化钠固体
去极化剂:重铬酸钾晶体
按照上述实验装置和操作方法进行实验,观察实验
现象。 实验结论:酸溶液优于碱溶液二、燃料电池1、写出氢氧燃料电池在不同介质中(Na2SO4、KOH、H2SO4)的电极反应式2、写出甲烷燃料电池在以KOH溶液为电解质条件下的电极反应式P64 制作氢氧燃料电池三、电化学腐蚀1、析氢腐蚀
条件:
电极反应式:较强酸性介质中2、吸氧腐蚀
条件:
电极反应式:中性、偏碱性或较弱酸性介质中P64 金属电化学腐蚀四、生活中常见电池的化学原理电池反应:
Zn + 2MnO2 + 2NH4+ = Mn2O3 + 2NH3??+ Zn2+ + H2O 1. 普通锌锰干电池四、生活中常见电池的化学原理2、铅蓄电池四、生活中常见电池的化学原理3、镍—镉可充电电池四、生活中常见电池的化学原理4. 银—锌可充电电池电池反应:
Ag2O + Zn + H2O == 2Ag + Zn(OH)2
同课章节目录
- 专题一 物质的分离与提纯
- 课题1 海带中碘元素的分离及检验
- 拓展课题1-1 茶叶中某些元素的鉴定
- 课题2 用纸层析法分离铁离子和铜离子
- 拓展课题1-2 菠菜的叶绿体中色素的提取和分离
- 拓展课题1-3 用粉笔进行层析分离
- 课题3 硝酸钾晶体的制备
- 拓展课题1-4 粗盐提纯
- 专题二 物质性质的研究
- 课题1 铝及其化合物的性质
- 拓展课题2-1 铝热反应
- 课题2 乙醇和苯酚的性质
- 拓展课题2-2 苯酚与甲醛的反应
- 专题三 物质的检验与鉴别
- 课题1 牙膏和火柴中某些成分的检验
- 拓展课题3-1 新装修居室内空气中甲醛浓度的检测
- 拓展课题3-2 汽车尾气成分的检验
- 课题2 亚硝酸钠和食盐的鉴别
- 拓展课题3-3 真假碘盐的鉴别
- 专题四 化学反应条件的控制
- 课题1 硫代硫酸钠与酸反应速率的影响因素
- 拓展课题4-1 “蓝瓶子”实验
- 课题2 催化剂对过氧化氢分解反应速率的影响
- 拓展课题4-2 过氧化氢酶的催化作用
- 拓展课题4-3 蔗糖的燃烧
- 课题3 反应条件对化学平衡的影响
- 拓展课题4-4 淀粉与碘显色现象的探究
- 拓展课题4-5 压强对化学平衡的影响
- 专题五 电化学问题研究
- 课题1 原电池
- 拓展课题5-1 干电池模拟实验
- 课题2 电解与电镀
- 拓展课题5-2 阿伏加德罗常数的测定
- 专题六 物质的定量分析
- 课题1 食醋总酸含量的测定
- 拓展课题6-1 配制并标定氢氧化钠溶液
- 课题2 镀锌铁皮锌镀层厚度的测定
- 拓展课题6-2 水果中维生素C含量的测定
- 专题七 物质的制备与合成
- 课题1 硫酸亚铁铵的制备
- 拓展课题7-1 用制氢废液制备硫酸锌晶体
- 课题2 阿司匹林的合成
- 拓展课题7-2 对氨基苯磺酸的合成
