化学式复习
图片预览




文档简介
课件18张PPT。第一章
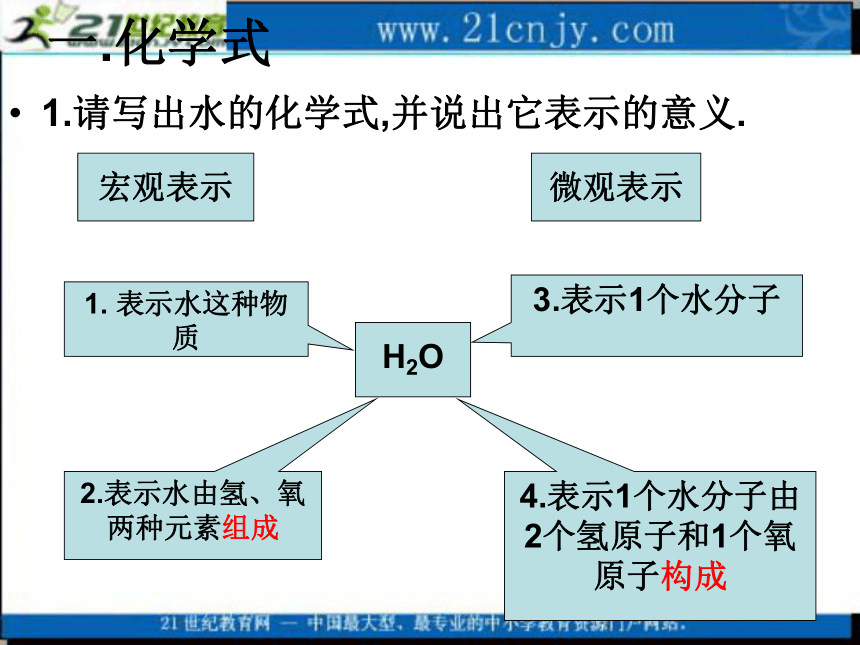
化合价和化学式的复习1.请写出以下物质的化学式: 水、二氧化碳、三氧化二铝、五氧化二磷 2.观察写出化学式中都有什么元素,每个化学式中各原子的个数比是多少? H2O CO2 Al2O3 P2O5 一.化学式1.请写出水的化学式,并说出它表示的意义.H2O宏观表示微观表示1. 表示水这种物质3.表示1个水分子2.表示水由氢、氧两种元素组成4.表示1个水分子由2个氢原子和1个氧原子构成
2.说出下列符号表示的意义. H 2H H2 2H2 3CO2 4SO4 3.化学式的书写规则:(1)氧化物: 氧元素在右,另一元素在左, 如:CO2,P2O5,H2O2等 (2)金属元素和非金属元素组成的化合物: 金属元素在左,非金属元素在右. 如:Na Cl、KI等 (3)单质: A.稀有气体、金属和非金属直接用元素符号表示
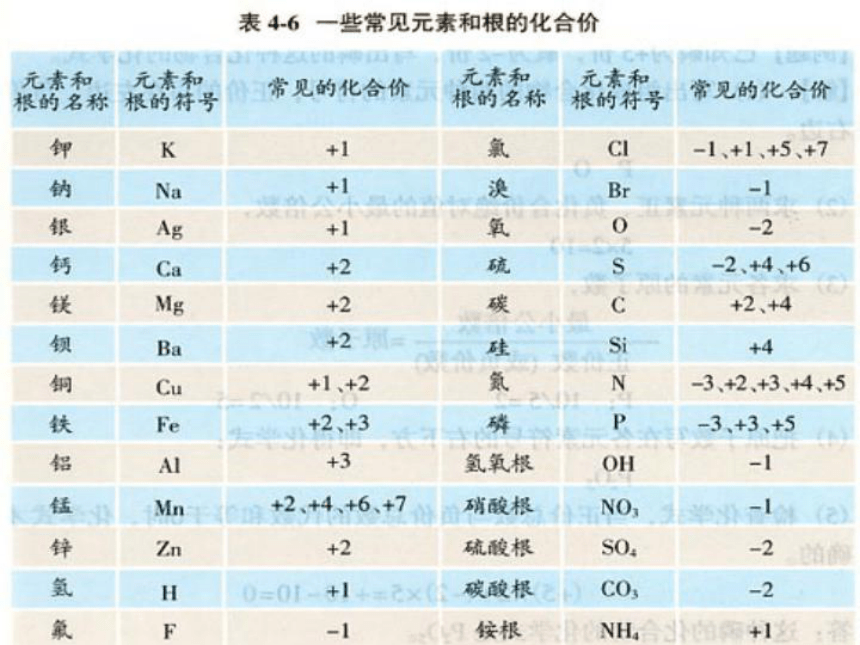
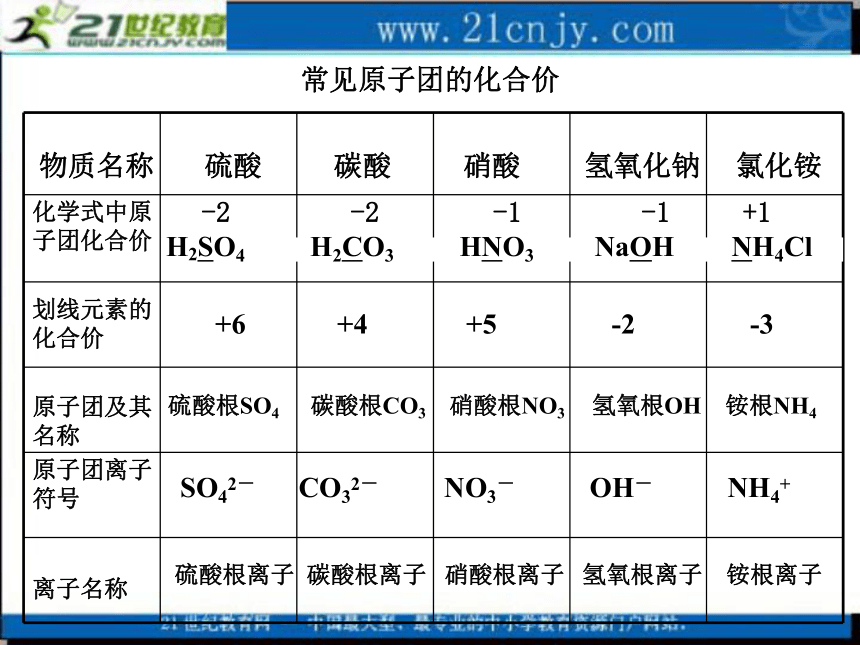
如:Ne,He,C,P,Fe等B.非金属气体:如:O2、Cl2、O3等(2)氢元素通常显+1价二、化合价的特点1、化合价有正价和负价。(1)氧元素通常显-2价。(3)金属元素显正价,非金属元素通常显负价(在氧化物中显正价)(4)一些元素在不同物质中可以显不同的化合价2、在化合物里正负化合价的代数和为0。3、在单质中,元素的化合价为0常见原子团的化合价物质名称 硫酸 碳酸 硝酸 氢氧化钠 氯化铵化学式中原子团化合价
划线元素的化合价
原子团及其名称
原子团离子符号
离子名称+6 +4 +5 -2 -3硫酸根SO4 碳酸根CO3 硝酸根NO3 氢氧根OH 铵根NH4SO42- CO32- NO3- OH- NH4+硫酸根离子 碳酸根离子 硝酸根离子 氢氧根离子 铵根离子 -2 -2 -1 -1 +1H2SO4 H2CO3 HNO3 NaOH NH4Cl单质元素价为零,一价氯氢钾钠银,
二价氧钙钡镁锌,三铝四硅五价磷,
二三铁,二四碳,二四六硫都齐全一价铵硝氢氧根,二价硫酸碳酸根。常见元素及原子团化合价的记忆口诀表示方法:在元素符号的正上方,
符号在前,数值在后读法:某元素的化合价为正(负)几价氧元素化合价为-2价
氧化钙中氧元素的化合价为-2价
氢氧化钠中氢氧根的化合价为-1价二、化合价H2O、 CO2、Al2O3、P2O5标出下列物质中元素的化合价正价前,负价后;
标价数,数交叉;
数最简,定个数。化学式的书写方法:三聚氰胺也被人称为“蛋白精”,C3H6N6、C3N3(NH2)3
分子量126.12 三聚氰胺性状为纯白色单斜棱晶体,无味,密度1.573g/cm3 (16℃)。常压熔点354℃(分解);快速加热升华,升华温度300℃。溶于热水,微溶于冷水,极微溶于热乙醇,不溶于醚、苯和四氯化碳,可溶于甲醇、甲醛、乙酸、热乙二醇、甘油、吡啶等。低毒。在一般情况下较稳定,但在高温下可能会分解放出氰化物。结构式(1)根据化合价确定物质的化学式:1、钙的化合价为+2价,氢氧根(OH)的化合价为-1价,写出它的化学式Ca(OH)2例如:铁有+2和+3价,写出它们的氧化物的化学式FeOFeO+2 -2Fe2O2+3 -2FeO Fe2O3氧化亚铁氧化铁2、填表:写出各物质的化学式-1-2+1+2+3HClMgCl2AlCl3H2SO4MgSO4Al 2(SO4)3(2)确定物质中某元素的化合价例1、试确定氯酸钾中氯元素和氯酸根的化合价【思路】先写出化学式KClO3解:设KClO3中Cl的化合价为X+1+X+(-2) ×3=0X=+5
答:氯酸钾中氯元素的化合价为+5+ 5ClO3的化合价为y+1+y=0y=-1在化合物里元素的正负化合价代数和为零。小结:根据在化合物里元素的正 负化合价代数和为零。3、说出下列物质中硫元素的化合价
H2S S H2SO3 H2SO4 -20+4+6小结化学式化合价 一、选择:
1、已知在H3RO4 中,氢元素为+1价,氧为-2价,则其中 R的化合价为( )
A +3 B +4 C +5 D +6
2、下列化合物中,氮元素为+5价的是( )
A N0 B NO2 C HNO2 D KNO3
3、元素R的氧化物的化学式为R2O3,则R 元素与OH-组 成 的物质的化学式为( )
A ROH B R(OH) 2 C R(OH) 3 D R(OH) 4CDC4、下列化学式如有错误请改在横线上:
氯化钠ClNa ______,
氧化钙Ca2S2 ______,
氢氧化钡BaOH2 ____ __ ,
氯化铁 FeCl2______。CaSFeCl3NaCl氯化亚铁Ba(OH)2二、化合价
1、化合价
2、化合价的表示方法:
在元素符号头顶上,符号在前,数值在后。
3、化合价的特点
化合价有正价和负价;单质中元素的化合价为零,化合物中元素化合价代数和为零。
4、化合价的应用。
(1)依据化合价书写化学式
书写的规律:正价先,负价后;
标价数,价交叉;数最简,定个数。
(2)计算化合物中某一元素的化合价
依据:在化合物中元素化合价代数和为零。
化合价和化学式的复习1.请写出以下物质的化学式: 水、二氧化碳、三氧化二铝、五氧化二磷 2.观察写出化学式中都有什么元素,每个化学式中各原子的个数比是多少? H2O CO2 Al2O3 P2O5 一.化学式1.请写出水的化学式,并说出它表示的意义.H2O宏观表示微观表示1. 表示水这种物质3.表示1个水分子2.表示水由氢、氧两种元素组成4.表示1个水分子由2个氢原子和1个氧原子构成
2.说出下列符号表示的意义. H 2H H2 2H2 3CO2 4SO4 3.化学式的书写规则:(1)氧化物: 氧元素在右,另一元素在左, 如:CO2,P2O5,H2O2等 (2)金属元素和非金属元素组成的化合物: 金属元素在左,非金属元素在右. 如:Na Cl、KI等 (3)单质: A.稀有气体、金属和非金属直接用元素符号表示
如:Ne,He,C,P,Fe等B.非金属气体:如:O2、Cl2、O3等(2)氢元素通常显+1价二、化合价的特点1、化合价有正价和负价。(1)氧元素通常显-2价。(3)金属元素显正价,非金属元素通常显负价(在氧化物中显正价)(4)一些元素在不同物质中可以显不同的化合价2、在化合物里正负化合价的代数和为0。3、在单质中,元素的化合价为0常见原子团的化合价物质名称 硫酸 碳酸 硝酸 氢氧化钠 氯化铵化学式中原子团化合价
划线元素的化合价
原子团及其名称
原子团离子符号
离子名称+6 +4 +5 -2 -3硫酸根SO4 碳酸根CO3 硝酸根NO3 氢氧根OH 铵根NH4SO42- CO32- NO3- OH- NH4+硫酸根离子 碳酸根离子 硝酸根离子 氢氧根离子 铵根离子 -2 -2 -1 -1 +1H2SO4 H2CO3 HNO3 NaOH NH4Cl单质元素价为零,一价氯氢钾钠银,
二价氧钙钡镁锌,三铝四硅五价磷,
二三铁,二四碳,二四六硫都齐全一价铵硝氢氧根,二价硫酸碳酸根。常见元素及原子团化合价的记忆口诀表示方法:在元素符号的正上方,
符号在前,数值在后读法:某元素的化合价为正(负)几价氧元素化合价为-2价
氧化钙中氧元素的化合价为-2价
氢氧化钠中氢氧根的化合价为-1价二、化合价H2O、 CO2、Al2O3、P2O5标出下列物质中元素的化合价正价前,负价后;
标价数,数交叉;
数最简,定个数。化学式的书写方法:三聚氰胺也被人称为“蛋白精”,C3H6N6、C3N3(NH2)3
分子量126.12 三聚氰胺性状为纯白色单斜棱晶体,无味,密度1.573g/cm3 (16℃)。常压熔点354℃(分解);快速加热升华,升华温度300℃。溶于热水,微溶于冷水,极微溶于热乙醇,不溶于醚、苯和四氯化碳,可溶于甲醇、甲醛、乙酸、热乙二醇、甘油、吡啶等。低毒。在一般情况下较稳定,但在高温下可能会分解放出氰化物。结构式(1)根据化合价确定物质的化学式:1、钙的化合价为+2价,氢氧根(OH)的化合价为-1价,写出它的化学式Ca(OH)2例如:铁有+2和+3价,写出它们的氧化物的化学式FeOFeO+2 -2Fe2O2+3 -2FeO Fe2O3氧化亚铁氧化铁2、填表:写出各物质的化学式-1-2+1+2+3HClMgCl2AlCl3H2SO4MgSO4Al 2(SO4)3(2)确定物质中某元素的化合价例1、试确定氯酸钾中氯元素和氯酸根的化合价【思路】先写出化学式KClO3解:设KClO3中Cl的化合价为X+1+X+(-2) ×3=0X=+5
答:氯酸钾中氯元素的化合价为+5+ 5ClO3的化合价为y+1+y=0y=-1在化合物里元素的正负化合价代数和为零。小结:根据在化合物里元素的正 负化合价代数和为零。3、说出下列物质中硫元素的化合价
H2S S H2SO3 H2SO4 -20+4+6小结化学式化合价 一、选择:
1、已知在H3RO4 中,氢元素为+1价,氧为-2价,则其中 R的化合价为( )
A +3 B +4 C +5 D +6
2、下列化合物中,氮元素为+5价的是( )
A N0 B NO2 C HNO2 D KNO3
3、元素R的氧化物的化学式为R2O3,则R 元素与OH-组 成 的物质的化学式为( )
A ROH B R(OH) 2 C R(OH) 3 D R(OH) 4CDC4、下列化学式如有错误请改在横线上:
氯化钠ClNa ______,
氧化钙Ca2S2 ______,
氢氧化钡BaOH2 ____ __ ,
氯化铁 FeCl2______。CaSFeCl3NaCl氯化亚铁Ba(OH)2二、化合价
1、化合价
2、化合价的表示方法:
在元素符号头顶上,符号在前,数值在后。
3、化合价的特点
化合价有正价和负价;单质中元素的化合价为零,化合物中元素化合价代数和为零。
4、化合价的应用。
(1)依据化合价书写化学式
书写的规律:正价先,负价后;
标价数,价交叉;数最简,定个数。
(2)计算化合物中某一元素的化合价
依据:在化合物中元素化合价代数和为零。
同课章节目录
