2009年福建省理综测试卷化学试题分析
图片预览






文档简介
课件78张PPT。 福建省普教室 黄丹青
2009年7月高三培训2009年福建省理综测试卷化学试题分析
主要内容 一、 2009年福建省理综测试卷化学试题分析 二、 关于2009年福建省高考考试说明 三、 2010年福建省高考化学学科自主命题走势 四. 2010年高考复习迎考热点、难点问题剖析2009年福建省理综测试卷化学试题分析
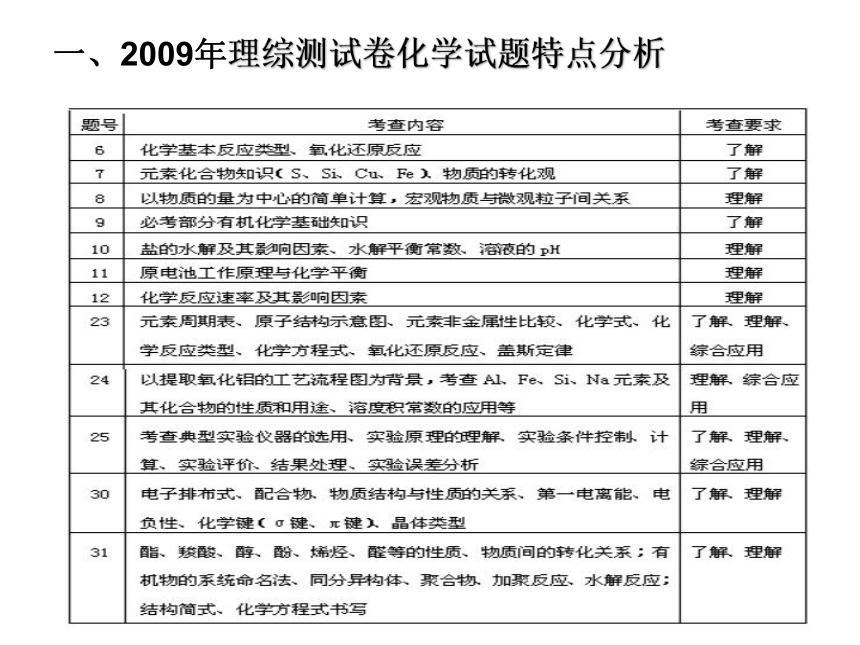
一、2009年理综测试卷化学试题特点分析物质的熔点差异S+2H2SO4(浓)= 3SO2↑+2H2O氧化还原反应沉淀溶解平衡 H-C C-H 3:2试题特点1 .突出化学核心内容考查,强调基础性
试题不排除考查应知应会的基础内容,同时,将氧化还原反应、化学反应速率和化学平衡、电离与水解、以物质的量为中心的简单计算、化学实验设计与评价等主干、核心知识内容作为考查的重点。
2 .加强学科内综合,重视学科能力
试题以推断、信息迁移、实验探究等综合题型的方式,通过学生在解题思路中的知识纵横延伸,考查学生“接受、吸收、整合化学信息的能力,分析问题和解决(解答)化学问题的能力,化学实验的探究能力”。体现“注重学科的内在联系和知识的综合”和“能力立意”的命题原则。
3 .表现新课程的核心理念,凸显导向性
试题重视对基本方法、基本思想、化学观的考查。如:分类比较的方法、定量研究的方法、物质转化观、绿色化学思想等。
4. 命题规范,体现简约性
试题力求文字凝练、表述明晰、图示简洁、结构严谨,剔除花哨的铺垫和生硬的拼凑,注意控制试题的阅读量、思维量和答题量。有关化学计算因素的试题都引入了简化的数值,多处设问只要求采用表达式作答,避免了考生在有限的时间里进行繁杂的数值运算。 关于2009年福建省《考试说明》
一、编写考试说明的指导思想
1.体现考试说明对2009年高考理综试卷命题的权威性
2.对高中新课程教学的指导性
3.体现厅领导新课程高考“平稳过渡”的思路
二、考试说明的结构
Ⅰ. 命题指导思想
Ⅱ. 考试形式与试卷结构
Ⅲ. 考试内容
Ⅳ . 参考试卷 分值比例 物理︰化学︰生物=120︰100︰80
设置选考卷 理综试卷中另设选考卷,选考卷共5题,考生选答3题,其中,物理为2选1,化学为2选1,生物为一道必答题。
题量与题型 根据高考命题改革趋势和“3+X”高考经验,试卷设置学生答题题量与原课程高考理综试卷题量相当,题型基本一致,以求平稳过渡。
试卷难度 全卷难度值:0.60左右 物理:0.55~0.60 化学:0.60~0.65 生物:0.60~0.65
(一)对化学学习能力的要求
(二)对知识内容的要求层次
(三)考试范围和内容
(题型示例)Ⅲ.考试内容知识内容要求原
考
纲新
考
纲选考模块 化学科学特点和化学研究基本方法 ①了解化学主要特点是在原子、分子水平上认识物质;了 解化学可以识别、改变和创造分子。
②了解科学探究的基本过程,学习运用以实验和推理为基础的科学探究方法;认识化学是以实验为基础的一门科学。
③了解物质的组成、结构和性质的关系。了解化学反应的本质、基本原理以及能量变化等规律。
④了解定量研究的方法是化学发展为一门科学的重要标志。理解摩尔(mol)是物质的量的基本单位,可用于进行简单化学计算。
⑤了解科学、技术、社会的相互关系(如化学与生活、材料、能源、环境、生命过程、信息技术的关系等);了解在化工生产中遵循“绿色化学”思想的重要性。 必考内容部分09省二检 0.874 09省一检 0.69 09省一检 0.63 化学基本概念和基本理论 (1)物质的组成、性质和分类
(2)化学用语及常用计量
(3)溶液
(4)物质结构和元素周期律
必考内容部分09省二检 0.845 09省一检 0.67 09省一检 0.73 09宁夏高考 (5)化学反应与能量 ① 了解氧化还原反应的本质。了解常见的氧化还原反应。
② 了解化学反应中能量转化的原因,能说出常见的能量转化形式。
③ 了解化学能与热能的相互转化。了解吸热反应、放热反应、反应热等概念。
④ 了解热化学方程式的含义,能正确书写热化学方程式,能用盖斯定律进行有关反应热的简单计算。
⑤ 了解能源是人类生存和社会发展的重要基础。了解化学在解决能源危机中的重要作用。
⑥ 了解原电池和电解池的工作原理,能写出电极反应和电池反应方程式。了解常见化学电源的种类及其工作原理。
⑦ 理解金属发生电化学腐蚀的原因,了解金属腐蚀的危害和防止金属腐蚀的措施。必考内容部分省一检 0.4509省一检 0.4509省二检 0.695(6)化学反应速率和化学平衡 ① 了解化学反应速率的概念、反应速率的定量表示方法。
② 了解催化剂在生产、生活和科学研究领域中的重大作用。
③ 了解化学反应的可逆性。
④ 了解化学平衡建立的过程。了解化学平衡常数的含义,能够利用化学平衡常数计算反应物的转化率。
⑤ 理解外界条件(浓度、温度、压强、催化剂等)对反应速率和化学平衡的影响,认识其一般规律。
⑥ 了解化学反应速率和化学平衡的调控在生活、生产和科学研究领域中的重要作用。必考内容部分(7)电解质溶液
① 了解电解质、强电解质和弱电解质的概念。
② 了解电解质在水溶液中的电离,以及电解质溶液的导电性。
③ 了解弱电解质在水溶液中的电离平衡。
④ 了解水的电离和水的离子积常数。
⑤ 了解溶液pH的定义,能进行pH的简单计算。
⑥ 了解盐类水解的原理、影响盐类水解程度的主要因素、盐类水解的应用。(弱酸弱碱盐的水解不作要求)
⑦ 了解离子反应的概念、离子反应发生的条件。
⑧ 了解难溶电解质的溶解平衡。必考内容部分09省一检0.5809省二检0.62709省一检 0.44省一检 0.3609省二检 0.628省二检 0.509 09省二检 0.509 常见无机物及其应用 删——
“ⅠA和ⅡA族元素——典型的金属”
“从原子的核外电子排布,理解卤族元素(单质、化合物)的相似性和递变性”
“以硫酸为例,了解化工生产化学反应原理的确定”
“了解常见盐类的性质和用途”
常见金属元素(如Na、Al、Fe、Cu等)
“了解常见金属的活动顺序”、“了解常见金属及其重要化合物的主要性质及其应用”、“了解合金的概念及其重要应用”
常见非金属元素(如H、C、N、O、Si、S、Cl等)
“了解常见非金属单质及其重要化合物的主要性质及应用”;“了解常见非金属单质及其重要化合物对环境质量的影响”;以及“以上各部分知识的综合应用”
必考内容部分 09省二检 0.743 09省一检 0.54 常见有机物及其应用 ①了解有机化合物中碳的成键特征。
②了解甲烷、乙烯、苯等有机化合物的主要性质。
③了解乙烯、氯乙烯、苯的衍生物等在化工生产中的重要作用。
④了解乙醇、乙酸的组成和主要性质及重要应用。
⑤了解糖类、油脂、蛋白质的组成和主要性质及重要应用。
⑥了解常见高分子材料的合成反应及重要应用。
⑦了解有机物的同分异构现象,了解有机物反应的类型。
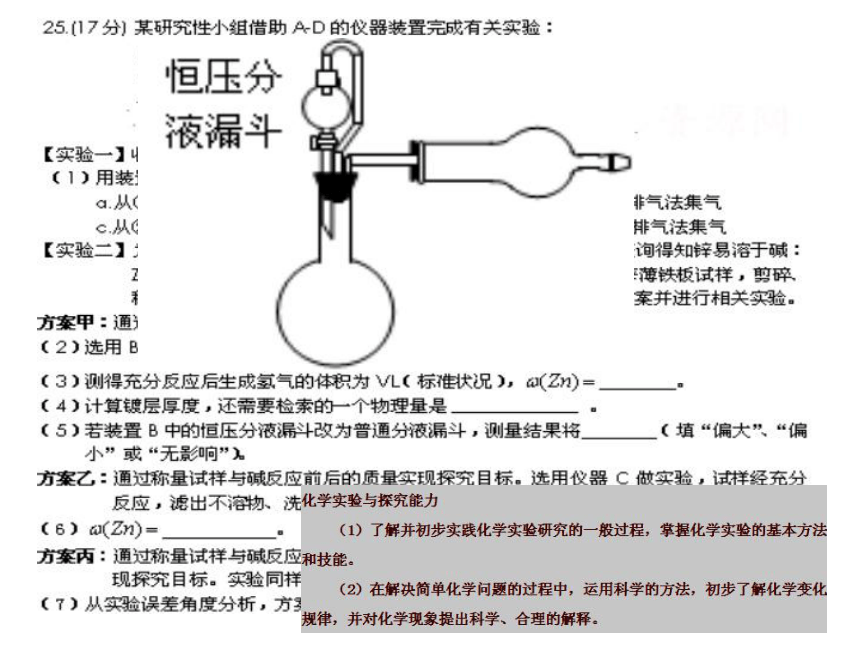
必考内容部分09省二检 0.924 09省一检 0. 81 化学实验基础 (1)了解化学实验是科学探究过程中的一种重要方法。
(2)了解化学实验室常用仪器的主要用途和使用方法。
(3)掌握化学实验的基本操作。能识别化学品安全使用
标识,了解实验室一般事故的预防和处理方法。
(4)掌握常见气体的实验室制法(包括所用试剂、仪器,
反应原理和收集方法)。
(5)了解常见离子的检验方法,能对常见的物质进行检
验、分离和提纯。
(6)能根据要求配制一定溶质质量分数、物质的量浓度
的溶液。了解测定溶液pH的方法。
(7)能根据实验试题要求,做到:① 设计、评价或改进
实验方案;②了解控制实验条件的方法;③ 分析或
处理实验数据,得出合理结论;④ 识别典型的实验
仪器装置图。
(8)以上各部分知识与技能的综合运用。必考内容部分09省一检 0.46 09省一检 0.41 09省二检 0.361 250mL容量瓶化学计算 对纯数学运算的要求降低,删去原考纲中的化学计算专题。将化学计算穿插分布在各模块的不同部分,强调计算与化学基本概念和理论、化学变化过程、工业流程等结合,体现计算为化学应用服务。 必考内容部分选考内容部分选考内容部分08宁夏物质结构35.[化学——选修物质结构与性质](15分)
X、Y、Z、Q、E五种元素中,X原子核外的M层中只有两对成对电子,Y原子核外的L层电子数是K层的两倍,Z是地壳内含量(质量分数)最高的元素,Q的核电荷数是X与Z的核电荷数之和,E在元素周期表的各元素中电负性最大。请回答下列问题:
(1)X、Y的元素符号依次为 、 ;
(2)XZ2与YZ2分子的立体结构分别是 和 ,相同条件下两者在水中的溶解度较大的是 (写分子式),理由是 ;
(3)Q的元素符号是 ,它属于第 周期,它的核外电子排布式为 ,在形成化合物时它的最高化合价为 ;
(4)用氢键表示式写出E的氢化物溶液中存在的所有氢键 。《有机化学基础》主
题
1
有机化合物的组成与结构主
题
2
烃及其衍生物的性质与应用主
题
3
糖类
、
氨基酸和蛋白质选考内容部分有机化化合物结构与性质的关系、有机反应与有机合成 有机化合物结构与性质的关系
碳键类型与有机物性质
官能团类型与有机物性质
分子中各基团的相互影响
分子空间结构对性质的影响有机化学反应原理
有机反应的主要类型
有机反应条件的控制
有机化合物合成基本思路和方法 《有机化学基础》
核心内容选考内容部分有机化合物的组成与结构 核心内容:认识有机化合物
认识有机化合物的组成和结构,了解自然界存在数千万种有机化合物的原因;
初步了解有机化合物的结构与性质的关系。
烃及其衍生物的性质与应用 核心内容:认识有机反应和转化
认识有机化合物性质,面对一个简单有机物时,知道怎样分析其具有的性质;
认识有机化学反应,了解有机化合物间的相互转化。3核心内容:认识有机化学的价值
了解糖类氨基酸和蛋白质的组成和性质特点以及其重要价值。
4核心内容:
知道学习有机化学的意义所在,认识有机合成的价值。33.[化学—有机化学基础]
苯丙酸诺龙是一种兴奋剂,结构简式为:
⑴由苯丙酸诺龙的结构推测,它能 (填代号)。
a.使溴的四氯化碳溶液褪色 b.使酸性KMnO4溶液褪色
c.与银氨溶液发生银镜反应 d.与Na2CO3溶液作用生成CO2
苯丙酸诺龙的一种同分异构体A,在一定条件下可发生下列反应:
据以上信息回答⑵~⑷题:
⑵B→D的反应类型是 。
⑶C的结构简式为 。
⑷F→G的化学方程式是 。08山东有机试题08海南有机试题21.(11分)A、B、C、D1、D2、E、F、G、H均为有机化合物,请根据下列图示回答问题。
(1)直链有机化合物A的结构简式是_________________________;
(2)①的反应试剂和反应条件是____________________;
(3)③的反应类型是_______________________________;
(4)B生成C的化学方程式是_______________________________;
D1或D2生成E的化学方程式是_____________________________;
(5)G可应用于医疗、爆破等,由F生成G的化学方程式是_________________。
08江苏有机试题 2009福建省一检 2009福建省二检2010年福建省高考化学学科
自主命题走势
1.高中新课程实施推进情况 三、 2010年福建省高考化学学科自主命题走势 2.实验区高考试题内容特点
认真分析近两年的实验区高考化学试题,可以发现其内容特点为:
? (1)重视三大反应原理(氧化还原反应、离子反应和热化学反应)、三大化学理论(平衡理论、结构理论和电离理论)的考查。这是化学学科的核心内容,在高考试卷中占很大的比重(约占35%);
(2)重视常见元素及其重要化合物性质的考查。元素化合物内容是化学理论知识、化学实验与探究等的载体,在试题中也得到很好的体现(约占35%); (3)重视检验测量、制备、分离提纯等化学实验基本技能的考查。化学实验是化学研究的手段,是科学探究的主要方法,高考试卷比例约占20%。
?
(4)渗透思想内容(对待物质世界应有的观点和价值取向)的考查。试题通过创设问题情景,精选与人类、环境、能源方面的信息为素材,渗透STSE要求。 (5)更加强调对实验探究能力和信息加工能力的考查。这两个方面的能力是具有学习潜能的重要体现,是学习化学的基本能力要求。试卷通过设置探究性实验、以信息图表流程等形式呈现试题信息等形式考查这两个方面的能力。2009浙江2009浙江2009安徽2010高考复习迎考热点难点问题剖析1.如何看待高中新课程的课程内容的系统性? 许多老师反映:高中化学新课程的课程内容的系统性“差”。如元素化合物知识,过去的教材用元素周期律指导,分律前元素和律后元素进行编排,线索十分明显。现在的教材没有按照这样的线索来组织了;又如,化学反应速率和化学平衡、电化学、有机化学等内容,以前是系统安排在一起的,现在《化学2》安排一些,然后在《化学反应原理》、《有机化学基础》模块中又进一步学习等等。
如何看待高中新课程课程内容的系统性?我们认为,应该从学科、模块和主体等三个层面进行分析。认识不同,教学策略也不同。是“一步到位”还是“螺旋上升”?
2.如何正确认识化学反应原理模块中的新增内容?
老师们对于选修模块新增学科内容的看法大体上源于两种立场。一种立场是理解欢迎的立场,另一种截然相反的立场,是担心和排斥。认为新增内容是大学内容下放,增加学生负担,干嘛要弄到这里头来?担心学生理解不了,担心课时不够用,担心自己没有办法把握。
如何正确认识化学反应原理模块中的新增内容?我们认为,应该从学科发展和国际视野两个层面进行分析。认识不同,教学要求也不同。是“因循守旧”还是“与时俱进”?3.如何把握化学反应原理模块教学内容的深广度?
既然“化学反应原理”模块是新课程高考的必考模块,那么新增教学内容的深广度就显得至关重要。教学时,我们要思考:是依据“课标”,还是依据“教材”?是 依据“教材”,还是依据“教参”?是“定性分析”,还是“定量计算”?
高考考试命题指导思想要求
一是以能力测试为主导,考查考生对所学相关课程基础知识、基本技能的掌握程度和综合运用所学知识发现问题、分析问题和解决问题的能力。
二是要求考生关注科学技术、社会经济和生态环境的协调发展,理论联系实际。并能分析解决联系科学技术、社会经济和生态环境的问题。
(1)夯实基础,把握主干知识
“双基”是学生能力提高的基础,是探究问题、解决问题的依据,在教学中,应注意研究教学要求和考试大纲的变化,立足“双基”,引导学生对知识之间整体联系的认识,加强对物质的变化本质及规律的理解。
化学的主干知识包括:
在原子、分子层次上认识物质的组成、结构及其与物质性能的关系,学会识别物质;
在原子、分子层次上研究物质组成、结构的变化(化学变化或化学反应)规律、伴随这些变化的效应(能量和质量变化),了解怎样利用化学反应创造新物质。
掌握并利用化学符号系统描述物质的组成、结构、性质与变化。
了解化学研究的方法、手段,掌握基本的化学实验方法和技能。 对新课程高考复习教学的启发
化学1、2 的主干知识
学习化学的基本概念,了解化学研究的基本方法,认识化学科学的价值。
了解典型的、与人类生产生活密切相关的元素化合物、简单有机化合物的组成、性质与应用。
学习原子结构常识,认识元素周期律和周期表。认识化学键,了解分子和晶体的结构常识。
认识化学反应速率、限度、反应中的能量变化与转化。
化学反应原理的主干知识
了解化学反应的基本规律---了解决定化学反应方向的因素;认识化学反应的速率,了解影响反应速率的因素,知道反应速率的控制;认识化学反应限度,理解化学平衡及其移动,知道怎样提高反应的转化率;认识化学反应中的化学能与电能、热能的转化及其应用。
理解氧化还原反应的本质、规律,离子反应的本质、规律和描述方法,能从平衡的观点看待电离平衡、水解平衡、难溶电解质的溶解平衡。
物质结构与性质的基础知识
原子核外电子层结构及其与元素性质的关系;
认识分子的形成、分子空间构型,了解分子结构与物质性质的关系;
晶体结构常识,四类晶体结构与性质的关系。
有机化学基础的主干知识
有机物的结构分析、有机物结构与性质的关系
认识有机物化学反应,利用有机反应实现物质间的转化和进行有机合成 (2)注重知识学习与能力培养的统一
能力测试是高考不变的主题。综合能力的培养、提高不仅需要知识、技能、方法的传授,更需要帮助学生了解知识形成过程,寻找发现问题、探究问题的方法,引导、鼓励学生利用所学知识,通过实验手段、运用数学工具,学习如何分析、解决简单的实际问题,积累经验,从而有效地提高智力和综合能力。
(3)关注实验与探究能力的培养,重视展现知识的 形成过程
实验能力包括:
按实验方案用正确实验操作程序完成实验的能力、通过感官和仪器观察实验现象的能力;
记录、分析实验现象、对实验结果或实验数据进行处理得出结论的能力;
为说明、验证或解决某个问题设计特定的实验方案(包括绘制实验装置图)的能力。
高中理科课程的宗旨—— 提高学生的科学素养。
实验的作用——体验科学研究过程,了解科学探究方法
教学方法——将科学探究的过程和方法作为学生学习的对象,将学科核心知识融入科学探究、展现知识的形成过程中。
(4)加强培养良好的学习习惯和考试心理
答题中因考试心理状态不佳、审题不慎而造成的失分十分严重。
此外,因考场心理紧张,无法正常思考,导致答案张冠李戴,字迹潦草、胡乱涂写,没有掌握应试时间分配策略,试题没有做完等非智力因素引起的失分现象十分普遍。
不良的学习习惯而导致高考失分的现象不可忽视。因此,在平时教学中应有机渗透良好的学习习惯和健康心理素质的培养。(5)渗透新课程理念,建立与发展学科基本观念
(学科基本观念--形成终身受用的关于化学与化学品的基本判据)
认识世界是物质的。可见物质分成两类:实物和场,化学从原子与分子层次研究物质。物质是多样的,但其元素组成是统一的。
认识物质结构决定性质。任何物质对于人类和环境都有客观性与两面性。要正确认识物质性质、趋利避害、合理使用。
认识化学运动是物质七大基本运动形式之一。(机械运动、热运动、电磁运动、基本粒子运动、化学运动、生命运动、意识与思维)通过化学反应能够认识、修饰、合成物质。
认识合成是化学家改造世界、保护世界的有力手段。化学品和传统化学过程给人类带来了负面影响,要积极治理污染、发展绿色化学。
认识人类不能缺少驾驭智慧的智慧,即人文智慧。科学是一把神奇的钥匙,可以打开天堂之门,也可能打开地狱之门。化学原理反映客观规律。人们利用客观规律进行实践活动,考虑“能不能做”,更应考虑“该不该做”。
谢谢!
2009年7月高三培训2009年福建省理综测试卷化学试题分析
主要内容 一、 2009年福建省理综测试卷化学试题分析 二、 关于2009年福建省高考考试说明 三、 2010年福建省高考化学学科自主命题走势 四. 2010年高考复习迎考热点、难点问题剖析2009年福建省理综测试卷化学试题分析
一、2009年理综测试卷化学试题特点分析物质的熔点差异S+2H2SO4(浓)= 3SO2↑+2H2O氧化还原反应沉淀溶解平衡 H-C C-H 3:2试题特点1 .突出化学核心内容考查,强调基础性
试题不排除考查应知应会的基础内容,同时,将氧化还原反应、化学反应速率和化学平衡、电离与水解、以物质的量为中心的简单计算、化学实验设计与评价等主干、核心知识内容作为考查的重点。
2 .加强学科内综合,重视学科能力
试题以推断、信息迁移、实验探究等综合题型的方式,通过学生在解题思路中的知识纵横延伸,考查学生“接受、吸收、整合化学信息的能力,分析问题和解决(解答)化学问题的能力,化学实验的探究能力”。体现“注重学科的内在联系和知识的综合”和“能力立意”的命题原则。
3 .表现新课程的核心理念,凸显导向性
试题重视对基本方法、基本思想、化学观的考查。如:分类比较的方法、定量研究的方法、物质转化观、绿色化学思想等。
4. 命题规范,体现简约性
试题力求文字凝练、表述明晰、图示简洁、结构严谨,剔除花哨的铺垫和生硬的拼凑,注意控制试题的阅读量、思维量和答题量。有关化学计算因素的试题都引入了简化的数值,多处设问只要求采用表达式作答,避免了考生在有限的时间里进行繁杂的数值运算。 关于2009年福建省《考试说明》
一、编写考试说明的指导思想
1.体现考试说明对2009年高考理综试卷命题的权威性
2.对高中新课程教学的指导性
3.体现厅领导新课程高考“平稳过渡”的思路
二、考试说明的结构
Ⅰ. 命题指导思想
Ⅱ. 考试形式与试卷结构
Ⅲ. 考试内容
Ⅳ . 参考试卷 分值比例 物理︰化学︰生物=120︰100︰80
设置选考卷 理综试卷中另设选考卷,选考卷共5题,考生选答3题,其中,物理为2选1,化学为2选1,生物为一道必答题。
题量与题型 根据高考命题改革趋势和“3+X”高考经验,试卷设置学生答题题量与原课程高考理综试卷题量相当,题型基本一致,以求平稳过渡。
试卷难度 全卷难度值:0.60左右 物理:0.55~0.60 化学:0.60~0.65 生物:0.60~0.65
(一)对化学学习能力的要求
(二)对知识内容的要求层次
(三)考试范围和内容
(题型示例)Ⅲ.考试内容知识内容要求原
考
纲新
考
纲选考模块 化学科学特点和化学研究基本方法 ①了解化学主要特点是在原子、分子水平上认识物质;了 解化学可以识别、改变和创造分子。
②了解科学探究的基本过程,学习运用以实验和推理为基础的科学探究方法;认识化学是以实验为基础的一门科学。
③了解物质的组成、结构和性质的关系。了解化学反应的本质、基本原理以及能量变化等规律。
④了解定量研究的方法是化学发展为一门科学的重要标志。理解摩尔(mol)是物质的量的基本单位,可用于进行简单化学计算。
⑤了解科学、技术、社会的相互关系(如化学与生活、材料、能源、环境、生命过程、信息技术的关系等);了解在化工生产中遵循“绿色化学”思想的重要性。 必考内容部分09省二检 0.874 09省一检 0.69 09省一检 0.63 化学基本概念和基本理论 (1)物质的组成、性质和分类
(2)化学用语及常用计量
(3)溶液
(4)物质结构和元素周期律
必考内容部分09省二检 0.845 09省一检 0.67 09省一检 0.73 09宁夏高考 (5)化学反应与能量 ① 了解氧化还原反应的本质。了解常见的氧化还原反应。
② 了解化学反应中能量转化的原因,能说出常见的能量转化形式。
③ 了解化学能与热能的相互转化。了解吸热反应、放热反应、反应热等概念。
④ 了解热化学方程式的含义,能正确书写热化学方程式,能用盖斯定律进行有关反应热的简单计算。
⑤ 了解能源是人类生存和社会发展的重要基础。了解化学在解决能源危机中的重要作用。
⑥ 了解原电池和电解池的工作原理,能写出电极反应和电池反应方程式。了解常见化学电源的种类及其工作原理。
⑦ 理解金属发生电化学腐蚀的原因,了解金属腐蚀的危害和防止金属腐蚀的措施。必考内容部分省一检 0.4509省一检 0.4509省二检 0.695(6)化学反应速率和化学平衡 ① 了解化学反应速率的概念、反应速率的定量表示方法。
② 了解催化剂在生产、生活和科学研究领域中的重大作用。
③ 了解化学反应的可逆性。
④ 了解化学平衡建立的过程。了解化学平衡常数的含义,能够利用化学平衡常数计算反应物的转化率。
⑤ 理解外界条件(浓度、温度、压强、催化剂等)对反应速率和化学平衡的影响,认识其一般规律。
⑥ 了解化学反应速率和化学平衡的调控在生活、生产和科学研究领域中的重要作用。必考内容部分(7)电解质溶液
① 了解电解质、强电解质和弱电解质的概念。
② 了解电解质在水溶液中的电离,以及电解质溶液的导电性。
③ 了解弱电解质在水溶液中的电离平衡。
④ 了解水的电离和水的离子积常数。
⑤ 了解溶液pH的定义,能进行pH的简单计算。
⑥ 了解盐类水解的原理、影响盐类水解程度的主要因素、盐类水解的应用。(弱酸弱碱盐的水解不作要求)
⑦ 了解离子反应的概念、离子反应发生的条件。
⑧ 了解难溶电解质的溶解平衡。必考内容部分09省一检0.5809省二检0.62709省一检 0.44省一检 0.3609省二检 0.628省二检 0.509 09省二检 0.509 常见无机物及其应用 删——
“ⅠA和ⅡA族元素——典型的金属”
“从原子的核外电子排布,理解卤族元素(单质、化合物)的相似性和递变性”
“以硫酸为例,了解化工生产化学反应原理的确定”
“了解常见盐类的性质和用途”
常见金属元素(如Na、Al、Fe、Cu等)
“了解常见金属的活动顺序”、“了解常见金属及其重要化合物的主要性质及其应用”、“了解合金的概念及其重要应用”
常见非金属元素(如H、C、N、O、Si、S、Cl等)
“了解常见非金属单质及其重要化合物的主要性质及应用”;“了解常见非金属单质及其重要化合物对环境质量的影响”;以及“以上各部分知识的综合应用”
必考内容部分 09省二检 0.743 09省一检 0.54 常见有机物及其应用 ①了解有机化合物中碳的成键特征。
②了解甲烷、乙烯、苯等有机化合物的主要性质。
③了解乙烯、氯乙烯、苯的衍生物等在化工生产中的重要作用。
④了解乙醇、乙酸的组成和主要性质及重要应用。
⑤了解糖类、油脂、蛋白质的组成和主要性质及重要应用。
⑥了解常见高分子材料的合成反应及重要应用。
⑦了解有机物的同分异构现象,了解有机物反应的类型。
必考内容部分09省二检 0.924 09省一检 0. 81 化学实验基础 (1)了解化学实验是科学探究过程中的一种重要方法。
(2)了解化学实验室常用仪器的主要用途和使用方法。
(3)掌握化学实验的基本操作。能识别化学品安全使用
标识,了解实验室一般事故的预防和处理方法。
(4)掌握常见气体的实验室制法(包括所用试剂、仪器,
反应原理和收集方法)。
(5)了解常见离子的检验方法,能对常见的物质进行检
验、分离和提纯。
(6)能根据要求配制一定溶质质量分数、物质的量浓度
的溶液。了解测定溶液pH的方法。
(7)能根据实验试题要求,做到:① 设计、评价或改进
实验方案;②了解控制实验条件的方法;③ 分析或
处理实验数据,得出合理结论;④ 识别典型的实验
仪器装置图。
(8)以上各部分知识与技能的综合运用。必考内容部分09省一检 0.46 09省一检 0.41 09省二检 0.361 250mL容量瓶化学计算 对纯数学运算的要求降低,删去原考纲中的化学计算专题。将化学计算穿插分布在各模块的不同部分,强调计算与化学基本概念和理论、化学变化过程、工业流程等结合,体现计算为化学应用服务。 必考内容部分选考内容部分选考内容部分08宁夏物质结构35.[化学——选修物质结构与性质](15分)
X、Y、Z、Q、E五种元素中,X原子核外的M层中只有两对成对电子,Y原子核外的L层电子数是K层的两倍,Z是地壳内含量(质量分数)最高的元素,Q的核电荷数是X与Z的核电荷数之和,E在元素周期表的各元素中电负性最大。请回答下列问题:
(1)X、Y的元素符号依次为 、 ;
(2)XZ2与YZ2分子的立体结构分别是 和 ,相同条件下两者在水中的溶解度较大的是 (写分子式),理由是 ;
(3)Q的元素符号是 ,它属于第 周期,它的核外电子排布式为 ,在形成化合物时它的最高化合价为 ;
(4)用氢键表示式写出E的氢化物溶液中存在的所有氢键 。《有机化学基础》主
题
1
有机化合物的组成与结构主
题
2
烃及其衍生物的性质与应用主
题
3
糖类
、
氨基酸和蛋白质选考内容部分有机化化合物结构与性质的关系、有机反应与有机合成 有机化合物结构与性质的关系
碳键类型与有机物性质
官能团类型与有机物性质
分子中各基团的相互影响
分子空间结构对性质的影响有机化学反应原理
有机反应的主要类型
有机反应条件的控制
有机化合物合成基本思路和方法 《有机化学基础》
核心内容选考内容部分有机化合物的组成与结构 核心内容:认识有机化合物
认识有机化合物的组成和结构,了解自然界存在数千万种有机化合物的原因;
初步了解有机化合物的结构与性质的关系。
烃及其衍生物的性质与应用 核心内容:认识有机反应和转化
认识有机化合物性质,面对一个简单有机物时,知道怎样分析其具有的性质;
认识有机化学反应,了解有机化合物间的相互转化。3核心内容:认识有机化学的价值
了解糖类氨基酸和蛋白质的组成和性质特点以及其重要价值。
4核心内容:
知道学习有机化学的意义所在,认识有机合成的价值。33.[化学—有机化学基础]
苯丙酸诺龙是一种兴奋剂,结构简式为:
⑴由苯丙酸诺龙的结构推测,它能 (填代号)。
a.使溴的四氯化碳溶液褪色 b.使酸性KMnO4溶液褪色
c.与银氨溶液发生银镜反应 d.与Na2CO3溶液作用生成CO2
苯丙酸诺龙的一种同分异构体A,在一定条件下可发生下列反应:
据以上信息回答⑵~⑷题:
⑵B→D的反应类型是 。
⑶C的结构简式为 。
⑷F→G的化学方程式是 。08山东有机试题08海南有机试题21.(11分)A、B、C、D1、D2、E、F、G、H均为有机化合物,请根据下列图示回答问题。
(1)直链有机化合物A的结构简式是_________________________;
(2)①的反应试剂和反应条件是____________________;
(3)③的反应类型是_______________________________;
(4)B生成C的化学方程式是_______________________________;
D1或D2生成E的化学方程式是_____________________________;
(5)G可应用于医疗、爆破等,由F生成G的化学方程式是_________________。
08江苏有机试题 2009福建省一检 2009福建省二检2010年福建省高考化学学科
自主命题走势
1.高中新课程实施推进情况 三、 2010年福建省高考化学学科自主命题走势 2.实验区高考试题内容特点
认真分析近两年的实验区高考化学试题,可以发现其内容特点为:
? (1)重视三大反应原理(氧化还原反应、离子反应和热化学反应)、三大化学理论(平衡理论、结构理论和电离理论)的考查。这是化学学科的核心内容,在高考试卷中占很大的比重(约占35%);
(2)重视常见元素及其重要化合物性质的考查。元素化合物内容是化学理论知识、化学实验与探究等的载体,在试题中也得到很好的体现(约占35%); (3)重视检验测量、制备、分离提纯等化学实验基本技能的考查。化学实验是化学研究的手段,是科学探究的主要方法,高考试卷比例约占20%。
?
(4)渗透思想内容(对待物质世界应有的观点和价值取向)的考查。试题通过创设问题情景,精选与人类、环境、能源方面的信息为素材,渗透STSE要求。 (5)更加强调对实验探究能力和信息加工能力的考查。这两个方面的能力是具有学习潜能的重要体现,是学习化学的基本能力要求。试卷通过设置探究性实验、以信息图表流程等形式呈现试题信息等形式考查这两个方面的能力。2009浙江2009浙江2009安徽2010高考复习迎考热点难点问题剖析1.如何看待高中新课程的课程内容的系统性? 许多老师反映:高中化学新课程的课程内容的系统性“差”。如元素化合物知识,过去的教材用元素周期律指导,分律前元素和律后元素进行编排,线索十分明显。现在的教材没有按照这样的线索来组织了;又如,化学反应速率和化学平衡、电化学、有机化学等内容,以前是系统安排在一起的,现在《化学2》安排一些,然后在《化学反应原理》、《有机化学基础》模块中又进一步学习等等。
如何看待高中新课程课程内容的系统性?我们认为,应该从学科、模块和主体等三个层面进行分析。认识不同,教学策略也不同。是“一步到位”还是“螺旋上升”?
2.如何正确认识化学反应原理模块中的新增内容?
老师们对于选修模块新增学科内容的看法大体上源于两种立场。一种立场是理解欢迎的立场,另一种截然相反的立场,是担心和排斥。认为新增内容是大学内容下放,增加学生负担,干嘛要弄到这里头来?担心学生理解不了,担心课时不够用,担心自己没有办法把握。
如何正确认识化学反应原理模块中的新增内容?我们认为,应该从学科发展和国际视野两个层面进行分析。认识不同,教学要求也不同。是“因循守旧”还是“与时俱进”?3.如何把握化学反应原理模块教学内容的深广度?
既然“化学反应原理”模块是新课程高考的必考模块,那么新增教学内容的深广度就显得至关重要。教学时,我们要思考:是依据“课标”,还是依据“教材”?是 依据“教材”,还是依据“教参”?是“定性分析”,还是“定量计算”?
高考考试命题指导思想要求
一是以能力测试为主导,考查考生对所学相关课程基础知识、基本技能的掌握程度和综合运用所学知识发现问题、分析问题和解决问题的能力。
二是要求考生关注科学技术、社会经济和生态环境的协调发展,理论联系实际。并能分析解决联系科学技术、社会经济和生态环境的问题。
(1)夯实基础,把握主干知识
“双基”是学生能力提高的基础,是探究问题、解决问题的依据,在教学中,应注意研究教学要求和考试大纲的变化,立足“双基”,引导学生对知识之间整体联系的认识,加强对物质的变化本质及规律的理解。
化学的主干知识包括:
在原子、分子层次上认识物质的组成、结构及其与物质性能的关系,学会识别物质;
在原子、分子层次上研究物质组成、结构的变化(化学变化或化学反应)规律、伴随这些变化的效应(能量和质量变化),了解怎样利用化学反应创造新物质。
掌握并利用化学符号系统描述物质的组成、结构、性质与变化。
了解化学研究的方法、手段,掌握基本的化学实验方法和技能。 对新课程高考复习教学的启发
化学1、2 的主干知识
学习化学的基本概念,了解化学研究的基本方法,认识化学科学的价值。
了解典型的、与人类生产生活密切相关的元素化合物、简单有机化合物的组成、性质与应用。
学习原子结构常识,认识元素周期律和周期表。认识化学键,了解分子和晶体的结构常识。
认识化学反应速率、限度、反应中的能量变化与转化。
化学反应原理的主干知识
了解化学反应的基本规律---了解决定化学反应方向的因素;认识化学反应的速率,了解影响反应速率的因素,知道反应速率的控制;认识化学反应限度,理解化学平衡及其移动,知道怎样提高反应的转化率;认识化学反应中的化学能与电能、热能的转化及其应用。
理解氧化还原反应的本质、规律,离子反应的本质、规律和描述方法,能从平衡的观点看待电离平衡、水解平衡、难溶电解质的溶解平衡。
物质结构与性质的基础知识
原子核外电子层结构及其与元素性质的关系;
认识分子的形成、分子空间构型,了解分子结构与物质性质的关系;
晶体结构常识,四类晶体结构与性质的关系。
有机化学基础的主干知识
有机物的结构分析、有机物结构与性质的关系
认识有机物化学反应,利用有机反应实现物质间的转化和进行有机合成 (2)注重知识学习与能力培养的统一
能力测试是高考不变的主题。综合能力的培养、提高不仅需要知识、技能、方法的传授,更需要帮助学生了解知识形成过程,寻找发现问题、探究问题的方法,引导、鼓励学生利用所学知识,通过实验手段、运用数学工具,学习如何分析、解决简单的实际问题,积累经验,从而有效地提高智力和综合能力。
(3)关注实验与探究能力的培养,重视展现知识的 形成过程
实验能力包括:
按实验方案用正确实验操作程序完成实验的能力、通过感官和仪器观察实验现象的能力;
记录、分析实验现象、对实验结果或实验数据进行处理得出结论的能力;
为说明、验证或解决某个问题设计特定的实验方案(包括绘制实验装置图)的能力。
高中理科课程的宗旨—— 提高学生的科学素养。
实验的作用——体验科学研究过程,了解科学探究方法
教学方法——将科学探究的过程和方法作为学生学习的对象,将学科核心知识融入科学探究、展现知识的形成过程中。
(4)加强培养良好的学习习惯和考试心理
答题中因考试心理状态不佳、审题不慎而造成的失分十分严重。
此外,因考场心理紧张,无法正常思考,导致答案张冠李戴,字迹潦草、胡乱涂写,没有掌握应试时间分配策略,试题没有做完等非智力因素引起的失分现象十分普遍。
不良的学习习惯而导致高考失分的现象不可忽视。因此,在平时教学中应有机渗透良好的学习习惯和健康心理素质的培养。(5)渗透新课程理念,建立与发展学科基本观念
(学科基本观念--形成终身受用的关于化学与化学品的基本判据)
认识世界是物质的。可见物质分成两类:实物和场,化学从原子与分子层次研究物质。物质是多样的,但其元素组成是统一的。
认识物质结构决定性质。任何物质对于人类和环境都有客观性与两面性。要正确认识物质性质、趋利避害、合理使用。
认识化学运动是物质七大基本运动形式之一。(机械运动、热运动、电磁运动、基本粒子运动、化学运动、生命运动、意识与思维)通过化学反应能够认识、修饰、合成物质。
认识合成是化学家改造世界、保护世界的有力手段。化学品和传统化学过程给人类带来了负面影响,要积极治理污染、发展绿色化学。
认识人类不能缺少驾驭智慧的智慧,即人文智慧。科学是一把神奇的钥匙,可以打开天堂之门,也可能打开地狱之门。化学原理反映客观规律。人们利用客观规律进行实践活动,考虑“能不能做”,更应考虑“该不该做”。
谢谢!
同课章节目录
