5-1 质量守恒定律
图片预览





文档简介
课件14张PPT。欢迎各位老师莅临指导宜兴市陶都中学 汤小锋复习旧课用符号表达式表示下列反应
1.铁在氧气中燃烧
2.在空气中燃烧红磷
3、碳在空气中燃烧5-1 质量守恒定律学习目标:
1、知识与技能:理解质量守恒定律以及守恒的原因;
2、过程与方法:
(1)通过对化学反应实质的分析及质量守恒原因的分析,培养学生的研究问题能力和逻辑推理能力;
(2)通过对实验的观察与操作,培养学生的动手实验能力及观察分析能力;
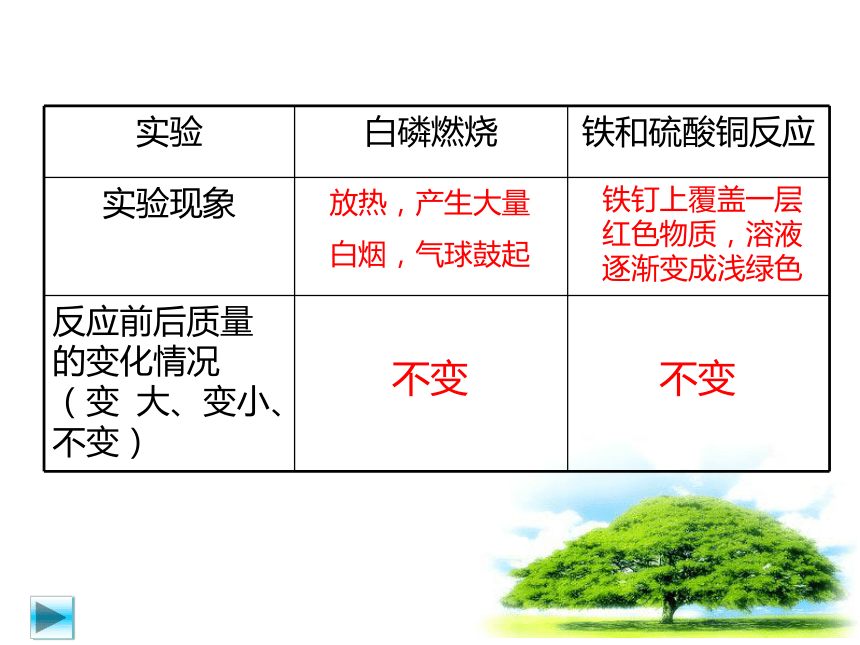
(3)使学生初步认识科学探究的意义及基本过程,能提出问题,并进行探究活动。放热,产生大量
白烟,气球鼓起不变铁钉上覆盖一层
红色物质,溶液
逐渐变成浅绿色不变从上面的两组实验中,同学们你们能得出什么样
的结论呢? 参加化学反应的各物质的质
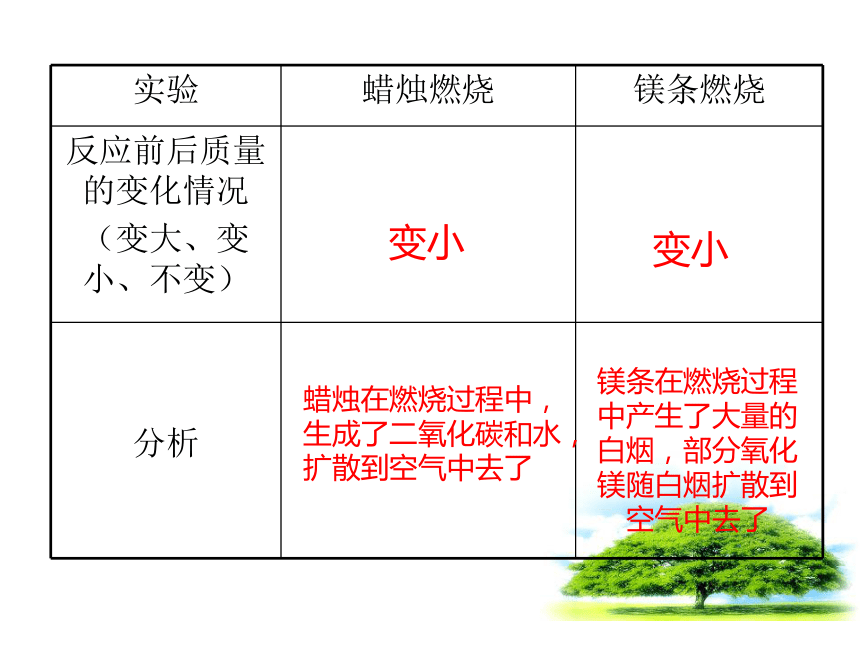
量总和等于反应后生成的各物质的质量总和。 想一想???○ ○质量守恒定律:思考?质量守恒定律是否对任何化学反应都适用呢?变小变小蜡烛在燃烧过程中,生成了二氧化碳和水,扩散到空气中去了镁条在燃烧过程中产生了大量的白烟,部分氧化镁随白烟扩散到空气中去了讨论上面两个实验的结果与你实验前的预测相同吗?为什么会出现这样的实验结果?小 结:只要是化学反应,必定符合质量守恒定律。大家欣赏并思考思考一下在化学反应前后物质的质量总和为什 么会守恒呢?1、原子是化学变化中的最小微粒归纳结论元素的种类没变种类数目质量课堂练习:
1、32g硫和32g氧气恰好完全反应,生成二氧化硫的质量为 克,现有32g的硫在64g的氧气中燃烧,完全反应后生成二氧化硫的质量为 克
2、12g的碳在空气中完全燃烧后,生成的二氧化碳的质量一定 12g.
3、12g的碳在氧气中完全燃烧后,生成二氧化碳的质量为44g,则参加反应的氧气的质量为 克。
64>3264本课小结:理解并掌握质量守恒定律及守恒的原因下课了,再见!!
1.铁在氧气中燃烧
2.在空气中燃烧红磷
3、碳在空气中燃烧5-1 质量守恒定律学习目标:
1、知识与技能:理解质量守恒定律以及守恒的原因;
2、过程与方法:
(1)通过对化学反应实质的分析及质量守恒原因的分析,培养学生的研究问题能力和逻辑推理能力;
(2)通过对实验的观察与操作,培养学生的动手实验能力及观察分析能力;
(3)使学生初步认识科学探究的意义及基本过程,能提出问题,并进行探究活动。放热,产生大量
白烟,气球鼓起不变铁钉上覆盖一层
红色物质,溶液
逐渐变成浅绿色不变从上面的两组实验中,同学们你们能得出什么样
的结论呢? 参加化学反应的各物质的质
量总和等于反应后生成的各物质的质量总和。 想一想???○ ○质量守恒定律:思考?质量守恒定律是否对任何化学反应都适用呢?变小变小蜡烛在燃烧过程中,生成了二氧化碳和水,扩散到空气中去了镁条在燃烧过程中产生了大量的白烟,部分氧化镁随白烟扩散到空气中去了讨论上面两个实验的结果与你实验前的预测相同吗?为什么会出现这样的实验结果?小 结:只要是化学反应,必定符合质量守恒定律。大家欣赏并思考思考一下在化学反应前后物质的质量总和为什 么会守恒呢?1、原子是化学变化中的最小微粒归纳结论元素的种类没变种类数目质量课堂练习:
1、32g硫和32g氧气恰好完全反应,生成二氧化硫的质量为 克,现有32g的硫在64g的氧气中燃烧,完全反应后生成二氧化硫的质量为 克
2、12g的碳在空气中完全燃烧后,生成的二氧化碳的质量一定 12g.
3、12g的碳在氧气中完全燃烧后,生成二氧化碳的质量为44g,则参加反应的氧气的质量为 克。
64>3264本课小结:理解并掌握质量守恒定律及守恒的原因下课了,再见!!
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
