第一单元 从铝土矿到铝合金
图片预览











文档简介
课件33张PPT。瑞安市隆山高中 张克龙第三专题从矿物到基础材料铝的性质 单元一第二课时近50年来,铝已成为世界上仅次于铁的广泛应用金属。一架飞机约由70%的铝及其合金构成。据报道,国外已铺设有铝质的火车轨道,其能量损耗约为普通铁轨的一半。
2006年8月份,全球铝产量为252万吨,中国的铝产量为64万吨。请你与同桌同学细细观察周围哪些物品是铝制品。阅读下列铝的用途归纳铝的物理性质铝在电器制造工业、电线电缆工业中有着广泛的应用。
在工业上铝制造各种热交换器、散热材料、炊具
铝用于制卷拉门
用于包装香烟、糖果、胶卷等。
铝粉俗称银粉,跟某些油料混合制成防锈油漆
常用来制造高质量的反射镜,如太阳灶反射镜
广播室、现代化大型建筑室内的天花板等常用铝来制作。一、铝单质的物理性质有良好的导电性、导热性、较软、延展性,银白色有金属光泽的固体,
对光反射性能好、吸音性能与音响效果好、熔沸点较高,密度较小。 铝很软,但铝制品大多较硬,有些几乎相当于钢材,且密度较小,因此广泛用于飞机、汽车、人造卫星等的制造。 知道为什么吗? 铝合金的性能强度和硬度高、密度小、易成型 硬铝的发现
20世纪初,德国化学家威姆制得含有铜、镁和锰的铝合金,很偶然的机会他发现凡是经过加热到高温,然后在水中急速冷却过的这种铝合金,在7天内,硬度和强度值是不断地增加的,且铜、镁和锰的含量及合金加热到高温的温度对合金的强度与硬度有影响。随后威姆继续开展研究。威姆把这种铝合金称为“硬铝”。硬铝的出现,给铝的应用开辟了更广阔的市场,成为一种在高科技领域中有特殊用途的材料。
问题:根据上面的描述,请你猜想威姆继续研究了哪些什么问题后,获得了工业制备“硬铝”具体方法。研究一:“硬铝”中含铜、镁及锰的含量
研究二: 加入其它元素是否会提高“硬铝” 的性能呢?
研究三:加热到多高的温度再放入水中冷却,所达到的增硬增强效果最好。 生活中你遇到的铝制品中的铝,你认为它的化学性质是稳定的呢,还是活泼的呢? 请你搜索初中科学学过的或者在你周围有
关证明铝单质的化学性质活泼的素材,同时
请你与你同桌一起浏览书65页至67
页内容,寻找与铝的化学性质有关的
铝的用途?
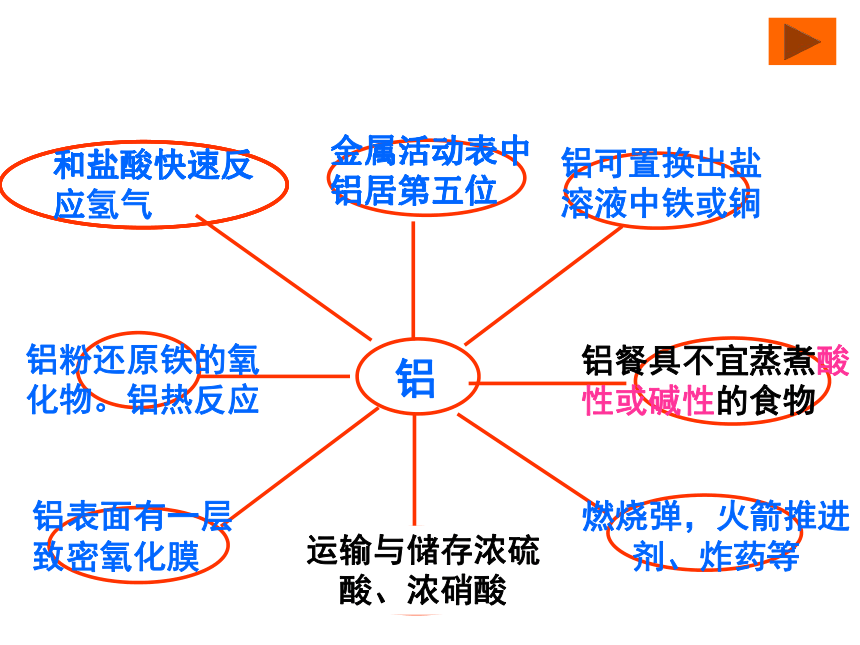
铝单质的化学性质是稳定的吗?金属活动表中铝居第五位和盐酸快速反应金属活动表中铝居第五位和盐酸快速反应铝铝可置换出盐溶液中铁或铜铝餐具不宜蒸煮酸性或碱性的食物铝表面有一层致密氧化膜铝粉还原铁的氧化物。铝热反应运输与储存浓硫酸、浓硝酸燃烧弹,火箭推进剂、炸药等金属活动表中铝居第五位和盐酸快速反应氢气观察与思考 实验一: 铝与稀盐酸,硫酸铜溶液反应
(在点滴板的孔穴中分别加入稀盐酸与硫酸铜溶液, 再取一片铝片分别加入到稀盐酸与硫酸铜溶液中参加反应。描述实验现象,写出化学方程式)实验现象:铝条逐渐溶解,有无色气体逸出实验现象:铝条表面上附着红色的铜实验二:铝与浓硫酸、浓硝酸的反应现象解释:铝的表面快速形成一层致密的氧化 膜,阻止内部金属进一步的反应应用:工业运输浓硫酸、浓硝酸用铝槽车。
储存浓硫酸、浓硝酸用铝罐观察与思考铝粉在氧气中燃烧现象:铝粉剧烈燃烧,发出耀眼的白光,
放出大量的热,生成白色固体。应用:制造燃烧弹、信号弹、火箭推进剂等燃烧弹火箭推进剂观察与思考 常温下,铝与空气中的氧气反应形成一层致密的氧化物薄膜,因此铝制品具有良好的抗腐蚀性。氧化膜 通过刚才的几个实验,你认为铝单质活泼吗?那么为什么铝制品是稳定的呢?铝表面氧化膜加厚与着色 电解法是增加铝表面的氧化膜厚度与着色的方法。如图所示,电压20V,电流1.5A,电解20分钟。取出铝片放入到硫酸铜溶液中30分钟,取出再放入到(NH4)2S溶液中,铝表面会有CuS沉积,取出冲洗,可以观察到铝表面呈绿色。为使颜色保持长久,可以放到沸水中煮沸10分钟。a问题1:根据与电源正极相连的电极会发生氧化反应,而
与负极相连的电极发生还原反应,请判断哪一极铝片会有
氧化膜生成?
问题2:写出CuSO4与(NH4)2S生成CuS沉淀的离子方程式?剧烈反应,从漏斗上方产生美丽的焰火,从漏斗底部,流出火红的液滴,在沙中很快变成黑色固体现象:观察与思考铝热反应铝热反应问题:每个铝原子失几个电子?
氧化铁中哪中哪一种元素得电子?
用氧化亚铁或四氧化三铁可以替代氧化铁吗?应用一:焊接铁轨应用二:
铝热剂还用于定向爆破时高温熔化建筑物中的钢筋迁移:应用:冶炼铜或冶炼钒、铬、锰等难熔金属。问题探究铝制餐具的说明书上写着不宜蒸煮或长期存放有酸性或碱性的食物,为什么? 实验三:铝与氢氧化钠溶液反应在点滴板的孔穴中加入氢氧化钠溶液,再将铝片放入到盛适量氢氧化钠溶液中,观察现象?思考这种气体是什么物质,如何检验? Al-3e_ = Al3+问题:结合本节课的内容,思考哪些微粒在一定条件下可以获得铝原子的最外层电子问题:元素的化学性质是由原子结构决定的。根据本节课的知识,你认为铝单质活泼吗?每个铝原子失去几个电子? 问题:请你画出铝原子结构示意图,用原子结构解释铝为什么铝原子易失去三个电子?请你用化学式表达每个铝原子失去三个电子的化学过程?
请同学们一点时间细细琢磨这节课的内容,这节课你获得了些什么知识,你对哪些感兴趣,你还想知道些什么,请你发表你的思考? 本节课,我们从生活实际出发,讨论了金属铝的物理性质。通过生活实际结合化学实验探究了铝的化学性质。
本节课的重点是铝与非金属单质、金属氧化物、酸、碱盐溶液的反应。
通过上述所有化学反应,表现了铝具有强还原性。 现有浓硫酸,硫酸铜,铝条及必要仪器,请你与你的同桌一起思考形成氧化膜后的铝,化学性质稳定1.下列关于铝的叙述中,不正确的是:
A.铝属于金属单质,不与任何碱反应
B.铝是地壳中含量最多的金属
C.在常温下,铝不能与氧气反应
D.铝既能与酸反应,也能与强碱反应A C12.铝具有较强的抗腐蚀性,主要因为:
A.铝不活泼??? B.具有两性??
C.铝与氧气在常温下不反应
D.铝表面在常温下能形成一层致密的氧化物薄膜D谢谢!作业:完成书上67页至68页的练习与实践3.将一个用金属铝做的易拉罐内充满CO2,然后往罐内注入足量的NaOH溶液,立即用胶布密封罐口。经过一段时间后,罐壁内凹而瘪,再过一段时间后,瘪了的罐壁重新鼓起来(用化学方程式表示)。
(1)罐壁内凹而瘪的原因是_____;
(2)罐再鼓起的原因是______。4.在加入铝粉能放出H2的溶液中,一定能大量 共存的离子组是:A.K+、Na+、CO32-、SO42- B.NH4+、Na+、Cl-、NO3-
C.K+、Na+、Cl-、SO42- D.K+、HCO3-、Cl- 、SO42-C
2006年8月份,全球铝产量为252万吨,中国的铝产量为64万吨。请你与同桌同学细细观察周围哪些物品是铝制品。阅读下列铝的用途归纳铝的物理性质铝在电器制造工业、电线电缆工业中有着广泛的应用。
在工业上铝制造各种热交换器、散热材料、炊具
铝用于制卷拉门
用于包装香烟、糖果、胶卷等。
铝粉俗称银粉,跟某些油料混合制成防锈油漆
常用来制造高质量的反射镜,如太阳灶反射镜
广播室、现代化大型建筑室内的天花板等常用铝来制作。一、铝单质的物理性质有良好的导电性、导热性、较软、延展性,银白色有金属光泽的固体,
对光反射性能好、吸音性能与音响效果好、熔沸点较高,密度较小。 铝很软,但铝制品大多较硬,有些几乎相当于钢材,且密度较小,因此广泛用于飞机、汽车、人造卫星等的制造。 知道为什么吗? 铝合金的性能强度和硬度高、密度小、易成型 硬铝的发现
20世纪初,德国化学家威姆制得含有铜、镁和锰的铝合金,很偶然的机会他发现凡是经过加热到高温,然后在水中急速冷却过的这种铝合金,在7天内,硬度和强度值是不断地增加的,且铜、镁和锰的含量及合金加热到高温的温度对合金的强度与硬度有影响。随后威姆继续开展研究。威姆把这种铝合金称为“硬铝”。硬铝的出现,给铝的应用开辟了更广阔的市场,成为一种在高科技领域中有特殊用途的材料。
问题:根据上面的描述,请你猜想威姆继续研究了哪些什么问题后,获得了工业制备“硬铝”具体方法。研究一:“硬铝”中含铜、镁及锰的含量
研究二: 加入其它元素是否会提高“硬铝” 的性能呢?
研究三:加热到多高的温度再放入水中冷却,所达到的增硬增强效果最好。 生活中你遇到的铝制品中的铝,你认为它的化学性质是稳定的呢,还是活泼的呢? 请你搜索初中科学学过的或者在你周围有
关证明铝单质的化学性质活泼的素材,同时
请你与你同桌一起浏览书65页至67
页内容,寻找与铝的化学性质有关的
铝的用途?
铝单质的化学性质是稳定的吗?金属活动表中铝居第五位和盐酸快速反应金属活动表中铝居第五位和盐酸快速反应铝铝可置换出盐溶液中铁或铜铝餐具不宜蒸煮酸性或碱性的食物铝表面有一层致密氧化膜铝粉还原铁的氧化物。铝热反应运输与储存浓硫酸、浓硝酸燃烧弹,火箭推进剂、炸药等金属活动表中铝居第五位和盐酸快速反应氢气观察与思考 实验一: 铝与稀盐酸,硫酸铜溶液反应
(在点滴板的孔穴中分别加入稀盐酸与硫酸铜溶液, 再取一片铝片分别加入到稀盐酸与硫酸铜溶液中参加反应。描述实验现象,写出化学方程式)实验现象:铝条逐渐溶解,有无色气体逸出实验现象:铝条表面上附着红色的铜实验二:铝与浓硫酸、浓硝酸的反应现象解释:铝的表面快速形成一层致密的氧化 膜,阻止内部金属进一步的反应应用:工业运输浓硫酸、浓硝酸用铝槽车。
储存浓硫酸、浓硝酸用铝罐观察与思考铝粉在氧气中燃烧现象:铝粉剧烈燃烧,发出耀眼的白光,
放出大量的热,生成白色固体。应用:制造燃烧弹、信号弹、火箭推进剂等燃烧弹火箭推进剂观察与思考 常温下,铝与空气中的氧气反应形成一层致密的氧化物薄膜,因此铝制品具有良好的抗腐蚀性。氧化膜 通过刚才的几个实验,你认为铝单质活泼吗?那么为什么铝制品是稳定的呢?铝表面氧化膜加厚与着色 电解法是增加铝表面的氧化膜厚度与着色的方法。如图所示,电压20V,电流1.5A,电解20分钟。取出铝片放入到硫酸铜溶液中30分钟,取出再放入到(NH4)2S溶液中,铝表面会有CuS沉积,取出冲洗,可以观察到铝表面呈绿色。为使颜色保持长久,可以放到沸水中煮沸10分钟。a问题1:根据与电源正极相连的电极会发生氧化反应,而
与负极相连的电极发生还原反应,请判断哪一极铝片会有
氧化膜生成?
问题2:写出CuSO4与(NH4)2S生成CuS沉淀的离子方程式?剧烈反应,从漏斗上方产生美丽的焰火,从漏斗底部,流出火红的液滴,在沙中很快变成黑色固体现象:观察与思考铝热反应铝热反应问题:每个铝原子失几个电子?
氧化铁中哪中哪一种元素得电子?
用氧化亚铁或四氧化三铁可以替代氧化铁吗?应用一:焊接铁轨应用二:
铝热剂还用于定向爆破时高温熔化建筑物中的钢筋迁移:应用:冶炼铜或冶炼钒、铬、锰等难熔金属。问题探究铝制餐具的说明书上写着不宜蒸煮或长期存放有酸性或碱性的食物,为什么? 实验三:铝与氢氧化钠溶液反应在点滴板的孔穴中加入氢氧化钠溶液,再将铝片放入到盛适量氢氧化钠溶液中,观察现象?思考这种气体是什么物质,如何检验? Al-3e_ = Al3+问题:结合本节课的内容,思考哪些微粒在一定条件下可以获得铝原子的最外层电子问题:元素的化学性质是由原子结构决定的。根据本节课的知识,你认为铝单质活泼吗?每个铝原子失去几个电子? 问题:请你画出铝原子结构示意图,用原子结构解释铝为什么铝原子易失去三个电子?请你用化学式表达每个铝原子失去三个电子的化学过程?
请同学们一点时间细细琢磨这节课的内容,这节课你获得了些什么知识,你对哪些感兴趣,你还想知道些什么,请你发表你的思考? 本节课,我们从生活实际出发,讨论了金属铝的物理性质。通过生活实际结合化学实验探究了铝的化学性质。
本节课的重点是铝与非金属单质、金属氧化物、酸、碱盐溶液的反应。
通过上述所有化学反应,表现了铝具有强还原性。 现有浓硫酸,硫酸铜,铝条及必要仪器,请你与你的同桌一起思考形成氧化膜后的铝,化学性质稳定1.下列关于铝的叙述中,不正确的是:
A.铝属于金属单质,不与任何碱反应
B.铝是地壳中含量最多的金属
C.在常温下,铝不能与氧气反应
D.铝既能与酸反应,也能与强碱反应A C12.铝具有较强的抗腐蚀性,主要因为:
A.铝不活泼??? B.具有两性??
C.铝与氧气在常温下不反应
D.铝表面在常温下能形成一层致密的氧化物薄膜D谢谢!作业:完成书上67页至68页的练习与实践3.将一个用金属铝做的易拉罐内充满CO2,然后往罐内注入足量的NaOH溶液,立即用胶布密封罐口。经过一段时间后,罐壁内凹而瘪,再过一段时间后,瘪了的罐壁重新鼓起来(用化学方程式表示)。
(1)罐壁内凹而瘪的原因是_____;
(2)罐再鼓起的原因是______。4.在加入铝粉能放出H2的溶液中,一定能大量 共存的离子组是:A.K+、Na+、CO32-、SO42- B.NH4+、Na+、Cl-、NO3-
C.K+、Na+、Cl-、SO42- D.K+、HCO3-、Cl- 、SO42-C
