《化学能转化为电能》教学课件
图片预览






文档简介
课件21张PPT。《化学能转化为电能》常见的电池干电池蓄电池手机用锂离子电池 摄相机电池电池释放的电能来自哪里?想一想探究实验:Zn与Cu插入稀H2SO4的现象与解释 稀H2SO4稀H2SO4Cu
Zn
稀H2SO4Cu
Zn
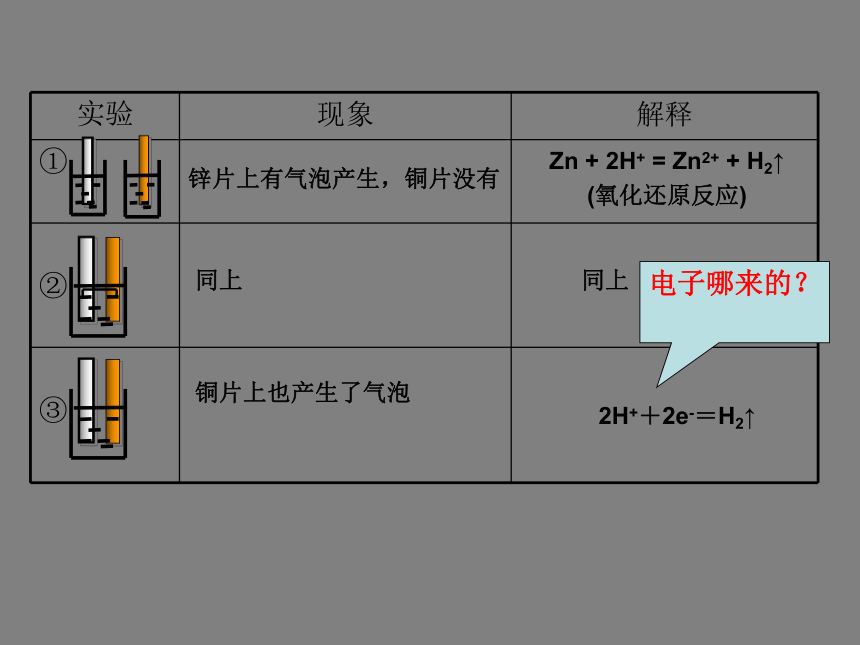
稀H2SO4导线[实验①][实验②][实验③]锌片上有气泡产生,铜片没有同上Zn + 2H+ = Zn2+ + H2↑
(氧化还原反应)
电子哪来的?同上铜片上也产生了气泡2H++2e-=H2↑推 测Zn CuZn - 2e- = Zn2+2H++2e-=H2↑如何通过实验证明?Cu
Zn
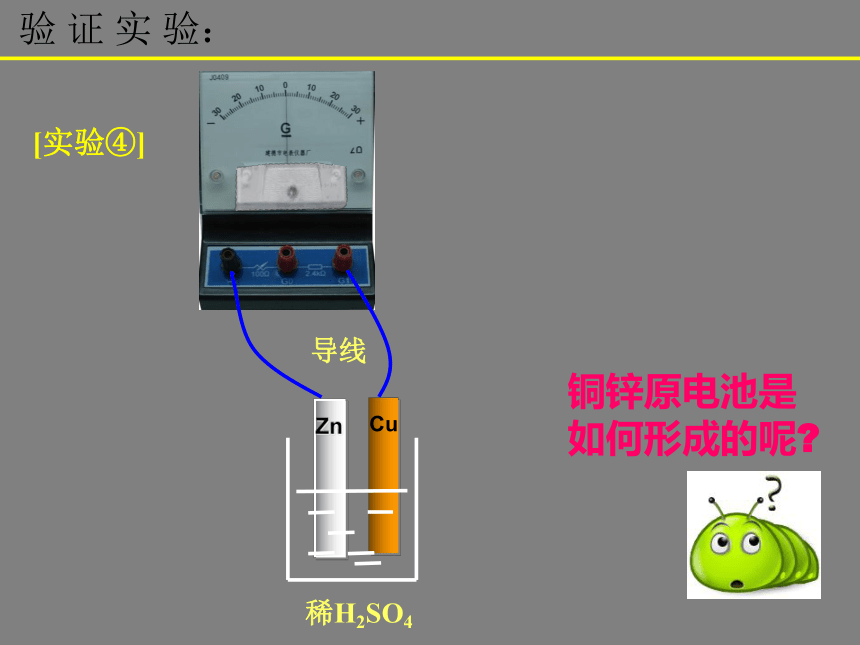
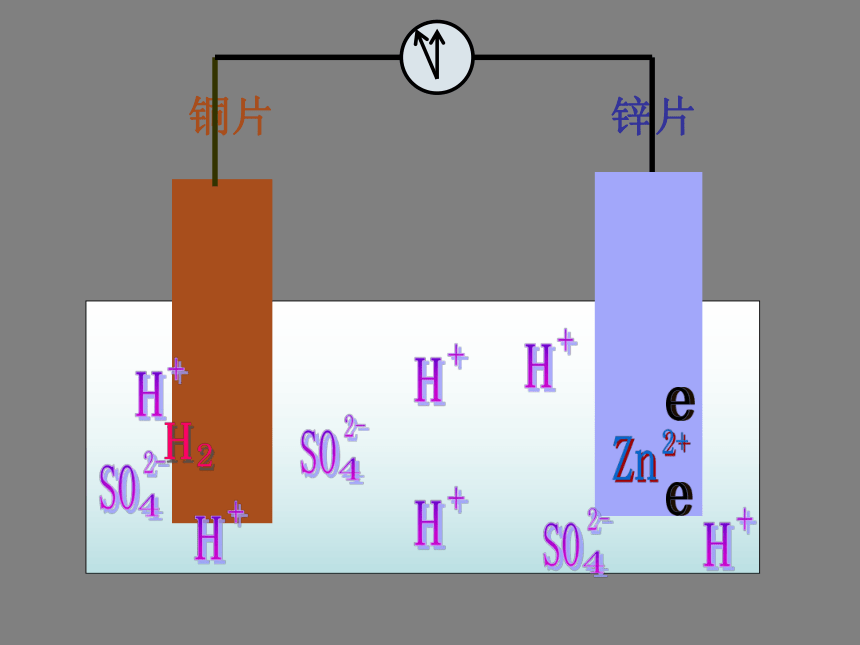
稀H2SO4验 证 实 验:[实验④]导线铜锌原电池是如何形成的呢? ee铜片锌片结 论 IZn CuZn - 2e- = Zn2+2H++2e-=H2↑一、原电池:(通过氧化还原反应)将化学能转化为电能的装置。 (氧化反应)(还原反应)负极正极电池总反应: Zn + 2H+ = Zn2+ + H2↑正极材料有参加反应吗?电池总反应:应是负极材料与溶液中氧化剂的氧化还原反应,正极不参加反应。二、原电池工作原理:
氧化还原反应分别在负、正两极进行,还原剂(负极)所失去的电子通过导线进入正极,转移给(附近溶液中)氧化剂,从而产生电流。结论1:必须有两个相连的电极
连接形式可以直接接触或用导线连接探究实验:原电池的构成条件第一组:判断能否构成原电池(改变连接方式)不可以 不可以 可以Cu
Zn
稀H2SO4稀H2SO4Cu
Zn
导线Zn
稀H2SO4Zn
稀H2SO4[实验⑤]可以第二组:观察电流计指针是否偏转? (改变电极)探究实验:原电池的构成条件稀H2SO4偏转[实验⑥]其中,较活泼金属作为负极;较不活泼金属或非金属(石墨)作为正极。稀H2SO4不偏转
Zn
Zn
[实验⑦]稀H2SO4偏转如何判断正极、负极呢?结论2:第三组:观察电流计指针是否偏转?(改变溶液:100ml烧杯中)探究实验:原电池的构成条件不偏转偏转结论3:必须有电解质溶液(酸、碱、盐的水溶液)
CuSO4溶液无水乙醇[实验⑨]偏转稀H2SO4[实验⑧]溶液中阳离子移向正极,阴离子移向负极。第四组:判断电流计指针是否能偏转?探究实验:原电池的构成条件不偏转结论4:电极与电解质溶液应构成闭合回路。偏转稀H2SO4三、原电池构成条件-----------“两极一液成回路”
Cu
√课 堂 练 习1、判断:以下装置能否构成原电池?并写出电极反应式
Cu
H2SO4溶液C
Fe
CuSO4溶液Fe
Zn
汽油A B C D Zn
ZnSO4溶液Fe
√××
2、由A、B、C、D四种金属按下表中装置进行实验,已知用C与B相连作电极放入硫酸铜溶液中B溶解。根据实验现象填表:?
C
Zn
NH4Cl、ZnCl2
混合溶液[小灯泡会不会亮?]学 以 致 用总 结
负
极
正
极
一、原电池构成条件:两极一液成回路金属或非
金属导体相对活
泼的金属总结二、原电池工作原理:锌铜作业1. 动手题:搜集废干电池并拆开,弄清它的构造及原理。
2. 动脑题:书本P46第1题谢谢
Zn
稀H2SO4Cu
Zn
稀H2SO4导线[实验①][实验②][实验③]锌片上有气泡产生,铜片没有同上Zn + 2H+ = Zn2+ + H2↑
(氧化还原反应)
电子哪来的?同上铜片上也产生了气泡2H++2e-=H2↑推 测Zn CuZn - 2e- = Zn2+2H++2e-=H2↑如何通过实验证明?Cu
Zn
稀H2SO4验 证 实 验:[实验④]导线铜锌原电池是如何形成的呢? ee铜片锌片结 论 IZn CuZn - 2e- = Zn2+2H++2e-=H2↑一、原电池:(通过氧化还原反应)将化学能转化为电能的装置。 (氧化反应)(还原反应)负极正极电池总反应: Zn + 2H+ = Zn2+ + H2↑正极材料有参加反应吗?电池总反应:应是负极材料与溶液中氧化剂的氧化还原反应,正极不参加反应。二、原电池工作原理:
氧化还原反应分别在负、正两极进行,还原剂(负极)所失去的电子通过导线进入正极,转移给(附近溶液中)氧化剂,从而产生电流。结论1:必须有两个相连的电极
连接形式可以直接接触或用导线连接探究实验:原电池的构成条件第一组:判断能否构成原电池(改变连接方式)不可以 不可以 可以Cu
Zn
稀H2SO4稀H2SO4Cu
Zn
导线Zn
稀H2SO4Zn
稀H2SO4[实验⑤]可以第二组:观察电流计指针是否偏转? (改变电极)探究实验:原电池的构成条件稀H2SO4偏转[实验⑥]其中,较活泼金属作为负极;较不活泼金属或非金属(石墨)作为正极。稀H2SO4不偏转
Zn
Zn
[实验⑦]稀H2SO4偏转如何判断正极、负极呢?结论2:第三组:观察电流计指针是否偏转?(改变溶液:100ml烧杯中)探究实验:原电池的构成条件不偏转偏转结论3:必须有电解质溶液(酸、碱、盐的水溶液)
CuSO4溶液无水乙醇[实验⑨]偏转稀H2SO4[实验⑧]溶液中阳离子移向正极,阴离子移向负极。第四组:判断电流计指针是否能偏转?探究实验:原电池的构成条件不偏转结论4:电极与电解质溶液应构成闭合回路。偏转稀H2SO4三、原电池构成条件-----------“两极一液成回路”
Cu
√课 堂 练 习1、判断:以下装置能否构成原电池?并写出电极反应式
Cu
H2SO4溶液C
Fe
CuSO4溶液Fe
Zn
汽油A B C D Zn
ZnSO4溶液Fe
√××
2、由A、B、C、D四种金属按下表中装置进行实验,已知用C与B相连作电极放入硫酸铜溶液中B溶解。根据实验现象填表:?
C
Zn
NH4Cl、ZnCl2
混合溶液[小灯泡会不会亮?]学 以 致 用总 结
负
极
正
极
一、原电池构成条件:两极一液成回路金属或非
金属导体相对活
泼的金属总结二、原电池工作原理:锌铜作业1. 动手题:搜集废干电池并拆开,弄清它的构造及原理。
2. 动脑题:书本P46第1题谢谢
