《沉淀溶解平衡的应用》教学课件
图片预览






文档简介
课件20张PPT。沉淀溶解平衡的应用1.什么是沉淀溶解平衡?2.溶度积规则:
(1).当 Q > Ksp,平衡向生成沉淀的方向移动——沉淀生成。
(2).当 Q = Ksp,沉淀与溶解达平衡状态。
(3).当 Q < Ksp,平衡向沉淀溶解的方向移动——沉淀溶解。 沉淀的生成和溶解本质上是沉淀溶解平衡的移动。
改变离子浓度的大小,可以使反应向所需要的方向转化。Ksp=c m (An + ) c n(Bm-)一、知识回顾二、应用
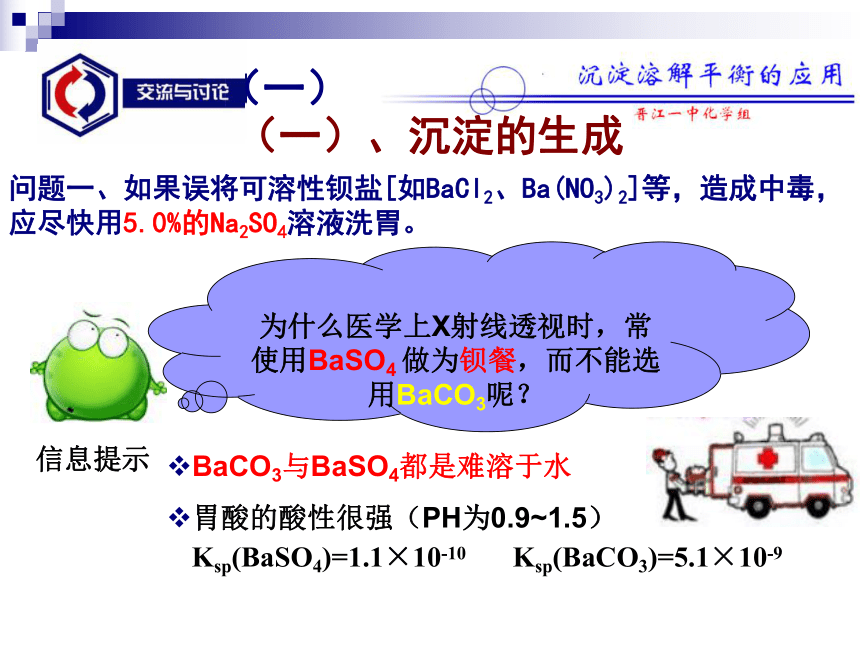
为什么医学上X射线透视时,常使用BaSO4 做为钡餐,而不能选用BaCO3呢?问题一、如果误将可溶性钡盐[如BaCl2、Ba(NO3)2]等,造成中毒,应尽快用5.0%的Na2SO4溶液洗胃。(一)、沉淀的生成(一)已知:Ksp(BaSO4)=1.1×10-10;
Ksp(BaCO3)=5.1×10-9Ba2+浓度增大问题解析CuSO4(aq)
Fe3+问题三、将溶液的PH调节到3~4,可除去硫酸铜溶液中的铁离子 (一)我们的目标是——没有蛀牙!(二) 中华口腔医学会公布的最新数据表明,龋齿病在我国依然是一个严峻的问题,据步完全统计,我国儿童乳牙龋齿病的患病率达到66%,成人恒牙龋齿病的患病率达到61%,老年人的龋齿病患病率为75%。 吃糖过多,真的容易导致龋齿吗?信息:
1.牙齿表面的牙釉质起着保护牙齿的作用,其主要成分为Ca5(PO4)3OH(羟基磷灰石), 它是一种难溶电解质,Ksp=6.8×10-37mol9·L-9;
2.残留在牙齿上的糖发酵会产生H+;(二)(二)、沉淀的溶解沉淀溶解的方法:沉淀溶解平衡体系中的离子浓度减小,即Q1.少吃糖或吃糖后及时漱口;2.使用牙膏补充Ca2+。3.使用含氟牙膏。氟磷灰石更能抵抗酸的侵蚀,使牙齿更坚固??(三)、沉淀的转化沉淀转化规律(一)问题:溶解能力较弱难溶物能否在一定条件下转化为溶解能力较强难溶物?BaSO4能否转化为BaCO3?(三)沉淀转化规律(二)当两种难溶物溶解能力差别不大时:溶解能力相对较弱的物质在一定条件下能转化为溶解能力相对较强的物质。锅炉水垢既会降低燃料的利用率,造成能源浪费,也会影响锅炉的使用寿命,造成安全隐患,因此要定期清除。(四) 锅炉水垢中含有CaSO4, 可用Na2CO3溶液处理,使之转化为疏松、易溶于酸的CaCO3,再用酸除去。
1. 分析将CaSO4转化为CaCO3的原理;
2. 写出除去CaSO4的化学方程式和离子方程式。(四)今天你学到什么?沉淀溶解平衡的应用
1.沉淀的生成;
2.沉淀的溶解;
2.沉淀的转化;信息:溶洞的主要成分是碳酸钙。【解析】三、拓展视野解决沉淀溶解平衡问题的一般思路“看到”微粒“找到”平衡“想到”移动依据 1.平衡移动规律
2.溶度积规则
作业必做题:课本:P86:1、3
导学:P106A组:7、8、9
选做题:导学:P106B组:6、7、9
(1).当 Q > Ksp,平衡向生成沉淀的方向移动——沉淀生成。
(2).当 Q = Ksp,沉淀与溶解达平衡状态。
(3).当 Q < Ksp,平衡向沉淀溶解的方向移动——沉淀溶解。 沉淀的生成和溶解本质上是沉淀溶解平衡的移动。
改变离子浓度的大小,可以使反应向所需要的方向转化。Ksp=c m (An + ) c n(Bm-)一、知识回顾二、应用
为什么医学上X射线透视时,常使用BaSO4 做为钡餐,而不能选用BaCO3呢?问题一、如果误将可溶性钡盐[如BaCl2、Ba(NO3)2]等,造成中毒,应尽快用5.0%的Na2SO4溶液洗胃。(一)、沉淀的生成(一)已知:Ksp(BaSO4)=1.1×10-10;
Ksp(BaCO3)=5.1×10-9Ba2+浓度增大问题解析CuSO4(aq)
Fe3+问题三、将溶液的PH调节到3~4,可除去硫酸铜溶液中的铁离子 (一)我们的目标是——没有蛀牙!(二) 中华口腔医学会公布的最新数据表明,龋齿病在我国依然是一个严峻的问题,据步完全统计,我国儿童乳牙龋齿病的患病率达到66%,成人恒牙龋齿病的患病率达到61%,老年人的龋齿病患病率为75%。 吃糖过多,真的容易导致龋齿吗?信息:
1.牙齿表面的牙釉质起着保护牙齿的作用,其主要成分为Ca5(PO4)3OH(羟基磷灰石), 它是一种难溶电解质,Ksp=6.8×10-37mol9·L-9;
2.残留在牙齿上的糖发酵会产生H+;(二)(二)、沉淀的溶解沉淀溶解的方法:沉淀溶解平衡体系中的离子浓度减小,即Q
1. 分析将CaSO4转化为CaCO3的原理;
2. 写出除去CaSO4的化学方程式和离子方程式。(四)今天你学到什么?沉淀溶解平衡的应用
1.沉淀的生成;
2.沉淀的溶解;
2.沉淀的转化;信息:溶洞的主要成分是碳酸钙。【解析】三、拓展视野解决沉淀溶解平衡问题的一般思路“看到”微粒“找到”平衡“想到”移动依据 1.平衡移动规律
2.溶度积规则
作业必做题:课本:P86:1、3
导学:P106A组:7、8、9
选做题:导学:P106B组:6、7、9
