《盐类的水解》教学课件
图片预览





文档简介
课件18张PPT。盐类的水解专题三 第三单元(第一课时)酸的水溶液呈酸性;
碱的水溶液呈碱性;
盐的水溶液的酸碱性如何呢?实验探究请同学们利用现有条件测定下面三种盐溶液的酸碱性:CH3COONa、NH4Cl、NaCl溶液,并将实验结果填入下面表格。盐溶液的酸碱性?思考与讨论 2、正盐溶液中为什么会含有H+、OH-?3、为什么不同正盐的水溶液中c(H+)、c(OH-)
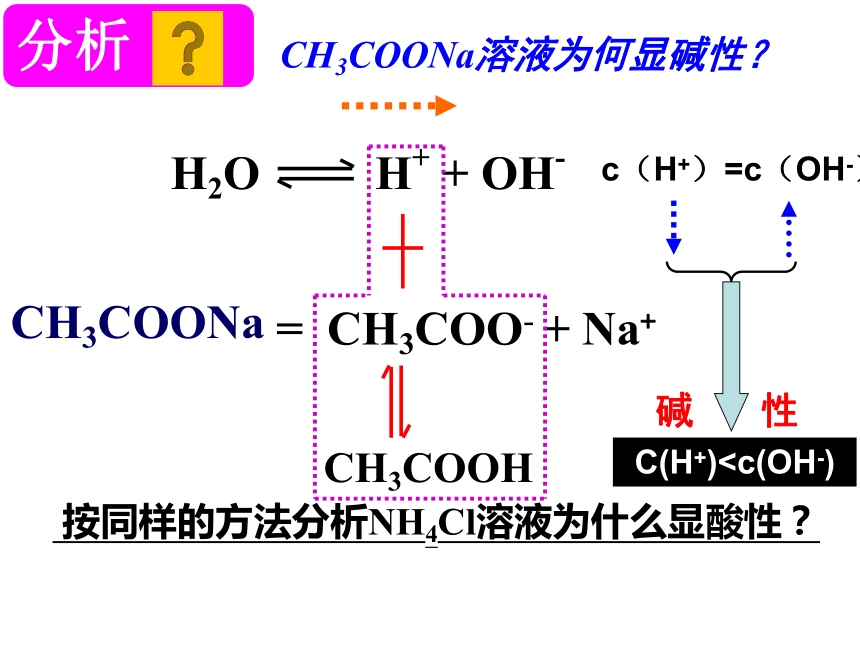
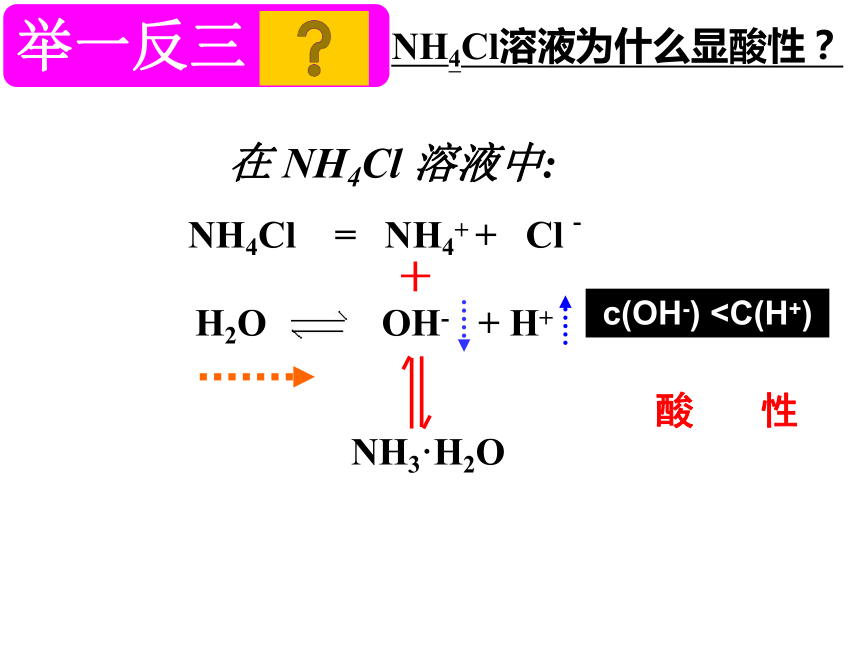
大小关系会不同? 1、溶液呈现酸或者碱性的根本原因是什么?为什么有的盐溶液显酸性,有的显碱性?思考与讨论4、 CH3COONa溶液存在哪些离子?CH3COONa溶液为何显碱性?5、 这些离子能否发生反应?6、 若能反应,对水的电离平衡有何影响?7、 溶液中H+和OH- 的浓度如何变化?CH3COONa溶液为何显碱性?CH3COONa= CH3COO- + Na+ H2Oc(H+)=c(OH-)碱 性 按同样的方法分析NH4Cl溶液为什么显酸性?NH4Cl溶液为什么显酸性?H2O OH- + H+ NH4Cl = NH4+ + Cl -NH3·H2O在 NH4Cl 溶液中:酸 性c(OH-)无__不水解;
谁__谁水解;
谁__显谁性。
(填强或弱)弱弱强弱 在溶液中,不能发生水解的离子是( )
A、ClO - B、CO32-
C、Fe3+ D、SO42--D随堂练习有弱才水解 无弱不水解
谁弱谁水解 谁强显谁性下列盐的水溶液中,哪些呈酸性( )
哪些呈碱性( )
(1) FeCl3 (2) NaClO (3) (NH4)2SO4
(4) AgNO3 (5)Na2S (6)K2SO413425随堂练习小结:这节课我们学习了什么?会判断盐溶液的酸碱性并分析原因盐的水解的定义、实质和规律小结:这节课我们要掌握什么能力?课后思考CH3COONH4是弱酸弱碱盐,其水溶液的酸碱性如何? 为什么?作业:1、书本P80:3、4和5:只做预测盐溶液的酸碱性(交)2、练习册:
必做:P100:A级:1 B级:4;
选做:P101:A:10再见
碱的水溶液呈碱性;
盐的水溶液的酸碱性如何呢?实验探究请同学们利用现有条件测定下面三种盐溶液的酸碱性:CH3COONa、NH4Cl、NaCl溶液,并将实验结果填入下面表格。盐溶液的酸碱性?思考与讨论 2、正盐溶液中为什么会含有H+、OH-?3、为什么不同正盐的水溶液中c(H+)、c(OH-)
大小关系会不同? 1、溶液呈现酸或者碱性的根本原因是什么?为什么有的盐溶液显酸性,有的显碱性?思考与讨论4、 CH3COONa溶液存在哪些离子?CH3COONa溶液为何显碱性?5、 这些离子能否发生反应?6、 若能反应,对水的电离平衡有何影响?7、 溶液中H+和OH- 的浓度如何变化?CH3COONa溶液为何显碱性?CH3COONa= CH3COO- + Na+ H2Oc(H+)=c(OH-)碱 性 按同样的方法分析NH4Cl溶液为什么显酸性?NH4Cl溶液为什么显酸性?H2O OH- + H+ NH4Cl = NH4+ + Cl -NH3·H2O在 NH4Cl 溶液中:酸 性c(OH-)
谁__谁水解;
谁__显谁性。
(填强或弱)弱弱强弱 在溶液中,不能发生水解的离子是( )
A、ClO - B、CO32-
C、Fe3+ D、SO42--D随堂练习有弱才水解 无弱不水解
谁弱谁水解 谁强显谁性下列盐的水溶液中,哪些呈酸性( )
哪些呈碱性( )
(1) FeCl3 (2) NaClO (3) (NH4)2SO4
(4) AgNO3 (5)Na2S (6)K2SO413425随堂练习小结:这节课我们学习了什么?会判断盐溶液的酸碱性并分析原因盐的水解的定义、实质和规律小结:这节课我们要掌握什么能力?课后思考CH3COONH4是弱酸弱碱盐,其水溶液的酸碱性如何? 为什么?作业:1、书本P80:3、4和5:只做预测盐溶液的酸碱性(交)2、练习册:
必做:P100:A级:1 B级:4;
选做:P101:A:10再见
