《化学平衡状态》教学课件
图片预览





文档简介
课件22张PPT。选修四 化学反应原理化学平衡状态 某工厂实验室研究在加入催化剂和加热的条件下在1L的容器中,将10mol SO2与5mol O2混合进行反应,测得数据列表如下:SO2与O2没有完全反应,反应有限度
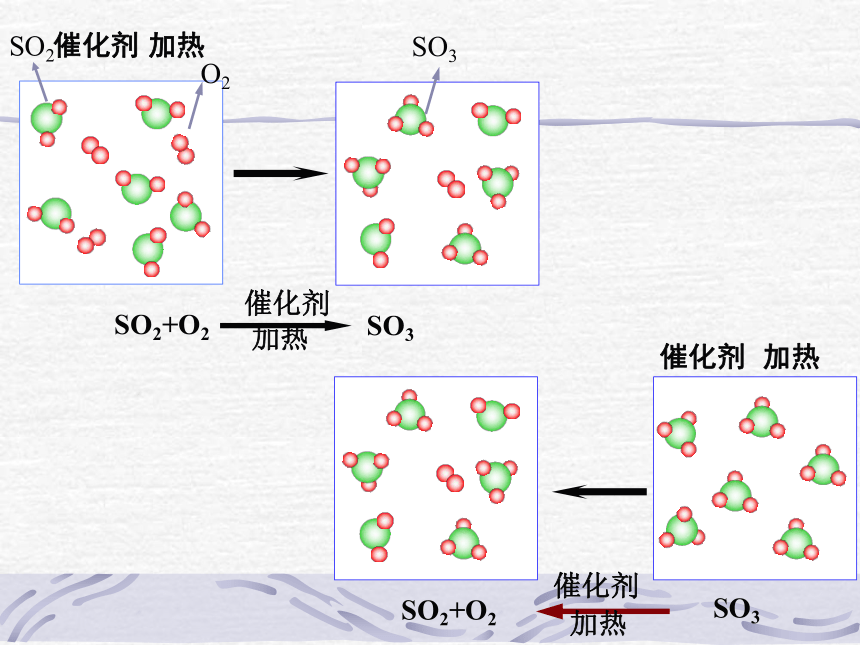
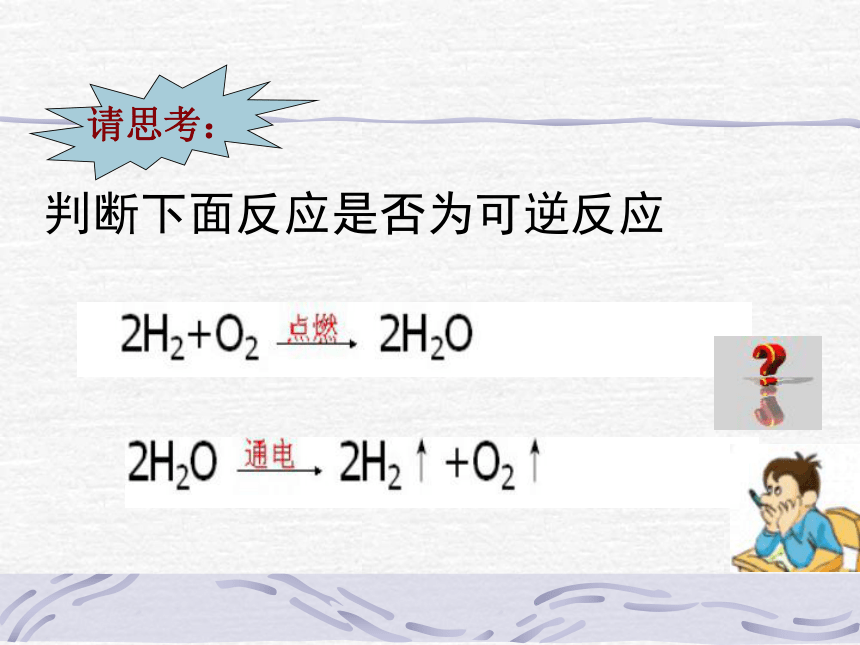
1、化学反应的限度 ①定义:化学反应所能达到或完成的最大程度。②意义:化学反应的限度决定了反应物在该反应条件下的最大转化率SO2与O2反应的动画SO2催化剂 加热催化剂 加热催化剂 加热正反应逆反应2.可逆反应在同一条件下,正反应和逆反应均能同时进行的反应判断下面反应是否为可逆反应
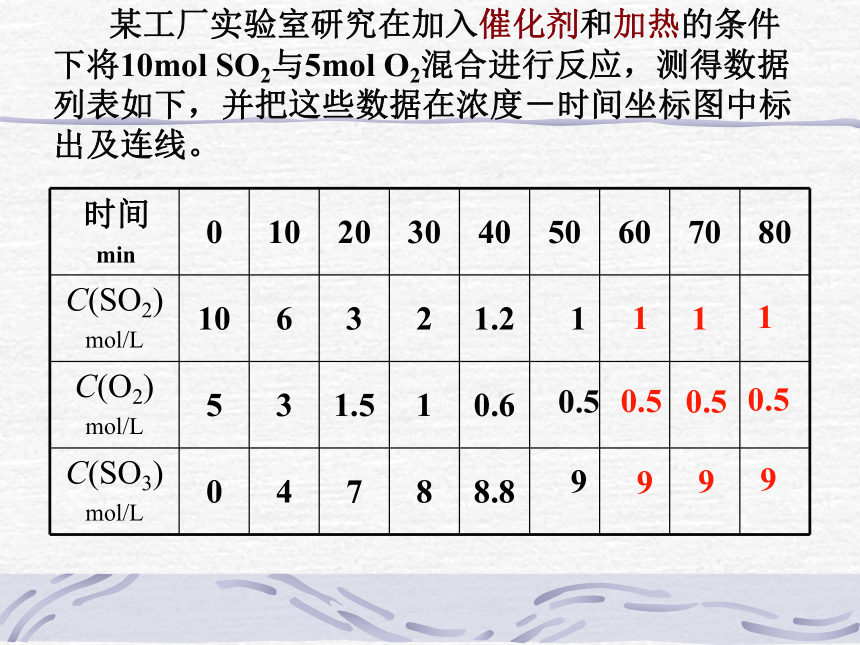
请思考: 某工厂实验室研究在加入催化剂和加热的条件下将10mol SO2与5mol O2混合进行反应,测得数据列表如下,并把这些数据在浓度-时间坐标图中标出及连线。80010203040506070C/mol/Lt/min V正 V逆2、在50—80min中 SO2、O2、SO3物质的量浓度如何变化?正、逆反应的速率如何变化?
1、在0—50min 中各物质的浓度如何变化?正、逆反应的速率如何变化?请思考:50—80min C(SO2) 、C(O2) 、 C(SO3)不再变化正反应速率等于逆反应速率反应仍然进行化学平衡状态 (1) 定义:指在一定条件下的可逆反应里,正反应速率和逆反应速率相等,反应物和生成物的浓度不再随时间而发生变化的状态。 3、化学平衡状态(化学平衡) 50—80min C(SO2) 、 C(O2) 、 C(SO3) 不再变化正反应速率等于逆反应速率反应仍然进行②反应物、生成物浓度不再变化(固定)动等定(2)化学平衡的特征化学平衡状态③正反应速率等于逆反应速率④条件发生改变,平衡发生改变变①动态平衡混合物体系中各成分的含量
1)各物质的物质的量一定
2)各物质的质量或各物质的质量分数一定
3)各气体的体积或体积分数一定
4)气体总压强、总体积、总物质的量一定
平衡不一定平衡平衡平衡状态的判断 正、逆反应速率的关系
1)在单位时间内消耗了 m mol A,同时生成了m mol A;
2)在单位时间内生成了 n mol B,同时消耗了q mol D。
3)在单位时间内消耗了 n mol B,同时生成了p mol C;
4)v (A)∶v (B) ∶ v (C) ∶ v (D) = m ∶ n ∶ p ∶ q ;
5)在单位时间内消耗了 n mol B,同时消耗了p mol C;v正=v逆 ,平衡v正=v逆 ,平衡未达到平衡时也符合此关系均指v逆,不一定平衡均指v正,不一定平衡平衡状态的判断 在一定温度下,向 a L 密闭容器中加入1 mol X 气体和 2 mol Y 气体,发生如下反应:
X (g) + 2 Y (g) 3 Z (g)此反应达到平衡的标志是( )
A、容器内压强不随时间变化
B、容器内各物质的浓度不随时间变化
C、容器内 X、Y、Z 的浓度之比为1∶2∶3
D、单位时间消耗 2 mol Y的同时生成 3 mol Z B正反应速率等
于逆反应速率 等各物质浓度不变 定小试牛刀 小结1.化学反应的限度
2.可逆反应
3.化学平衡状态的定义和特征
练习●活动12SO2+O2 2SO3催化剂 在一密闭容器中加入 2 molSO2和 1 mol18O2,
(1)最终反应容器中有哪些物质?
(2)18O存在于哪些物质中?SO2、O2 、SO3SO2、O2 、SO3练习●活动2 在一定温度下,可逆反应 A (g) + 3 B (g) 2 C (g)达到平衡的标志是( ) A.C的生成速率与C的分解速率相等 B.单位时间内生成 n mol A的同时生成 3n mol B C.A、B、C的浓度不再发生变化 D.A、B、C的物质的量之比为1:3:2各物质浓度不变 定正反应速率等
于逆反应速率 等A、C工业上用下面的反应合成氨气
N2 + 3H2 2NH3,下列描述能否说明该反应已经处于化学平衡状态:( )
① N2生成速率=N2消耗速率
② NH3的物质的量浓度不再发生变化
③单位时间内消耗1molN2 ,同时生成2molNH3
④固定容积内气体的压强不随时间变化
⑤单位时间内消耗1molN2 ,同时生成 3molH2
⑥3v正(H2) = 2v逆(NH3) 等定正反应速率等
于逆反应速率 各物质浓度不变 练习●活动3① ② ④ ⑤在一定条件下,某容器中充入N2和H2合成NH3,以下叙述错误的是( )
A.开始反应时,正反应速率最大,逆反应速率为零
B.随着反应的进行,正反应速率逐渐减小,最后减小为零
C.随着反应的进行逆反应速率逐渐增大,后保持恒定
D.随着反应的进行,正反应速率逐渐减小,最后与逆反应速率相等且都保持恒定练习●活动4B作业与延伸《名校学案》 P34 第2题
P37 第3题
1、化学反应的限度 ①定义:化学反应所能达到或完成的最大程度。②意义:化学反应的限度决定了反应物在该反应条件下的最大转化率SO2与O2反应的动画SO2催化剂 加热催化剂 加热催化剂 加热正反应逆反应2.可逆反应在同一条件下,正反应和逆反应均能同时进行的反应判断下面反应是否为可逆反应
请思考: 某工厂实验室研究在加入催化剂和加热的条件下将10mol SO2与5mol O2混合进行反应,测得数据列表如下,并把这些数据在浓度-时间坐标图中标出及连线。80010203040506070C/mol/Lt/min V正 V逆2、在50—80min中 SO2、O2、SO3物质的量浓度如何变化?正、逆反应的速率如何变化?
1、在0—50min 中各物质的浓度如何变化?正、逆反应的速率如何变化?请思考:50—80min C(SO2) 、C(O2) 、 C(SO3)不再变化正反应速率等于逆反应速率反应仍然进行化学平衡状态 (1) 定义:指在一定条件下的可逆反应里,正反应速率和逆反应速率相等,反应物和生成物的浓度不再随时间而发生变化的状态。 3、化学平衡状态(化学平衡) 50—80min C(SO2) 、 C(O2) 、 C(SO3) 不再变化正反应速率等于逆反应速率反应仍然进行②反应物、生成物浓度不再变化(固定)动等定(2)化学平衡的特征化学平衡状态③正反应速率等于逆反应速率④条件发生改变,平衡发生改变变①动态平衡混合物体系中各成分的含量
1)各物质的物质的量一定
2)各物质的质量或各物质的质量分数一定
3)各气体的体积或体积分数一定
4)气体总压强、总体积、总物质的量一定
平衡不一定平衡平衡平衡状态的判断 正、逆反应速率的关系
1)在单位时间内消耗了 m mol A,同时生成了m mol A;
2)在单位时间内生成了 n mol B,同时消耗了q mol D。
3)在单位时间内消耗了 n mol B,同时生成了p mol C;
4)v (A)∶v (B) ∶ v (C) ∶ v (D) = m ∶ n ∶ p ∶ q ;
5)在单位时间内消耗了 n mol B,同时消耗了p mol C;v正=v逆 ,平衡v正=v逆 ,平衡未达到平衡时也符合此关系均指v逆,不一定平衡均指v正,不一定平衡平衡状态的判断 在一定温度下,向 a L 密闭容器中加入1 mol X 气体和 2 mol Y 气体,发生如下反应:
X (g) + 2 Y (g) 3 Z (g)此反应达到平衡的标志是( )
A、容器内压强不随时间变化
B、容器内各物质的浓度不随时间变化
C、容器内 X、Y、Z 的浓度之比为1∶2∶3
D、单位时间消耗 2 mol Y的同时生成 3 mol Z B正反应速率等
于逆反应速率 等各物质浓度不变 定小试牛刀 小结1.化学反应的限度
2.可逆反应
3.化学平衡状态的定义和特征
练习●活动12SO2+O2 2SO3催化剂 在一密闭容器中加入 2 molSO2和 1 mol18O2,
(1)最终反应容器中有哪些物质?
(2)18O存在于哪些物质中?SO2、O2 、SO3SO2、O2 、SO3练习●活动2 在一定温度下,可逆反应 A (g) + 3 B (g) 2 C (g)达到平衡的标志是( ) A.C的生成速率与C的分解速率相等 B.单位时间内生成 n mol A的同时生成 3n mol B C.A、B、C的浓度不再发生变化 D.A、B、C的物质的量之比为1:3:2各物质浓度不变 定正反应速率等
于逆反应速率 等A、C工业上用下面的反应合成氨气
N2 + 3H2 2NH3,下列描述能否说明该反应已经处于化学平衡状态:( )
① N2生成速率=N2消耗速率
② NH3的物质的量浓度不再发生变化
③单位时间内消耗1molN2 ,同时生成2molNH3
④固定容积内气体的压强不随时间变化
⑤单位时间内消耗1molN2 ,同时生成 3molH2
⑥3v正(H2) = 2v逆(NH3) 等定正反应速率等
于逆反应速率 各物质浓度不变 练习●活动3① ② ④ ⑤在一定条件下,某容器中充入N2和H2合成NH3,以下叙述错误的是( )
A.开始反应时,正反应速率最大,逆反应速率为零
B.随着反应的进行,正反应速率逐渐减小,最后减小为零
C.随着反应的进行逆反应速率逐渐增大,后保持恒定
D.随着反应的进行,正反应速率逐渐减小,最后与逆反应速率相等且都保持恒定练习●活动4B作业与延伸《名校学案》 P34 第2题
P37 第3题
