《共价键的形成》教学课件
图片预览









文档简介
课件31张PPT。专题3微粒间作用力第三单元 共价键化学键离子键共价键金属键复习2、共价键的成键微粒:1、共价键:通过必修2的学习,我们了解到:是原子间通过共用电子对所形成的的化学键。原子非金属单质
共价化合物
离子化合物a、电子式:4、共价键的表示方法请与离子化合物的电子式进行比较注意:1、共价化合物的电子式不出现方括号和离子电荷数。
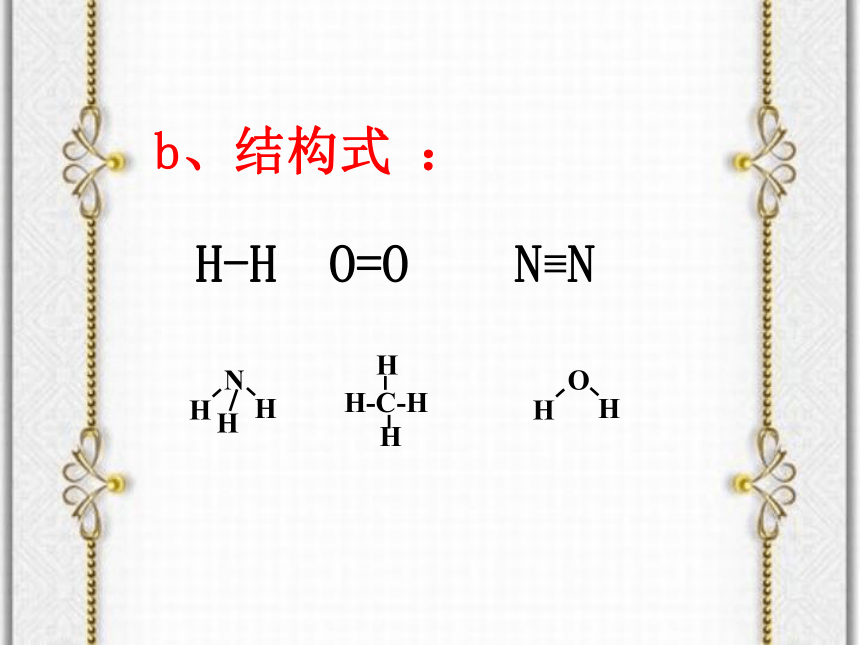
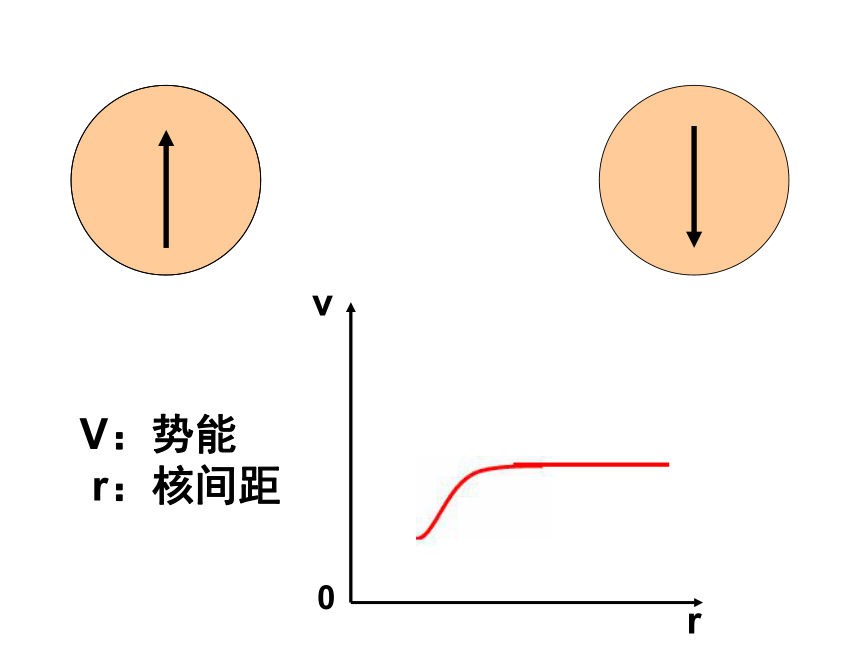
2、不要混淆“用电子式表示结构”和“用电子式表示 形成过程。b、结构式 :练习: 用电子式表示HCl、K2S的形成过程值得思考的问题:1、是否所有的非金属单质中都存在共价键?2、2个氢原子一定能形成氢分子吗?两个核外电子自旋方向相反的氢原子靠近vr0V:势能
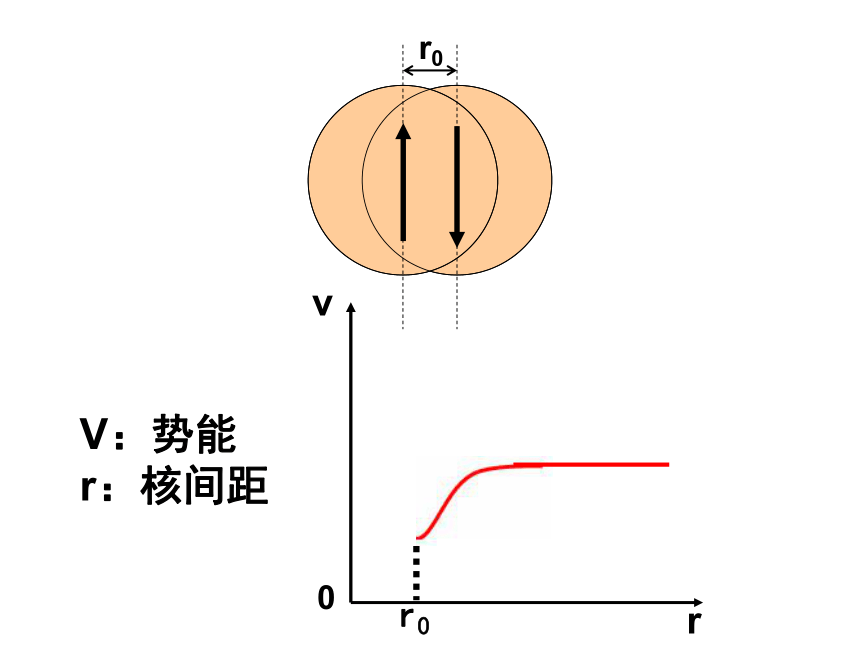
r:核间距r0vr0r0V:势能
r:核间距r0vr0r0V:势能
r:核间距r0vr0r0V:势能
r:核间距两个核外电子自旋方向相同的氢原子靠近vr0V:势能
r:核间距一、共价键的形成本质 成键原子相互接近时,原子轨道发生 ,自旋方向 的 电子形成 ,两原子核间的电子密度 ,体系的能量 。重叠相反未成对 共用电子对增 加降低返回二、共价键的形成条件A、有自旋方向相反的未成对电子。B、原子轨道要实现最大限度的重叠。返回值得思考的问题:3、 金属键、离子键不具有饱和性和方向性,共价键是否也没有饱和性和方向性?为什么N、O、F与H形成简单的化合 物(NH3、H2O、HF)中H原子数不等?三、共价键的特点1、具有饱和性形成的共价键数 = 未成对电子数 在成键原子中,有几个未成对电子通常就只能形成几个共价键,所以在共价分子中每个原子形成共价键数目是一定的。XZXZ2、具有方向性返回因为S轨道是球形对称的,所以S轨道与S轨道形成的共价键没有方向性。是不是所有的共价键都具有方向性?问题:小结:2.共价键的形成条件1.共价键的本质3.共价键的特征1、下列物质中,既含有离子键,又含有共价键的是( )
A.H2O B.CaCl2 C.NaOH D.Cl2C2、下列元素的原子在形成不同物质时,既能形成离子键,又能形成共价键的是( )
A.K B.Ca C.I D.NeC练 习3、下列说法正确的是 ( )
A、有共价键的化合物一定是共价化合物
B、分子中只有共价键的化合物一定是共价化合物
C、由共价键形成的分子一定是共价化合物
D、只有非金属原子间才能形成共价键 B4、相距很远的两个自旋方向相反的H原子相互逐渐接近,在这一过程中体系能量将( )
A、先变大后变小 B、先变小后变大
C、逐渐变小 D、逐渐增大B5、下列不属于共价键的成键因素的是 ( )
A、共用电子对在两核间高频率出现
B、共用的电子必须配对
C、成键后体系能量降低,趋于稳定
D、两原子核体积大小要适中D6、写出下列物质的电子式
(1)Br2;(2)CO2 ;(3)PH3
(4)NaOH; (5)Na2O2;
作业:(1)课本P48:1、2、3、4
(2)预习共价键的类型
谢谢再见
共价化合物
离子化合物a、电子式:4、共价键的表示方法请与离子化合物的电子式进行比较注意:1、共价化合物的电子式不出现方括号和离子电荷数。
2、不要混淆“用电子式表示结构”和“用电子式表示 形成过程。b、结构式 :练习: 用电子式表示HCl、K2S的形成过程值得思考的问题:1、是否所有的非金属单质中都存在共价键?2、2个氢原子一定能形成氢分子吗?两个核外电子自旋方向相反的氢原子靠近vr0V:势能
r:核间距r0vr0r0V:势能
r:核间距r0vr0r0V:势能
r:核间距r0vr0r0V:势能
r:核间距两个核外电子自旋方向相同的氢原子靠近vr0V:势能
r:核间距一、共价键的形成本质 成键原子相互接近时,原子轨道发生 ,自旋方向 的 电子形成 ,两原子核间的电子密度 ,体系的能量 。重叠相反未成对 共用电子对增 加降低返回二、共价键的形成条件A、有自旋方向相反的未成对电子。B、原子轨道要实现最大限度的重叠。返回值得思考的问题:3、 金属键、离子键不具有饱和性和方向性,共价键是否也没有饱和性和方向性?为什么N、O、F与H形成简单的化合 物(NH3、H2O、HF)中H原子数不等?三、共价键的特点1、具有饱和性形成的共价键数 = 未成对电子数 在成键原子中,有几个未成对电子通常就只能形成几个共价键,所以在共价分子中每个原子形成共价键数目是一定的。XZXZ2、具有方向性返回因为S轨道是球形对称的,所以S轨道与S轨道形成的共价键没有方向性。是不是所有的共价键都具有方向性?问题:小结:2.共价键的形成条件1.共价键的本质3.共价键的特征1、下列物质中,既含有离子键,又含有共价键的是( )
A.H2O B.CaCl2 C.NaOH D.Cl2C2、下列元素的原子在形成不同物质时,既能形成离子键,又能形成共价键的是( )
A.K B.Ca C.I D.NeC练 习3、下列说法正确的是 ( )
A、有共价键的化合物一定是共价化合物
B、分子中只有共价键的化合物一定是共价化合物
C、由共价键形成的分子一定是共价化合物
D、只有非金属原子间才能形成共价键 B4、相距很远的两个自旋方向相反的H原子相互逐渐接近,在这一过程中体系能量将( )
A、先变大后变小 B、先变小后变大
C、逐渐变小 D、逐渐增大B5、下列不属于共价键的成键因素的是 ( )
A、共用电子对在两核间高频率出现
B、共用的电子必须配对
C、成键后体系能量降低,趋于稳定
D、两原子核体积大小要适中D6、写出下列物质的电子式
(1)Br2;(2)CO2 ;(3)PH3
(4)NaOH; (5)Na2O2;
作业:(1)课本P48:1、2、3、4
(2)预习共价键的类型
谢谢再见
