物质的量第一课时
图片预览







文档简介
课件20张PPT。讲 课 人
善 国 中 学 王 梅第3节 化学中常用的物理量——物质的量(第1课时)1、生活中,大米为什么通常用千克作为单位,而不用米粒来计量?火柴为什么成盒销售?2、化学中描述 C + O2 = CO2
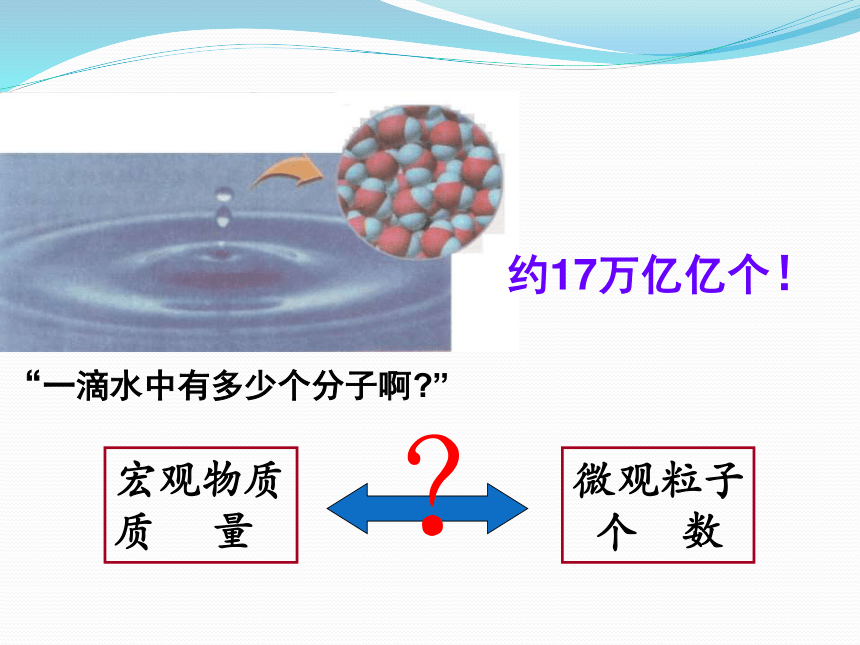
质量可以通过天平称量,当我们在分子原子水平上研究时,12gC中有多少个碳原子你又将如何知道呢?宏观上 12克 32克 44克约17万亿亿个!“一滴水中有多少个分子啊?”物质的量教 学 目 标:
(一)知识目标
1、使学生了解物质的量及其单位——摩尔,了解物质的量与微观粒子之间的关系。
2、使学生了解物质的量、阿伏加德罗常数、微粒个数之间的关系。
(二)能力目标
初步培养学生演绎推理、归纳推理、逻辑推理和运用化学知识进行计算能力。
(三)情感目标
通过对概念的透彻理解,培养学生严谨、认真的学习态度,使学生掌握科学的学习方法。
教 学 重 点:物质的量及其单位
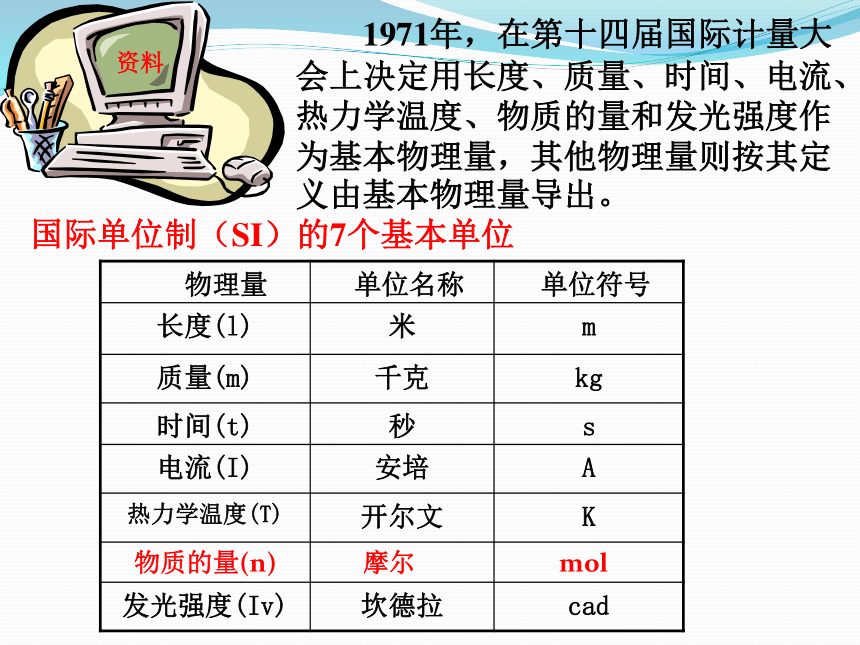
教 学 难 点:物质的量及其单位资料{分子、原子、离子、电子、质子、中子或这些粒子的特定组合。一、物质的量及其单位——摩尔1.物质的量 ①是国际单位制七个基本物理量之一,符号为n 。 ②是表示含有一定数目微观粒子的集体。③单位:摩尔 简称:摩 符号:mol注意②摩尔作为物质的量的单位,这一单位只适用于微观粒子,不适用于宏观物质。③使用摩尔作为单位表示物质的量时,必须指明微粒的种类,如原子、分子、离子等, 或者用化学式来表示。例:1molNa+或n(Na+)=1mol①“物质的量”是一个统一、不可分割的整体,这四个字缺一不可,不能把它理解为“物质的质量”或“物质的数量”错误。没有指明微粒的种类。改成1molO,1molO2都是正确的。因此使用摩尔作单位时,所指微粒必须十分明确,且微粒的种类一般用化学符号表示。 正确。 不能,因为物质的量及其单位的使用对象只能是微观粒子,不能用来描述宏观物质.
学以致用1mol任何微粒所含的微粒数与0.012kg12C
中所含的碳原子数相同已知:一个碳原子的质量为 1.993 × 10-23g
求: 0.012kg 碳-12 中所含的碳原数?解:2.阿伏加徳罗常数① 符号:NA② NA = 6.02 ×1023mol-1③单位: mol-1 (每摩尔)④物质的量(n)、阿伏加德罗常数( NA )、 微粒数(N)之间的关系式 9.03×1023个氧分子的物质的量是多少?
小试牛刀迁移应用2mol 1mol 6.02×1023 1.204×10241个水分子中有2个氢原子和1个氧原子,有如下关系:
H2O——2H—— O 即H2O——2H——O
1 2 1 1mol 2mol 1mol
分子中原子的物质的量之比==分子中原子个数之比启示1.1molCO2分子中有 molC, molO,共有 mol原子.3.1mol CO2与 molO2所含原子数相等。 121.52. 0.3 mol H2SO4含有 个硫酸分子 molO,
molS molH1.806×10231.20.30.63 巩固提高阿伏加德罗常数微粒个数物质的量NNA n=归纳整合小结?通过本节课的学习,你能计算出18g水中含有多少个水分子了吗?你知道吗谢谢
善 国 中 学 王 梅第3节 化学中常用的物理量——物质的量(第1课时)1、生活中,大米为什么通常用千克作为单位,而不用米粒来计量?火柴为什么成盒销售?2、化学中描述 C + O2 = CO2
质量可以通过天平称量,当我们在分子原子水平上研究时,12gC中有多少个碳原子你又将如何知道呢?宏观上 12克 32克 44克约17万亿亿个!“一滴水中有多少个分子啊?”物质的量教 学 目 标:
(一)知识目标
1、使学生了解物质的量及其单位——摩尔,了解物质的量与微观粒子之间的关系。
2、使学生了解物质的量、阿伏加德罗常数、微粒个数之间的关系。
(二)能力目标
初步培养学生演绎推理、归纳推理、逻辑推理和运用化学知识进行计算能力。
(三)情感目标
通过对概念的透彻理解,培养学生严谨、认真的学习态度,使学生掌握科学的学习方法。
教 学 重 点:物质的量及其单位
教 学 难 点:物质的量及其单位资料{分子、原子、离子、电子、质子、中子或这些粒子的特定组合。一、物质的量及其单位——摩尔1.物质的量 ①是国际单位制七个基本物理量之一,符号为n 。 ②是表示含有一定数目微观粒子的集体。③单位:摩尔 简称:摩 符号:mol注意②摩尔作为物质的量的单位,这一单位只适用于微观粒子,不适用于宏观物质。③使用摩尔作为单位表示物质的量时,必须指明微粒的种类,如原子、分子、离子等, 或者用化学式来表示。例:1molNa+或n(Na+)=1mol①“物质的量”是一个统一、不可分割的整体,这四个字缺一不可,不能把它理解为“物质的质量”或“物质的数量”错误。没有指明微粒的种类。改成1molO,1molO2都是正确的。因此使用摩尔作单位时,所指微粒必须十分明确,且微粒的种类一般用化学符号表示。 正确。 不能,因为物质的量及其单位的使用对象只能是微观粒子,不能用来描述宏观物质.
学以致用1mol任何微粒所含的微粒数与0.012kg12C
中所含的碳原子数相同已知:一个碳原子的质量为 1.993 × 10-23g
求: 0.012kg 碳-12 中所含的碳原数?解:2.阿伏加徳罗常数① 符号:NA② NA = 6.02 ×1023mol-1③单位: mol-1 (每摩尔)④物质的量(n)、阿伏加德罗常数( NA )、 微粒数(N)之间的关系式 9.03×1023个氧分子的物质的量是多少?
小试牛刀迁移应用2mol 1mol 6.02×1023 1.204×10241个水分子中有2个氢原子和1个氧原子,有如下关系:
H2O——2H—— O 即H2O——2H——O
1 2 1 1mol 2mol 1mol
分子中原子的物质的量之比==分子中原子个数之比启示1.1molCO2分子中有 molC, molO,共有 mol原子.3.1mol CO2与 molO2所含原子数相等。 121.52. 0.3 mol H2SO4含有 个硫酸分子 molO,
molS molH1.806×10231.20.30.63 巩固提高阿伏加德罗常数微粒个数物质的量NNA n=归纳整合小结?通过本节课的学习,你能计算出18g水中含有多少个水分子了吗?你知道吗谢谢
