2010届高三化学100分突破专题训练:第1课时《物质的组成、性质及分类》
文档属性
| 名称 | 2010届高三化学100分突破专题训练:第1课时《物质的组成、性质及分类》 |
|
|
| 格式 | rar | ||
| 文件大小 | 94.7KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2009-10-24 00:00:00 | ||
图片预览





文档简介
本资料来自于资源最齐全的21世纪教育网www.21cnjy.com
第1课时 物质的组成、性质和分类 (A卷)
考测点导航
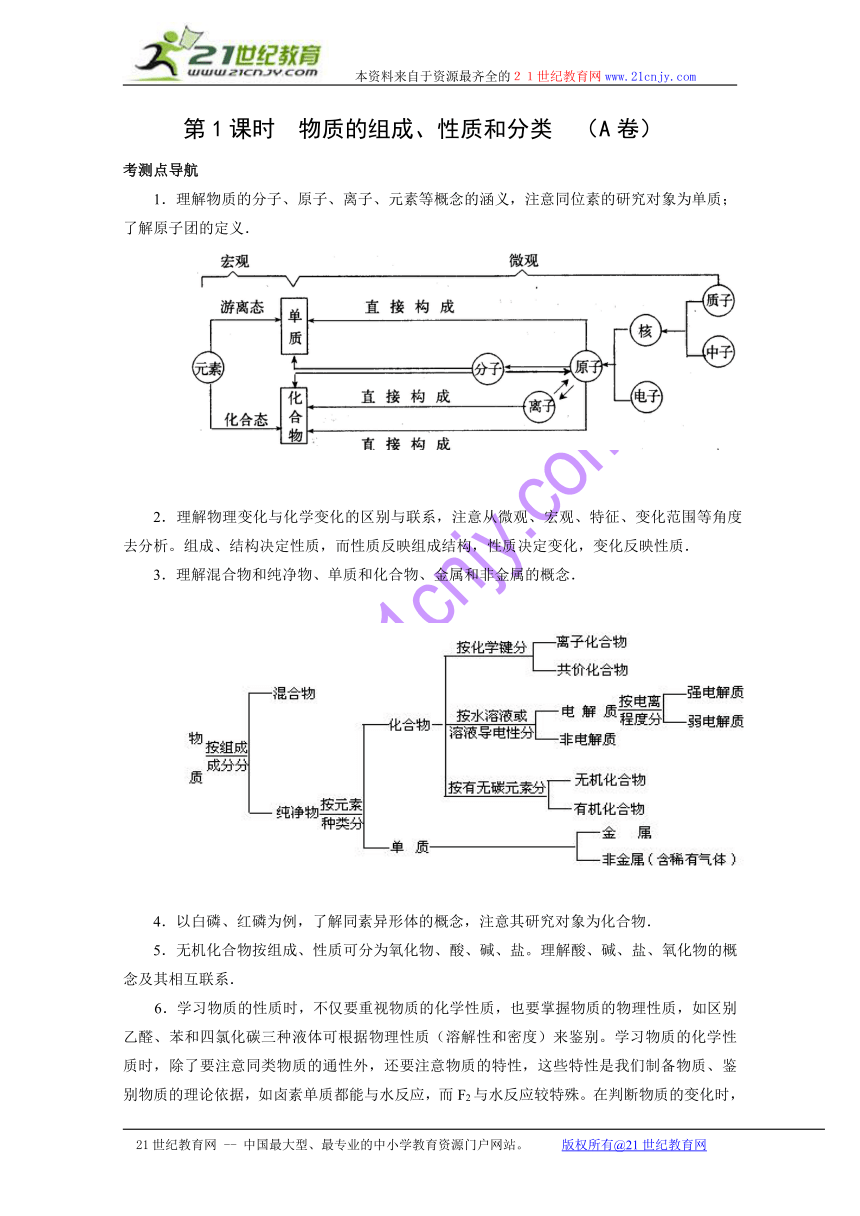
1.理解物质的分子、原子、离子、元素等概念的涵义,注意同位素的研究对象为单质;了解原子团的定义.
2.理解物理变化与化学变化的区别与联系,注意从微观、宏观、特征、变化范围等角度去分析。组成、结构决定性质,而性质反映组成结构,性质决定变化,变化反映性质.
3.理解混合物和纯净物、单质和化合物、金属和非金属的概念.
4.以白磷、红磷为例,了解同素异形体的概念,注意其研究对象为化合物.
5.无机化合物按组成、性质可分为氧化物、酸、碱、盐。理解酸、碱、盐、氧化物的概念及其相互联系.
6.学习物质的性质时,不仅要重视物质的化学性质,也要掌握物质的物理性质,如区别乙醛、苯和四氯化碳三种液体可根据物理性质(溶解性和密度)来鉴别。学习物质的化学性质时,除了要注意同类物质的通性外,还要注意物质的特性,这些特性是我们制备物质、鉴别物质的理论依据,如卤素单质都能与水反应,而F2与水反应较特殊。在判断物质的变化时,要抓住变化后有无新物质生成者一关键点,如变色、导电、爆炸既可能是物理变化,也可能是化学变化。
典型题点击
1. 试分析下列说法是否正确?对错误的说法应通过举例指出错误之所在。
A.由不同原子组成的纯净物一定是化合物
B.非金属氧化物一定是酸性氧化物;碱性氧化物一定是金属氧化物
C.含金属元素的离子不一定都是阳离子
D.胆矾是纯净物,水泥是混合物
(该题考查学生对化合物、纯净物、酸性氧化物、碱性氧化物、非金属氧化物、金属氧化物、结晶水合物、同位素等概念的理解,答题时注意分析问题的全面性及典型反例的寻找。)
2. (2001全国高考题)下列过程中,不涉及化学变化的是( )
A.甘油加水作护肤剂 B.用明矾净化水
C.烹鱼时加入少量料酒和食醋可减少腥味,增加香味
D.烧菜用过的铁锅,经放置常出现红棕色斑迹
(该题考查学生对化学变化的理解以及现实生活中的一些现象所隐含的化学原理的分析,答题时注意分析其中的原理和化学变化与物理变化的本质区别。解题关键在于对概念本质的深刻理解,此类题目选项内容范围广,贴近生产生活实际,要求学生不仅掌握课本知识,还应有一定的生活常识和思维方法。)
3.学生用滤纸折成一只纸蝴碟并在纸蝴碟上喷洒某种试剂,挂在铁架台上。另取一个盛有某种溶液的烧杯,放在纸蝴碟的下方(如图1—1—1所示)。过一会儿,发现纸蝴碟的颜色由白色转变为红色,喷洒在纸蝴碟上的试剂与小烧杯中的溶液是( )
A B C D
纸蝴碟上的喷洒液 石蕊 酚酞 酚酞 石蕊
小烧杯中的溶液 浓盐酸 浓氨水 NaOH溶液 浓硫酸
(本题主要考查一些指示剂遇酸性或碱性物质后的颜色变化及一些酸、碱的物理性质)
4、已知反应:2A + 3B = 6C + D中,A是由 X、Y两种元素组成,B是由 Z元素组成的单质,C、D都是双原子分子。根据以上条件,填写下表空格:
物质代号 A B C D
该物质中元素的种类 2 1
每个分子中原子的总数目 2 2
其中可能的一种分子组成
(该题考查学生质量守恒定律即反应前后原子个数相等的应用能力,解题时注意通过讨论确定其组成。)
新活题网站
1.(2000广东高考题)只含有一种元素的物质( )
A.可能是纯净物也可能是混合物
B.可能是单质也可能是化合物
C.一定是纯净物
D.一定是一种单质
(本题考查纯净物、混合物、单质、化合物的概念)
2.(2001广东河南高考题)下列说法,违反科学原理的是
A. AgI可用于人工降雨
B. 闪电时空气中的N2可变为氮的化合物
C. 加少量某物质可将水变成燃料油
D. 一定温度、压强下石墨会变成金刚石
(本题考查用化学原理分析一些“现象”是否成立)
3.对于原子的下列叙述正确的是 ( ) A.不能再分的最小微粒 B.同位素原子的质量数不同,化学性质也不同 C.化学变化中的最小微粒 D.构成物质的一种微粒
4.下列变化:①导电、②爆炸、③缓慢氧化、④变色、⑤无水硫酸铜吸水、⑥工业制氧气、⑦白磷变成红磷、⑧久置浓HNO3变黄,一定属于化学变化的是 ( )
A.①④ B.⑥⑧
C.②⑥⑦ D.③⑤⑦⑧
(本题考查对化学变化本质的理解)
5.(99上海)下列各组物质中不易用物理性质区别的是 ( )
A.苯和四氯化碳 B.酒精和汽油
C.氯化铵和硝酸铵晶体 D.碘和高锰酸钾固体
(本题考查如何用物理性质区别化学物质)
6.炸弹爆炸时能在方圆几百米范围内撒下大量石墨纤维,造成输电线、电厂设备损坏。这是由于石墨( )
A.有放射性 B.易燃、易爆
C.能导电 D.有剧毒
7.下列物质中,属于物质化学性质的是( )
A. 氧气能在-183℃时变为淡蓝色液体
B. 镁能在空气中燃烧生成氧化镁
C. 水在4℃时密度(g/cm3)最大
D. 氢气难溶于水
(本题考查化学性质与物理性质的区别)
8.下列变化一定是化学变化的是( )
A.构成物质的分子改变了
B.构成物质的分子间距离改变了
C.物质的状态改变了
D.两种稀有气体混在一起
(本题考查化学变化的本质)
9.想一想,次氯酸、稀硝酸、浓硫酸三种酸为什么可归为一类?与它们同为一类的酸是( )
A.盐酸 B.稀硫酸
C.浓磷酸 D.浓硝酸
10.下列物质都能使品红溶液褪色,其中褪色的原因与化学反应无关的是 ( )
A.过氧化钠 B.漂白粉与盐酸的混合物
C.活性炭 D.二氧化硫
(本题考查一些物质的漂白性质的本质)
11.下列属性属化学性质的是( )
A.金刚石硬度大 B.苯酚露置在空气中变色
C.石灰水受热变浑浊 D.氨气的刺激性气味
12.将下列各组物质按酸、碱、盐分类顺次排列。正确的( )
A.硫酸,纯碱,石膏 B.氢硫酸,烧碱,绿矾
C.石炭酸,乙醇,醋酸钠 D.磷酸,熟石灰,苛性钾
13.为了控制温室效应。各国科学家提出了不少方法和设想。有人根据液态CO2密度大于海水密度的事实,设想将CO2液化后,送入深海海底。以减小大气中CO2的浓度。为使CO2液化,可采用的措施是( )。
A.减压、升温 B.增压、升温
C.减压、降温 D.增压、降温
14.下列各组物理量中,都不随取水量的变化而变化的是( )
A.水的沸点;蒸发水所需热量
B.水的密度;水中通人足量CO2后溶液的pH
C.水的体积;电解水所消耗的电量
D.水的物质的量;水的摩尔质量
15. 从下列括号中选择合适的用语,填写在①-⑩的横线上,使它跟各种变化的情况相符(分解、潮解、溶解、蒸发、干馏、蒸馏、结晶、化合、挥发、升华、风化);
1 食盐放入水中逐渐消失 ;
2 碘加热逐渐消失 ;
3 不盖灯帽的酒精灯,灯内酒精会逐渐减少,以至消失 ;
4 烧碱固体吸收空气中的水分 ;
5 生石灰吸收空气中的水分 ;
6 胆矾受热后变成白色粉末 ;
7 石碱晶体在空气中变成白色粉末 ;
8 氢氧化铜加热后变成黑色固体 ;
9 煤隔绝空气加强热后生成黑色固体 ;
⑩ 饱和KNO3溶液降温,出现晶体 。
(本题考查对一些化学专用名词概念的理解和掌握)
16.有相对原子质量均大于10的A、B两种元素,能形成两种化合物X和Y。已知等物质的量的 X和 Y的混合气体密度为相同条件下氢气的 18.5倍,其中 X和 Y的质量比为 3:4.4,经测定Y的组成为AnB。试通过计算:
⑴确定A、B两元素的名称。
⑵写出X、Y的化学式。
(本题考查对相对原子质量及相对密度的理解和应用)
17.(1)由2个C原子、1个O原子、1个N原子和若干个H原子组成的共价化合物,H的原子数目最多为
个,试写出其中一例的结构简式 。
(2)若某共价化合物分子只含有C、N、H三种元素,且以a(C)和n(N)分别表示C和N的原子数目,则H原子数目最多等于 。
(3)若某共价化合物分子中只含有C、N、O、H四种元素,且以n(C),n(N)和n(O)分别表示C、N和O的原子数目,则H原子数目最多等于 。
(本题主要考查共价化合物分子中一些原子的成键的本质)
第1课时 物质的组成、性质和分类 (B卷)
易错现象
1、注意同位素和同素异形体两概念的适用范围,防止混淆。
2、要熟悉物质分类的典型实例,还要注意一些物质分类的常见的特例及实例。如:
⑴同素异形体的混合物只含一种元素;同分异构体的混合物有确定的化学式;
⑵NO2不是硝酐,CO不是甲酸酐,Na2O2不是烧碱的碱酐等;
⑶乙酸酐(CH3CO)2O不是氧化物;
⑷变色、导电、爆炸既可能是物理变化也可能是化学变化。
3、通常易忽视的物理变化是电泳、盐析、焰色反应、聚沉;易忽视的化学变化是同素异形体之间的转化,电解质溶液导电,NO2气体受热或遇冷时颜色变化等。
纠错训练
1.关于元素和原子的关系有如下各种说法:①若是同种元素,则一定是同种原子;②若是同种原子,则一定是同种元素;③若是不同种元素,则一定是不同种原子;④若是不同种原子,则一定是不同种元素。其中正确的是( )
A. ①② B.②③ C.③④ D.①④
2.美国科学家发现的C60是一种新的分子,它具有空心的类似足球的结构,被称为“分子足球”。最近日本科学家确认世界上还存在着另一种“分子足球”N60,它与C60的结构相似,并且在高温或机械撞击后,其中积蓄的巨大能量会在一瞬间放出来。对于N60下列说法中正确的是( )
A.N60是由共价键构成的空心圆球面结构,所以它是一种原子晶体
B.N60和14N都是氮的同位素
C.N60没有同素异形体
D.N60的发现开辟了能源新天地,将来会成为很好的火箭燃料
3.下列各组物质中,肯定全都属于纯净物的是( )
A.液氯和氯水 B.二氯甲烷和丁醇
C.七水合硫酸亚铁和硫酸亚铁 D.分散系和淀粉
4.铜锌合金制成的假金元宝欺骗行人的事件屡有发生下列不易区别其真伪的方法是( )
A.测定密度 B.放入硝酸中
C.放入盐酸中 D.观察外观
5.下列实验或生产操作:①蛋白质溶液中加入硫酸铵后形成沉淀;②除去混在氢氧化铁胶体中的氯化铁;③二氧化氮经加压凝成无色液体;④溴水滴入植物油中振荡褪色;⑤水泥、砂子和水混合后硬化; ⑥照相底片感光,其中没有新物质生成的是 ( )
A.①②③ B.②④⑥ C.①② D.③⑤
6.下列性质中,属于物理性质的是( )
A. 物质的金属性和非金属性 B.CuCl2溶液的导电性
C.双氧水的氧化性 D.浓硫酸的不挥发性
7.下列变化一定属于物理变化的是( )
A.钠、钾元素的焰色反应 B.橡胶制品的老化
C.用明矾使水净化 D.用加热法分离SiO2和NH4CI
8.下列反应中,加入的物质能加快反应速率,但不起催化作用的是( )
A. 在过氧化氢中加入二氧化锰
B. 在盛有锌粒和稀硫酸的试管中加入氧化铜
C. 在热的乙酸乙酯中加入稀硫酸
D. 在苯和液溴混合物中加铁屑
检测提高
1.某药品说明书中标明:本品每克含碘15mg,镁65mg,铜2mg,锌1.5mg,锰1mg,这里所标的各成分是( )
A.分子 B.元素 C.单质 D.离子
2.想一想,NaOH(固)、P2O5(固)、无水CaCl2(固),为什么可归为一类。据此从A~D中选出一种最适宜与这三种物质归为一类的是( )
A.浓硫酸 B.氯化钠
C.碱石灰 D.生石灰
3.保持CO2化学性质的是 ( )
A. 氧元素和碳元素
B.两个氧原子和一个碳原子
C.二氧化碳分子中的电子数
D.二氧化碳分子
4.1995年诺贝尔化学奖授予致力于研究臭氧层被破坏问题的三位环境化学家。大气中的臭氧层可滤除大量的紫外光,保护地球上的生物。氟利昂(如CCl2F2可在光的作用下分解产生Cl原子,Cl原子会对臭氧层产生长久的破坏作用
(臭氧的分子式为O3)。有关反应为: O3 O2+O Cl+ O3→ClO+ O2 ClO+O→Cl+ O2
总反应:2 O3→3O3
⑴在上述臭氧变成氧气的反应过程中,Cl是
A.反应物 B.生成物
C.中间产物 D.催化剂
⑵O3和O2是
A.同分异构体 B.同系物
C.氧的同素异形体 D.氧的同位素
5.下列物质肯定为纯净物的是
A. 只由一种元素构成的物质
B.只由一种原子构成的物质
C.只由一种分子构成的物质
D.只由一种元素的阳离子跟另一种元素的阴离子构成的物质
6.下列广告用语在科学性上没有错误的是( )
A. 这种饮料中不含任何化学物质
B. 这种蒸馏水绝对纯净,其中不含任何离子
C. 这种口服液含有丰富的氮、磷、锌等微量元素
D. 没有水就没有生命
7.下列各组物质中不易用物理性质区别的是( )
A.苯和四氯化碳 B.酒精和汽油
C.氯化铵和硝酸铵晶体 D.碘和高锰酸钾固体
8.下列实验或生产操作:①石灰水受热变浑浊;②除去混在氢氧化铁胶体中的氯化铁;③二氧化氮经加压凝成无色液体;④溴水滴入植物油中振荡褪色;⑤苯酚露置在空气中变色; ⑥照相底片感光,其中没有新物质生成的是 ( )
A.①②③ B.②④⑥
C.①② D.③⑤
9.从化学原理上说,下面四项变化中的一项与其它三项不同,这一项的标号是 ( )
A.碳铵分解 B.白磷自燃
C.煤尘爆炸 D.镁条燃烧
10.下列物质的性质都属于物理性质的是( )
A. 二氧化硫气体的还原性和漂白性
B.氨气的无色和刺激性
C.浓硝酸的挥发性和不稳定性
D.氯化铜的溶解性和水溶液的导电性
11.发生变化的物质是纯净物,但该变化不属于化学变化的是 ( )
A.热碱溶液洗涤油污
B.散失到地面上的水银逐渐消失
C.鸡蛋白溶液加入Na2SO4溶液会有沉淀析出
D.亚硫酸钠久置变质
12.1998年诺贝尔化学奖授予科恩(美)和波普尔(英),以表彰他们在理论化学领域作出的重大贡献。他们的工作使实验和理论能够共同协力探讨分子体系的性质,引起整个化学领域正在经历一场革命性的变化。下列说法正确的是( )
A. 化学不再是纯实验科学
B.化学不再需要实验
C.化学不做实验,就什么都不知道
D.未来化学的方向还是经验化
13.下列指定的微粒数目之比不等于1:1的是( )
A.NaF溶液中的Na+ 和F-
B. 中的质子和中子
C.食盐晶体中的 N a+和Cl—
D.N a H S O4稀溶液中的N a+和 S O42-
14.下列各小题均由两句话组成。请按下表选出对各题每两句话的正确判断
A B C D E
第一句话 对 对 对 错 错
第二句话 对,是对第一句话的正确解释 对,不是对第一句话的正确解释 错 对 错
⑴H2O2是氧化物,因为H2O2是由两种元素组成,且其中含氧元素 ( )
⑵NO2是硝酸的酸酐,因为NO2能与水化合生成硝酸 ( )
⑶质量比为7:4的CO和O2反应后,可得到纯净物,因为生成物是CO2 ( )
⑷氧化铁是碱性氧化物,因为铁是金属,所有金属氧化物都是碱性氧化物 ( )
15.常温下A和B两种气体组成的混合气(A的式量大于B的式量),经分析混合气体只含有氮和氢两种元素,而且不论A和B以何种比例混合,氮和氢的质量比总大于14/3。由此可确定A为 ,B为 ,其理由是
。
16.某学生课外活动小组利用图1—1—2所示装置分别做如下实验:
⑴在试管中注入某红色溶液,加热试管,溶液颜色逐
渐变浅,冷却后恢复红色,则原溶液可能是_______________
溶液;加热时溶液由红色逐渐变浅的原因是:_____________
_____________________________________________________。
⑵在试管中注入某无色溶液,加热试管,溶液变为红色,
冷却后恢复无色,则此溶液可能是________________溶液;加热时溶液由无色变为红色的原因是: __________________________________________________。
17.我国规定饮用水质量标准必须符合下列要求:
PH值 6.5-8.5
Ca2+,Mg2+总浓度 <0.0045mol/L
细菌总数 <100个/mL
以下是源水处理成自来水的工艺流程示意图
⑴源水中含Ca2+、Mg2+、HCO3—、Cl— 等,加入石灰后生成Ca(OH)2,进而发生若干复分解反应,写出其中一个离子方程式
⑵凝聚剂除去悬浮固体颗粒的过程__________(填写编号,多选倒扣)
①只有物理过程 ②只是化学过程 ③是物理和化学过程
FeSO4·7H2O常用的凝聚剂,它在水中最终生成___________沉淀。
⑶通入二氧化碳的目的是 和 。
⑷气体A的作用是__________。这种作用是基于气体A和水反应的产物具有______________性。
⑸下列物质中,______________可以作为气体A的代用品。(填写编号,多选倒扣)
①Ca(ClO)2 ②NH3(液) ③K2FeO4 ④SO2
参考答案
第1课时 (A卷)
典型题点击
1.CD 2.A 3.
讲析:1. A不正确。关键词“不同原子”要注意,因为许多元素都有同位素,若是同种元素的不同原子,如氯元素有35Cl、37Cl两种氯原子,构成氯单质的氯气分子,可能是35Cl—35Cl、35Cl—37Cl、37Cl—37Cl,他们仍属于纯净物中的单质,不属于化合物;若是不同种元素的原子组成的纯净物,则一定是化合物。B前半句不正确。因非金属氧化物可能是不成盐氧化物(CO、NO等),它们既不能跟碱反应生成盐和水,也不能跟酸反应生成盐和水。前半句反过来也不正确,如Mn2O7的相应水化物为HMnO4,所以Mn2O7是酸性氧化物,但它是金属氧化物。B
后半句正确,但后半句反过来就不正确了,如Mn2O7是酸性氧化物,Al2O3是两性氧化物。C正确。含金属元素的离子,例如:K+、[Ag(NH3)2]+、AlO2-、MnO4-等,说明金属元素也可以构成阴离子。D正确。结晶水合物有固定的化学组成,属纯净物而不是混合物。胆矾和无水CuSO4不是同一种物质,无论是胆矾分解成无水CuSO4,还是无水CuSO4水合成胆矾,都是化学变化过程。2.化学变化与物理变化的本质区别是:是否有新物质生成。甘油稀释后仍具有吸湿性,可做护肤剂,该过程中不涉及化学变化;明矾溶于水后,发生反应Al3++3H2O
Al(OH)3 +3H+,产生了Al(OH)3胶体,从而可净化水;烹鱼时加入少量的料酒和食醋可减少腥味,增加香味的原因是过程中发生了CH3COOH+C2H5OH→CH3COOC2H5+ H2O,产生了具有果香味的乙酸乙酯的缘故;烧菜用过的铁锅,由于在潮湿的环境中发生了电化腐蚀,Fe最终被氧化成Fe2O3·nH2O,而出现红棕色斑迹。后三者都是化学变化过程。
4.
物质代号 A B C D
该物质中元素的种类 2 1
每个分子中原子的总数目 4 2
其中可能的一种分子组成 X3Y或XY3 Z2 XZ或YZ X2或Y2
讲析:根据化学反应原子守恒原理,由反应:2A + 3B = 6C + D和C、D都是双原子分子可知,2个A分子 和3个B分子共有14个原子,B又是单质,通过讨论确定组成。
新活题网站
1.A 2.C 3.CD 4.D 5.C 6.C 7.B 8.A 9.D 10.C 11.B 12.B 13.D 14.B
15、①溶解 ②升华 ③挥发 ④潮解 ⑤化合 ⑥分解 ⑦风化 ⑧分解 ⑨干馏 ⑩结晶
16、⑴氮 氧 ⑵X——NO Y——N2O
17、(1)7; (其他合理答案也给分)
(2)2n(C)+n(N)+2
(3)2n(C)+n(N)+2
第1课时 (B卷)
纠错训练
1.B 2.D 3.C 4.D 5.C 6.D 7.A 8.B
检测提高
1.B 2.D 3.D 4.⑴D ⑵C 5.C 6.D 7.C 8.C 9.A 10.B 11.B 12.A 13.D 14.⑴A ⑵ E ⑶ B ⑷ C
15.N2 NH3 因为NH3中的氮和氢的质量比等于14/3
16.(1)稀氨水和酚酞 稀氨水中的NH3气逸出,所以溶液的颜色变浅
(2)溶有SO2的品红 SO2气体逸出,品红溶液恢复红色
17.(1)HCO3—+ OH—= CO32—+ H2O
Mg2++2OH-= Mg(OH)2↓
Ca2++ HCO3—+ OH-= CaCO3↓+H2O
任选其一,其他合理解也对。
(2)③ 胶状Fe(OH)3
(3)除去Ca2+ 调节PH值
(4)杀菌消毒 强氧化
(5)① ③
图1—1—1
图1—1—2
21世纪教育网 -- 中国最大型、最专业的中小学教育资源门户网站。 版权所有@21世纪教育网
第1课时 物质的组成、性质和分类 (A卷)
考测点导航
1.理解物质的分子、原子、离子、元素等概念的涵义,注意同位素的研究对象为单质;了解原子团的定义.
2.理解物理变化与化学变化的区别与联系,注意从微观、宏观、特征、变化范围等角度去分析。组成、结构决定性质,而性质反映组成结构,性质决定变化,变化反映性质.
3.理解混合物和纯净物、单质和化合物、金属和非金属的概念.
4.以白磷、红磷为例,了解同素异形体的概念,注意其研究对象为化合物.
5.无机化合物按组成、性质可分为氧化物、酸、碱、盐。理解酸、碱、盐、氧化物的概念及其相互联系.
6.学习物质的性质时,不仅要重视物质的化学性质,也要掌握物质的物理性质,如区别乙醛、苯和四氯化碳三种液体可根据物理性质(溶解性和密度)来鉴别。学习物质的化学性质时,除了要注意同类物质的通性外,还要注意物质的特性,这些特性是我们制备物质、鉴别物质的理论依据,如卤素单质都能与水反应,而F2与水反应较特殊。在判断物质的变化时,要抓住变化后有无新物质生成者一关键点,如变色、导电、爆炸既可能是物理变化,也可能是化学变化。
典型题点击
1. 试分析下列说法是否正确?对错误的说法应通过举例指出错误之所在。
A.由不同原子组成的纯净物一定是化合物
B.非金属氧化物一定是酸性氧化物;碱性氧化物一定是金属氧化物
C.含金属元素的离子不一定都是阳离子
D.胆矾是纯净物,水泥是混合物
(该题考查学生对化合物、纯净物、酸性氧化物、碱性氧化物、非金属氧化物、金属氧化物、结晶水合物、同位素等概念的理解,答题时注意分析问题的全面性及典型反例的寻找。)
2. (2001全国高考题)下列过程中,不涉及化学变化的是( )
A.甘油加水作护肤剂 B.用明矾净化水
C.烹鱼时加入少量料酒和食醋可减少腥味,增加香味
D.烧菜用过的铁锅,经放置常出现红棕色斑迹
(该题考查学生对化学变化的理解以及现实生活中的一些现象所隐含的化学原理的分析,答题时注意分析其中的原理和化学变化与物理变化的本质区别。解题关键在于对概念本质的深刻理解,此类题目选项内容范围广,贴近生产生活实际,要求学生不仅掌握课本知识,还应有一定的生活常识和思维方法。)
3.学生用滤纸折成一只纸蝴碟并在纸蝴碟上喷洒某种试剂,挂在铁架台上。另取一个盛有某种溶液的烧杯,放在纸蝴碟的下方(如图1—1—1所示)。过一会儿,发现纸蝴碟的颜色由白色转变为红色,喷洒在纸蝴碟上的试剂与小烧杯中的溶液是( )
A B C D
纸蝴碟上的喷洒液 石蕊 酚酞 酚酞 石蕊
小烧杯中的溶液 浓盐酸 浓氨水 NaOH溶液 浓硫酸
(本题主要考查一些指示剂遇酸性或碱性物质后的颜色变化及一些酸、碱的物理性质)
4、已知反应:2A + 3B = 6C + D中,A是由 X、Y两种元素组成,B是由 Z元素组成的单质,C、D都是双原子分子。根据以上条件,填写下表空格:
物质代号 A B C D
该物质中元素的种类 2 1
每个分子中原子的总数目 2 2
其中可能的一种分子组成
(该题考查学生质量守恒定律即反应前后原子个数相等的应用能力,解题时注意通过讨论确定其组成。)
新活题网站
1.(2000广东高考题)只含有一种元素的物质( )
A.可能是纯净物也可能是混合物
B.可能是单质也可能是化合物
C.一定是纯净物
D.一定是一种单质
(本题考查纯净物、混合物、单质、化合物的概念)
2.(2001广东河南高考题)下列说法,违反科学原理的是
A. AgI可用于人工降雨
B. 闪电时空气中的N2可变为氮的化合物
C. 加少量某物质可将水变成燃料油
D. 一定温度、压强下石墨会变成金刚石
(本题考查用化学原理分析一些“现象”是否成立)
3.对于原子的下列叙述正确的是 ( ) A.不能再分的最小微粒 B.同位素原子的质量数不同,化学性质也不同 C.化学变化中的最小微粒 D.构成物质的一种微粒
4.下列变化:①导电、②爆炸、③缓慢氧化、④变色、⑤无水硫酸铜吸水、⑥工业制氧气、⑦白磷变成红磷、⑧久置浓HNO3变黄,一定属于化学变化的是 ( )
A.①④ B.⑥⑧
C.②⑥⑦ D.③⑤⑦⑧
(本题考查对化学变化本质的理解)
5.(99上海)下列各组物质中不易用物理性质区别的是 ( )
A.苯和四氯化碳 B.酒精和汽油
C.氯化铵和硝酸铵晶体 D.碘和高锰酸钾固体
(本题考查如何用物理性质区别化学物质)
6.炸弹爆炸时能在方圆几百米范围内撒下大量石墨纤维,造成输电线、电厂设备损坏。这是由于石墨( )
A.有放射性 B.易燃、易爆
C.能导电 D.有剧毒
7.下列物质中,属于物质化学性质的是( )
A. 氧气能在-183℃时变为淡蓝色液体
B. 镁能在空气中燃烧生成氧化镁
C. 水在4℃时密度(g/cm3)最大
D. 氢气难溶于水
(本题考查化学性质与物理性质的区别)
8.下列变化一定是化学变化的是( )
A.构成物质的分子改变了
B.构成物质的分子间距离改变了
C.物质的状态改变了
D.两种稀有气体混在一起
(本题考查化学变化的本质)
9.想一想,次氯酸、稀硝酸、浓硫酸三种酸为什么可归为一类?与它们同为一类的酸是( )
A.盐酸 B.稀硫酸
C.浓磷酸 D.浓硝酸
10.下列物质都能使品红溶液褪色,其中褪色的原因与化学反应无关的是 ( )
A.过氧化钠 B.漂白粉与盐酸的混合物
C.活性炭 D.二氧化硫
(本题考查一些物质的漂白性质的本质)
11.下列属性属化学性质的是( )
A.金刚石硬度大 B.苯酚露置在空气中变色
C.石灰水受热变浑浊 D.氨气的刺激性气味
12.将下列各组物质按酸、碱、盐分类顺次排列。正确的( )
A.硫酸,纯碱,石膏 B.氢硫酸,烧碱,绿矾
C.石炭酸,乙醇,醋酸钠 D.磷酸,熟石灰,苛性钾
13.为了控制温室效应。各国科学家提出了不少方法和设想。有人根据液态CO2密度大于海水密度的事实,设想将CO2液化后,送入深海海底。以减小大气中CO2的浓度。为使CO2液化,可采用的措施是( )。
A.减压、升温 B.增压、升温
C.减压、降温 D.增压、降温
14.下列各组物理量中,都不随取水量的变化而变化的是( )
A.水的沸点;蒸发水所需热量
B.水的密度;水中通人足量CO2后溶液的pH
C.水的体积;电解水所消耗的电量
D.水的物质的量;水的摩尔质量
15. 从下列括号中选择合适的用语,填写在①-⑩的横线上,使它跟各种变化的情况相符(分解、潮解、溶解、蒸发、干馏、蒸馏、结晶、化合、挥发、升华、风化);
1 食盐放入水中逐渐消失 ;
2 碘加热逐渐消失 ;
3 不盖灯帽的酒精灯,灯内酒精会逐渐减少,以至消失 ;
4 烧碱固体吸收空气中的水分 ;
5 生石灰吸收空气中的水分 ;
6 胆矾受热后变成白色粉末 ;
7 石碱晶体在空气中变成白色粉末 ;
8 氢氧化铜加热后变成黑色固体 ;
9 煤隔绝空气加强热后生成黑色固体 ;
⑩ 饱和KNO3溶液降温,出现晶体 。
(本题考查对一些化学专用名词概念的理解和掌握)
16.有相对原子质量均大于10的A、B两种元素,能形成两种化合物X和Y。已知等物质的量的 X和 Y的混合气体密度为相同条件下氢气的 18.5倍,其中 X和 Y的质量比为 3:4.4,经测定Y的组成为AnB。试通过计算:
⑴确定A、B两元素的名称。
⑵写出X、Y的化学式。
(本题考查对相对原子质量及相对密度的理解和应用)
17.(1)由2个C原子、1个O原子、1个N原子和若干个H原子组成的共价化合物,H的原子数目最多为
个,试写出其中一例的结构简式 。
(2)若某共价化合物分子只含有C、N、H三种元素,且以a(C)和n(N)分别表示C和N的原子数目,则H原子数目最多等于 。
(3)若某共价化合物分子中只含有C、N、O、H四种元素,且以n(C),n(N)和n(O)分别表示C、N和O的原子数目,则H原子数目最多等于 。
(本题主要考查共价化合物分子中一些原子的成键的本质)
第1课时 物质的组成、性质和分类 (B卷)
易错现象
1、注意同位素和同素异形体两概念的适用范围,防止混淆。
2、要熟悉物质分类的典型实例,还要注意一些物质分类的常见的特例及实例。如:
⑴同素异形体的混合物只含一种元素;同分异构体的混合物有确定的化学式;
⑵NO2不是硝酐,CO不是甲酸酐,Na2O2不是烧碱的碱酐等;
⑶乙酸酐(CH3CO)2O不是氧化物;
⑷变色、导电、爆炸既可能是物理变化也可能是化学变化。
3、通常易忽视的物理变化是电泳、盐析、焰色反应、聚沉;易忽视的化学变化是同素异形体之间的转化,电解质溶液导电,NO2气体受热或遇冷时颜色变化等。
纠错训练
1.关于元素和原子的关系有如下各种说法:①若是同种元素,则一定是同种原子;②若是同种原子,则一定是同种元素;③若是不同种元素,则一定是不同种原子;④若是不同种原子,则一定是不同种元素。其中正确的是( )
A. ①② B.②③ C.③④ D.①④
2.美国科学家发现的C60是一种新的分子,它具有空心的类似足球的结构,被称为“分子足球”。最近日本科学家确认世界上还存在着另一种“分子足球”N60,它与C60的结构相似,并且在高温或机械撞击后,其中积蓄的巨大能量会在一瞬间放出来。对于N60下列说法中正确的是( )
A.N60是由共价键构成的空心圆球面结构,所以它是一种原子晶体
B.N60和14N都是氮的同位素
C.N60没有同素异形体
D.N60的发现开辟了能源新天地,将来会成为很好的火箭燃料
3.下列各组物质中,肯定全都属于纯净物的是( )
A.液氯和氯水 B.二氯甲烷和丁醇
C.七水合硫酸亚铁和硫酸亚铁 D.分散系和淀粉
4.铜锌合金制成的假金元宝欺骗行人的事件屡有发生下列不易区别其真伪的方法是( )
A.测定密度 B.放入硝酸中
C.放入盐酸中 D.观察外观
5.下列实验或生产操作:①蛋白质溶液中加入硫酸铵后形成沉淀;②除去混在氢氧化铁胶体中的氯化铁;③二氧化氮经加压凝成无色液体;④溴水滴入植物油中振荡褪色;⑤水泥、砂子和水混合后硬化; ⑥照相底片感光,其中没有新物质生成的是 ( )
A.①②③ B.②④⑥ C.①② D.③⑤
6.下列性质中,属于物理性质的是( )
A. 物质的金属性和非金属性 B.CuCl2溶液的导电性
C.双氧水的氧化性 D.浓硫酸的不挥发性
7.下列变化一定属于物理变化的是( )
A.钠、钾元素的焰色反应 B.橡胶制品的老化
C.用明矾使水净化 D.用加热法分离SiO2和NH4CI
8.下列反应中,加入的物质能加快反应速率,但不起催化作用的是( )
A. 在过氧化氢中加入二氧化锰
B. 在盛有锌粒和稀硫酸的试管中加入氧化铜
C. 在热的乙酸乙酯中加入稀硫酸
D. 在苯和液溴混合物中加铁屑
检测提高
1.某药品说明书中标明:本品每克含碘15mg,镁65mg,铜2mg,锌1.5mg,锰1mg,这里所标的各成分是( )
A.分子 B.元素 C.单质 D.离子
2.想一想,NaOH(固)、P2O5(固)、无水CaCl2(固),为什么可归为一类。据此从A~D中选出一种最适宜与这三种物质归为一类的是( )
A.浓硫酸 B.氯化钠
C.碱石灰 D.生石灰
3.保持CO2化学性质的是 ( )
A. 氧元素和碳元素
B.两个氧原子和一个碳原子
C.二氧化碳分子中的电子数
D.二氧化碳分子
4.1995年诺贝尔化学奖授予致力于研究臭氧层被破坏问题的三位环境化学家。大气中的臭氧层可滤除大量的紫外光,保护地球上的生物。氟利昂(如CCl2F2可在光的作用下分解产生Cl原子,Cl原子会对臭氧层产生长久的破坏作用
(臭氧的分子式为O3)。有关反应为: O3 O2+O Cl+ O3→ClO+ O2 ClO+O→Cl+ O2
总反应:2 O3→3O3
⑴在上述臭氧变成氧气的反应过程中,Cl是
A.反应物 B.生成物
C.中间产物 D.催化剂
⑵O3和O2是
A.同分异构体 B.同系物
C.氧的同素异形体 D.氧的同位素
5.下列物质肯定为纯净物的是
A. 只由一种元素构成的物质
B.只由一种原子构成的物质
C.只由一种分子构成的物质
D.只由一种元素的阳离子跟另一种元素的阴离子构成的物质
6.下列广告用语在科学性上没有错误的是( )
A. 这种饮料中不含任何化学物质
B. 这种蒸馏水绝对纯净,其中不含任何离子
C. 这种口服液含有丰富的氮、磷、锌等微量元素
D. 没有水就没有生命
7.下列各组物质中不易用物理性质区别的是( )
A.苯和四氯化碳 B.酒精和汽油
C.氯化铵和硝酸铵晶体 D.碘和高锰酸钾固体
8.下列实验或生产操作:①石灰水受热变浑浊;②除去混在氢氧化铁胶体中的氯化铁;③二氧化氮经加压凝成无色液体;④溴水滴入植物油中振荡褪色;⑤苯酚露置在空气中变色; ⑥照相底片感光,其中没有新物质生成的是 ( )
A.①②③ B.②④⑥
C.①② D.③⑤
9.从化学原理上说,下面四项变化中的一项与其它三项不同,这一项的标号是 ( )
A.碳铵分解 B.白磷自燃
C.煤尘爆炸 D.镁条燃烧
10.下列物质的性质都属于物理性质的是( )
A. 二氧化硫气体的还原性和漂白性
B.氨气的无色和刺激性
C.浓硝酸的挥发性和不稳定性
D.氯化铜的溶解性和水溶液的导电性
11.发生变化的物质是纯净物,但该变化不属于化学变化的是 ( )
A.热碱溶液洗涤油污
B.散失到地面上的水银逐渐消失
C.鸡蛋白溶液加入Na2SO4溶液会有沉淀析出
D.亚硫酸钠久置变质
12.1998年诺贝尔化学奖授予科恩(美)和波普尔(英),以表彰他们在理论化学领域作出的重大贡献。他们的工作使实验和理论能够共同协力探讨分子体系的性质,引起整个化学领域正在经历一场革命性的变化。下列说法正确的是( )
A. 化学不再是纯实验科学
B.化学不再需要实验
C.化学不做实验,就什么都不知道
D.未来化学的方向还是经验化
13.下列指定的微粒数目之比不等于1:1的是( )
A.NaF溶液中的Na+ 和F-
B. 中的质子和中子
C.食盐晶体中的 N a+和Cl—
D.N a H S O4稀溶液中的N a+和 S O42-
14.下列各小题均由两句话组成。请按下表选出对各题每两句话的正确判断
A B C D E
第一句话 对 对 对 错 错
第二句话 对,是对第一句话的正确解释 对,不是对第一句话的正确解释 错 对 错
⑴H2O2是氧化物,因为H2O2是由两种元素组成,且其中含氧元素 ( )
⑵NO2是硝酸的酸酐,因为NO2能与水化合生成硝酸 ( )
⑶质量比为7:4的CO和O2反应后,可得到纯净物,因为生成物是CO2 ( )
⑷氧化铁是碱性氧化物,因为铁是金属,所有金属氧化物都是碱性氧化物 ( )
15.常温下A和B两种气体组成的混合气(A的式量大于B的式量),经分析混合气体只含有氮和氢两种元素,而且不论A和B以何种比例混合,氮和氢的质量比总大于14/3。由此可确定A为 ,B为 ,其理由是
。
16.某学生课外活动小组利用图1—1—2所示装置分别做如下实验:
⑴在试管中注入某红色溶液,加热试管,溶液颜色逐
渐变浅,冷却后恢复红色,则原溶液可能是_______________
溶液;加热时溶液由红色逐渐变浅的原因是:_____________
_____________________________________________________。
⑵在试管中注入某无色溶液,加热试管,溶液变为红色,
冷却后恢复无色,则此溶液可能是________________溶液;加热时溶液由无色变为红色的原因是: __________________________________________________。
17.我国规定饮用水质量标准必须符合下列要求:
PH值 6.5-8.5
Ca2+,Mg2+总浓度 <0.0045mol/L
细菌总数 <100个/mL
以下是源水处理成自来水的工艺流程示意图
⑴源水中含Ca2+、Mg2+、HCO3—、Cl— 等,加入石灰后生成Ca(OH)2,进而发生若干复分解反应,写出其中一个离子方程式
⑵凝聚剂除去悬浮固体颗粒的过程__________(填写编号,多选倒扣)
①只有物理过程 ②只是化学过程 ③是物理和化学过程
FeSO4·7H2O常用的凝聚剂,它在水中最终生成___________沉淀。
⑶通入二氧化碳的目的是 和 。
⑷气体A的作用是__________。这种作用是基于气体A和水反应的产物具有______________性。
⑸下列物质中,______________可以作为气体A的代用品。(填写编号,多选倒扣)
①Ca(ClO)2 ②NH3(液) ③K2FeO4 ④SO2
参考答案
第1课时 (A卷)
典型题点击
1.CD 2.A 3.
讲析:1. A不正确。关键词“不同原子”要注意,因为许多元素都有同位素,若是同种元素的不同原子,如氯元素有35Cl、37Cl两种氯原子,构成氯单质的氯气分子,可能是35Cl—35Cl、35Cl—37Cl、37Cl—37Cl,他们仍属于纯净物中的单质,不属于化合物;若是不同种元素的原子组成的纯净物,则一定是化合物。B前半句不正确。因非金属氧化物可能是不成盐氧化物(CO、NO等),它们既不能跟碱反应生成盐和水,也不能跟酸反应生成盐和水。前半句反过来也不正确,如Mn2O7的相应水化物为HMnO4,所以Mn2O7是酸性氧化物,但它是金属氧化物。B
后半句正确,但后半句反过来就不正确了,如Mn2O7是酸性氧化物,Al2O3是两性氧化物。C正确。含金属元素的离子,例如:K+、[Ag(NH3)2]+、AlO2-、MnO4-等,说明金属元素也可以构成阴离子。D正确。结晶水合物有固定的化学组成,属纯净物而不是混合物。胆矾和无水CuSO4不是同一种物质,无论是胆矾分解成无水CuSO4,还是无水CuSO4水合成胆矾,都是化学变化过程。2.化学变化与物理变化的本质区别是:是否有新物质生成。甘油稀释后仍具有吸湿性,可做护肤剂,该过程中不涉及化学变化;明矾溶于水后,发生反应Al3++3H2O
Al(OH)3 +3H+,产生了Al(OH)3胶体,从而可净化水;烹鱼时加入少量的料酒和食醋可减少腥味,增加香味的原因是过程中发生了CH3COOH+C2H5OH→CH3COOC2H5+ H2O,产生了具有果香味的乙酸乙酯的缘故;烧菜用过的铁锅,由于在潮湿的环境中发生了电化腐蚀,Fe最终被氧化成Fe2O3·nH2O,而出现红棕色斑迹。后三者都是化学变化过程。
4.
物质代号 A B C D
该物质中元素的种类 2 1
每个分子中原子的总数目 4 2
其中可能的一种分子组成 X3Y或XY3 Z2 XZ或YZ X2或Y2
讲析:根据化学反应原子守恒原理,由反应:2A + 3B = 6C + D和C、D都是双原子分子可知,2个A分子 和3个B分子共有14个原子,B又是单质,通过讨论确定组成。
新活题网站
1.A 2.C 3.CD 4.D 5.C 6.C 7.B 8.A 9.D 10.C 11.B 12.B 13.D 14.B
15、①溶解 ②升华 ③挥发 ④潮解 ⑤化合 ⑥分解 ⑦风化 ⑧分解 ⑨干馏 ⑩结晶
16、⑴氮 氧 ⑵X——NO Y——N2O
17、(1)7; (其他合理答案也给分)
(2)2n(C)+n(N)+2
(3)2n(C)+n(N)+2
第1课时 (B卷)
纠错训练
1.B 2.D 3.C 4.D 5.C 6.D 7.A 8.B
检测提高
1.B 2.D 3.D 4.⑴D ⑵C 5.C 6.D 7.C 8.C 9.A 10.B 11.B 12.A 13.D 14.⑴A ⑵ E ⑶ B ⑷ C
15.N2 NH3 因为NH3中的氮和氢的质量比等于14/3
16.(1)稀氨水和酚酞 稀氨水中的NH3气逸出,所以溶液的颜色变浅
(2)溶有SO2的品红 SO2气体逸出,品红溶液恢复红色
17.(1)HCO3—+ OH—= CO32—+ H2O
Mg2++2OH-= Mg(OH)2↓
Ca2++ HCO3—+ OH-= CaCO3↓+H2O
任选其一,其他合理解也对。
(2)③ 胶状Fe(OH)3
(3)除去Ca2+ 调节PH值
(4)杀菌消毒 强氧化
(5)① ③
图1—1—1
图1—1—2
21世纪教育网 -- 中国最大型、最专业的中小学教育资源门户网站。 版权所有@21世纪教育网
同课章节目录
