山东名校2009高三化学试题分类汇编(无机推断1)
文档属性
| 名称 | 山东名校2009高三化学试题分类汇编(无机推断1) |

|
|
| 格式 | rar | ||
| 文件大小 | 418.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 其它版本 | ||
| 科目 | 化学 | ||
| 更新时间 | 2009-11-13 00:00:00 | ||
图片预览

文档简介
山东名校2009高三化学试题汇编(无机推断1)
1.(山东省金乡第一中学2008-2009高三期中考试)(7分)A~I是溶质或纯净物,其中A是生活中常用的金属单质。它们之间有如下关系:
(部分产物和反应条件略)
根据上述信息,回答下列问题:
(1)写出下列物质的化学式A ,B 。
(2) G和 SO2生成强酸F,此反应中氧化剂是_____________________________。
(3)写出①的离子方程式: 。
(4)写出②的化学方程式 。
答案..(1)Fe HNO3 (各1分,共2分) (2)H2O2 (1分)
(3)3 Fe2++4H++NO3-=3 Fe3++NO↑+2H2O (2分)
(4)3NO2+H2O=2HNO3+NO (2分)
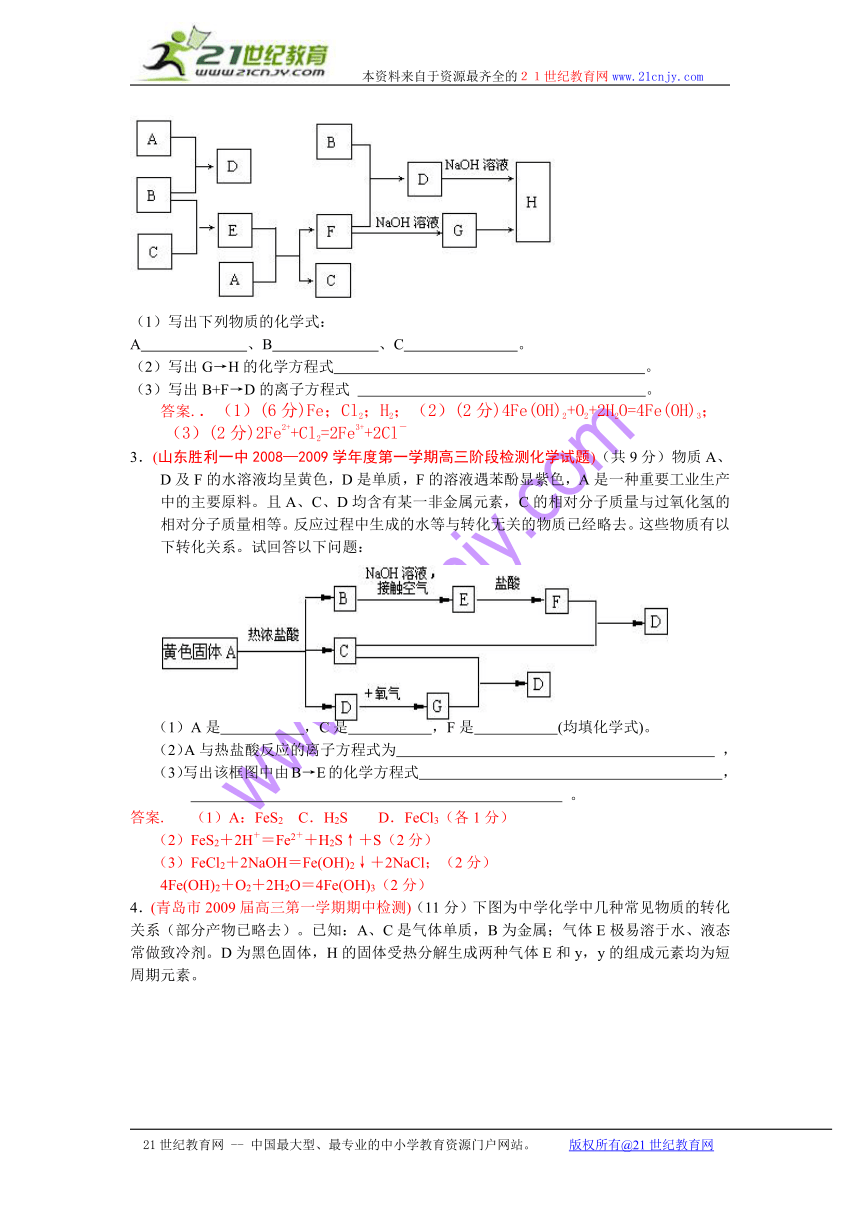
2.(山东省日照一中2009届高三阶段性测试化学试题 ) (10分)室温下,单质A、B、C分别为固体、黄绿色气体与无色气体,在合适条件下,它们可以按下面的流程进行反应。又知E溶液是无色的。请回答:
(1)写出下列物质的化学式:
A 、B 、C 。
(2)写出G→H的化学方程式 。
(3)写出B+F→D的离子方程式 。
答案..(1)(6分)Fe;Cl2;H2;(2)(2分)4Fe(OH)2+O2+2H2O=4Fe(OH)3;
(3)(2分)2Fe2++Cl2=2Fe3++2Cl-
3.(山东胜利一中2008—2009学年度第一学期高三阶段检测化学试题)(共9分)物质A、D及F的水溶液均呈黄色,D是单质,F的溶液遇苯酚显紫色,A是一种重要工业生产中的主要原料。且A、C、D均含有某一非金属元素,C的相对分子质量与过氧化氢的相对分子质量相等。反应过程中生成的水等与转化无关的物质已经略去。这些物质有以下转化关系。试回答以下问题:
(1)A是 ,C是 ,F是 (均填化学式)。
(2)A与热盐酸反应的离子方程式为 ,
(3)写出该框图中由B→E的化学方程式 ,
。
答案. (1)A:FeS2 C.H2S D.FeCl3(各1分)
(2)FeS2+2H+=Fe2++H2S↑+S(2分)
(3)FeCl2+2NaOH=Fe(OH)2↓+2NaCl;(2分)
4Fe(OH)2+O2+2H2O=4Fe(OH)3(2分)
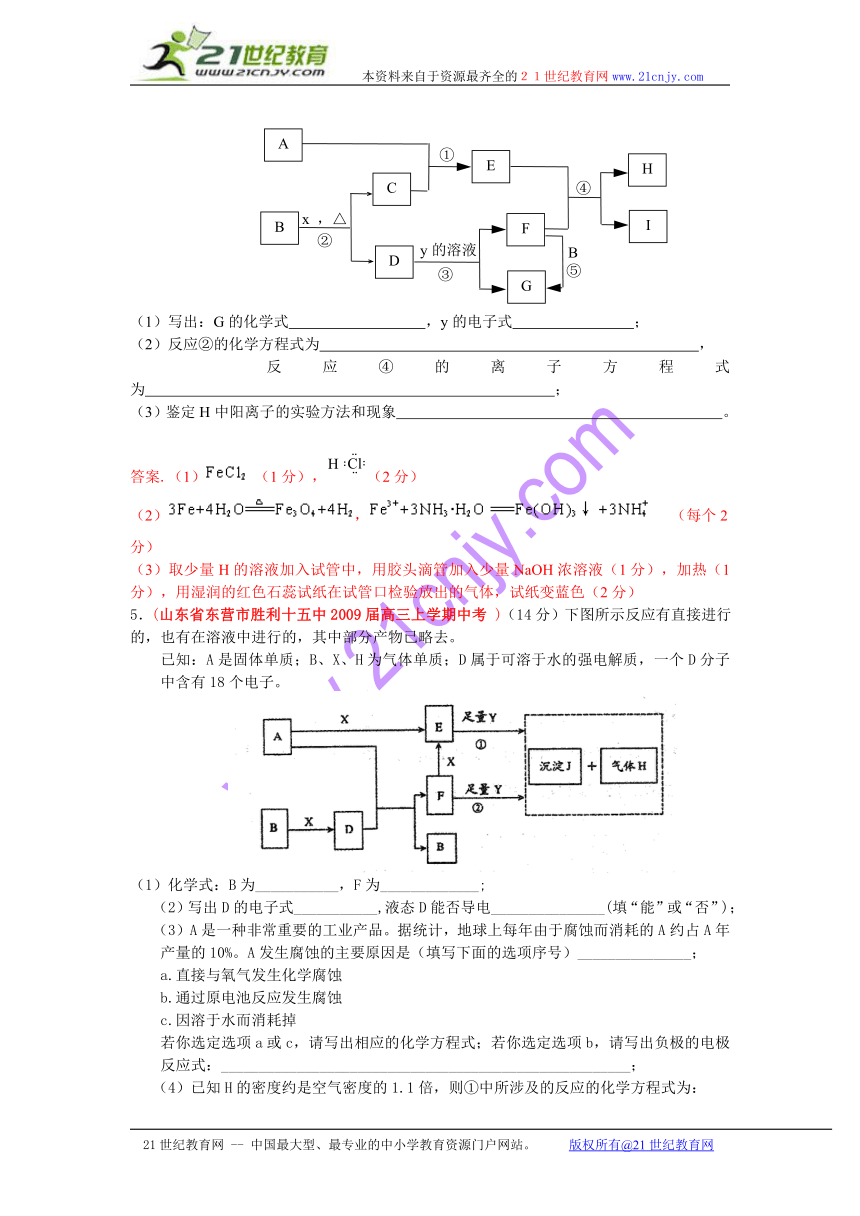
4.(青岛市2009届高三第一学期期中检测)(11分)下图为中学化学中几种常见物质的转化关系(部分产物已略去)。已知:A、C是气体单质,B为金属;气体E极易溶于水、液态常做致冷剂。D为黑色固体,H的固体受热分解生成两种气体E和y,y的组成元素均为短周期元素。
(1)写出:G的化学式 ,y的电子式 ;
(2)反应②的化学方程式为 ,
反应④的离子方程式为 ;
(3)鉴定H中阳离子的实验方法和现象 。
答案.(1) (1分),(2分)
(2), (每个2分)
(3)取少量H的溶液加入试管中,用胶头滴管加入少量NaOH浓溶液(1分),加热(1分),用湿润的红色石蕊试纸在试管口检验放出的气体,试纸变蓝色(2分)
5.(山东省东营市胜利十五中2009届高三上学期中考 )(14分)下图所示反应有直接进行的,也有在溶液中进行的,其中部分产物已略去。
已知:A是固体单质;B、X、H为气体单质;D属于可溶于水的强电解质,一个D分子中含有18个电子。
(1)化学式:B为___________,F为_____________;
(2)写出D的电子式___________,液态D能否导电_______________(填“能”或“否”);
(3)A是一种非常重要的工业产品。据统计,地球上每年由于腐蚀而消耗的A约占A年产量的10%。A发生腐蚀的主要原因是(填写下面的选项序号)_______________;
a.直接与氧气发生化学腐蚀
b.通过原电池反应发生腐蚀
c.因溶于水而消耗掉
若你选定选项a或c,请写出相应的化学方程式;若你选定选项b,请写出负极的电极反应式:______________________________________________________;
(4)已知H的密度约是空气密度的1.1倍,则①中所涉及的反应的化学方程式为:
__________________________________,_______________________________。
答案..(1)H2 FeCl2
(2) 否
(3)b Fe-2e-=Fe2+
(4)2Na2O2+2H2O=4NaOH+O2↑ FeCl3+3NaOH=Fe(OH)3↓+3NaCl
6.(山东省和兴中学2009届高三年级10月月考)(9分)下图是中学化学常见物质的转化关系(某些反应条件及部分产物已略去),A、G为日常生活中的常见金属。B、C、E、I、J为气体,其中C为黄绿色气体,J为红棕色气体。D为黑色固体,M为红褐色胶体。
请回答下列问题:
(1)A元素在周期表中位于 周期 族。
(2)以F饱和溶液制备M胶体的操作为
。
(3)鉴别L溶液和N溶液的最简单的物理方法是
。
(4)反应③的离方程式为 。
7.(1)四(1分),Ⅷ(1分)
(2)取一个烧杯,加入20mL蒸馏水,加热至沸,然后向沸水中滴加FeCl3饱和溶液
1mL~2mL,继续煮沸,待溶液呈红褐色为止;(3分)
(3)观察溶液的颜色(2分);
(4)3Fe+2NO3-+8H+==3Fe2++2NO↑+4H2O(2分);
8.(山东省和兴中学2009届高三年级10月月考)(10分)重铬酸钾是工业生产和实验室的重要氧化剂,工业上常用铬铁矿(主要成份为FeO·Cr2O3)为原料生产,实验室模拟工业法用铬铁矿制K2Cr2O7的主要工艺如下,涉及的主要反应是:6FeO·Cr2O3 + 24NaOH +7KClO3 12Na2CrO4 + 3Fe2O3 +7KCl + 12H2O,
试回答下列问题
(1)在反应器①中,有Na2CrO4生成,同时Fe2O3转变为NaFeO2,杂质SiO2、Al2O3与纯碱反应转变为可溶性盐,写出氧化铝与碳酸钠反应的化学方程式:
。
(2)NaFeO2能强烈水解,在操作②生成沉淀而除去,写出该反应的化学方程式: 。
(3)操作③的目的是什么,用简要的文字说明: 。
(4)操作④中,酸化时,CrO42-转化为Cr2O72-,写出平衡转化的离子方程式:
。
(5)称取重铬酸钾试样2.5000g配成250mL溶液,取出25.00mL于碘量瓶中,加入10mL 2mol/LH2SO4和足量碘化钾(铬的还原产物为Cr3+),放于暗处5min,然后加入100mL水,加入3mL淀粉指示剂,用0.1200mol/LNa2S2O3标准溶液滴定(I2+2S2O32-=2I-+S4O62-)。
判断达到滴定终点的依据是: 。
答案. (1)Al2O3 + Na2CO32NaAlO2 +CO2↑;(2分)
(2)NaFeO2 + 2H2O = Fe(OH)3↓ + NaOH(2分)。
(3)由于溶液在硅酸钠和偏铝酸钠发生水解,降低pH值有利于水解平衡向正反应方向移动,当pH调到7~8时,使它们水解完全,从而除去SiO32-和AlO2-。(共2分)
(4)2CrO42-+2H+ Cr2O72-+H2O(2分)
(5)当滴加最后一滴硫代硫酸钠溶液,溶液蓝色褪去,半分钟内不复现(2分)
9.(山东09德州高中三年级教学质量检测) (12分)已知B、D、E、I为五色气体,常温下C为液体,F为红棕色气体,H为淡黄色固体,L为银白色固体,M为黑色固体,其转化关系如下图所示:
(1)写出下列物质的化学式
B__________、C__________、L__________
(2)写出M的自然界中的两种常见同素异形体的名称____________________
(3)写出下列反应的化学方程式
B+I→E______________________________
K→L______________________________
答案.(1)B NH3 G HNO3 L Mg
(2)金刚石、石墨
(3)4NH3+5O24NO+6H2O MgCl2Mg+Cl2↑
10(山东青岛一中2009级高三第二次月考) (13分) A、B、C、D均为短周期元素,B与A可形成两种液态化合物,其原子个数比分别为1∶1和2∶1,且分子中电子总数分别为18和10;B与D能形成一种极易溶于水的碱性气体X,B与C能形成极易溶于水的酸性气体Y。Y分子中的电子数为18,A、B、D可形成离子化合物,其化学式为B4A3D2,其水溶液呈弱酸性。请回答:
元素符号:A ,B ,C ,D 。
写出化学方程式:
A2和X反应___________________________________________________。
B4A3D2的化学式 ,其水溶液呈酸性的离子方程式 ______________________________________________________________。
X是由___________分子(填“极性”或“非极性”),它的空间构型是___________;液态X能电离(可根据B2A电离推知),写出其电离方程式
答案. (1) A:O B:H C:Cl D:N
(2) 5O2 + 4NH34NO + 6H2O
(3) NH4NO3 NH4++ H2ONH3·H2O + H+
(4) 极性 三角锥形 2NH3NH4++ NH2-
1.(山东省金乡第一中学2008-2009高三期中考试)(7分)A~I是溶质或纯净物,其中A是生活中常用的金属单质。它们之间有如下关系:
(部分产物和反应条件略)
根据上述信息,回答下列问题:
(1)写出下列物质的化学式A ,B 。
(2) G和 SO2生成强酸F,此反应中氧化剂是_____________________________。
(3)写出①的离子方程式: 。
(4)写出②的化学方程式 。
答案..(1)Fe HNO3 (各1分,共2分) (2)H2O2 (1分)
(3)3 Fe2++4H++NO3-=3 Fe3++NO↑+2H2O (2分)
(4)3NO2+H2O=2HNO3+NO (2分)
2.(山东省日照一中2009届高三阶段性测试化学试题 ) (10分)室温下,单质A、B、C分别为固体、黄绿色气体与无色气体,在合适条件下,它们可以按下面的流程进行反应。又知E溶液是无色的。请回答:
(1)写出下列物质的化学式:
A 、B 、C 。
(2)写出G→H的化学方程式 。
(3)写出B+F→D的离子方程式 。
答案..(1)(6分)Fe;Cl2;H2;(2)(2分)4Fe(OH)2+O2+2H2O=4Fe(OH)3;
(3)(2分)2Fe2++Cl2=2Fe3++2Cl-
3.(山东胜利一中2008—2009学年度第一学期高三阶段检测化学试题)(共9分)物质A、D及F的水溶液均呈黄色,D是单质,F的溶液遇苯酚显紫色,A是一种重要工业生产中的主要原料。且A、C、D均含有某一非金属元素,C的相对分子质量与过氧化氢的相对分子质量相等。反应过程中生成的水等与转化无关的物质已经略去。这些物质有以下转化关系。试回答以下问题:
(1)A是 ,C是 ,F是 (均填化学式)。
(2)A与热盐酸反应的离子方程式为 ,
(3)写出该框图中由B→E的化学方程式 ,
。
答案. (1)A:FeS2 C.H2S D.FeCl3(各1分)
(2)FeS2+2H+=Fe2++H2S↑+S(2分)
(3)FeCl2+2NaOH=Fe(OH)2↓+2NaCl;(2分)
4Fe(OH)2+O2+2H2O=4Fe(OH)3(2分)
4.(青岛市2009届高三第一学期期中检测)(11分)下图为中学化学中几种常见物质的转化关系(部分产物已略去)。已知:A、C是气体单质,B为金属;气体E极易溶于水、液态常做致冷剂。D为黑色固体,H的固体受热分解生成两种气体E和y,y的组成元素均为短周期元素。
(1)写出:G的化学式 ,y的电子式 ;
(2)反应②的化学方程式为 ,
反应④的离子方程式为 ;
(3)鉴定H中阳离子的实验方法和现象 。
答案.(1) (1分),(2分)
(2), (每个2分)
(3)取少量H的溶液加入试管中,用胶头滴管加入少量NaOH浓溶液(1分),加热(1分),用湿润的红色石蕊试纸在试管口检验放出的气体,试纸变蓝色(2分)
5.(山东省东营市胜利十五中2009届高三上学期中考 )(14分)下图所示反应有直接进行的,也有在溶液中进行的,其中部分产物已略去。
已知:A是固体单质;B、X、H为气体单质;D属于可溶于水的强电解质,一个D分子中含有18个电子。
(1)化学式:B为___________,F为_____________;
(2)写出D的电子式___________,液态D能否导电_______________(填“能”或“否”);
(3)A是一种非常重要的工业产品。据统计,地球上每年由于腐蚀而消耗的A约占A年产量的10%。A发生腐蚀的主要原因是(填写下面的选项序号)_______________;
a.直接与氧气发生化学腐蚀
b.通过原电池反应发生腐蚀
c.因溶于水而消耗掉
若你选定选项a或c,请写出相应的化学方程式;若你选定选项b,请写出负极的电极反应式:______________________________________________________;
(4)已知H的密度约是空气密度的1.1倍,则①中所涉及的反应的化学方程式为:
__________________________________,_______________________________。
答案..(1)H2 FeCl2
(2) 否
(3)b Fe-2e-=Fe2+
(4)2Na2O2+2H2O=4NaOH+O2↑ FeCl3+3NaOH=Fe(OH)3↓+3NaCl
6.(山东省和兴中学2009届高三年级10月月考)(9分)下图是中学化学常见物质的转化关系(某些反应条件及部分产物已略去),A、G为日常生活中的常见金属。B、C、E、I、J为气体,其中C为黄绿色气体,J为红棕色气体。D为黑色固体,M为红褐色胶体。
请回答下列问题:
(1)A元素在周期表中位于 周期 族。
(2)以F饱和溶液制备M胶体的操作为
。
(3)鉴别L溶液和N溶液的最简单的物理方法是
。
(4)反应③的离方程式为 。
7.(1)四(1分),Ⅷ(1分)
(2)取一个烧杯,加入20mL蒸馏水,加热至沸,然后向沸水中滴加FeCl3饱和溶液
1mL~2mL,继续煮沸,待溶液呈红褐色为止;(3分)
(3)观察溶液的颜色(2分);
(4)3Fe+2NO3-+8H+==3Fe2++2NO↑+4H2O(2分);
8.(山东省和兴中学2009届高三年级10月月考)(10分)重铬酸钾是工业生产和实验室的重要氧化剂,工业上常用铬铁矿(主要成份为FeO·Cr2O3)为原料生产,实验室模拟工业法用铬铁矿制K2Cr2O7的主要工艺如下,涉及的主要反应是:6FeO·Cr2O3 + 24NaOH +7KClO3 12Na2CrO4 + 3Fe2O3 +7KCl + 12H2O,
试回答下列问题
(1)在反应器①中,有Na2CrO4生成,同时Fe2O3转变为NaFeO2,杂质SiO2、Al2O3与纯碱反应转变为可溶性盐,写出氧化铝与碳酸钠反应的化学方程式:
。
(2)NaFeO2能强烈水解,在操作②生成沉淀而除去,写出该反应的化学方程式: 。
(3)操作③的目的是什么,用简要的文字说明: 。
(4)操作④中,酸化时,CrO42-转化为Cr2O72-,写出平衡转化的离子方程式:
。
(5)称取重铬酸钾试样2.5000g配成250mL溶液,取出25.00mL于碘量瓶中,加入10mL 2mol/LH2SO4和足量碘化钾(铬的还原产物为Cr3+),放于暗处5min,然后加入100mL水,加入3mL淀粉指示剂,用0.1200mol/LNa2S2O3标准溶液滴定(I2+2S2O32-=2I-+S4O62-)。
判断达到滴定终点的依据是: 。
答案. (1)Al2O3 + Na2CO32NaAlO2 +CO2↑;(2分)
(2)NaFeO2 + 2H2O = Fe(OH)3↓ + NaOH(2分)。
(3)由于溶液在硅酸钠和偏铝酸钠发生水解,降低pH值有利于水解平衡向正反应方向移动,当pH调到7~8时,使它们水解完全,从而除去SiO32-和AlO2-。(共2分)
(4)2CrO42-+2H+ Cr2O72-+H2O(2分)
(5)当滴加最后一滴硫代硫酸钠溶液,溶液蓝色褪去,半分钟内不复现(2分)
9.(山东09德州高中三年级教学质量检测) (12分)已知B、D、E、I为五色气体,常温下C为液体,F为红棕色气体,H为淡黄色固体,L为银白色固体,M为黑色固体,其转化关系如下图所示:
(1)写出下列物质的化学式
B__________、C__________、L__________
(2)写出M的自然界中的两种常见同素异形体的名称____________________
(3)写出下列反应的化学方程式
B+I→E______________________________
K→L______________________________
答案.(1)B NH3 G HNO3 L Mg
(2)金刚石、石墨
(3)4NH3+5O24NO+6H2O MgCl2Mg+Cl2↑
10(山东青岛一中2009级高三第二次月考) (13分) A、B、C、D均为短周期元素,B与A可形成两种液态化合物,其原子个数比分别为1∶1和2∶1,且分子中电子总数分别为18和10;B与D能形成一种极易溶于水的碱性气体X,B与C能形成极易溶于水的酸性气体Y。Y分子中的电子数为18,A、B、D可形成离子化合物,其化学式为B4A3D2,其水溶液呈弱酸性。请回答:
元素符号:A ,B ,C ,D 。
写出化学方程式:
A2和X反应___________________________________________________。
B4A3D2的化学式 ,其水溶液呈酸性的离子方程式 ______________________________________________________________。
X是由___________分子(填“极性”或“非极性”),它的空间构型是___________;液态X能电离(可根据B2A电离推知),写出其电离方程式
答案. (1) A:O B:H C:Cl D:N
(2) 5O2 + 4NH34NO + 6H2O
(3) NH4NO3 NH4++ H2ONH3·H2O + H+
(4) 极性 三角锥形 2NH3NH4++ NH2-
同课章节目录
