第三节 化学中常用的物理量-物质的量(潍坊市教学能手)
文档属性
| 名称 | 第三节 化学中常用的物理量-物质的量(潍坊市教学能手) |

|
|
| 格式 | rar | ||
| 文件大小 | 286.9KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁科版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2009-11-16 00:00:00 | ||
图片预览





文档简介
课件17张PPT。物质的量
(mol) 体积
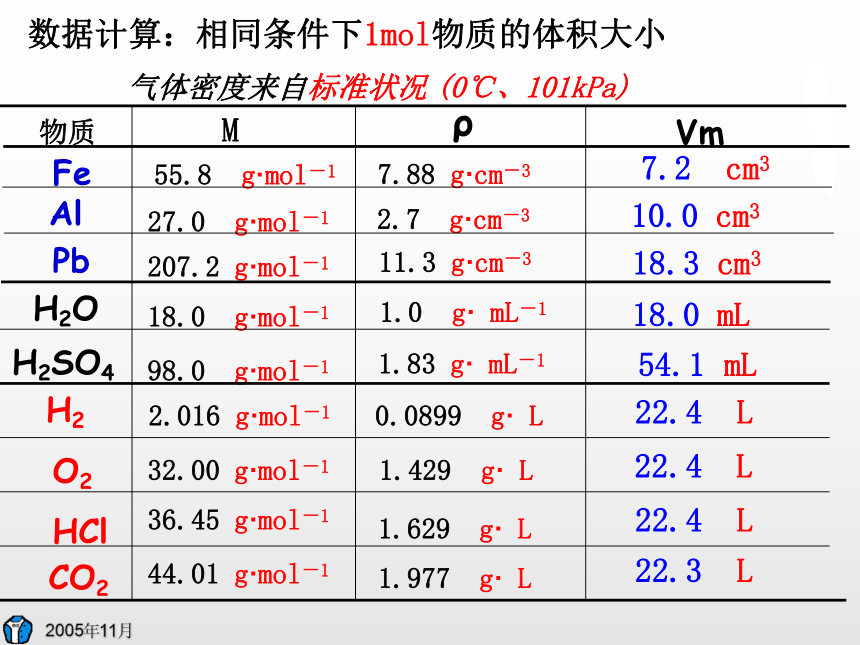
(L或mL)1mol物质的体积(Vm)主题: 研究1mol 物质所占的体积物质FeAlPbH2OH2SO4数据计算:相同条件下1mol物质的体积大小Mρ1.0 g· mL-155.8 g·mol-127.0 g·mol-1207.2 g·mol-118.0 g·mol-198.0 g·mol-11.83 g· mL-1 11.3 g·cm-32.7 g·cm-37.88 g·cm-318.3 cm310.0 cm37.2 cm3Vm18.0 mL 54.1 mLH2O2HClCO2 2.016 g·mol-132.00 g·mol-136.45 g·mol-144.01 g·mol-10.0899 g· L1.429 g· L
1.629 g· L1.977 g· L22.4 L22.4 L
22.4 L22.3 L
气体密度来自标准状况(0℃、101kPa) 相同条件下,1mol的气体体积要比固体、液体大得多。 在标准状况下,1mol 任何气体的体积大约为 22.4 L 我们发现的规律: 相同条件下, 1mol的固体、液体体积一般是不同的。
而相同条件下,1mol的不同气体体积几乎相同.简化处理:
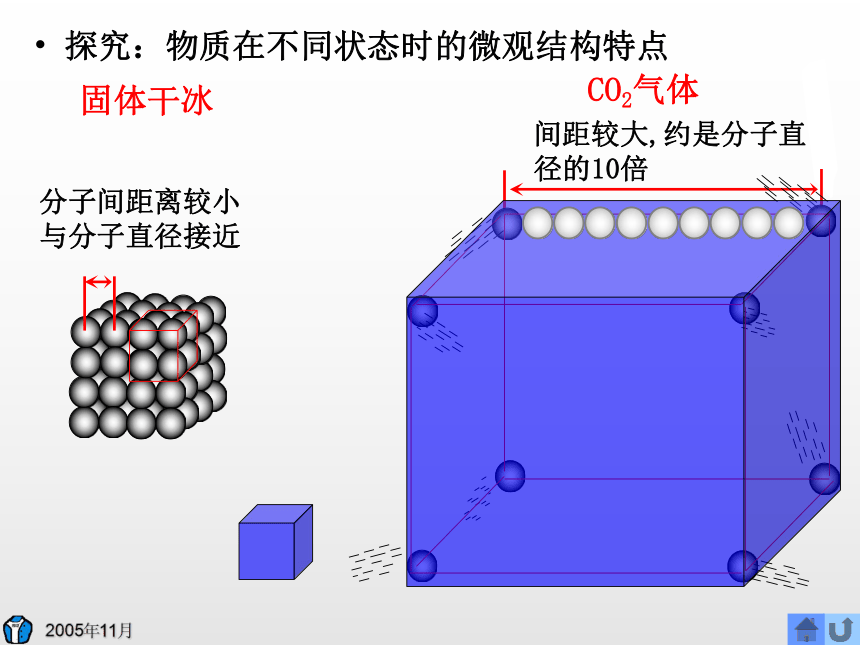
1 mol 同种物质在气态、液态时的体积有何关系?气态远远大于液态。构成物质的粒子间有间隙,不同条件下,粒子间距不同。气体的粒子间距比固体、液体大很多。我们发现的规律:探究微观原因:相同条件下,1mol的气体体积要比固体、液体大得多。固体干冰CO2气体探究:物质在不同状态时的微观结构特点气体加压气体压强和温度对气体体积的影响示意图探究:粒子大小和粒子间距
对物质体积的影响示意图我们再进一步发现的规律:在同温同压下,1 mol 不同气体具有几乎相同的体积。在同温同压下,不同气体的粒子平均间距相同导致 同温同压下
相同体积的任何气体都含有相同的物质的量。 同温同压下
相同物质的量的任何气体都有相同的体积。理想化处理:相同体积的任何气体都含有相同的分子数。气体摩尔体积 概念:单位物质的量的气体所占的体积。 同温同压下,Vm任何气体的气体摩尔体积几乎相等 辨析和应用1mol任何物质的体积在标准状况下都约为22.4 L。1mol气体的体积约为22.4 L。任何气体的体积在标准状况约为22.4 L 。1mol空气的体积在标准状况下约是22.4 L。标准状况下,22.4 L任何气体约含6.02×1023个分子。物质缺少条件物质的量√√√标准状况下,n mol任何气体的体积约为 22.4n L。 在某温度和压强时,若气体摩尔体积为 Vm L/mol,
则该条件下, n mol任何气体的体积约为 n×Vm L。√ 在同温同压下,若两种气体的均为1 L,则它们的物质的量相等,它们的质量也相等。质量不相等 同温同压下
不同气体的密度之比等于它们的摩尔质量之比。 辨析和应用实验、数据归纳发现规律讨论、探究进一步发现规律形成结论课堂主题反馈、应用1mol 物质所占的体积质量 物质的量 微粒的个数
标准状况下气体体积 ÷M×M×NA÷NA×22.4L/mol÷ 22.4L/mol研究性课题在非标准状况下,气体的摩尔体积是否可能也
为22.4升?请设计实验证明你的结论。FePbH2OH2SO4
(mol) 体积
(L或mL)1mol物质的体积(Vm)主题: 研究1mol 物质所占的体积物质FeAlPbH2OH2SO4数据计算:相同条件下1mol物质的体积大小Mρ1.0 g· mL-155.8 g·mol-127.0 g·mol-1207.2 g·mol-118.0 g·mol-198.0 g·mol-11.83 g· mL-1 11.3 g·cm-32.7 g·cm-37.88 g·cm-318.3 cm310.0 cm37.2 cm3Vm18.0 mL 54.1 mLH2O2HClCO2 2.016 g·mol-132.00 g·mol-136.45 g·mol-144.01 g·mol-10.0899 g· L1.429 g· L
1.629 g· L1.977 g· L22.4 L22.4 L
22.4 L22.3 L
气体密度来自标准状况(0℃、101kPa) 相同条件下,1mol的气体体积要比固体、液体大得多。 在标准状况下,1mol 任何气体的体积大约为 22.4 L 我们发现的规律: 相同条件下, 1mol的固体、液体体积一般是不同的。
而相同条件下,1mol的不同气体体积几乎相同.简化处理:
1 mol 同种物质在气态、液态时的体积有何关系?气态远远大于液态。构成物质的粒子间有间隙,不同条件下,粒子间距不同。气体的粒子间距比固体、液体大很多。我们发现的规律:探究微观原因:相同条件下,1mol的气体体积要比固体、液体大得多。固体干冰CO2气体探究:物质在不同状态时的微观结构特点气体加压气体压强和温度对气体体积的影响示意图探究:粒子大小和粒子间距
对物质体积的影响示意图我们再进一步发现的规律:在同温同压下,1 mol 不同气体具有几乎相同的体积。在同温同压下,不同气体的粒子平均间距相同导致 同温同压下
相同体积的任何气体都含有相同的物质的量。 同温同压下
相同物质的量的任何气体都有相同的体积。理想化处理:相同体积的任何气体都含有相同的分子数。气体摩尔体积 概念:单位物质的量的气体所占的体积。 同温同压下,Vm任何气体的气体摩尔体积几乎相等 辨析和应用1mol任何物质的体积在标准状况下都约为22.4 L。1mol气体的体积约为22.4 L。任何气体的体积在标准状况约为22.4 L 。1mol空气的体积在标准状况下约是22.4 L。标准状况下,22.4 L任何气体约含6.02×1023个分子。物质缺少条件物质的量√√√标准状况下,n mol任何气体的体积约为 22.4n L。 在某温度和压强时,若气体摩尔体积为 Vm L/mol,
则该条件下, n mol任何气体的体积约为 n×Vm L。√ 在同温同压下,若两种气体的均为1 L,则它们的物质的量相等,它们的质量也相等。质量不相等 同温同压下
不同气体的密度之比等于它们的摩尔质量之比。 辨析和应用实验、数据归纳发现规律讨论、探究进一步发现规律形成结论课堂主题反馈、应用1mol 物质所占的体积质量 物质的量 微粒的个数
标准状况下气体体积 ÷M×M×NA÷NA×22.4L/mol÷ 22.4L/mol研究性课题在非标准状况下,气体的摩尔体积是否可能也
为22.4升?请设计实验证明你的结论。FePbH2OH2SO4
