第三节 化学中常用的物理量-物质的量第二课时气体摩尔体积 物质的量浓度溶液课件(潍坊教学能手)
文档属性
| 名称 | 第三节 化学中常用的物理量-物质的量第二课时气体摩尔体积 物质的量浓度溶液课件(潍坊教学能手) |

|
|
| 格式 | rar | ||
| 文件大小 | 206.2KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁科版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2009-11-16 00:00:00 | ||
图片预览





文档简介
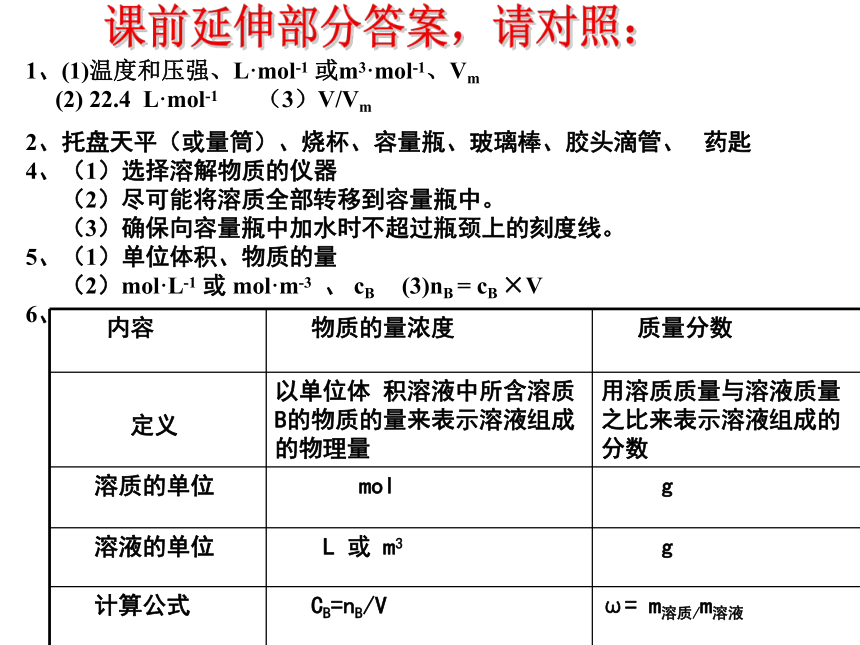
课件14张PPT。第3节 化学中常用的物理量——物质的量第二课时 气体摩尔体积 物质的量浓度讲课人:刘秀英2009.91、(1)温度和压强、L·mol-1?或m3·mol-1、Vm
(2) 22.4 L·mol-1 (3)V/Vm
2、托盘天平(或量筒)、烧杯、容量瓶、玻璃棒、胶头滴管、 药匙
4、(1)选择溶解物质的仪器
(2)尽可能将溶质全部转移到容量瓶中。
(3)确保向容量瓶中加水时不超过瓶颈上的刻度线。
5、(1)单位体积、物质的量
(2)mol·L-1 或 mol·m-3 、 cB (3)nB = cB ×V
6、 课前延伸部分答案,请对照:
1、如何理解和应用气体摩尔体积?
2、如何正确配制一定物质的量浓度的溶液 ?
3、如何理解物质的量浓度概念?
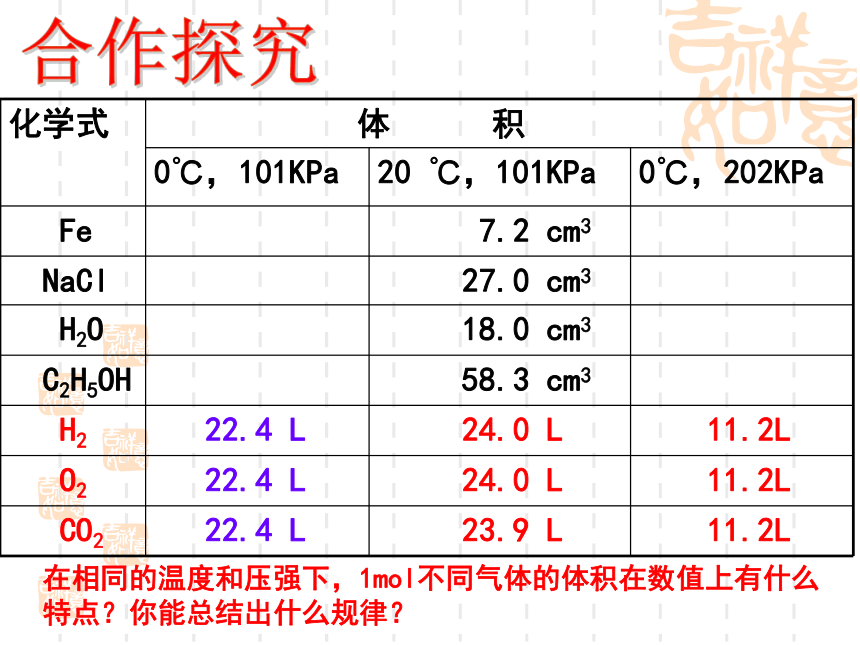
主要的问题:?在相同的温度和压强下,1mol不同气体的体积在数值上有什么特点?你能总结出什么规律? 合作探究规律在相同的温度和压强下,1mol任何气体所占的体积在数值上近似相等。精讲点拨(1)气体摩尔体积:一定的温度和压强下,单位物质的量的气体所占的体积。(2)标准状况下,Vm约为22.4 L·mol-1
例1.你能判断下列说法中哪些是正确的吗?说出你的理由。
A. 1 mol O2 和1molN2 所占的体积都约为22.4L
B. H2的气体摩尔体积约为22.4L
C. 在标准状况下,1mol H2O 所占的体积约为 22.4L
D. 在标准状况下,22.4L Cl2的物质的量约为1 mol精讲点拨 使用标准状况下的气体摩尔体积时应注意的问题:
(1)注意条件,必须是标准状况(0℃、101kPa)。
(2)注意适用对象,气体摩尔体积适用的对象只限于 气体,不管是 纯净气体还是 混合气体。
(3)注意22.4 L·mol-1 是近似值。 合作探究 试着配置0.1 L NaCl溶液,其中溶质的物质的量
为 0.04 mol。请评价下列实验方案是否可行:
方案一、用量筒量100mL水,将0.04×58.5g即2.3 g NaCl溶于其中。
方案二、将2.3 g NaCl溶于水里,加水至烧杯100mL刻度线处。
方案三、将2.3 g NaCl装入100mL容量瓶中,加水至刻度线。
方案四、将2.3 g NaCl溶于水里,再将溶液转移至容量瓶,加水至刻度线处。 为保证你配置的溶液浓度的准确性,请讨论以下
问题并说明理由:
(1)?你选择的溶解物质的仪器是什么?
(2)怎样尽可能将溶质全部转移到容量瓶中?
(3)?如何确保向容量瓶中加水时不超过瓶颈上的刻度线?
合作探究配制一定体积的溶液的实验步骤及注意事项:
(1)计算
(2)称量
(3)溶解 应在烧杯中溶解并用玻璃棒搅拌促溶。
(4)转移 为避免液体洒在外面,一般用玻璃棒引流。
(5)洗涤 用少量蒸馏水洗涤烧杯和玻璃棒2-3次,
洗涤液要全部转移到容量瓶中。
(6)定容 向容量瓶中加入蒸馏水,在距离刻度1-2厘米时,
改用胶头滴管滴加蒸馏水至刻度线。
(7)摇匀
(8)装瓶 容量瓶中不能存放溶液,因此要把配制好的
溶液转移到试剂瓶中,贴好标签。 精讲点拨如何理解物质的量浓度的概念?合作探究例2 判断下列说法是否正确,并说明理由:
(1)1L水中溶解了1molNaCl,该溶液的物质的量浓度为1mol/L
(2)从2 mol/L的H2SO4溶液中取出0.5L, 该溶液的物质的量浓度
为1mol/L
(3)2 mol·L-1的NaOH溶液是指每升溶液中含有2 mol NaOH a.溶质的物质的量、溶液的体积、物质的量浓度之间存在的关系
是CB=
b.体积是指 的体积,而不是 的体积;
c.溶质的量用 表示,不能用质量表示;
d.从一定物质的量浓度的溶液中取出任意体积的溶液其浓度 。 精讲点拨溶液溶剂物质的量不变本节回顾二、配制一定物质的量浓度的溶液
计算→称量→溶解→转移→洗涤→定容→摇匀→装瓶1. D
2. 1、 1
3. (1)①②③④⑤ 500mL容量瓶
(2)搅拌;引流
(3)②①③⑧⑤⑥⑦④
你做对了吗?谢谢指导!容量瓶
(2) 22.4 L·mol-1 (3)V/Vm
2、托盘天平(或量筒)、烧杯、容量瓶、玻璃棒、胶头滴管、 药匙
4、(1)选择溶解物质的仪器
(2)尽可能将溶质全部转移到容量瓶中。
(3)确保向容量瓶中加水时不超过瓶颈上的刻度线。
5、(1)单位体积、物质的量
(2)mol·L-1 或 mol·m-3 、 cB (3)nB = cB ×V
6、 课前延伸部分答案,请对照:
1、如何理解和应用气体摩尔体积?
2、如何正确配制一定物质的量浓度的溶液 ?
3、如何理解物质的量浓度概念?
主要的问题:?在相同的温度和压强下,1mol不同气体的体积在数值上有什么特点?你能总结出什么规律? 合作探究规律在相同的温度和压强下,1mol任何气体所占的体积在数值上近似相等。精讲点拨(1)气体摩尔体积:一定的温度和压强下,单位物质的量的气体所占的体积。(2)标准状况下,Vm约为22.4 L·mol-1
例1.你能判断下列说法中哪些是正确的吗?说出你的理由。
A. 1 mol O2 和1molN2 所占的体积都约为22.4L
B. H2的气体摩尔体积约为22.4L
C. 在标准状况下,1mol H2O 所占的体积约为 22.4L
D. 在标准状况下,22.4L Cl2的物质的量约为1 mol精讲点拨 使用标准状况下的气体摩尔体积时应注意的问题:
(1)注意条件,必须是标准状况(0℃、101kPa)。
(2)注意适用对象,气体摩尔体积适用的对象只限于 气体,不管是 纯净气体还是 混合气体。
(3)注意22.4 L·mol-1 是近似值。 合作探究 试着配置0.1 L NaCl溶液,其中溶质的物质的量
为 0.04 mol。请评价下列实验方案是否可行:
方案一、用量筒量100mL水,将0.04×58.5g即2.3 g NaCl溶于其中。
方案二、将2.3 g NaCl溶于水里,加水至烧杯100mL刻度线处。
方案三、将2.3 g NaCl装入100mL容量瓶中,加水至刻度线。
方案四、将2.3 g NaCl溶于水里,再将溶液转移至容量瓶,加水至刻度线处。 为保证你配置的溶液浓度的准确性,请讨论以下
问题并说明理由:
(1)?你选择的溶解物质的仪器是什么?
(2)怎样尽可能将溶质全部转移到容量瓶中?
(3)?如何确保向容量瓶中加水时不超过瓶颈上的刻度线?
合作探究配制一定体积的溶液的实验步骤及注意事项:
(1)计算
(2)称量
(3)溶解 应在烧杯中溶解并用玻璃棒搅拌促溶。
(4)转移 为避免液体洒在外面,一般用玻璃棒引流。
(5)洗涤 用少量蒸馏水洗涤烧杯和玻璃棒2-3次,
洗涤液要全部转移到容量瓶中。
(6)定容 向容量瓶中加入蒸馏水,在距离刻度1-2厘米时,
改用胶头滴管滴加蒸馏水至刻度线。
(7)摇匀
(8)装瓶 容量瓶中不能存放溶液,因此要把配制好的
溶液转移到试剂瓶中,贴好标签。 精讲点拨如何理解物质的量浓度的概念?合作探究例2 判断下列说法是否正确,并说明理由:
(1)1L水中溶解了1molNaCl,该溶液的物质的量浓度为1mol/L
(2)从2 mol/L的H2SO4溶液中取出0.5L, 该溶液的物质的量浓度
为1mol/L
(3)2 mol·L-1的NaOH溶液是指每升溶液中含有2 mol NaOH a.溶质的物质的量、溶液的体积、物质的量浓度之间存在的关系
是CB=
b.体积是指 的体积,而不是 的体积;
c.溶质的量用 表示,不能用质量表示;
d.从一定物质的量浓度的溶液中取出任意体积的溶液其浓度 。 精讲点拨溶液溶剂物质的量不变本节回顾二、配制一定物质的量浓度的溶液
计算→称量→溶解→转移→洗涤→定容→摇匀→装瓶1. D
2. 1、 1
3. (1)①②③④⑤ 500mL容量瓶
(2)搅拌;引流
(3)②①③⑧⑤⑥⑦④
你做对了吗?谢谢指导!容量瓶
