化学平衡课件
图片预览


文档简介
课件12张PPT。化学平衡图像化学平衡图象题型化学平衡图象分析的一般方法:
一看面:看清图象中横坐标和纵坐标的含义。
二看线:弄清图象中线的斜率或线走势的意义
三看点:明确曲线的起点、终点、交点及拐点等
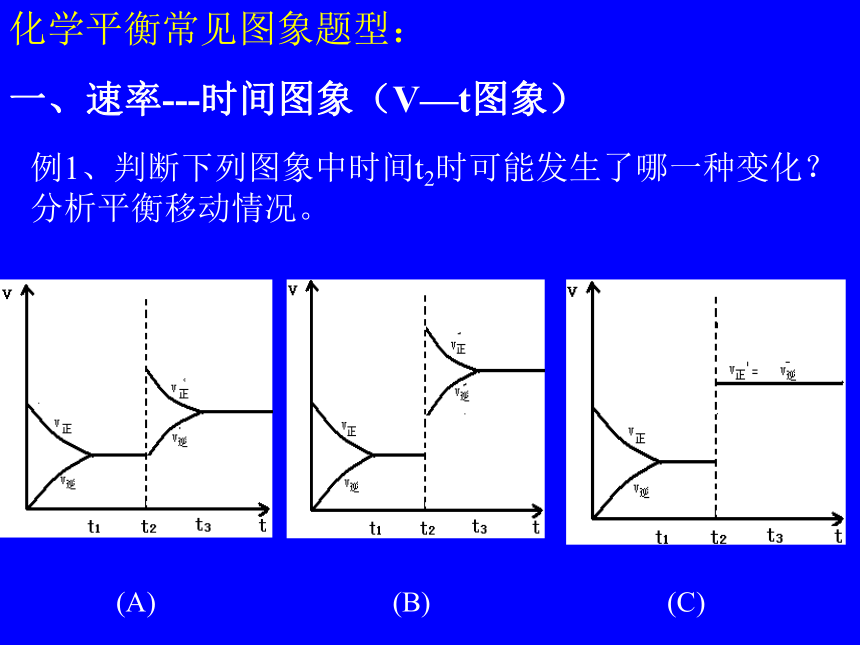
四看是否需要辅助线。化学平衡常见图象题型:一、速率---时间图象(V—t图象)例1、判断下列图象中时间t2时可能发生了哪一种变化? 分析平衡移动情况。 (A) (B) (C)1、对于可逆反应:N2(g)+3H2(g) 2NH3(g)
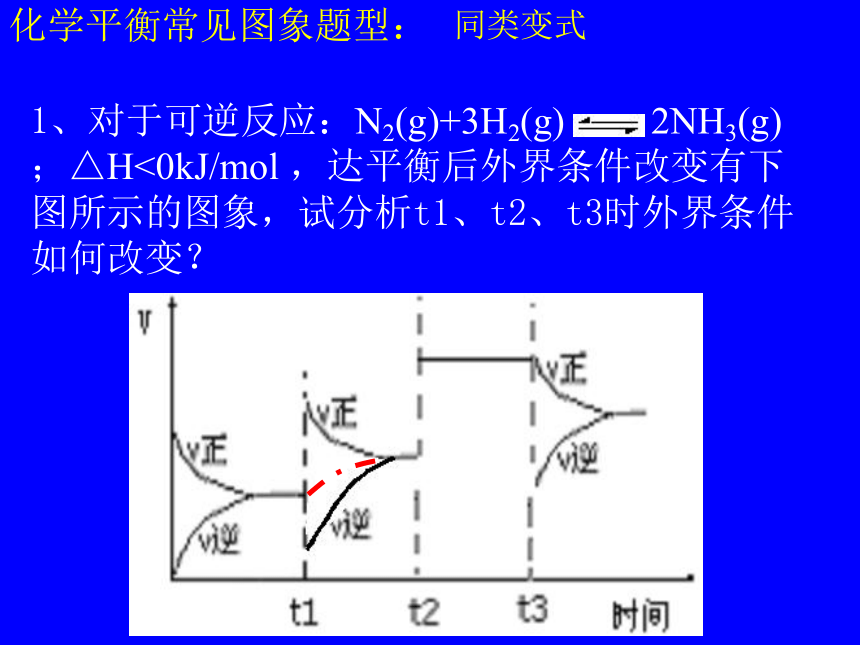
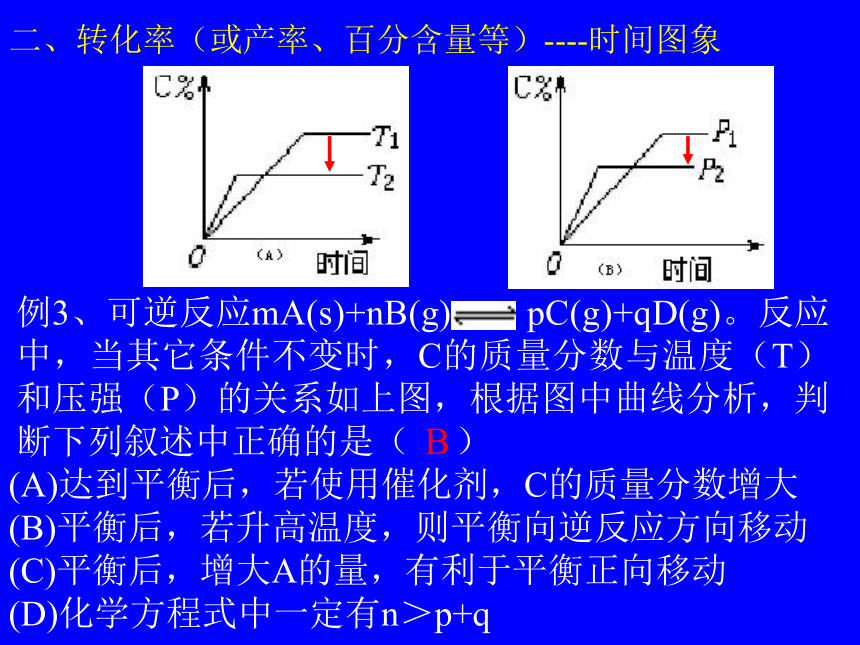
;△H<0kJ/mol ,达平衡后外界条件改变有下图所示的图象,试分析t1、t2、t3时外界条件如何改变?化学平衡常见图象题型:同类变式(A)达到平衡后,若使用催化剂,C的质量分数增大
(B)平衡后,若升高温度,则平衡向逆反应方向移动
(C)平衡后,增大A的量,有利于平衡正向移动
(D)化学方程式中一定有n>p+q例3、可逆反应mA(s)+nB(g) pC(g)+qD(g)。反应中,当其它条件不变时,C的质量分数与温度(T)和压强(P)的关系如上图,根据图中曲线分析,判断下列叙述中正确的是( )B二、转化率(或产率、百分含量等)----时间图象化学平衡常见图象题型:可采取的措施是( )
A、加入催化剂
B、增大Y的浓度
C、降低温度
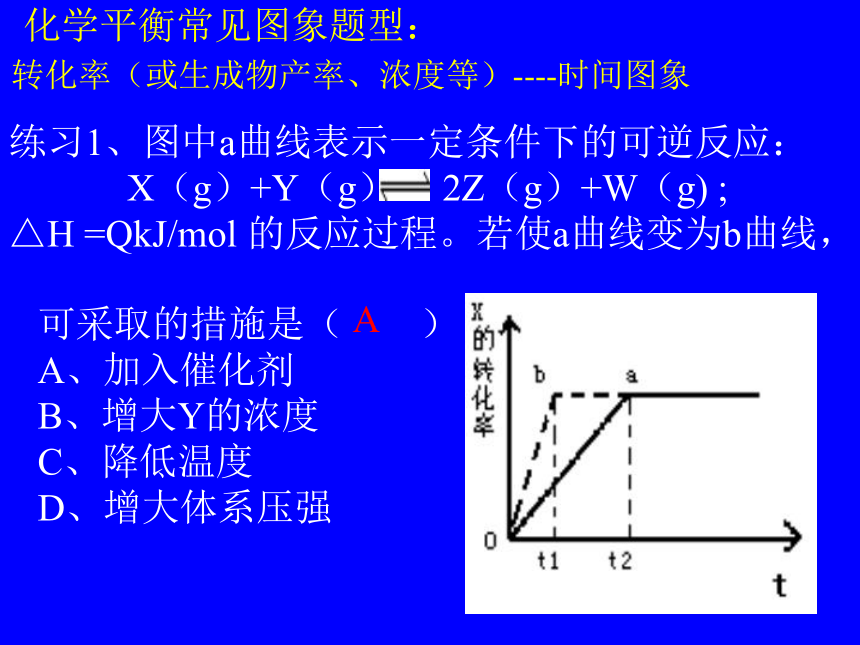
D、增大体系压强A二、转化率(或生成物产率、浓度等)----时间图象练习1、图中a曲线表示一定条件下的可逆反应:
X(g)+Y(g) 2Z(g)+W(g) ;
△H =QkJ/mol 的反应过程。若使a曲线变为b曲线,化学平衡常见图象题型:2、在密闭容器中进行下列反应:
M(g)+N(g) R(g)+2L,在不同条件下R的百分含量R%的变化情况如下图,下列叙述正确的是( )
A、正反应吸热,L是气体
B、正反应吸热,L是固体
C、正反应放热,L是气体
D、正反应放热,L是固体或液体C同类变式例4、在可逆反应mA(g)+nB(g) pC(g);△H<0中m、n、p为系数,且m+n>p。分析下列各图,在平衡体系中A的质量分数与温度t℃、压强P关系正确的是( )化学平衡常见图象题型:三、百分含量(转化率或产率)--压强(或温度)图象B化学平衡常见图象题型:同类变式1.如图所示,反应:X(气)+3Y(气) 2Z(气);△H<0 。在不同温度、不同压强(P1>P2)下达到平衡时,混合气体中Z的百分含量随温度变化的曲线应为( )C化学平衡常见图象题型:2、mA(s)+nB(g) qC(g);ΔH<0的可逆反应,在一定温度下的密闭容器中进行,平衡时B的体积分数V(B)%与压强(P)关系如下图所示,下列叙述正确的是( )
A、m+n
一看面:看清图象中横坐标和纵坐标的含义。
二看线:弄清图象中线的斜率或线走势的意义
三看点:明确曲线的起点、终点、交点及拐点等
四看是否需要辅助线。化学平衡常见图象题型:一、速率---时间图象(V—t图象)例1、判断下列图象中时间t2时可能发生了哪一种变化? 分析平衡移动情况。 (A) (B) (C)1、对于可逆反应:N2(g)+3H2(g) 2NH3(g)
;△H<0kJ/mol ,达平衡后外界条件改变有下图所示的图象,试分析t1、t2、t3时外界条件如何改变?化学平衡常见图象题型:同类变式(A)达到平衡后,若使用催化剂,C的质量分数增大
(B)平衡后,若升高温度,则平衡向逆反应方向移动
(C)平衡后,增大A的量,有利于平衡正向移动
(D)化学方程式中一定有n>p+q例3、可逆反应mA(s)+nB(g) pC(g)+qD(g)。反应中,当其它条件不变时,C的质量分数与温度(T)和压强(P)的关系如上图,根据图中曲线分析,判断下列叙述中正确的是( )B二、转化率(或产率、百分含量等)----时间图象化学平衡常见图象题型:可采取的措施是( )
A、加入催化剂
B、增大Y的浓度
C、降低温度
D、增大体系压强A二、转化率(或生成物产率、浓度等)----时间图象练习1、图中a曲线表示一定条件下的可逆反应:
X(g)+Y(g) 2Z(g)+W(g) ;
△H =QkJ/mol 的反应过程。若使a曲线变为b曲线,化学平衡常见图象题型:2、在密闭容器中进行下列反应:
M(g)+N(g) R(g)+2L,在不同条件下R的百分含量R%的变化情况如下图,下列叙述正确的是( )
A、正反应吸热,L是气体
B、正反应吸热,L是固体
C、正反应放热,L是气体
D、正反应放热,L是固体或液体C同类变式例4、在可逆反应mA(g)+nB(g) pC(g);△H<0中m、n、p为系数,且m+n>p。分析下列各图,在平衡体系中A的质量分数与温度t℃、压强P关系正确的是( )化学平衡常见图象题型:三、百分含量(转化率或产率)--压强(或温度)图象B化学平衡常见图象题型:同类变式1.如图所示,反应:X(气)+3Y(气) 2Z(气);△H<0 。在不同温度、不同压强(P1>P2)下达到平衡时,混合气体中Z的百分含量随温度变化的曲线应为( )C化学平衡常见图象题型:2、mA(s)+nB(g) qC(g);ΔH<0的可逆反应,在一定温度下的密闭容器中进行,平衡时B的体积分数V(B)%与压强(P)关系如下图所示,下列叙述正确的是( )
A、m+n
q
C、X点时的状态,V正>V逆
D、X点比Y点混和物的正
反应速率慢B、C小结小结:本节课主要复习了化学平衡的几种典型的图象题型,只有在正确理解化学平衡相关规律及准确识图的基础上,才能较好地解题。再见
