化学:8.2《铝和吕合金的崛起》学案(沪科版高二第一学期)
文档属性
| 名称 | 化学:8.2《铝和吕合金的崛起》学案(沪科版高二第一学期) |

|
|
| 格式 | rar | ||
| 文件大小 | 51.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪科版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2009-11-29 00:00:00 | ||
图片预览


文档简介
本资料来自于资源最齐全的21世纪教育网www.21cnjy.com
铝和铝合金的崛起
一、铝的单质和化合物的相互转化关系图:
(一)有关铝及其化合物转化的离子方程式:
铝与酸的反应:2Al+6H+=2Al3++3H2↑
铝与碱溶液的反应:2Al+2OH-+2H2O=2AlO2-+3H2↑
氧化铝与酸的反应:Al2O3+6H+=2Al3++3H2O
氧化铝与碱溶液的反应:Al2O3+2OH-=2AlO2-+H2O
Al3+与强碱和弱碱的反应
Al3++3OH-=Al(OH)3↓ (碱少量)Al3++4OH-=AlO2-+2H2O(碱过量)
Al3++3NH3·H2O=Al(OH)3↓+3NH4+
氢氧化铝与强酸和强碱的反应:
Al(OH)3+3H+=Al3++3H2O Al(OH)3+OH-=AlO2-+2H2O
偏铝酸根与强酸和弱酸的反应:
AlO2-+H++H2O=Al(OH)3↓(酸少量)AlO2-+4H+=Al3++2H2O(酸过量)
2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32-(CO2少量)
AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-(CO2过量)
(二)氢氧化铝的酸式电离和碱式电离:
AlO2-+H++H2OAl(OH)3Al3++3OH-
(三)Al3+与AlO2-的有关水解反应:
Al3++3H2OAl(OH)3+3H+ AlO2-+2H2OAl(OH)3+OH-
Al3++3AlO2-+6H2O=4Al(OH)3↓
*Al3++3HCO3-=Al(OH)3↓+3CO2↑(泡沫灭火器工作原理)
*2Al3++3S2-+6H2O=2Al(OH)3↓+3H2S↑(Al2S3只能以固体方式存在)
*2Al3++3CO32-+3H2O=2Al(OH)3↓+3CO2↑
[同步练习]:
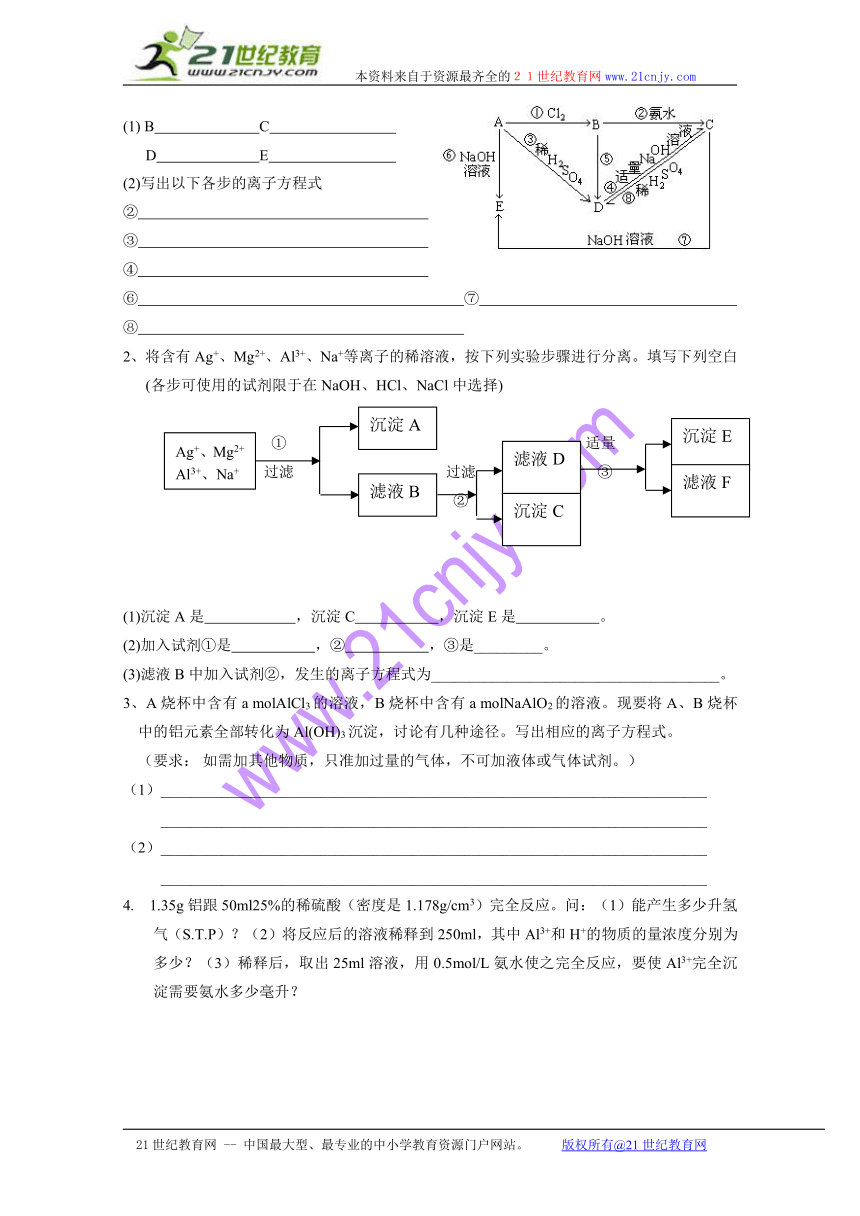
1、已知A为金属单质Al, 根据下列变化判断A、B、C、D、E各是什么物质?写出有关的离子方程式
(1) B C
D E
(2)写出以下各步的离子方程式
② ③
④ ⑥ ⑦ ⑧
2、将含有Ag+、Mg2+、Al3+、Na+等离子的稀溶液,按下列实验步骤进行分离。填写下列空白(各步可使用的试剂限于在NaOH、HCl、NaCl中选择)
① 适量
过滤 过滤 ③
②
(1)沉淀A是 ,沉淀C ,沉淀E是 。
(2)加入试剂①是 ,② ,③是_________。
(3)滤液B中加入试剂②,发生的离子方程式为______________________________________。
3、A烧杯中含有a molAlCl3的溶液,B烧杯中含有a molNaAlO2的溶液。现要将A、B烧杯中的铝元素全部转化为Al(OH)3沉淀,讨论有几种途径。写出相应的离子方程式。
(要求: 如需加其他物质,只准加过量的气体,不可加液体或气体试剂。)
(1)________________________________________________________________________
________________________________________________________________________
(2)________________________________________________________________________
________________________________________________________________________
4. 1.35g铝跟50ml25%的稀硫酸(密度是1.178g/cm3)完全反应。问:(1)能产生多少升氢气(S.T.P)?(2)将反应后的溶液稀释到250ml,其中Al3+和H+的物质的量浓度分别为多少?(3)稀释后,取出25ml溶液,用0.5mol/L氨水使之完全反应,要使Al3+完全沉淀需要氨水多少毫升?
5、在240ml0.2mol/LAl2(SO4)3溶液中加入多少1mol/LNaOH溶液,才能得到3.9g沉淀?
二、有关图像问题与计算
[例]在下图中,横坐标为向一定量的某溶液中加入某种物质的量,纵坐标为生成沉淀的量。从图中,选择适合表中各题要求的序号填入表中
溶液 加(或通入)物质 序号
⑴饱和石灰水 通入过量CO2
⑵AlCl3溶液 加入过量浓氨水
⑶含少量NaOH的NaAlO 2溶液 通入过量CO2
⑷含少量NaOH的NaAlO 2溶液 逐滴加入稀盐酸
⑸MgCl2、AlCl3混合溶液 逐滴加入NaOH溶液至过量
⑹NaOH溶液 逐滴加入Al2(SO4)3溶液至过量
⑺稀硫酸溶液 逐滴加入NaAlO 2溶液至过量
⑻含少量盐酸的AlCl3溶液 逐滴加入KOH溶液至过量
[同步练习]
1、现有0.1mol/L的AlCl3溶液和0.1mol/L的氢氧化钠溶液,进行下面的实验。
(1)在试管中盛有上述AlCl3溶液10mL,向其中逐渐滴入上述的NaOH溶液。
①根据加入氢氧化钠溶液用量,画出加入NaOH溶液与生成沉淀的关系图。
②生成沉淀质量最多时,需NaOH溶液____________mL。
(2)向盛有10mLNaOH溶液的试管中滴入AlCl3溶液,同时不停摇动试管,出现的现象是什么?写出上述过程的有关离子方程式。
2、向100 ml水中投入由4.6gNa和5.4gAl组成的混合物,充分反应后,
(1)计算放出H2多少升(标准状况下)?
(2)向滤液中逐滴加入2 mol/L的H2SO4溶液,生成沉淀的最大值是多少,此时消耗H2SO4溶液的体积是多少?
(3)生成沉淀后,再加入H2SO4溶液,使沉淀刚好完全溶解,此时消耗H2SO4溶液的体积是多少?
(4)在右图中画出相应的图像。
3、往未知浓度的AlCl3和MgCl2混合溶液100mL中逐滴加入0.1mol/LNaOH溶液,沉淀质量随加入碱液体积变化关系如图所示。求MgCl2和AlCl3的物质的量浓度。
4、将一定质量的Mg、Al合金全部溶解在500mL盐酸中(体积变化不计),取10mL反应后的溶液,用1mol/LNaOH溶液滴定得下图关系。
(1)求Mg,Al质量各是多少?
(2)求盐酸的物质的量浓度为多少mol/L
参考答案:
三、填空题
27、(1)A.Al B.AlCl3 C.Al(OH)3 D.Al2(SO4)3 E.NaAlO2
(2) ②
③ ④
⑥
⑦ ⑧
30、由50→60mL时,可知10mLNaOH溶液刚好溶解了Al(OH)3,故产生这些Al(OH)3需30mLNaOH,则在50mLNaOH溶液中有20mL与Mg2+反应,∴n(Al3+):n(Mg2+)=1:1,则Al2(SO4)3与MgSO4的物质的量浓度之比为1:2。
31、(1)Mg 3.6 Al 2.7(2)1.4mol/L 32、(a) 1.8g (b)0.6675g (c) 0.95g (d) 90ml
21、解:发生反应Al(OH)3+OH-=AlO2-+2H2O所消耗NaOH的物质的量为:0.1mol/L×(0.08L-0.07L)=0.001mol
则n(AlCl3)=0.001mol
n(MgCl2)=(0.07L×0.1mol/L-0.001mol×3)÷2=0.02mol
c(AlCl3)=0.001mol÷0.1L=0.01mol/L
c(MgCl2)=0.002mol÷0.1L=0.02mol/L
(1)当NaOH溶液滴入10mL0.1mol/LAlCl3溶液中时,整个过程可用图象表示如下:
因为nAl3+=0.1×10×10-3=0.001(mol)
所以①当加入10mLNaOH溶液时现象是产生白色沉淀;加入30mL时,沉淀量最多;加入35mL时,沉淀部分溶解。 ②生成沉淀最多时,需NaOH溶液30mL。
(2)当AlCl3溶液滴入NaOH溶液时,由于NaOH溶液是过量的,所以反应如下:
Al3++3OH-====Al(OH)3↓,Al(OH)3+OH-====AlO2-+2H2O上述两个方程式合并为: Al3++4OH-====AlO2-+2H2O 3AlO2-+Al3++6H2O====4Al(OH)3↓
可用图象表示如下:
21世纪教育网
www.
w.w.w.k.s.5.u.c.o.m
www.
Ag+、Mg2+
Al3+、Na+
沉淀A
滤液B
滤液D
沉淀C
沉淀E
滤液F
V (NaOH)
沉淀量m
V (H2SO4)
沉淀量m
21世纪教育网 -- 中国最大型、最专业的中小学教育资源门户网站。 版权所有@21世纪教育网
铝和铝合金的崛起
一、铝的单质和化合物的相互转化关系图:
(一)有关铝及其化合物转化的离子方程式:
铝与酸的反应:2Al+6H+=2Al3++3H2↑
铝与碱溶液的反应:2Al+2OH-+2H2O=2AlO2-+3H2↑
氧化铝与酸的反应:Al2O3+6H+=2Al3++3H2O
氧化铝与碱溶液的反应:Al2O3+2OH-=2AlO2-+H2O
Al3+与强碱和弱碱的反应
Al3++3OH-=Al(OH)3↓ (碱少量)Al3++4OH-=AlO2-+2H2O(碱过量)
Al3++3NH3·H2O=Al(OH)3↓+3NH4+
氢氧化铝与强酸和强碱的反应:
Al(OH)3+3H+=Al3++3H2O Al(OH)3+OH-=AlO2-+2H2O
偏铝酸根与强酸和弱酸的反应:
AlO2-+H++H2O=Al(OH)3↓(酸少量)AlO2-+4H+=Al3++2H2O(酸过量)
2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32-(CO2少量)
AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-(CO2过量)
(二)氢氧化铝的酸式电离和碱式电离:
AlO2-+H++H2OAl(OH)3Al3++3OH-
(三)Al3+与AlO2-的有关水解反应:
Al3++3H2OAl(OH)3+3H+ AlO2-+2H2OAl(OH)3+OH-
Al3++3AlO2-+6H2O=4Al(OH)3↓
*Al3++3HCO3-=Al(OH)3↓+3CO2↑(泡沫灭火器工作原理)
*2Al3++3S2-+6H2O=2Al(OH)3↓+3H2S↑(Al2S3只能以固体方式存在)
*2Al3++3CO32-+3H2O=2Al(OH)3↓+3CO2↑
[同步练习]:
1、已知A为金属单质Al, 根据下列变化判断A、B、C、D、E各是什么物质?写出有关的离子方程式
(1) B C
D E
(2)写出以下各步的离子方程式
② ③
④ ⑥ ⑦ ⑧
2、将含有Ag+、Mg2+、Al3+、Na+等离子的稀溶液,按下列实验步骤进行分离。填写下列空白(各步可使用的试剂限于在NaOH、HCl、NaCl中选择)
① 适量
过滤 过滤 ③
②
(1)沉淀A是 ,沉淀C ,沉淀E是 。
(2)加入试剂①是 ,② ,③是_________。
(3)滤液B中加入试剂②,发生的离子方程式为______________________________________。
3、A烧杯中含有a molAlCl3的溶液,B烧杯中含有a molNaAlO2的溶液。现要将A、B烧杯中的铝元素全部转化为Al(OH)3沉淀,讨论有几种途径。写出相应的离子方程式。
(要求: 如需加其他物质,只准加过量的气体,不可加液体或气体试剂。)
(1)________________________________________________________________________
________________________________________________________________________
(2)________________________________________________________________________
________________________________________________________________________
4. 1.35g铝跟50ml25%的稀硫酸(密度是1.178g/cm3)完全反应。问:(1)能产生多少升氢气(S.T.P)?(2)将反应后的溶液稀释到250ml,其中Al3+和H+的物质的量浓度分别为多少?(3)稀释后,取出25ml溶液,用0.5mol/L氨水使之完全反应,要使Al3+完全沉淀需要氨水多少毫升?
5、在240ml0.2mol/LAl2(SO4)3溶液中加入多少1mol/LNaOH溶液,才能得到3.9g沉淀?
二、有关图像问题与计算
[例]在下图中,横坐标为向一定量的某溶液中加入某种物质的量,纵坐标为生成沉淀的量。从图中,选择适合表中各题要求的序号填入表中
溶液 加(或通入)物质 序号
⑴饱和石灰水 通入过量CO2
⑵AlCl3溶液 加入过量浓氨水
⑶含少量NaOH的NaAlO 2溶液 通入过量CO2
⑷含少量NaOH的NaAlO 2溶液 逐滴加入稀盐酸
⑸MgCl2、AlCl3混合溶液 逐滴加入NaOH溶液至过量
⑹NaOH溶液 逐滴加入Al2(SO4)3溶液至过量
⑺稀硫酸溶液 逐滴加入NaAlO 2溶液至过量
⑻含少量盐酸的AlCl3溶液 逐滴加入KOH溶液至过量
[同步练习]
1、现有0.1mol/L的AlCl3溶液和0.1mol/L的氢氧化钠溶液,进行下面的实验。
(1)在试管中盛有上述AlCl3溶液10mL,向其中逐渐滴入上述的NaOH溶液。
①根据加入氢氧化钠溶液用量,画出加入NaOH溶液与生成沉淀的关系图。
②生成沉淀质量最多时,需NaOH溶液____________mL。
(2)向盛有10mLNaOH溶液的试管中滴入AlCl3溶液,同时不停摇动试管,出现的现象是什么?写出上述过程的有关离子方程式。
2、向100 ml水中投入由4.6gNa和5.4gAl组成的混合物,充分反应后,
(1)计算放出H2多少升(标准状况下)?
(2)向滤液中逐滴加入2 mol/L的H2SO4溶液,生成沉淀的最大值是多少,此时消耗H2SO4溶液的体积是多少?
(3)生成沉淀后,再加入H2SO4溶液,使沉淀刚好完全溶解,此时消耗H2SO4溶液的体积是多少?
(4)在右图中画出相应的图像。
3、往未知浓度的AlCl3和MgCl2混合溶液100mL中逐滴加入0.1mol/LNaOH溶液,沉淀质量随加入碱液体积变化关系如图所示。求MgCl2和AlCl3的物质的量浓度。
4、将一定质量的Mg、Al合金全部溶解在500mL盐酸中(体积变化不计),取10mL反应后的溶液,用1mol/LNaOH溶液滴定得下图关系。
(1)求Mg,Al质量各是多少?
(2)求盐酸的物质的量浓度为多少mol/L
参考答案:
三、填空题
27、(1)A.Al B.AlCl3 C.Al(OH)3 D.Al2(SO4)3 E.NaAlO2
(2) ②
③ ④
⑥
⑦ ⑧
30、由50→60mL时,可知10mLNaOH溶液刚好溶解了Al(OH)3,故产生这些Al(OH)3需30mLNaOH,则在50mLNaOH溶液中有20mL与Mg2+反应,∴n(Al3+):n(Mg2+)=1:1,则Al2(SO4)3与MgSO4的物质的量浓度之比为1:2。
31、(1)Mg 3.6 Al 2.7(2)1.4mol/L 32、(a) 1.8g (b)0.6675g (c) 0.95g (d) 90ml
21、解:发生反应Al(OH)3+OH-=AlO2-+2H2O所消耗NaOH的物质的量为:0.1mol/L×(0.08L-0.07L)=0.001mol
则n(AlCl3)=0.001mol
n(MgCl2)=(0.07L×0.1mol/L-0.001mol×3)÷2=0.02mol
c(AlCl3)=0.001mol÷0.1L=0.01mol/L
c(MgCl2)=0.002mol÷0.1L=0.02mol/L
(1)当NaOH溶液滴入10mL0.1mol/LAlCl3溶液中时,整个过程可用图象表示如下:
因为nAl3+=0.1×10×10-3=0.001(mol)
所以①当加入10mLNaOH溶液时现象是产生白色沉淀;加入30mL时,沉淀量最多;加入35mL时,沉淀部分溶解。 ②生成沉淀最多时,需NaOH溶液30mL。
(2)当AlCl3溶液滴入NaOH溶液时,由于NaOH溶液是过量的,所以反应如下:
Al3++3OH-====Al(OH)3↓,Al(OH)3+OH-====AlO2-+2H2O上述两个方程式合并为: Al3++4OH-====AlO2-+2H2O 3AlO2-+Al3++6H2O====4Al(OH)3↓
可用图象表示如下:
21世纪教育网
www.
w.w.w.k.s.5.u.c.o.m
www.
Ag+、Mg2+
Al3+、Na+
沉淀A
滤液B
滤液D
沉淀C
沉淀E
滤液F
V (NaOH)
沉淀量m
V (H2SO4)
沉淀量m
21世纪教育网 -- 中国最大型、最专业的中小学教育资源门户网站。 版权所有@21世纪教育网
