化学:8.1《应用广泛的金属材料-钢铁》课件(第3课时)(沪科版高二第一学期)
文档属性
| 名称 | 化学:8.1《应用广泛的金属材料-钢铁》课件(第3课时)(沪科版高二第一学期) |

|
|
| 格式 | rar | ||
| 文件大小 | 457.7KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪科版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2009-12-01 00:00:00 | ||
图片预览





文档简介
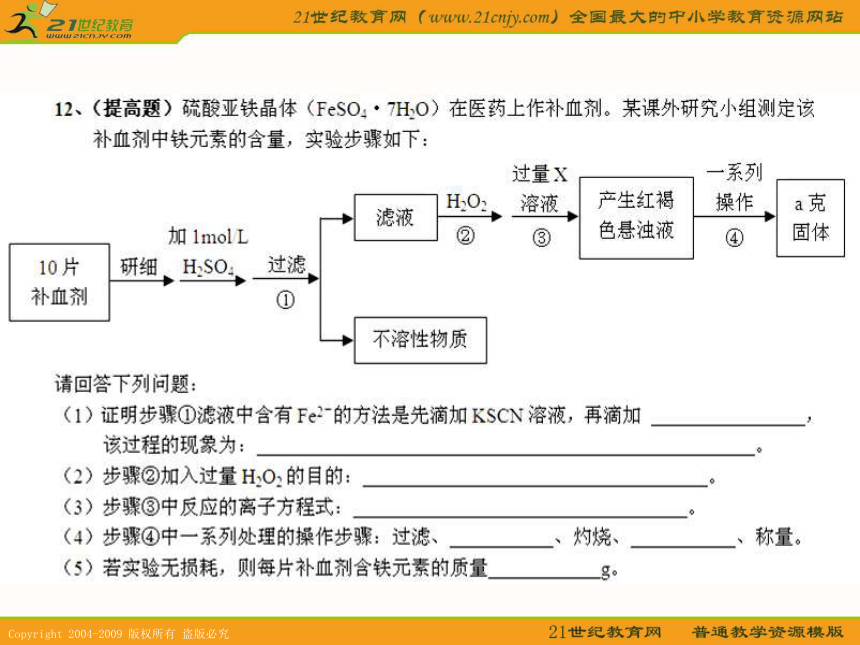
课件17张PPT。第3课时 铁单质及其化合物8.1《应用广泛的金属材料——钢铁》铁单质物理性质
化学性质
还原性
与氧气、氯气、硫磺……非金属单质
与H(+1)、Cu(+2)发生置换反应
与含高价元素的化合物,Mn(+7)、Cl(+7)、
Cr(+6)、 S(+6)、N(+5)、HClO、O3、H2O2、Fe(+3)
5.铁及其化合物Fe与Fe3+反应的离子方程式
Fe与Fe2(SO4)3反应的化学方程式
应用:实验室配制硫酸亚铁溶液时,为了防止所配溶液久置变质,常常加入_______试剂。 由反应:2FeCl3 +Cu → 2FeCl2 + CuCl2 推断出的氧化性或还原性强弱的结论,正确的是( )
A.氧化性 Cu2 + > Fe2+
B.氧化性 Fe3+ > Cu2 +
C.还原性 Fe2+ > Cu
D.还原性 Fe > Cu
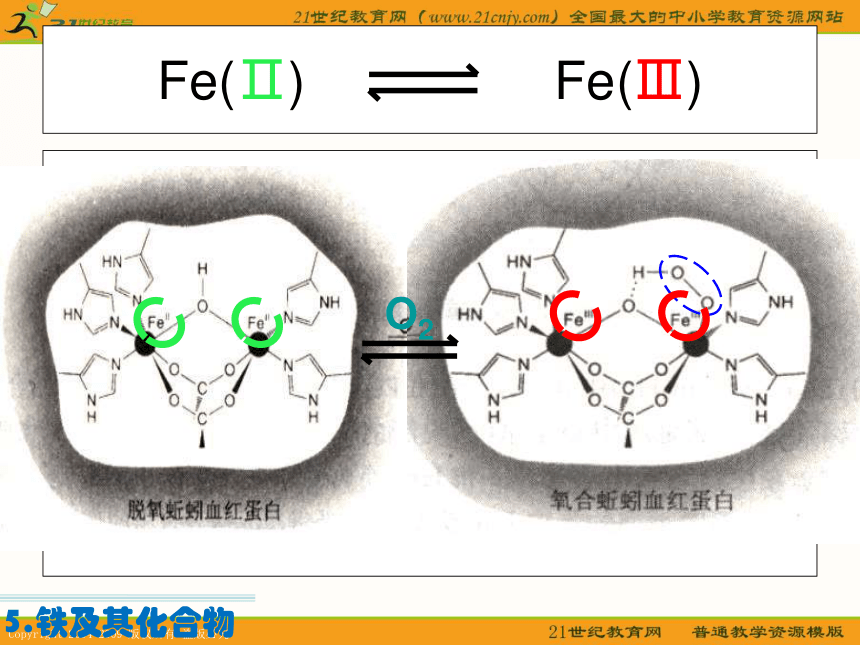
人体血液中,未携带的血红蛋白中应含Fe2+,若食用了亚硝酸盐,则导致血红蛋白中的Fe2+转化为Fe3+则会中毒。
医生提出服用维生素C可解除亚硝酸盐中毒。 当人体患缺铁性贫血时,可以服用亚铁盐作为补血剂。5.铁及其化合物Fe(Ⅱ) Fe(Ⅲ)O25.铁及其化合物FeO Fe3O4 Fe2O3
练习:
①FeO+HCl ④ Fe2O3+稀H2SO4
*②FeO+稀HNO3 ⑤ Fe2O3+稀HNO3
③FeO+CO ⑥ Fe2O3+CO
⑦Fe3O4 +HCl ? 1、氧化物物理性质: 黑色 黑色磁性 红棕色(颜料)
都不溶于水
化学性质: 不与水反应的碱性氧化物
都有氧化性,可以被CO、H2、C还原5.铁及其化合物铁的氧化物的性质比较5.铁及其化合物
在烧制砖瓦时,用粘土做成的坯
经过焙烧后,铁的化合物转化成
_______而制得红色砖瓦;若烘热后
期从窑顶向下慢慢浇水,窑内会
产生大量的________气体,它们把该
红色物质还原成黑色的化合物是
_________5.铁及其化合物Fe(OH)2、 Fe(OH)32、氢氧化物练习:
1)Fe(OH)3+稀H2SO4
2)Fe(OH)2+稀HNO3
3)Fe(OH)3失水
物理性质: 白色 红褐色
都不溶于水
化学性质: 弱碱与酸反应
不溶于水的碱受热分解
*Fe(OH)2有还原性:
4Fe(OH)2+O2 +2H2O→4Fe(OH)3
现象:白色→灰绿色→红褐色5.铁及其化合物3、铁的可溶性盐类化合物(Fe2+、Fe3+的性质) Fe2+ Fe3+离子颜色: 浅绿色 棕黄色
化学性质: ①都可以与OH-产生沉淀,颜色不同。
②都可以水解,显极弱的酸性。
Fe3+ + 3H2O Fe(OH)3 + 3H+
(复习:氯化亚铁溶液蒸干至恒重,得到的固体产物是______)
③Fe3+可与KSCN(SCN-)显血红色;
Fe2+没有这一性质
④Fe2+→Fe3+的转化:
Cl2、O2、H2O2、KMnO4、HNO3
⑤Fe3+→Fe2+的转化:
与Cu、Fe甚至更活泼的金属
典型的还原性离子I-、S2-
含有较低价元素的某些化合物SO2(+4→+6)
5.铁及其化合物FeFe2+Fe3+5.铁及其化合物Fe2+ 、Fe3+的鉴别方法归纳显色反应 直 接 观 色与KSCN与 铜 片与 淀 粉
KI 试 纸鉴 别 浅 绿 色 棕 黄 色血 红 色不显红色 无明显现象 Cu被腐蚀溶液变绿色 试纸不变蓝 试纸变蓝色白色沉淀迅速变灰
绿色最后呈红褐色立即产生红褐
色沉淀5.铁及其化合物 …… …… …… …… …… …… ……氢气保护下的Fe(OH)2制备a mol Fe和b mol(a>0,b>0) S加热条件下反应,将反应后的混合物与足量的稀硫酸溶液反应,通过讨论计算回答:
(1)所生成的气体在标准状况下的体积(L)_____。
(2)a、b取值不同时,气体成分,各有几mol?
①……;
②……;
③……。
(3)生成气体在标准状况下的密度d(g/L)的取值范围___ ≥d >___。
(3)生成的气体不少于b mol时,属于哪种情况?
(4)产生气体的密度为最大值时,属于哪种情况?
化学性质
还原性
与氧气、氯气、硫磺……非金属单质
与H(+1)、Cu(+2)发生置换反应
与含高价元素的化合物,Mn(+7)、Cl(+7)、
Cr(+6)、 S(+6)、N(+5)、HClO、O3、H2O2、Fe(+3)
5.铁及其化合物Fe与Fe3+反应的离子方程式
Fe与Fe2(SO4)3反应的化学方程式
应用:实验室配制硫酸亚铁溶液时,为了防止所配溶液久置变质,常常加入_______试剂。 由反应:2FeCl3 +Cu → 2FeCl2 + CuCl2 推断出的氧化性或还原性强弱的结论,正确的是( )
A.氧化性 Cu2 + > Fe2+
B.氧化性 Fe3+ > Cu2 +
C.还原性 Fe2+ > Cu
D.还原性 Fe > Cu
人体血液中,未携带的血红蛋白中应含Fe2+,若食用了亚硝酸盐,则导致血红蛋白中的Fe2+转化为Fe3+则会中毒。
医生提出服用维生素C可解除亚硝酸盐中毒。 当人体患缺铁性贫血时,可以服用亚铁盐作为补血剂。5.铁及其化合物Fe(Ⅱ) Fe(Ⅲ)O25.铁及其化合物FeO Fe3O4 Fe2O3
练习:
①FeO+HCl ④ Fe2O3+稀H2SO4
*②FeO+稀HNO3 ⑤ Fe2O3+稀HNO3
③FeO+CO ⑥ Fe2O3+CO
⑦Fe3O4 +HCl ? 1、氧化物物理性质: 黑色 黑色磁性 红棕色(颜料)
都不溶于水
化学性质: 不与水反应的碱性氧化物
都有氧化性,可以被CO、H2、C还原5.铁及其化合物铁的氧化物的性质比较5.铁及其化合物
在烧制砖瓦时,用粘土做成的坯
经过焙烧后,铁的化合物转化成
_______而制得红色砖瓦;若烘热后
期从窑顶向下慢慢浇水,窑内会
产生大量的________气体,它们把该
红色物质还原成黑色的化合物是
_________5.铁及其化合物Fe(OH)2、 Fe(OH)32、氢氧化物练习:
1)Fe(OH)3+稀H2SO4
2)Fe(OH)2+稀HNO3
3)Fe(OH)3失水
物理性质: 白色 红褐色
都不溶于水
化学性质: 弱碱与酸反应
不溶于水的碱受热分解
*Fe(OH)2有还原性:
4Fe(OH)2+O2 +2H2O→4Fe(OH)3
现象:白色→灰绿色→红褐色5.铁及其化合物3、铁的可溶性盐类化合物(Fe2+、Fe3+的性质) Fe2+ Fe3+离子颜色: 浅绿色 棕黄色
化学性质: ①都可以与OH-产生沉淀,颜色不同。
②都可以水解,显极弱的酸性。
Fe3+ + 3H2O Fe(OH)3 + 3H+
(复习:氯化亚铁溶液蒸干至恒重,得到的固体产物是______)
③Fe3+可与KSCN(SCN-)显血红色;
Fe2+没有这一性质
④Fe2+→Fe3+的转化:
Cl2、O2、H2O2、KMnO4、HNO3
⑤Fe3+→Fe2+的转化:
与Cu、Fe甚至更活泼的金属
典型的还原性离子I-、S2-
含有较低价元素的某些化合物SO2(+4→+6)
5.铁及其化合物FeFe2+Fe3+5.铁及其化合物Fe2+ 、Fe3+的鉴别方法归纳显色反应 直 接 观 色与KSCN与 铜 片与 淀 粉
KI 试 纸鉴 别 浅 绿 色 棕 黄 色血 红 色不显红色 无明显现象 Cu被腐蚀溶液变绿色 试纸不变蓝 试纸变蓝色白色沉淀迅速变灰
绿色最后呈红褐色立即产生红褐
色沉淀5.铁及其化合物 …… …… …… …… …… …… ……氢气保护下的Fe(OH)2制备a mol Fe和b mol(a>0,b>0) S加热条件下反应,将反应后的混合物与足量的稀硫酸溶液反应,通过讨论计算回答:
(1)所生成的气体在标准状况下的体积(L)_____。
(2)a、b取值不同时,气体成分,各有几mol?
①……;
②……;
③……。
(3)生成气体在标准状况下的密度d(g/L)的取值范围___ ≥d >___。
(3)生成的气体不少于b mol时,属于哪种情况?
(4)产生气体的密度为最大值时,属于哪种情况?
