钠的化合物
图片预览






文档简介
课件20张PPT。第二节 几种重要的金属化合物第一课时 钠的化合物Na2O+H2O=2NaOH氧化钠溶于水,反应生成氢氧化钠Na2O+2HCl=2NaCl+H2O
.氧化钠与盐酸反应:
一 氧化钠(Na2O)结论: Na2O属于碱性氧化物二 过氧化钠 (Na2O2) 颜色:淡黄色
状态:粉末状固体 思考:溶解度 ? 钠的另一个含氧化合物——Na2O与水发生化学反应,生成NaOH.
Na2O2与水反应是否也会生成NaOH?退 出过氧化钠的物理性质过氧化钠的化学性质(1) 实验 (动画)
1、取一支装有Na2O2的试管,打开
试管胶塞 缓慢加入少量水,并用
拇指堵住试管口。
(观察到有什么现象?)
(用手摸一下试管,有什么感觉?)
2、? 用带火星的木条伸入试管。
(观察到什么现象?)
3、? 向试管中加入几滴无色酚酞。
(观察到什么现象?)
(振荡后又是什么现象?)退 出1、跟水反应
过氧化钠的化学性质反应生成有O2;反应放热;反应生成 NaOH;Na2O2具有漂白性;(2)实验结论:退 出1、试管中发生剧烈反应, 产生大量无色气泡,且此气体能使带火星木条复燃;
2、试管发烫;
3、无色酚酞变红;
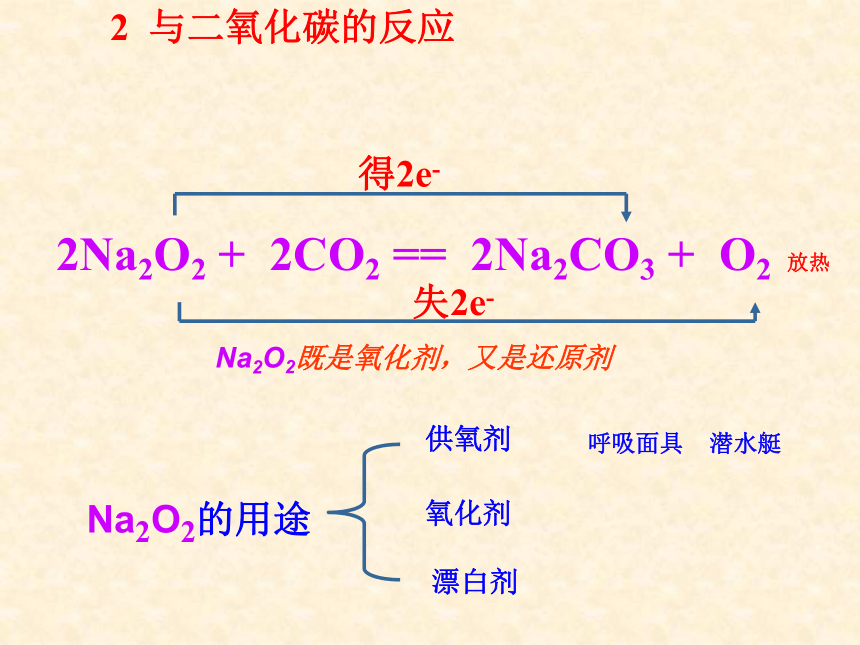
4、振荡后红色褪去; 过氧化钠的化学性质(3)实验结论: 2 Na2O2 + 2H2O === 4NaOH + O2↑ 既是氧化剂,又是还原剂。那么Na2O2在这个反应中充当了什么角色呢? 有哪些元素发生了化合价的变化了呢? 只有氧元素;退 出失2e-得2e-1-20 2 与二氧化碳的反应2Na2O2 + 2CO2 == 2Na2CO3 + O2 放热
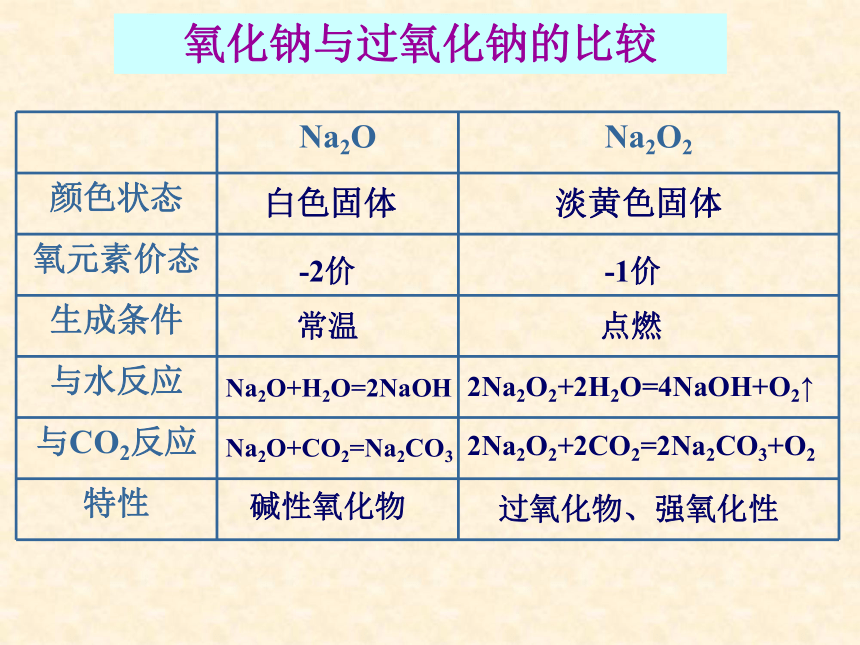
失2e-得2e-Na2O2既是氧化剂,又是还原剂Na2O2的用途氧化钠与过氧化钠的比较淡黄色固体白色固体 -2价 -1价 常温 点燃 Na2O+H2O=2NaOH 2Na2O2+2H2O=4NaOH+O2↑ Na2O+CO2=Na2CO3 2Na2O2+2CO2=2Na2CO3+O2过氧化物、强氧化性碱性氧化物练习: 1.在通常情况下,下列物质因发生氧化还原反应而变质的是( )
A NaOH B Na2CO3.10H2O C Na2O2 D Na2O 2.向紫色石蕊溶液中加入过量Na2O2粉末,振荡,可观察到
的现象为( )
A 溶液仍为紫色 B 溶液最终变为蓝色
C 最终溶液褪色,无其他现象 D 有气泡产生,溶液最终为无色CD三 碳酸钠和碳酸氢钠俗 名纯碱或苏打小苏打Na2CO3.10H2O—— Na2CO3和NaHCO3在水中的溶解性 __总结仍有固体残留溶液变微红色 白色粉未,加水结块成晶体,放热 白色粉未,加水部分溶解,感受不到热量变化振荡长时间可溶解溶液变红色 加水先变成含结晶水的晶体,溶液的碱性比NaHCO3强
加水部分溶解,溶液的碱性比Na2CO3弱初步结论(1)Na2CO3和NaHCO3的热稳定性 化学性质
热稳定性
与酸反应
与碱反应
与盐反应
现象:1号试管: 澄 清石灰水变浑浊2号试管: 澄 清石灰水不变浑浊② Na2CO3 稳定, 受热不分解① NaHCO3不稳定,受热可分解结论:2NaHCO3===Na2CO3+H2O+CO2总结 : 热稳定性:Na2CO3 > NaHCO3应用: 此性质可鉴别NaHCO3固体和NaHCO3固体(2)与 酸 反 应与酸反应与碱反应与盐反应化学性质
碳酸钠和碳酸氢钠都易与酸反应,但是
碳酸氢钠与酸反应比碳酸钠更剧烈为什么?热稳定性结论:(4)与 碱 反 应与酸反应与碱反应与盐反应能与所有可溶碱反应生成碳酸正盐和水NaHCO3+NaOH=Na2CO3+H2OHCO3-+OH -=CO32-+H2O 但会与NaOH反应吗?思考:
NaHCO3与Ca(OH)2是否反应?若反应,反应
用量不同,离子方程式是否相同?热稳定性化学性质化学性质(5)与 盐 反 应与酸反应与碱反应与盐反应与可溶性的钙盐、钡盐反应生成沉淀可与NaHSO4反应HCO3- + H+ =CO2 +H2O热稳定性〖讨 论〗
1、如何除去Na2CO3中少量的NaHCO3?
2、如何除去NaHCO3溶液中少量的Na2CO3?
加适量NaOH溶液;加热通入过量CO2:CO2+H2O
1加热
2OH-
Na2CO3 +CO2 +H2O = 2NaHCO3
用 途制玻璃制 皂造 纸纺织等 发酵剂灭火剂等Na2CO3NaHCO3制 药课堂练习1.分别向下列物质的水溶液加入Na2O2少量固体,不会出现浑烛
的是( )
A CuCl2 B Ca(HCO3)2 C MgCl2 D BaCl2D2、某化学兴趣小组欲制作一泡沫灭火器。现有:盐酸、碳酸钠、
碳酸氢钠,请问他们最好选用 和 反应,为什么?
盐酸 碳酸氢钠三、焰色反应一些焰色反应:钠 黄色
钾 紫色注意:1、焰色反应属于元素的性质
2、焰色反应实验操作
3、钾的焰色反应的观察要透过蓝色钴玻璃
实验3-6
.氧化钠与盐酸反应:
一 氧化钠(Na2O)结论: Na2O属于碱性氧化物二 过氧化钠 (Na2O2) 颜色:淡黄色
状态:粉末状固体 思考:溶解度 ? 钠的另一个含氧化合物——Na2O与水发生化学反应,生成NaOH.
Na2O2与水反应是否也会生成NaOH?退 出过氧化钠的物理性质过氧化钠的化学性质(1) 实验 (动画)
1、取一支装有Na2O2的试管,打开
试管胶塞 缓慢加入少量水,并用
拇指堵住试管口。
(观察到有什么现象?)
(用手摸一下试管,有什么感觉?)
2、? 用带火星的木条伸入试管。
(观察到什么现象?)
3、? 向试管中加入几滴无色酚酞。
(观察到什么现象?)
(振荡后又是什么现象?)退 出1、跟水反应
过氧化钠的化学性质反应生成有O2;反应放热;反应生成 NaOH;Na2O2具有漂白性;(2)实验结论:退 出1、试管中发生剧烈反应, 产生大量无色气泡,且此气体能使带火星木条复燃;
2、试管发烫;
3、无色酚酞变红;
4、振荡后红色褪去; 过氧化钠的化学性质(3)实验结论: 2 Na2O2 + 2H2O === 4NaOH + O2↑ 既是氧化剂,又是还原剂。那么Na2O2在这个反应中充当了什么角色呢? 有哪些元素发生了化合价的变化了呢? 只有氧元素;退 出失2e-得2e-1-20 2 与二氧化碳的反应2Na2O2 + 2CO2 == 2Na2CO3 + O2 放热
失2e-得2e-Na2O2既是氧化剂,又是还原剂Na2O2的用途氧化钠与过氧化钠的比较淡黄色固体白色固体 -2价 -1价 常温 点燃 Na2O+H2O=2NaOH 2Na2O2+2H2O=4NaOH+O2↑ Na2O+CO2=Na2CO3 2Na2O2+2CO2=2Na2CO3+O2过氧化物、强氧化性碱性氧化物练习: 1.在通常情况下,下列物质因发生氧化还原反应而变质的是( )
A NaOH B Na2CO3.10H2O C Na2O2 D Na2O 2.向紫色石蕊溶液中加入过量Na2O2粉末,振荡,可观察到
的现象为( )
A 溶液仍为紫色 B 溶液最终变为蓝色
C 最终溶液褪色,无其他现象 D 有气泡产生,溶液最终为无色CD三 碳酸钠和碳酸氢钠俗 名纯碱或苏打小苏打Na2CO3.10H2O—— Na2CO3和NaHCO3在水中的溶解性 __总结仍有固体残留溶液变微红色 白色粉未,加水结块成晶体,放热 白色粉未,加水部分溶解,感受不到热量变化振荡长时间可溶解溶液变红色 加水先变成含结晶水的晶体,溶液的碱性比NaHCO3强
加水部分溶解,溶液的碱性比Na2CO3弱初步结论(1)Na2CO3和NaHCO3的热稳定性 化学性质
热稳定性
与酸反应
与碱反应
与盐反应
现象:1号试管: 澄 清石灰水变浑浊2号试管: 澄 清石灰水不变浑浊② Na2CO3 稳定, 受热不分解① NaHCO3不稳定,受热可分解结论:2NaHCO3===Na2CO3+H2O+CO2总结 : 热稳定性:Na2CO3 > NaHCO3应用: 此性质可鉴别NaHCO3固体和NaHCO3固体(2)与 酸 反 应与酸反应与碱反应与盐反应化学性质
碳酸钠和碳酸氢钠都易与酸反应,但是
碳酸氢钠与酸反应比碳酸钠更剧烈为什么?热稳定性结论:(4)与 碱 反 应与酸反应与碱反应与盐反应能与所有可溶碱反应生成碳酸正盐和水NaHCO3+NaOH=Na2CO3+H2OHCO3-+OH -=CO32-+H2O 但会与NaOH反应吗?思考:
NaHCO3与Ca(OH)2是否反应?若反应,反应
用量不同,离子方程式是否相同?热稳定性化学性质化学性质(5)与 盐 反 应与酸反应与碱反应与盐反应与可溶性的钙盐、钡盐反应生成沉淀可与NaHSO4反应HCO3- + H+ =CO2 +H2O热稳定性〖讨 论〗
1、如何除去Na2CO3中少量的NaHCO3?
2、如何除去NaHCO3溶液中少量的Na2CO3?
加适量NaOH溶液;加热通入过量CO2:CO2+H2O
1加热
2OH-
Na2CO3 +CO2 +H2O = 2NaHCO3
用 途制玻璃制 皂造 纸纺织等 发酵剂灭火剂等Na2CO3NaHCO3制 药课堂练习1.分别向下列物质的水溶液加入Na2O2少量固体,不会出现浑烛
的是( )
A CuCl2 B Ca(HCO3)2 C MgCl2 D BaCl2D2、某化学兴趣小组欲制作一泡沫灭火器。现有:盐酸、碳酸钠、
碳酸氢钠,请问他们最好选用 和 反应,为什么?
盐酸 碳酸氢钠三、焰色反应一些焰色反应:钠 黄色
钾 紫色注意:1、焰色反应属于元素的性质
2、焰色反应实验操作
3、钾的焰色反应的观察要透过蓝色钴玻璃
实验3-6
