化学:1.2.1《物质的分离与提纯》课件(1)(苏教版必修1)
文档属性
| 名称 | 化学:1.2.1《物质的分离与提纯》课件(1)(苏教版必修1) |

|
|
| 格式 | rar | ||
| 文件大小 | 174.6KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2009-12-03 00:00:00 | ||
图片预览




文档简介
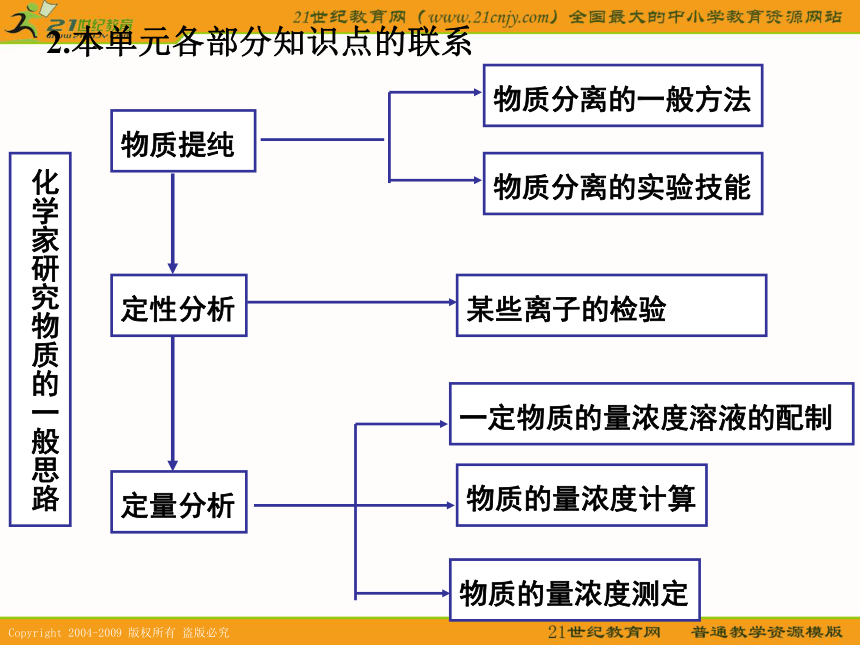
课件13张PPT。第二单元:研究物质的实验方法一、物质的分离和提纯2.本单元各部分知识点的联系 物质的分离:利用物理或化学方法将混合物的各种成分分开
物质的提纯:除去杂质目的:一、物质的分离和提纯(1)不增加新的杂质,
(2)不减少主要成分的含量,
(3)操作方法简单,易于进行分离,
(4)如果将主要成分进行了转化,最后要能将其还原转来。原则:“不增、不减、易分、复原”主要是利用化学反应把杂质转化为气体或不溶物
(有时恰好相反)而分离除去(去除法),或把
杂质转化为所需物质(转化法),但应注意不能
因加入试剂又引入新的杂质。即:分离类型:固体(不溶)一液体分离(1)对折法折叠滤纸后紧贴漏斗壁,用水打湿不出气泡为止,滤纸边缘低于漏斗;过滤时加入漏斗的溶液面低于滤纸边缘,即“一贴两低三靠”。
(2)过滤时:烧杯嘴与玻璃棒接触;玻璃棒与三层滤纸处相接触;漏斗嘴紧靠玻璃烧杯壁。
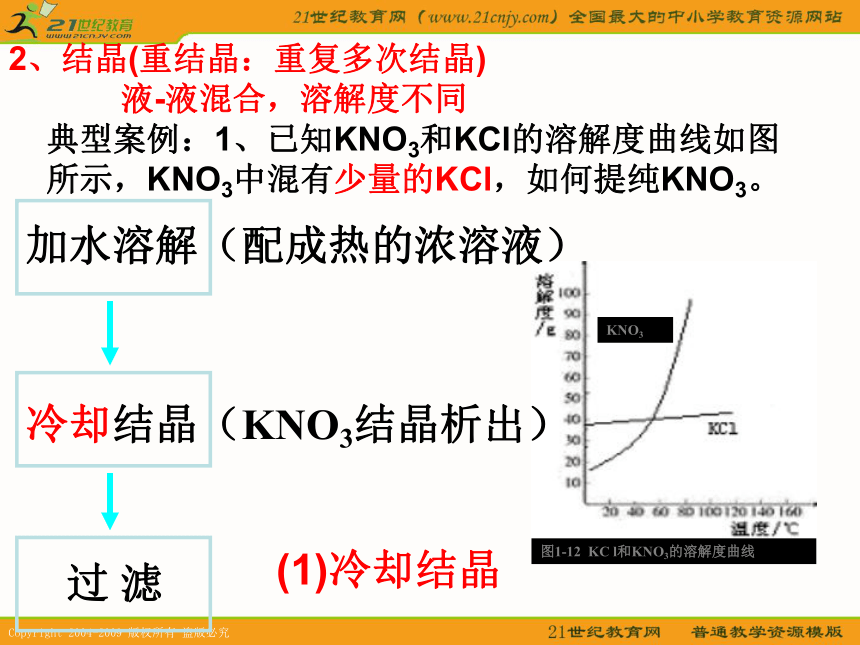
(3)加水,水面高于沉淀,浸洗三次,达到净化沉淀。 典型案例:除去粗盐中的泥沙 1、过滤典型案例:1、已知KNO3和KCl的溶解度曲线如图所示,KNO3中混有少量的KCl,如何提纯KNO3。2、结晶(重结晶:重复多次结晶)
液-液混合,溶解度不同(1)冷却结晶典型案例:2、已知KNO3和KCl的溶解度曲线如图所示, KCl中混有少量的KNO3 ,如何提纯KCl。(2)蒸发结晶2、结晶(重结晶:重复多次结晶)
液-液混合,溶解度不同典型案例:某地区的自来水中混有少量Fe3+,实验室如何获得少量纯净的蒸馏水。3、蒸馏:液-液混合,沸点不同 图1-16 蒸馏蒸馏烧瓶冷凝管牛角管温
度计位置典型案例:溴水中溶有少量的溴,如何将溴从水中分离出来(溴在水中的溶解度较小)。4、萃取:互不相溶,密度不同,溶质在不同溶剂中
溶解度相差很大。典型案例:溴水中溶有少量的溴,如何将溴从水中分离出来(溴在水中的溶解度较小)。4、萃取分液:互不相溶,密度不同,溶质在不同溶剂中
溶解度相差很大。操作要点:
(1)将溶液注入分液漏斗,
溶液总量不超过其容积3/4,
如图所示,两手握住分液漏
斗、倒转分液漏斗并反复、
用力振荡。
(2)把分液漏斗放在铁架
台的铁圈中静置、分层。
(3)打开旋塞,使下层液
体流出。小结:1、过滤:用于固液混合的分离。2、结晶:用来分离和提纯几种可溶性固体的混合物
(蒸发结晶和冷却结晶)3、蒸馏:提纯或分离沸点不同的液体混合物。
防止液体暴沸,加入碎瓷片。温度计水银球的位置。4、萃取:利用溶质在互不相溶的溶剂里的溶解度不同,
用一种溶剂把溶质从它与另一种溶剂所组成的溶液中
提取出来的方法,叫萃取。
萃取剂的选择要求:和原溶液中的溶剂互不相溶;
两溶剂密度不同,对溶质的溶解度要远大于原溶剂。5、分液:分离互不相溶的液体
物质的提纯:除去杂质目的:一、物质的分离和提纯(1)不增加新的杂质,
(2)不减少主要成分的含量,
(3)操作方法简单,易于进行分离,
(4)如果将主要成分进行了转化,最后要能将其还原转来。原则:“不增、不减、易分、复原”主要是利用化学反应把杂质转化为气体或不溶物
(有时恰好相反)而分离除去(去除法),或把
杂质转化为所需物质(转化法),但应注意不能
因加入试剂又引入新的杂质。即:分离类型:固体(不溶)一液体分离(1)对折法折叠滤纸后紧贴漏斗壁,用水打湿不出气泡为止,滤纸边缘低于漏斗;过滤时加入漏斗的溶液面低于滤纸边缘,即“一贴两低三靠”。
(2)过滤时:烧杯嘴与玻璃棒接触;玻璃棒与三层滤纸处相接触;漏斗嘴紧靠玻璃烧杯壁。
(3)加水,水面高于沉淀,浸洗三次,达到净化沉淀。 典型案例:除去粗盐中的泥沙 1、过滤典型案例:1、已知KNO3和KCl的溶解度曲线如图所示,KNO3中混有少量的KCl,如何提纯KNO3。2、结晶(重结晶:重复多次结晶)
液-液混合,溶解度不同(1)冷却结晶典型案例:2、已知KNO3和KCl的溶解度曲线如图所示, KCl中混有少量的KNO3 ,如何提纯KCl。(2)蒸发结晶2、结晶(重结晶:重复多次结晶)
液-液混合,溶解度不同典型案例:某地区的自来水中混有少量Fe3+,实验室如何获得少量纯净的蒸馏水。3、蒸馏:液-液混合,沸点不同 图1-16 蒸馏蒸馏烧瓶冷凝管牛角管温
度计位置典型案例:溴水中溶有少量的溴,如何将溴从水中分离出来(溴在水中的溶解度较小)。4、萃取:互不相溶,密度不同,溶质在不同溶剂中
溶解度相差很大。典型案例:溴水中溶有少量的溴,如何将溴从水中分离出来(溴在水中的溶解度较小)。4、萃取分液:互不相溶,密度不同,溶质在不同溶剂中
溶解度相差很大。操作要点:
(1)将溶液注入分液漏斗,
溶液总量不超过其容积3/4,
如图所示,两手握住分液漏
斗、倒转分液漏斗并反复、
用力振荡。
(2)把分液漏斗放在铁架
台的铁圈中静置、分层。
(3)打开旋塞,使下层液
体流出。小结:1、过滤:用于固液混合的分离。2、结晶:用来分离和提纯几种可溶性固体的混合物
(蒸发结晶和冷却结晶)3、蒸馏:提纯或分离沸点不同的液体混合物。
防止液体暴沸,加入碎瓷片。温度计水银球的位置。4、萃取:利用溶质在互不相溶的溶剂里的溶解度不同,
用一种溶剂把溶质从它与另一种溶剂所组成的溶液中
提取出来的方法,叫萃取。
萃取剂的选择要求:和原溶液中的溶剂互不相溶;
两溶剂密度不同,对溶质的溶解度要远大于原溶剂。5、分液:分离互不相溶的液体
