化学:1.2《化学计量在实验中的应用》课件(2)(新人教版必修1)
文档属性
| 名称 | 化学:1.2《化学计量在实验中的应用》课件(2)(新人教版必修1) |  | |
| 格式 | rar | ||
| 文件大小 | 204.6KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2009-12-03 18:48:00 | ||
图片预览











文档简介
课件45张PPT。化学计量在实验中的应用 如何称量一头大象的质量
曹冲称象的故事
指导思想:化整为零称量一粒小米 怎样完成下列任务?---称量10克小米 回忆与思考C + O2 = CO2质量 克 克 克粒子数 个碳原子 个氧分子 个CO2分子物质的量点燃1、物质的量: 1)是一个物理量,表示含有一定数目粒子的
集合体。①“物质的量”是一个物理量的名称(国际单位制七个基本物理量 之一) ,是专有名词, 使用时四个字不能拆分!
②物质的量计量对象——微观粒子;
微观粒子—分子、原子、离子、电子、
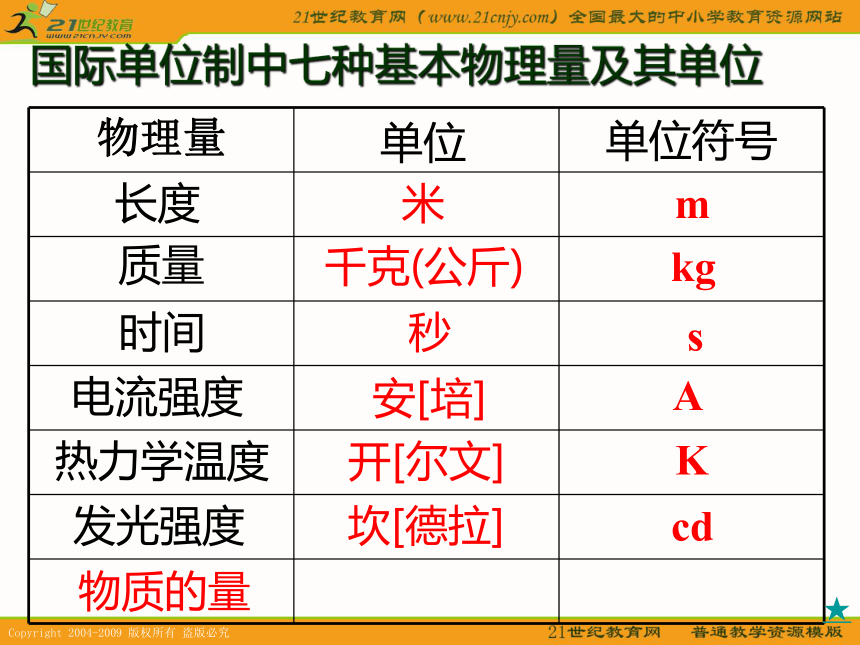
质子、中子(表示符号:n)国际单位制中七种基本物理量及其单位 ★2)单位:①摩尔仅仅是一个单位;
---物质的量的单位!
②摩尔计量对象——微观粒子;表示符号:mol摩尔:简称摩
【学生练习】:判断下列说法是否正确?①1molH2; ② 1mol氧;
③ 1molH2O ; ④ 1mol氧元素;
⑤ 1molNa+ ; ⑥ 1摩尔氧原子。 当物质所含的微粒数是多少时,其物质的量是1mol呢?当物质所含粒子数与0.012kg12C所含的碳原子数相同时,它的物质的量就是1摩。3)1mol的规定已知一个碳原子的质量: 1.99×10-23克2、阿伏加德罗常数 : 1mol任何粒子所含有的粒子数叫做阿伏加德罗常数。①基准数:0.012kg12C所含的碳原子数;
②近似值:6.02×1023;表示符号:NA; 单位mol-1 假设有6.02×1023粒大米,每粒大米重0.025g。把它分给全世界的人,全世界约50亿人口:每人可分得大米趣味问题228万吨。若每人每年平均消费粮食400kg,那么,
可供全世界的人口食用570万年【学生练习】:
(1)1molH2SO4中约含有 个硫酸分子;
(2)0.5molH2O中约含有 个水分子;
(3)1mol H2约含有 个氢原子。
(4)1mol NaCl中约含有 个Na+、含有 个Cl-。 6.02×10236.02×10231. 204×10246.02×10233.01×1023 (1)1mol O中约含有 个O
(2)2mol H2O中约含有 个H2O
(3)3NA个H+是 mol H+
(4)5NA个水分子的物质的量是 mol H2O
(5)N个水分子的物质的量是 mol6.02 × 1023 2×6.02×10233N/NA5【学生练习】:粒子个数阿伏加德罗常数物质的量N = NA÷ n公式一一、物质的量的单位 —— 摩尔描述物质所含粒子多少的专有名词,“物质的量”四个字不可拆分物理量1.物质的量注意2、阿伏加德罗常数 : 1mol任何粒子所含有的粒子数叫做阿伏加德罗常数。符号:NA单位:mol-1近似值:6.02×1023
符号:n2. 5mol的O2中有多少个氧气分子?练习1:1. 3.01×1023个H,其物质的量是多少3 . 1.204×1024个N2的物质的量为 ,氮原子的物质的量为 。练习2:
1. 0.5mol水中含有 个水分子?2. 2mol水中含有 个水分子, 个氢原子?3. 1molH2SO4溶于水,水中存在的溶质粒子是什么?它们的物质的量各是多少?4. 1个水分子有 个电子,1mol H2O中呢?3.01×1023个CO2的物质的量是多少?● 2 mol H2O中含有氢原子多少个?●2 mol Mg变成Mg2+时失去电子数是多少?0.5molCO2电子物质的量是多少? 0.5 mol2.408×1024 2×2×6.02×1023 个练习:●含有2 mol氢原子的H2O中水分子有多少个?6.02×1023 11 mol● 1 mol H2中含有电子多少个?1.204×1024 1. 1molH3PO4分子中含有()个 H3PO4分子,()个氢原子,()mol氢原子
()个P原子,()molP原子
()个O原子,()molO原子
2. 1molSO42-中有()个 SO42-,所带电荷为()个。
3. 1molO中有()个O原子,()个电子,()mol电子。
4. 2molH2SO4中有()mol氢原子,()molS原子,()molO原子,()mol原子5. 1.5molNH3有 个NH3分子, molH, mol电子
6. 1molNa+中有( )个Na+,( )mol电子
7. 2molOH-有( )个OH-,( )mol电子
8. 含0.3molSO42-的Fe2(SO4)3的物质的量是( )mol,Fe3+有( )mol
9. 等物质的量的SO2和SO3分子个数之比为( ),原子个数之比为( ),O原子个数之比为( )。【课堂练习】1.下列关于物质的量的说法中不正确的是( )
A.物质的量是国际单位制的7个基本单位之一
B.物质的量实际上是表示含有一定数目的粒子集体
C.物质的量的单位是“摩尔”
D.物质的量是表示物质数量的单位AD2、下列表示方法中,错误的是( )
A.2 mol氢 B. 1 mol H2O
4 mol e- D. 0.5 mol H2SO4
E。 2 mol钢笔 AE3、下列关于阿伏加德罗常数的说法正确的是 ( )
A.阿伏加德罗常数是一个纯数,没有单位
B.阿伏加德罗常数就是6.02×1023
C.阿伏加德罗常数是指1 mol 的任何粒子的
粒子数
D.阿伏加德罗常数的近似值为:
6.02×1023 mol-1CD4.1mol物质的含义是( )
A、0.012Kg碳
B、含有6.02×1023个微粒的物质
C、含有阿伏加德罗常数个微粒的物质
D、含有与6.02×1023个碳原子等质量的物质C5.在0.5mol O2中含有的氧分子数目
是多少?解:O2的分子数为N = n × NA =0.5 mol× 6.02 ×1023mol-1= 3.01 × 1023 答:O2的分子数为3.01 × 1023个。6.在0.5mol O2中含有的氧原子数目
是多少?解:O2的氧原子数为N = n ×2 × NA =0.5 mol×2× 6.02 ×1023mol-1
= 6.02 × 1023 答:O2的氧原子数为6.02 × 1023个。1mol几种物质的质量64 g Cu182712569818g27g12g56g98g结论: 1mol任何粒子或物质的质量以g为单位时,其数值都与该粒子的相对原子质量或相对分子质量相等。1molH2O的质量
1molH2SO4的质量
1molCO2的质量
1mol蔗糖(C12H22O11)的质量1molNa+的质量、 1molCl -的质量
1molSO42-的质量3.摩尔质量定义:单位物质的量(即1mol)的物质所具有的质量符号:M
单位: g/mol 或 g·mol-1
kg/mol 或 kg·mol-1练一练11 g / mol34 g / mol3417 g ? mol-1172323 g ? mol-1摩尔质量1 g 34 g 17 g 23 g练一练◆ 2mol (n)H2SO4的质量(m)
为 。◆ 5.6g(m)铁中含Fe的物质的量(n)
是 。196g0.1 mol摩尔质量M的应用◆ 80g(m)O2的物质的量(n)是 。2.5 mol质量摩尔质量物质的量m = M÷ n1、 M(H2O)= 。
2、M( NaCl)= 。
3、M(H2SO4)= 。
4 、M(OH-)=_________________练习17g · mol-158.5g · mol-198g · mol-118g · mol-1例题、 71gNa2SO4中含有的Na+和SO42-的物质的量多少?【练习】1.课本P13学与问2.等质量的下列物质中,所含分子数最少的是 ( )
A、Cl2 B、 HCl C、NH3 D、H2SO4
D3、1g H2O中含有a个氢原子,则阿伏加德罗常数为( )
A、(a/9)mol-1 B、 9a mol-1
C、 2a mol-1 D、a mol-1B5.等质量的SO2和SO3分子个数之比为( ),原子个数之比为( ),O原子个数之比为( )。5:35:410:94.含3.01×1023个O原子的O2的质量为g粒子数目
(N) ×NA ÷ NA质量
(m)n ÷ M ×M联系宏观和微观物质的桥梁[例 ] 4. 9 g硫酸里含有多少个硫酸分子?解: 硫酸的相对分子质量是98,硫酸的摩尔质量是 98g/mol 。n (H2SO4) = 4. 9 g98g/mol= 0.05 mol答:4.9克硫酸里含有 3.01×1022个硫酸分子。N (H2SO4) =0.05 mol×6.02×1023/mol= 3.01×1022[练习] 20. 2 g硝酸钾中,氧原子的质量是多少g?解: 硝酸钾的相对分子质量是101,硝酸钾的摩尔质量是 101g/mol 。n (KNO3) = 20.2 g101g/mol= 0.2 mol答:20.2g硝酸钾中,氧元素的质量是 9. 6 g 。n (O) =0.2 mol×3 = 0.6 molm (O) = 0. 6 mol×16g/mol= 9.6 g二、1摩尔任何原子、分子、离子的质量:1、1摩尔任何原子的质量以克为单位时,在数值上等于其相对原子质量。2、1摩尔任何分子的质量以克为单位时,在数值上等于其相对分子质量。3、1摩尔任何离子的质量以克为单位时,在数值上等于其化学式的式量。1molH2O的质量
1molH2SO4的质量
1molCO2的质量
1mol蔗糖(C12H22O11)的质量1molNa+的质量、 1molCl -的质量
1molSO42-的质量1、 M(H2O)= 。
2、M( NaCl)= 。
3、M(H2SO4)= 。
4 、M(OH-)=_________________练习17g · mol-158.5g · mol-198g · mol-118g · mol-1摩尔质量: 单位物质的量的物质所具有的质量叫摩尔质量。符号:M
单位: g/mol 或 g·mol-1
kg/mol 或 kg·mol-1【课堂小结】:【巩固练习】:
计算:前面出示的342g蔗糖、18g水、58.5g氯化钠、32g硫、65g锌所含分子数、原子数或离子数? 【巩固练习】:有五种物质:①6gH2;
②0.5molCO2;③1.204×1024个HCl分子;
④147gH2SO4;⑤92g乙醇(C2H5OH);
请回答:
⑴物质的量最大的是 ;
⑵所含分子数最多的是 ;
⑶所含原子数最多的是 ;
曹冲称象的故事
指导思想:化整为零称量一粒小米 怎样完成下列任务?---称量10克小米 回忆与思考C + O2 = CO2质量 克 克 克粒子数 个碳原子 个氧分子 个CO2分子物质的量点燃1、物质的量: 1)是一个物理量,表示含有一定数目粒子的
集合体。①“物质的量”是一个物理量的名称(国际单位制七个基本物理量 之一) ,是专有名词, 使用时四个字不能拆分!
②物质的量计量对象——微观粒子;
微观粒子—分子、原子、离子、电子、
质子、中子(表示符号:n)国际单位制中七种基本物理量及其单位 ★2)单位:①摩尔仅仅是一个单位;
---物质的量的单位!
②摩尔计量对象——微观粒子;表示符号:mol摩尔:简称摩
【学生练习】:判断下列说法是否正确?①1molH2; ② 1mol氧;
③ 1molH2O ; ④ 1mol氧元素;
⑤ 1molNa+ ; ⑥ 1摩尔氧原子。 当物质所含的微粒数是多少时,其物质的量是1mol呢?当物质所含粒子数与0.012kg12C所含的碳原子数相同时,它的物质的量就是1摩。3)1mol的规定已知一个碳原子的质量: 1.99×10-23克2、阿伏加德罗常数 : 1mol任何粒子所含有的粒子数叫做阿伏加德罗常数。①基准数:0.012kg12C所含的碳原子数;
②近似值:6.02×1023;表示符号:NA; 单位mol-1 假设有6.02×1023粒大米,每粒大米重0.025g。把它分给全世界的人,全世界约50亿人口:每人可分得大米趣味问题228万吨。若每人每年平均消费粮食400kg,那么,
可供全世界的人口食用570万年【学生练习】:
(1)1molH2SO4中约含有 个硫酸分子;
(2)0.5molH2O中约含有 个水分子;
(3)1mol H2约含有 个氢原子。
(4)1mol NaCl中约含有 个Na+、含有 个Cl-。 6.02×10236.02×10231. 204×10246.02×10233.01×1023 (1)1mol O中约含有 个O
(2)2mol H2O中约含有 个H2O
(3)3NA个H+是 mol H+
(4)5NA个水分子的物质的量是 mol H2O
(5)N个水分子的物质的量是 mol6.02 × 1023 2×6.02×10233N/NA5【学生练习】:粒子个数阿伏加德罗常数物质的量N = NA÷ n公式一一、物质的量的单位 —— 摩尔描述物质所含粒子多少的专有名词,“物质的量”四个字不可拆分物理量1.物质的量注意2、阿伏加德罗常数 : 1mol任何粒子所含有的粒子数叫做阿伏加德罗常数。符号:NA单位:mol-1近似值:6.02×1023
符号:n2. 5mol的O2中有多少个氧气分子?练习1:1. 3.01×1023个H,其物质的量是多少3 . 1.204×1024个N2的物质的量为 ,氮原子的物质的量为 。练习2:
1. 0.5mol水中含有 个水分子?2. 2mol水中含有 个水分子, 个氢原子?3. 1molH2SO4溶于水,水中存在的溶质粒子是什么?它们的物质的量各是多少?4. 1个水分子有 个电子,1mol H2O中呢?3.01×1023个CO2的物质的量是多少?● 2 mol H2O中含有氢原子多少个?●2 mol Mg变成Mg2+时失去电子数是多少?0.5molCO2电子物质的量是多少? 0.5 mol2.408×1024 2×2×6.02×1023 个练习:●含有2 mol氢原子的H2O中水分子有多少个?6.02×1023 11 mol● 1 mol H2中含有电子多少个?1.204×1024 1. 1molH3PO4分子中含有()个 H3PO4分子,()个氢原子,()mol氢原子
()个P原子,()molP原子
()个O原子,()molO原子
2. 1molSO42-中有()个 SO42-,所带电荷为()个。
3. 1molO中有()个O原子,()个电子,()mol电子。
4. 2molH2SO4中有()mol氢原子,()molS原子,()molO原子,()mol原子5. 1.5molNH3有 个NH3分子, molH, mol电子
6. 1molNa+中有( )个Na+,( )mol电子
7. 2molOH-有( )个OH-,( )mol电子
8. 含0.3molSO42-的Fe2(SO4)3的物质的量是( )mol,Fe3+有( )mol
9. 等物质的量的SO2和SO3分子个数之比为( ),原子个数之比为( ),O原子个数之比为( )。【课堂练习】1.下列关于物质的量的说法中不正确的是( )
A.物质的量是国际单位制的7个基本单位之一
B.物质的量实际上是表示含有一定数目的粒子集体
C.物质的量的单位是“摩尔”
D.物质的量是表示物质数量的单位AD2、下列表示方法中,错误的是( )
A.2 mol氢 B. 1 mol H2O
4 mol e- D. 0.5 mol H2SO4
E。 2 mol钢笔 AE3、下列关于阿伏加德罗常数的说法正确的是 ( )
A.阿伏加德罗常数是一个纯数,没有单位
B.阿伏加德罗常数就是6.02×1023
C.阿伏加德罗常数是指1 mol 的任何粒子的
粒子数
D.阿伏加德罗常数的近似值为:
6.02×1023 mol-1CD4.1mol物质的含义是( )
A、0.012Kg碳
B、含有6.02×1023个微粒的物质
C、含有阿伏加德罗常数个微粒的物质
D、含有与6.02×1023个碳原子等质量的物质C5.在0.5mol O2中含有的氧分子数目
是多少?解:O2的分子数为N = n × NA =0.5 mol× 6.02 ×1023mol-1= 3.01 × 1023 答:O2的分子数为3.01 × 1023个。6.在0.5mol O2中含有的氧原子数目
是多少?解:O2的氧原子数为N = n ×2 × NA =0.5 mol×2× 6.02 ×1023mol-1
= 6.02 × 1023 答:O2的氧原子数为6.02 × 1023个。1mol几种物质的质量64 g Cu182712569818g27g12g56g98g结论: 1mol任何粒子或物质的质量以g为单位时,其数值都与该粒子的相对原子质量或相对分子质量相等。1molH2O的质量
1molH2SO4的质量
1molCO2的质量
1mol蔗糖(C12H22O11)的质量1molNa+的质量、 1molCl -的质量
1molSO42-的质量3.摩尔质量定义:单位物质的量(即1mol)的物质所具有的质量符号:M
单位: g/mol 或 g·mol-1
kg/mol 或 kg·mol-1练一练11 g / mol34 g / mol3417 g ? mol-1172323 g ? mol-1摩尔质量1 g 34 g 17 g 23 g练一练◆ 2mol (n)H2SO4的质量(m)
为 。◆ 5.6g(m)铁中含Fe的物质的量(n)
是 。196g0.1 mol摩尔质量M的应用◆ 80g(m)O2的物质的量(n)是 。2.5 mol质量摩尔质量物质的量m = M÷ n1、 M(H2O)= 。
2、M( NaCl)= 。
3、M(H2SO4)= 。
4 、M(OH-)=_________________练习17g · mol-158.5g · mol-198g · mol-118g · mol-1例题、 71gNa2SO4中含有的Na+和SO42-的物质的量多少?【练习】1.课本P13学与问2.等质量的下列物质中,所含分子数最少的是 ( )
A、Cl2 B、 HCl C、NH3 D、H2SO4
D3、1g H2O中含有a个氢原子,则阿伏加德罗常数为( )
A、(a/9)mol-1 B、 9a mol-1
C、 2a mol-1 D、a mol-1B5.等质量的SO2和SO3分子个数之比为( ),原子个数之比为( ),O原子个数之比为( )。5:35:410:94.含3.01×1023个O原子的O2的质量为g粒子数目
(N) ×NA ÷ NA质量
(m)n ÷ M ×M联系宏观和微观物质的桥梁[例 ] 4. 9 g硫酸里含有多少个硫酸分子?解: 硫酸的相对分子质量是98,硫酸的摩尔质量是 98g/mol 。n (H2SO4) = 4. 9 g98g/mol= 0.05 mol答:4.9克硫酸里含有 3.01×1022个硫酸分子。N (H2SO4) =0.05 mol×6.02×1023/mol= 3.01×1022[练习] 20. 2 g硝酸钾中,氧原子的质量是多少g?解: 硝酸钾的相对分子质量是101,硝酸钾的摩尔质量是 101g/mol 。n (KNO3) = 20.2 g101g/mol= 0.2 mol答:20.2g硝酸钾中,氧元素的质量是 9. 6 g 。n (O) =0.2 mol×3 = 0.6 molm (O) = 0. 6 mol×16g/mol= 9.6 g二、1摩尔任何原子、分子、离子的质量:1、1摩尔任何原子的质量以克为单位时,在数值上等于其相对原子质量。2、1摩尔任何分子的质量以克为单位时,在数值上等于其相对分子质量。3、1摩尔任何离子的质量以克为单位时,在数值上等于其化学式的式量。1molH2O的质量
1molH2SO4的质量
1molCO2的质量
1mol蔗糖(C12H22O11)的质量1molNa+的质量、 1molCl -的质量
1molSO42-的质量1、 M(H2O)= 。
2、M( NaCl)= 。
3、M(H2SO4)= 。
4 、M(OH-)=_________________练习17g · mol-158.5g · mol-198g · mol-118g · mol-1摩尔质量: 单位物质的量的物质所具有的质量叫摩尔质量。符号:M
单位: g/mol 或 g·mol-1
kg/mol 或 kg·mol-1【课堂小结】:【巩固练习】:
计算:前面出示的342g蔗糖、18g水、58.5g氯化钠、32g硫、65g锌所含分子数、原子数或离子数? 【巩固练习】:有五种物质:①6gH2;
②0.5molCO2;③1.204×1024个HCl分子;
④147gH2SO4;⑤92g乙醇(C2H5OH);
请回答:
⑴物质的量最大的是 ;
⑵所含分子数最多的是 ;
⑶所含原子数最多的是 ;
