物质的量
图片预览









文档简介
课件38张PPT。丰富多彩的化学物质
专题一第一单元 物 质 的 量
第一课时 1、曹冲称象的故事中解决问题的主导思想是什么?
(化整为零,化大为小)2、已知托盘天平的最小刻度为0.1克,你能用托盘天平称一粒米的质量吗?(积小成大,聚微为宏)生活小常识一打铅笔12支一刀纸100张 一盒火柴
1滴水大约有6×1020个水
分子,若取1mL,1L……
数值更大
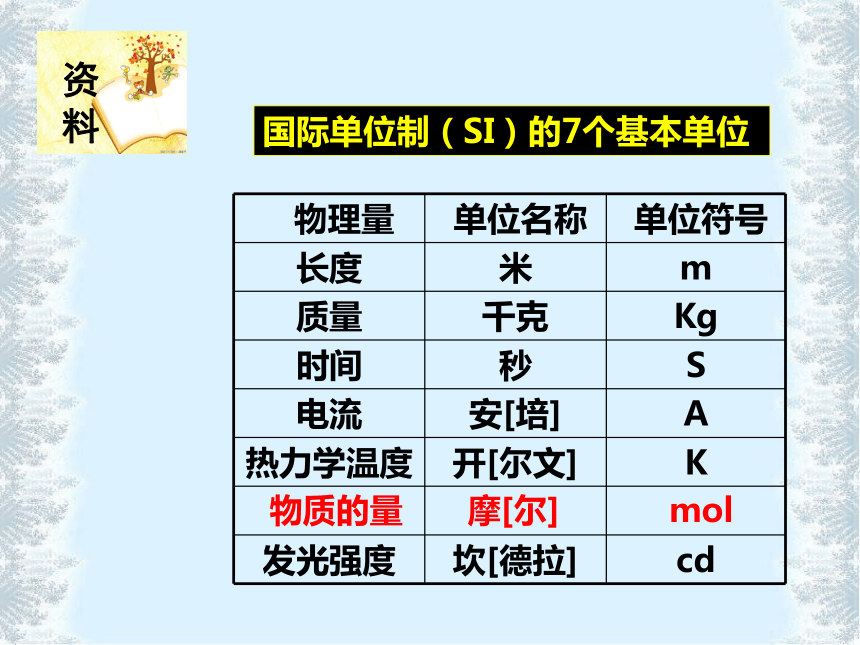
若要得到这个数值需什么数据?国际单位制(SI)的7个基本单位物质的量 摩[尔]mol资料 下列关于物质的量的说法中不正确的是( )
A.物质的量是国际单位制的7个基本单位之一
B.物质的量实际上是表示含有一定数目的粒子集体
C.物质的量的单位是“摩尔”
D.物质的量是表示物质数量的单位【随堂检测】米:光在真空中 s的时间间隔内所进行的路程的长度为1 m。千克:国际千克原器是1889年第一届国际权度大会批准制造的。它是一个高度和直径均为39mm的,用铂铱合金制成的圆柱体。原型保存在巴黎国际计量局。基本物理量的单位需要统一的度量衡温馨提示0.012kg 12C微观构成?已知:一个碳原子的质量为 1.993 × 10-26kg
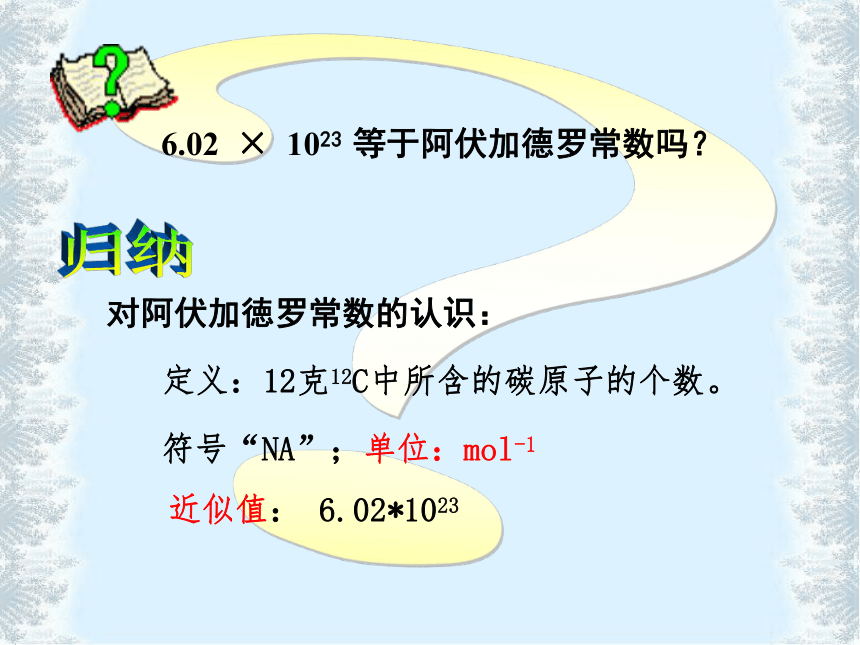
求: 0.012kg 碳-12 中所含的碳原子数?[思考]解: ≈ 6.02×1023 0.012kg1.993 × 10-26kg碳原子数=?6.02 × 1023 等于阿伏加德罗常数吗?对阿伏加徳罗常数的认识: 定义:12克12C中所含的碳原子的个数。近似值: 6.02*1023归纳符号“NA”;单位:mol-1NA--一个惊人的数字将6.02 ? 1023个一毛硬币排起来,可来回地球和太阳间400亿次之多。设每公斤约有2万粒米,全国约有12亿人口,再以每人每天消费粮食400克计, 6.02?1023粒米若供我国人民食用可用多长时间?约1.7 × 108 年5摩尔硫酸根离子2摩尔氢原子如1mol金刚石2摩尔氢气2摩尔水2 摩尔氢分子2 摩尔氢离子1mol质子1:1mol猪八戒
2:1 摩尔氧
3:1 摩尔氧原子
4:2 摩尔分子氢
5:3 摩尔水
6:0.5摩尔二氧化碳
7:1mol钠元素
8:1 摩尔NaCl错误,指代不明,可指氧原子也可指氧分子、氧离子 正确 ,表示为1mol O错误,正确表示为2mol H2正确,表示为 3mol H2O正确 ,表示为0.5mol CO2 错误,不是微观粒子不对,元素是宏观概念,只能说种类正确,特定组合原子、分子、离子、 质子、中子、 电子、原子团等归纳4、0.3molH2SO4含有 个硫酸分子?
5、1molNa2CO3中约含有 molNa+,
molCO32-离子,共含有离子的个数为
个。
1、一个O2分子有 个O原子?
2、100个O2分子有 个O原子?
3、1mol O2分子有 mol O原子? 个O原子?算一算?物质的量基本物理量单位:摩尔基准:NA知识小结【课堂练习】
1. 下列数量的各物质中,含原子个数最多的是( )
A.1mol HCl B.3.01 x 1023 个碘分子
C.12g 12C D.0.5mol CH4
2. 与0.3 mol H2O 含有相同氢原子数的是( )
0.3 mol HNO3
B.3.612 X 10 23个 HNO3分子
0.2 mol H3PO4
0.1mol NH3丰富多彩的化学物质
专题一第一单元 物 质 的 量
第二课时物质的量基本物理量单位:摩尔基准:NA温故知新复习巩固1.某盐的溶液中含有Na+、Mg2+、Cl- 、SO42-四种离子,若Na+为
0.2 mol, Mg2+为0.4 mol, Cl- 为0.4 mol, 则SO42-物质的量为:
0.1 mol B. 0.3mol
C. 0.5mol D. 0.15mol2.一定量某营养液中溶质的配方分别如下:
配方一:0.3mol KCl,0.2mol K2SO4,0.1 molZnSO4
配方二:0.1mol KCl,0.3mol K2SO4,0.1 molZnCl2
对于两种营养液的成分,下列说法中正确的是( )
A. 只有n(K+)相同 B. 只有n (Cl-)相同
C. 完全相同 D. 各离子的物质的量完全不同 2.990×10-231.993×10-233.821×10-231.628×10-226.02×10236.02×10236.02×10236.02×10231818122398122398请完成下表:1mol任何微观粒子(原子、分子、离子)的质量以克为单位时, 其数值都与该粒子的相对原子质量或相对分子质量相等。结论 数值:等于该物质的相对原子质量或者相对分子质量。摩尔质量M注意【随堂检测】1mol Cu的质量是__________。
1mol HNO3的质量是__________。
1.5mol OH-的质量是__________。
64g O2的物质的量是__________。
100gNaOH的物质的量是__________。
__________gH2SO4的物质的量为0.5mol,其中H的物质的量是__________,含有________个S原子,O的质量是__________。
【例题1】483g Na2SO4·10H2O中所含的Na+和SO42-的物质的量各是多少?所含H2O分子的数目是多少?【解】 Na2SO4·10H2O的相对分子质量为322,
摩尔质量为322 g·mol-1。
例题分析则Na+的物质的量为3.00mol,SO42-的物质的量为 1.50mol,H2O的物质的量为15.0mol。一瓶农夫山泉的净含量为550ml,里面约含的水分子个数是多少?
又:N(H2O)=n(H2O)·NA
=30.56mol × 6.02×1023mol-1
=1.84×1025【随堂检测】 根据上述计算,归纳n、m、M、NA、N之间的关系 物质的量的意义:
是联系宏观和微观的纽带或桥梁。物质的量在化学反应计算 化学方程式中的化学计量数可以代表分子或原子数,也可以代表物质的物质的量,若如此,
则2H2+O2=2H2O可以读作:
_____________________________。【概念辨析 】下列说法是否正确:A、 6.02 ×1023个12C原子的质量为1gB、 H的摩尔质量为1gC、 H2SO4的摩尔质量等于6.02 ×1023个
H2SO4 分子的质量D、 NaOH的摩尔质量为40g·mol-1√×××下列数量的物质中含原子个数最多的是( )
A.0.4摩尔氧气
B.3.01×1022CO2分子
C.4℃时5.4毫升水
D.10g氖
C【随堂检测】0.8g某物质含有3.01×1022个分子,该物质的相对分子的质量约为( )
A.8 B.16 C.64 D.160 B
【随堂检测】在反应X+2Y=R+2M中,已知R和M的摩尔质量之比为22∶9,当1.6gX与Y完全反应后,生成4.4gR。则在此反应中Y和M的质量之比为( )
A.16∶9 B.23∶9 C.32∶9 D.46∶9
A【随堂检测】 相同质量的SO2和SO3, 下列关系正确的是( )
含氧原子的个数比为2:3
含硫元素的质量比为5:4
含氧元素的质量比为5:6
含硫原子的个数比为1:1【随堂检测】【随堂检测】 NA表示阿伏加德罗常数,下列说法不正确的是( )A、醋酸的摩尔质量与NA个醋酸分子的
质量在数值上相等 B、NA个氧分子和NA个氢分子的质量比
等于16:1 C、17gNH3所含的原子数目为4NA,所
含电子数目为10NA D、2.4g金属镁变成离子时失去的电子
数目为0.1NA下面有关摩尔的说法不正确的是( )
A、摩尔是国际单位制的一种基本单位
B、摩尔是表示物质微粒数量的单位
C、摩尔是以阿伏加德罗常数为衡量标准的物质的量的单位
D、摩尔是表示物质质量的单位。B D【随堂检测】 多少克尿素[CO(NH2)2]所含的氮原子个数与15.8g氯化铵所含的氮原子个数相等?
专题一第一单元 物 质 的 量
第一课时 1、曹冲称象的故事中解决问题的主导思想是什么?
(化整为零,化大为小)2、已知托盘天平的最小刻度为0.1克,你能用托盘天平称一粒米的质量吗?(积小成大,聚微为宏)生活小常识一打铅笔12支一刀纸100张 一盒火柴
1滴水大约有6×1020个水
分子,若取1mL,1L……
数值更大
若要得到这个数值需什么数据?国际单位制(SI)的7个基本单位物质的量 摩[尔]mol资料 下列关于物质的量的说法中不正确的是( )
A.物质的量是国际单位制的7个基本单位之一
B.物质的量实际上是表示含有一定数目的粒子集体
C.物质的量的单位是“摩尔”
D.物质的量是表示物质数量的单位【随堂检测】米:光在真空中 s的时间间隔内所进行的路程的长度为1 m。千克:国际千克原器是1889年第一届国际权度大会批准制造的。它是一个高度和直径均为39mm的,用铂铱合金制成的圆柱体。原型保存在巴黎国际计量局。基本物理量的单位需要统一的度量衡温馨提示0.012kg 12C微观构成?已知:一个碳原子的质量为 1.993 × 10-26kg
求: 0.012kg 碳-12 中所含的碳原子数?[思考]解: ≈ 6.02×1023 0.012kg1.993 × 10-26kg碳原子数=?6.02 × 1023 等于阿伏加德罗常数吗?对阿伏加徳罗常数的认识: 定义:12克12C中所含的碳原子的个数。近似值: 6.02*1023归纳符号“NA”;单位:mol-1NA--一个惊人的数字将6.02 ? 1023个一毛硬币排起来,可来回地球和太阳间400亿次之多。设每公斤约有2万粒米,全国约有12亿人口,再以每人每天消费粮食400克计, 6.02?1023粒米若供我国人民食用可用多长时间?约1.7 × 108 年5摩尔硫酸根离子2摩尔氢原子如1mol金刚石2摩尔氢气2摩尔水2 摩尔氢分子2 摩尔氢离子1mol质子1:1mol猪八戒
2:1 摩尔氧
3:1 摩尔氧原子
4:2 摩尔分子氢
5:3 摩尔水
6:0.5摩尔二氧化碳
7:1mol钠元素
8:1 摩尔NaCl错误,指代不明,可指氧原子也可指氧分子、氧离子 正确 ,表示为1mol O错误,正确表示为2mol H2正确,表示为 3mol H2O正确 ,表示为0.5mol CO2 错误,不是微观粒子不对,元素是宏观概念,只能说种类正确,特定组合原子、分子、离子、 质子、中子、 电子、原子团等归纳4、0.3molH2SO4含有 个硫酸分子?
5、1molNa2CO3中约含有 molNa+,
molCO32-离子,共含有离子的个数为
个。
1、一个O2分子有 个O原子?
2、100个O2分子有 个O原子?
3、1mol O2分子有 mol O原子? 个O原子?算一算?物质的量基本物理量单位:摩尔基准:NA知识小结【课堂练习】
1. 下列数量的各物质中,含原子个数最多的是( )
A.1mol HCl B.3.01 x 1023 个碘分子
C.12g 12C D.0.5mol CH4
2. 与0.3 mol H2O 含有相同氢原子数的是( )
0.3 mol HNO3
B.3.612 X 10 23个 HNO3分子
0.2 mol H3PO4
0.1mol NH3丰富多彩的化学物质
专题一第一单元 物 质 的 量
第二课时物质的量基本物理量单位:摩尔基准:NA温故知新复习巩固1.某盐的溶液中含有Na+、Mg2+、Cl- 、SO42-四种离子,若Na+为
0.2 mol, Mg2+为0.4 mol, Cl- 为0.4 mol, 则SO42-物质的量为:
0.1 mol B. 0.3mol
C. 0.5mol D. 0.15mol2.一定量某营养液中溶质的配方分别如下:
配方一:0.3mol KCl,0.2mol K2SO4,0.1 molZnSO4
配方二:0.1mol KCl,0.3mol K2SO4,0.1 molZnCl2
对于两种营养液的成分,下列说法中正确的是( )
A. 只有n(K+)相同 B. 只有n (Cl-)相同
C. 完全相同 D. 各离子的物质的量完全不同 2.990×10-231.993×10-233.821×10-231.628×10-226.02×10236.02×10236.02×10236.02×10231818122398122398请完成下表:1mol任何微观粒子(原子、分子、离子)的质量以克为单位时, 其数值都与该粒子的相对原子质量或相对分子质量相等。结论 数值:等于该物质的相对原子质量或者相对分子质量。摩尔质量M注意【随堂检测】1mol Cu的质量是__________。
1mol HNO3的质量是__________。
1.5mol OH-的质量是__________。
64g O2的物质的量是__________。
100gNaOH的物质的量是__________。
__________gH2SO4的物质的量为0.5mol,其中H的物质的量是__________,含有________个S原子,O的质量是__________。
【例题1】483g Na2SO4·10H2O中所含的Na+和SO42-的物质的量各是多少?所含H2O分子的数目是多少?【解】 Na2SO4·10H2O的相对分子质量为322,
摩尔质量为322 g·mol-1。
例题分析则Na+的物质的量为3.00mol,SO42-的物质的量为 1.50mol,H2O的物质的量为15.0mol。一瓶农夫山泉的净含量为550ml,里面约含的水分子个数是多少?
又:N(H2O)=n(H2O)·NA
=30.56mol × 6.02×1023mol-1
=1.84×1025【随堂检测】 根据上述计算,归纳n、m、M、NA、N之间的关系 物质的量的意义:
是联系宏观和微观的纽带或桥梁。物质的量在化学反应计算 化学方程式中的化学计量数可以代表分子或原子数,也可以代表物质的物质的量,若如此,
则2H2+O2=2H2O可以读作:
_____________________________。【概念辨析 】下列说法是否正确:A、 6.02 ×1023个12C原子的质量为1gB、 H的摩尔质量为1gC、 H2SO4的摩尔质量等于6.02 ×1023个
H2SO4 分子的质量D、 NaOH的摩尔质量为40g·mol-1√×××下列数量的物质中含原子个数最多的是( )
A.0.4摩尔氧气
B.3.01×1022CO2分子
C.4℃时5.4毫升水
D.10g氖
C【随堂检测】0.8g某物质含有3.01×1022个分子,该物质的相对分子的质量约为( )
A.8 B.16 C.64 D.160 B
【随堂检测】在反应X+2Y=R+2M中,已知R和M的摩尔质量之比为22∶9,当1.6gX与Y完全反应后,生成4.4gR。则在此反应中Y和M的质量之比为( )
A.16∶9 B.23∶9 C.32∶9 D.46∶9
A【随堂检测】 相同质量的SO2和SO3, 下列关系正确的是( )
含氧原子的个数比为2:3
含硫元素的质量比为5:4
含氧元素的质量比为5:6
含硫原子的个数比为1:1【随堂检测】【随堂检测】 NA表示阿伏加德罗常数,下列说法不正确的是( )A、醋酸的摩尔质量与NA个醋酸分子的
质量在数值上相等 B、NA个氧分子和NA个氢分子的质量比
等于16:1 C、17gNH3所含的原子数目为4NA,所
含电子数目为10NA D、2.4g金属镁变成离子时失去的电子
数目为0.1NA下面有关摩尔的说法不正确的是( )
A、摩尔是国际单位制的一种基本单位
B、摩尔是表示物质微粒数量的单位
C、摩尔是以阿伏加德罗常数为衡量标准的物质的量的单位
D、摩尔是表示物质质量的单位。B D【随堂检测】 多少克尿素[CO(NH2)2]所含的氮原子个数与15.8g氯化铵所含的氮原子个数相等?
