第四章《非金属及其化合物》单元测试(新人教版必修1)
文档属性
| 名称 | 第四章《非金属及其化合物》单元测试(新人教版必修1) |

|
|
| 格式 | rar | ||
| 文件大小 | 92.9KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2009-12-26 00:00:00 | ||
图片预览




文档简介
第四章 非金属及其化合物
一、选择题(每小题2.5分,共60分)
1.用氯气消毒的自来水配制下列溶液时,会使配得的溶液变质的是
①NaOH; ②AgNO3; ③Na2CO3; ④NaBr; ⑤FeCl2
A.只有②④ B.只有④⑤ C.只有②④⑤ D.全部
2.在一种pH=1的溶液中可能存在NO3―,I―,Cl―,Fe3+中的一种或几种.向该溶液中滴入溴水,单质溴被还原.由此推断该溶液
3.下列物质在一定条件下与碳作用所产生的无色气体能与H2S反应的是
A.二氧化硅 B.浓硫酸 C.浓硝酸 D.水
4.下列物质中,既能同强酸或强碱作用,一定条件下又能作氧化剂或还原剂的是
A.(NH4)2S B.NaHSO3 C.Al(OH)3 D.FeS
5.不能说明氯元素的非金属性比硫元素强的事实是
A.Cl2与H2S溶液发生置换反应 B.受热时H2S能分解,HCl则不能 C.单质硫可在空气中燃烧,Cl2不能 D.溶于水时HCl是强酸,H2S是弱酸
6.将20mL充满NO和NO2混合气体的试管倒立于水中,过一会儿,当试管内有6mL水上升时,液面不再变化. 原混合气体中NO和NO2的体积比为(在相同条件下)
A.9:11 B.11:9 C.7:3 D.3:7
7.取相同物质的量浓度、相同体积的(NH4)3PO4,(NH4)2HPO4,NH4H2PO43种溶液,分别滴加NaOH溶液直至恰好完全反应,则3种溶液耗用NaOH溶液的体积之比是
A.1:2:3 B.3:2:1 C.1:1:1 D.6:3:2
8.室温时,两个容积相同的烧瓶中分别盛有M和N两种气体(同温同压),取下弹簧夹A,使两烧瓶内的气体接触(如图),容器内的压强由大到小的顺序是
A.①②③④ B.②④①③ C. ④①②③ D.①④③②
9.在水溶液中能大量共存,加入过量的稀H2SO4后有沉淀和气体产生的离子组是
A.HCO,Cl-,Na+,Ba2+ B.AlO2―,S2―,Na+,K+ C.SiO32-,CO32-,K+,Na+ D.Ba2+,Al3+,NO3―,Cl-
10.a,b,c,d,e五种无色气体,进行如下实验:
实验步聚 实验现象
①a,b相混合 气体变成棕色 ②c,d相混合 产生白烟 ③c,e分别通入少量溴水中 溴水均成无色透明溶液 ④b,e分别通入氢硫酸中 都产生淡黄色的沉淀
则a,b,c,d,e可能依次是
A.O2,NO,HCl,NH3,CO2 B.O2,NO,NH3,HCl,SO2 C.NO,O2,NH3,HCl,SO2 D.HBr,Cl2,NH3,H2S,C2H4
11.某混合气体中可能含有H2,CO,CO2,HCl,NH3和H2O(气)中的两种或多种,当混合气体依次通过①澄清的石灰水(无浑浊现象)、②氢氧化钡溶液(有浑浊现象)、③浓硫酸(无明显现象)、④灼热的氧化铜(变红)、⑤无水硫酸铜(变蓝)对该混合气体成分的正确判断是
A.一定没有CO2,肯定有H2 B.一定有CO2,CO和H2O(气) C.可能有CO2,NH3和H2O(气) D.一定有H2,CO2和HCl
12.限用一种试剂即可区别Na2S,Na2S2O3,Na2CO3,NaAlO2,Na2SO4五种无色溶液,这种试剂应选用
A.烧碱溶液 B.盐酸 C. 氨水 D.氯化钡溶液
13.有Na2CO3,Ba(OH)2,H2SO4三种体积和物质的量浓度都相等的溶液,几位同学按不同的顺序将它们混合(产生沉淀立即过滤掉),对于所得溶液,下列结论正确的是
A.溶液一定显碱性 B.溶液不可能显碱性 C.溶液可能显碱性 D.溶液不可能显酸性
14.下列各组物质都能使溴水退色的是
A.石灰水、裂化汽油 B.NaHS溶液、SO2 C. NaCl溶液、NaI溶液 D.CaCl2溶液、Na2S溶液
15.我国城市环境中的大气污染物主要是
A.CO2,Cl2,N2,酸雨 B.SO2,CO,NO2,烟尘 C.NH3,CO2,NO,雾 D.HCl,SO2,N2,粉尘
16.有X,Y,Z三种物质,把过量的X与Y共热,有气体产生,把该气体通入少量Z的溶液中,会产生白色沉淀,则X,Y,Z可能是
X Y Z
A.浓硫酸 NaCl+MnO2 AgNO3 B.NaOH溶液 Ca(HCO3)2 Ca(OH)2 C.NaOH溶液 (NH4)2SO4 KAl(SO4)2 D.浓硫酸 NaCl H2S
17.下列每组均有三种等物质的量浓度、等体积的溶液,若将它们混合起来,无沉淀物产生的是
A.AlCl3,H2SO4,KOH B.BaCl2,NaOH,KHCO3 C.AgNO3,HNO3,NaBr D.FeCl3,HNO3,Ca(OH)2
18.某单质甲及其化合物乙、丙、丁、戊在一定条件下发生如图所示的变化,乙可以是
A.PH3 B.H2S C.HCl D.NH3
19.下列物质的用途错误的是
A.食盐用于制纯碱 B.硅藻土作吸咐剂 C.用硫酸铜配制农药 D.乙二醇作医用消毒剂
20.下列变化肯定不可逆的组是
①晶体的溶解; ②盐溶液的电解;
③盐的水解; ④电解质的电离;
⑤乙酸乙酯的生成; ⑥Fe(OH)3溶液与硅酸溶胶混合;
⑦蛋白质溶液中加入饱和的硫酸铵溶液;
⑧蛋白质溶液中加入福尔马林;
⑨合成氨.
A.①②③④⑦⑨ B.②⑤⑥⑧
C.⑤⑥⑦⑧ D.②⑥⑧
21.下列各组盐的混合物加热或溶于水均有CO2气体放出的是
A.Al2(SO4)3和NaHCO3 B.Na2SO4和NH4HCO3 C.MgSO4和Na2CO3 D.NaHCO3和NaHSO4
22.由H2SO4,Al2O3,NaOH,Mg,Cl2两两之间进行反应,可制得的正盐有
A.五种 B.六种 C.七种 D.八种
23.下列各组中的两种物质,能直接相互转变的是
A.NH3,NO B.O2,F2 C.NO,NO2 D.H2S,SO2
24.把两种固体混合加入水中,可产生能使澄清的石灰水变浑浊的气体,这两种固体可能是
A.NaHCO3和Na2O2 B.铝粉和NaOH C.Na2SO3和SO3 D.Na2CO3和P2O5
二 填空题(共15.5分)
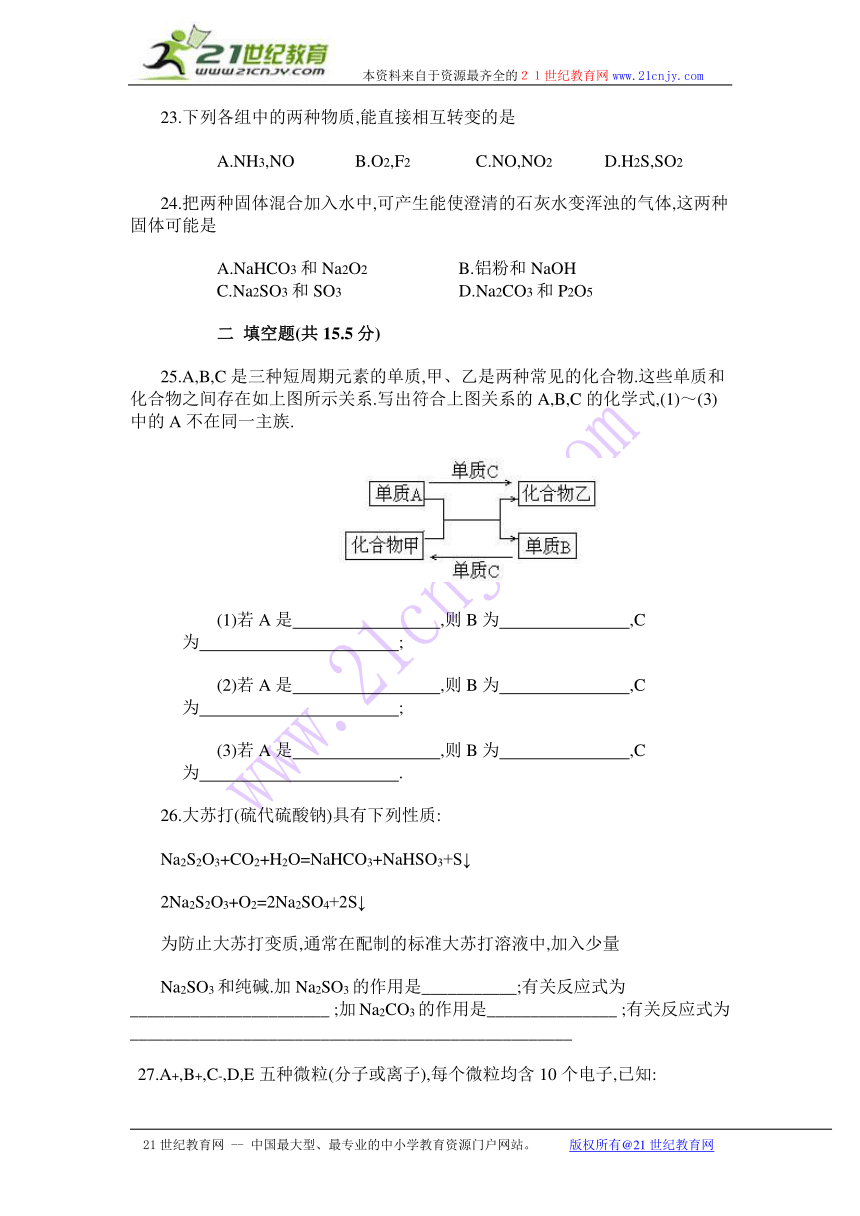
25.A,B,C是三种短周期元素的单质,甲、乙是两种常见的化合物.这些单质和化合物之间存在如上图所示关系.写出符合上图关系的A,B,C的化学式,(1)~(3)中的A不在同一主族.
(1)若A是 ,则B为 ,C为 ;
(2)若A是 ,则B为 ,C为 ;
(3)若A是 ,则B为 ,C为 .
26.大苏打(硫代硫酸钠)具有下列性质:
Na2S2O3+CO2+H2O=NaHCO3+NaHSO3+S↓
2Na2S2O3+O2=2Na2SO4+2S↓
为防止大苏打变质,通常在配制的标准大苏打溶液中,加入少量
Na2SO3和纯碱.加Na2SO3的作用是___________;有关反应式为_______________________ ;加Na2CO3的作用是_______________ ;有关反应式为___________________________________________________
27.A+,B+,C-,D,E五种微粒(分子或离子),每个微粒均含10个电子,已知:
①A++C-D+E↑ ②B++C-→2D
请回答以下问题:
(1)C-的电子式为 .
(2)具有相同空间构型的微粒是 和 .已知XYn型的分子或离子,当X原子上无孤对电子时,Y原子在空间呈对称排列,则A+中的键角为 .
(3)分别写出A+和D反应、B和E反应的离子方程式.
A++D: ,B++E: .
28.常温常压下,A,B,C,D是四种气体,W,T,X,Y,Z是五种固体,其中固体Z是Y和W组成的混合物,已知构成W的阴阳离子的电子层结构完全相同,它们有如下的转化关系(固体用方框表示):
请填写以下空白:
(1)X是 ,B是 .
(2)写出下列转化的反应方程式,是氧化还原反应的要标明电子转移方向和数目.W→D+T: ,Z→C: .
三、简答题(共5.5分)
29.将两种不含结晶水的白色晶体A和B以等物质的量混合后,放入硬质试管中,加强热能放出无色气体C,C溶于水至饱和,得无色液体D,将试管内残留的固体E取出,溶于水,其水溶液里+1价的阳离子的离子结构示意图为
阴离子和Ba(NO3)2反应生成不溶于盐酸的白色沉淀.D的浓溶液与KMnO4混合,生成的气体能使石蕊溶液褪色,A的水溶液显酸性.用化学式表示A、B、C、D、E各是什么物质.写出有关化学方程式.
四、实验题(共6分)
30.CuSO4在一定条件下发生如下分解:CuSO4======CuO+SO2+SO3+O2,
有人设计通过实验测定反应产生的SO2,SO3,O2的物质的量的方法,并经计算确定该条件下分解反应式各物质的系数.
实验可能需要的仪器如下图所示:
实验测得数据及有关结果如下:
①准确称量无水硫酸铜6.0g.
②测出量筒中水的体积后,折算成排水之气体在标准状况下的体积为280mL.
③干燥管质量在实验结束时增加2.4g.
④实验结束时,装置F中的溶液变为NaHSO4溶液(不含其他溶质)
请回答以下问题:
(1)按装置从左至右的方向,各仪器接口连接顺序为 .
(2)装置F的作用是 .
(3)装置D的作用是 .
(4)确定装置E的进、出口的原则是 .
(5)首先应计算的物质是 .通过计算推断,该条件下反应的化学方程式为 .
(6)该实验设计中,可能给测定带来的误差最大的装置是 .
五、计算题(共13分)
31.把标准状况下总体积为10L的NO2、NH3、N2组成的混合气体通过足量的硝酸溶液,结果比溶液的质量增加了12.5g,原气体体积缩小为3.28L,求此混合气体中各成分分别是多少升?
32.在50mL 4mol/L的氢氧化钠溶液中,通入一定量的硫化氢,反应完毕,在常温减压条件下,用氮气把溶液吹干,得到白色固体7.92g,通过计算确定白色固体的组成及各组分的质量.
参考答案
一、共60分
1.D 2.B ?3.B 4.B 5.D 6.B 7.C 8.B
9.AC 10.C 11.D 12.B 13.CD 14.AB 15.B 16.AC
17.A 18.BD 19.D 20.D 21.AD 22.C 23.C 24.CD
二、25.(共4.5分)
(1)Mg C O2
(2)F2 O2 H2(或Cl2 S H2)
(3)O2 S H2
26.(共4分)
吸收空气中的O2,防止Na2S2O3被氧化;
2Na2SO3+O2=2Na2SO4
吸收空气中CO2;
Na2CO3+CO2+H2O=2NaHCO3
27.(共4分)
(1)
(2)NH3; H+3O; 109°28’
(3)NH4++H2ONH3·H2O+H+;
?
28.(共3分)
(1)KClO3;H2
(2)2KCl+H2SO4(浓)K2SO4+2HCl↑;
?
三、29.(共5.5分)
A:NaHSO4 B:NaCl C:HCl D: 盐酸 E:Na2SO4
NaHSO4+NaClNa2SO4+HCl↑
Na2SO4+Ba(NO3)2=BaSO4↓+2NaNO3
2KMnO4+16HCl(浓)=2KCl+2MnCl2+8H2O+5Cl2↑
四、(共6分)
30.(1)①⑨⑩⑥⑤③④⑧⑦②
(2)吸收SO3,放出等物质的量的SO2
(3)干燥SO2和O2
(4)保证气体将瓶中水压出,进入量筒
(5)O2 3CuSO43CuO+2SO2↑+O2+SO3↑
(6)F
31.(共6分)
解:设NO2为xL, NH3为yL, N2为zL.
混合气体通过足量硝酸溶液时NH3+HNO3=NH4NO3
NO2与硝酸溶液中的水反应:3NO2+H2O=2HNO3+NO
所以最后剩余的气体应是N2和NO.
?
?
解得 x=6.72L y=2.24L z=1.04L
答:混合气体中NO2为6.72L、NH3为2.24L、N2为1.04L.
32.(共7分)
解: NaOH的物质的量为:0.05L×4mol/L=0.2mol
0.2mol的NaOH跟H2S反应,若全部生成Na2S时,
?
0.2mol的NaOH跟H2S反应,若全部生成NaHS时,
白色固体(NaHS)的质量为: 56g/mol×0.2mol=11.2g
因为7.8g<7.92g<11.2g
所以得到的白色固体有两种可能的组合,
一种是Na2S和NaOH的混合物;
另一种是Na2S和NaHS的混合物.
设Na2S为xmol,则有(0.2-2x)mol NaOH.
78g/mol×xmol+40g/mol(0.2-2x)=7.92g
x=0.04mol
Na2S的质量:0.04mol×78g/mol=3.12g
NaOH的质量:7.92g-3.12g=4.80g
设Na2S为ymol,则有(0.2-2y)mol NaHS.
78g/mol×ymol+56g/mol(0.2-2y)mol=7.92g
y=0.0965mol
Na2S的质量为:78g/mol×0.0965mol=7.52g
NaHS的质量为:7.92g-7.52g=0.40g
答:白色固体有一种是由Na2S(3.12g)和NaOH(4.80g)组成的混合物.
另一种是由Na2S(7.52g)和NaHS(0.40g)组成的混合物.
?
