化学能与电能
图片预览




文档简介
课件14张PPT。第二节
化学能与电能
电力在当今社会的应用和作用。
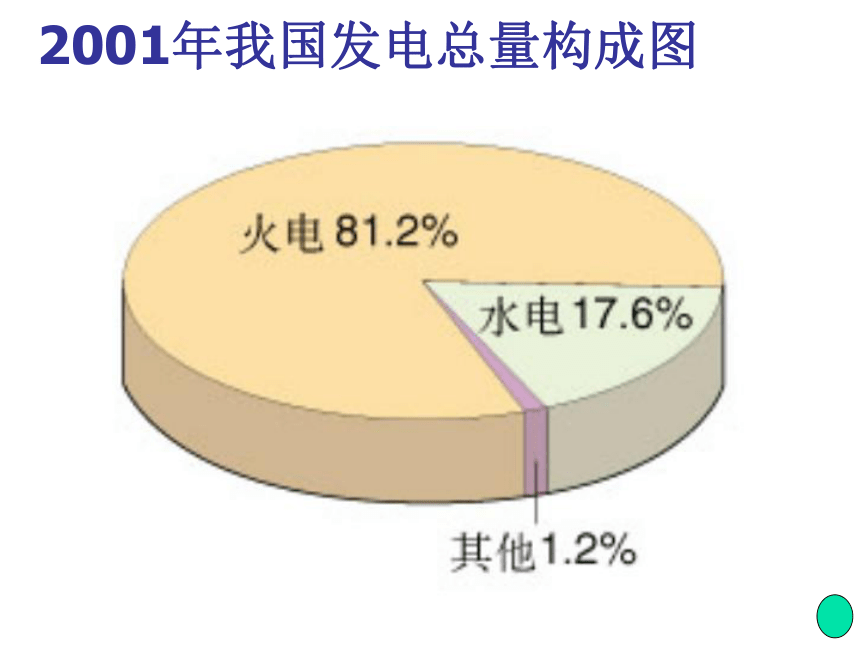
我国目前和未来发电总量的构成。
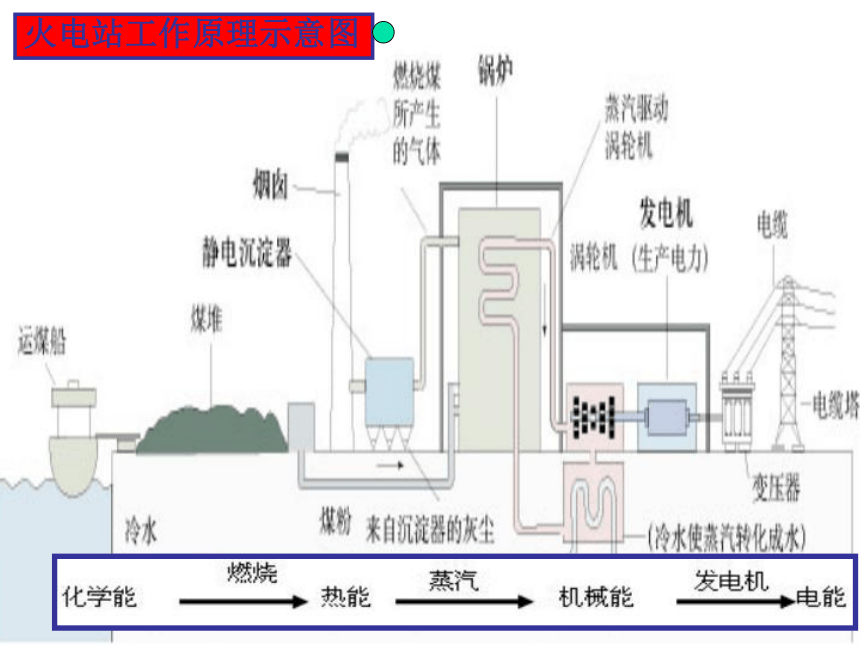
火力发电的原理是什么?
火力发电有什么利和弊?
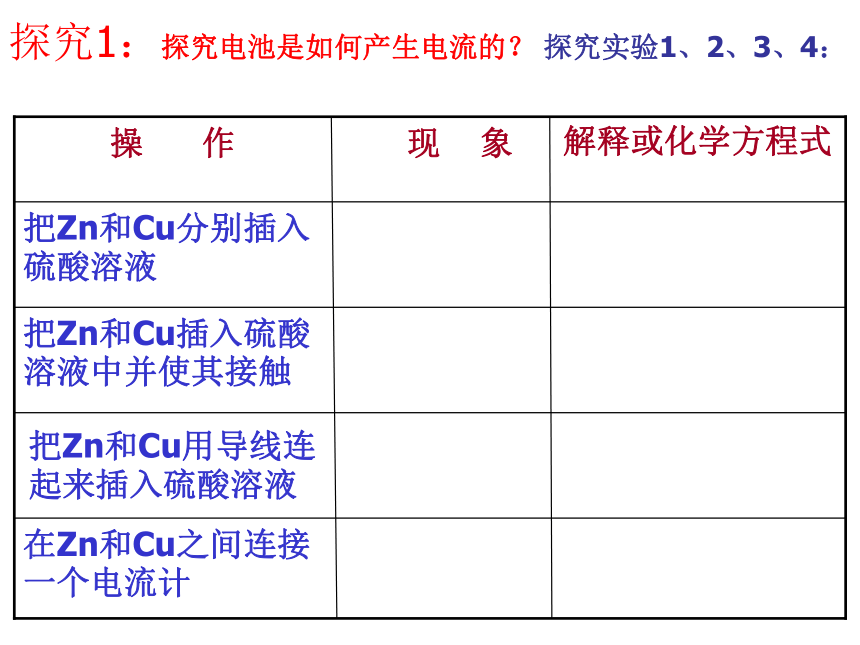
问:如何把化学能直接转化为电能呢?思考:2001年我国发电总量构成图火电站工作原理示意图探究1:探究电池是如何产生电流的? 探究实验1、2、3、4:思考:铜片上是什么气体?铜片上的电子从哪来?
锌片的质量有什么变化?
锌片和铜片上各发生什么反应?
从能量角度看,能量的转化形式是什么?
分析:锌片和铜片上发生的反应:
Zn片: Zn -2e- = Zn2+(氧化反应)
Cu片:2H++2e- = H2 ↑ (还原反应)
当使氧化反应和还原反应在不同的区域进行,并用导线把两个区域连起来时,还原剂发生氧化反应失去的电子通过导线移动到还原反应区域使氧化剂得到电子发生还原反应。结论:在氧化还原反应的基础上,让氧化反应和还原反应分别在两极发生,化学能就直接转化成电能,从而产生电流。
能把化学能直接转化为电能的装置叫原电池。 思考:镁片和铜片各是什么极?
探究2:形成原电池的条件:结论:形成原电池的条件为:两极:
两种活动性不同的金属(或非金属单质)
溶液:
电解质溶液,而且电极均插入电解质溶液。
能自发的发生氧化还原反应
闭合:
两电极与电解质溶液形成闭合回路。思考:原电池中的电极如何称呼和判断?
(从电极材料和电极反应两个方面判断)
两个电极各发生什么反应?
影响原电池电流强弱的因素有哪些?
一个原电池的使用寿命跟哪些因素有关?
哪些电池能充电?1.X、Y、Z都是金属,把X浸入Z的硝酸盐溶液中,X的表面有Z析出,X和Y组成原电池时,Y为电池的负极。X、Y、Z三种金属的活动性顺序为( ?)
(A)X>Y>Z (B)X>Z>Y
(C)Y>X>Z (D)Y>Z>X
2.下列装置哪些可以形成原电池? 形成原电池的写出电极反应式,并指出电子流动方向。
【练习巩固】小结:原电池装置特点:化学能转化为电能
形成条件:⑴两个活泼性不同的电极;
⑵电解质溶液;
⑶形成闭合回路
电极名称:负极:较活泼金属;
正极:较不活泼金属或能导电的非金属。
反应原理:
负极:发生氧化反应: 负极本身失电子 。
正极:发生还原反应: 溶液中阳离子得电子。
电子流向:
负极正极习题参考 1.化学电池是把化学能直接转化为电能的装置。其反应的基础是氧化还原反应。 2.一次性干电池中的氧化还原反应是不可逆的,放完电之后就不能再使用。而蓄电池中的氧化还原反应是可逆的,它在放电时所进行的氧化还原反应,在充电时可以逆向进行,使生成物恢复原状。 3.从电极材料判断:活泼金属作负极,不活泼金属(或石墨)作正极。从发生的反应判断:发生氧化反应的电极是负极,发生还原反应的电极是正极。 4.家用电器的普及和种类的增加,使得电池的使用量随之剧增。废电池混在垃圾中,不仅污染环境,而且造成浪费。据报道,全国的电池年消耗量为30亿只,因疏于回收而丢失铜740吨,锌1.6万吨,锰粉9.7万吨。另外,普通干电池里含有镉和汞两种元素,这两种元素若污染了土壤和水源,进入人类的食物链,就会发生“水俣病”(汞中毒)和“痛痛病”(镉中毒),这两种工业公害病,都在日本发生过,造成很多人死亡。 为防止悲剧重演,我们应该把废旧电池与其他垃圾分开,集中回收。许多国家都很重视废旧电池的回收,如德国的很多商店要求顾客在购买电池时,同时要把废旧电池交回商店;日本的分类垃圾箱里有一种专门放废旧电池的黄色垃圾箱,垃圾箱的投入口有三个,分别标有普通电池、纽扣电池和其他电池。
化学能与电能
电力在当今社会的应用和作用。
我国目前和未来发电总量的构成。
火力发电的原理是什么?
火力发电有什么利和弊?
问:如何把化学能直接转化为电能呢?思考:2001年我国发电总量构成图火电站工作原理示意图探究1:探究电池是如何产生电流的? 探究实验1、2、3、4:思考:铜片上是什么气体?铜片上的电子从哪来?
锌片的质量有什么变化?
锌片和铜片上各发生什么反应?
从能量角度看,能量的转化形式是什么?
分析:锌片和铜片上发生的反应:
Zn片: Zn -2e- = Zn2+(氧化反应)
Cu片:2H++2e- = H2 ↑ (还原反应)
当使氧化反应和还原反应在不同的区域进行,并用导线把两个区域连起来时,还原剂发生氧化反应失去的电子通过导线移动到还原反应区域使氧化剂得到电子发生还原反应。结论:在氧化还原反应的基础上,让氧化反应和还原反应分别在两极发生,化学能就直接转化成电能,从而产生电流。
能把化学能直接转化为电能的装置叫原电池。 思考:镁片和铜片各是什么极?
探究2:形成原电池的条件:结论:形成原电池的条件为:两极:
两种活动性不同的金属(或非金属单质)
溶液:
电解质溶液,而且电极均插入电解质溶液。
能自发的发生氧化还原反应
闭合:
两电极与电解质溶液形成闭合回路。思考:原电池中的电极如何称呼和判断?
(从电极材料和电极反应两个方面判断)
两个电极各发生什么反应?
影响原电池电流强弱的因素有哪些?
一个原电池的使用寿命跟哪些因素有关?
哪些电池能充电?1.X、Y、Z都是金属,把X浸入Z的硝酸盐溶液中,X的表面有Z析出,X和Y组成原电池时,Y为电池的负极。X、Y、Z三种金属的活动性顺序为( ?)
(A)X>Y>Z (B)X>Z>Y
(C)Y>X>Z (D)Y>Z>X
2.下列装置哪些可以形成原电池? 形成原电池的写出电极反应式,并指出电子流动方向。
【练习巩固】小结:原电池装置特点:化学能转化为电能
形成条件:⑴两个活泼性不同的电极;
⑵电解质溶液;
⑶形成闭合回路
电极名称:负极:较活泼金属;
正极:较不活泼金属或能导电的非金属。
反应原理:
负极:发生氧化反应: 负极本身失电子 。
正极:发生还原反应: 溶液中阳离子得电子。
电子流向:
负极正极习题参考 1.化学电池是把化学能直接转化为电能的装置。其反应的基础是氧化还原反应。 2.一次性干电池中的氧化还原反应是不可逆的,放完电之后就不能再使用。而蓄电池中的氧化还原反应是可逆的,它在放电时所进行的氧化还原反应,在充电时可以逆向进行,使生成物恢复原状。 3.从电极材料判断:活泼金属作负极,不活泼金属(或石墨)作正极。从发生的反应判断:发生氧化反应的电极是负极,发生还原反应的电极是正极。 4.家用电器的普及和种类的增加,使得电池的使用量随之剧增。废电池混在垃圾中,不仅污染环境,而且造成浪费。据报道,全国的电池年消耗量为30亿只,因疏于回收而丢失铜740吨,锌1.6万吨,锰粉9.7万吨。另外,普通干电池里含有镉和汞两种元素,这两种元素若污染了土壤和水源,进入人类的食物链,就会发生“水俣病”(汞中毒)和“痛痛病”(镉中毒),这两种工业公害病,都在日本发生过,造成很多人死亡。 为防止悲剧重演,我们应该把废旧电池与其他垃圾分开,集中回收。许多国家都很重视废旧电池的回收,如德国的很多商店要求顾客在购买电池时,同时要把废旧电池交回商店;日本的分类垃圾箱里有一种专门放废旧电池的黄色垃圾箱,垃圾箱的投入口有三个,分别标有普通电池、纽扣电池和其他电池。
