溶解度课件第二课时
图片预览










文档简介
课件31张PPT。溶解度课题二 第二课时饱和溶液蒸发溶剂或加溶质或变温加溶剂或变温不饱和溶液1、饱和溶液与不饱和溶液的概念知识回顾2、饱和溶液与不饱和溶液之间的转化
回忆并思考实验:把高锰酸钾和碘分别加入一定量的水中。
现象:高锰酸钾_溶于水中,而碘__溶于水。
结论:不同的物质在同种溶剂中溶解能力__。
不能不同实验:把碘分别加入一定量的水中和酒精中。
现象:碘__溶于水中,却__溶于酒精中。
小结:同种物质在不同的溶剂中溶解能力__。不能能不同能实验: 200C时把51.6克硝酸钾放到100克水中,充分搅拌 后仍有20克剩余,给混合物加热到400C时
现象: 剩下的20克又溶解了
结论: 物质的溶解能力和 有关.温度二、固体物质的溶解度1、溶解性
①定义:一种物质在另一种物质里的溶解能力。
②影响因素:溶质和溶剂本身的性质(内因)
温度、压强(外因)
③ 表示方法:溶解度2、溶解度
①定义:在一定温度下,某固态物质
在100克溶剂里达到饱和状态
时所溶解的质量,叫做这种
物质在种溶剂里的溶解度。
②要素 条件:在一定温度下 标准:100克溶剂(一般指水) 状态:溶液是饱和状态 单位:克③涵义例如: NaCl在20 ℃的溶解度为36 g
表示的意义就是:在20 ℃时,100 g水中溶解36 g氯化钠时溶液恰好达到饱和状态。或者说,在20 ℃时,100 g水中最多能
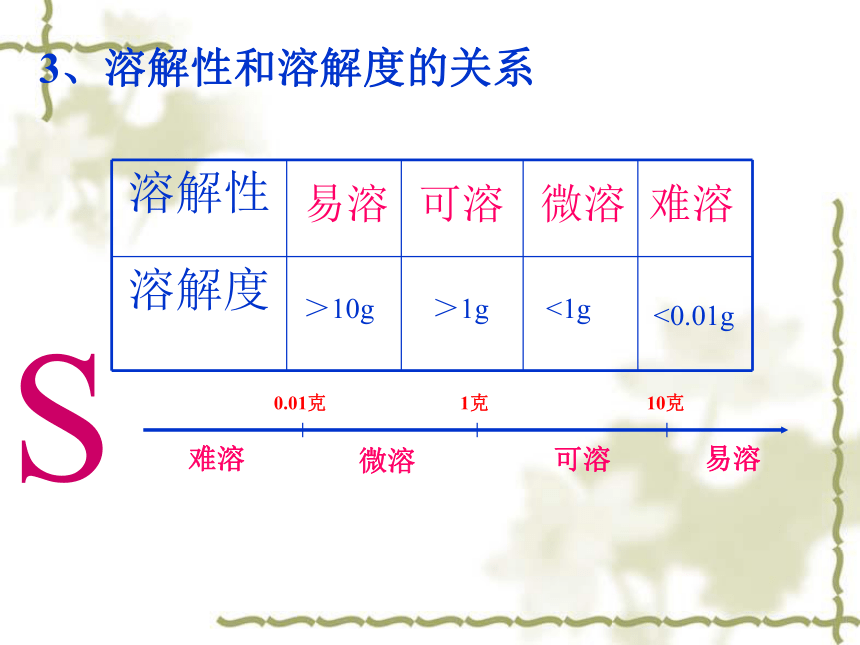
溶解36 g氯化钠。易溶可溶微溶难溶>10g>1g<1g<0.01g3、溶解性和溶解度的关系
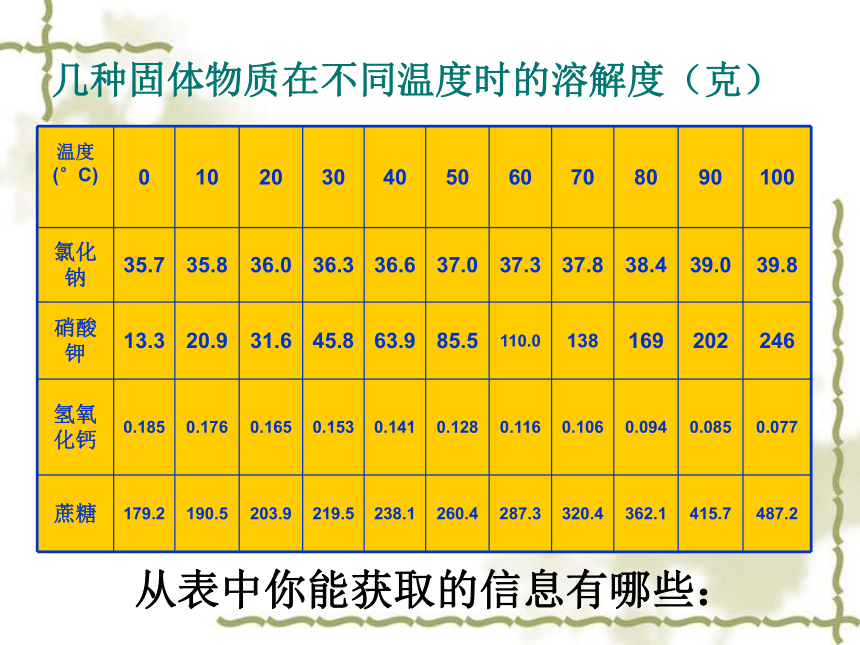
0.01克1克10克难溶微溶可溶易溶S 几种固体物质在不同温度时的溶解度(克)从表中你能获取的信息有哪些:温度:在溶质和溶剂一定的情况下,温度是影响固体溶解度的重要因素。
4、影响固体物质的溶解度的因素:
一般规律如下:
①大部分固体物质的溶解度随着温度的升高而增大(如硝酸钾);
②少数固体物质的溶解度受温度变化影响较小(如氯化钠);
③极少数固体物质的溶解度随着温度的升高而减小(如氢氧化钙)。
1、下列关于溶解度的叙述是否正确。
①.100g水中最多能溶解NaCl36g,NaCl的溶解度是36g。
②.20℃时,90g水最多能溶解NaCl32g,20℃时NaCl的溶解度是32g。
③.20℃时,100g水中溶解有32gNaCl,20℃时NaCl的溶解度是32g。
④.20℃时,100g水最多能溶解36gNaCl,20℃时NaCl的溶解度是36g。
思考判断下列说法是否正确(从条件、标准、状态、单位等四个方面去分析)2、20℃时,KNO3的溶解度为31.6g,
这句话的含义是什么?思考3、20℃时,50克水中最多能溶解某物质0.8克,则这种物质属于( )
A难溶物质 B 微溶物质
C 可溶物质 D 易溶物质C4、 20℃时,20克水中最多能溶解5克某物质,则这种物质的溶解度是多少克?解:设这种物质200C时的溶解度为S克,则:溶质 溶剂 溶液5克 20克 25克S克 100克 S+100克即: S=25克思考 下面是几种固体物质在不同温度时的溶解度(g)你能将它们的溶解度在坐标系中画出来吗?溶解度(克)温度(oc)0 10 20 30 40 50 6080
70
60
50
40
30
20
10KNO31、溶解度曲线: 由于固体物质的溶解度随温度变化而变化,随温度一定而一定,这种变化可以用溶解度曲线来表示。我们用纵坐标表示溶解度,横坐标表示温度,绘出固体物质的溶解度随温度变化的曲线,这种曲线叫做溶解度曲线。
三、溶解度曲线 溶解度(克)温度(℃)1601501401301201101009080706050403020102001901801701010090807060504030200硝酸铵硝酸钾硝酸钠氯化铵氯化钠硼酸几种物质的溶解度曲线.a从这些溶解度曲线图你能获取哪些信息?熟石灰的溶解度曲线2、溶解度曲线受温度影响的变化趋势 ①曲线陡升:物质的溶解度随温度升高而增大
如:硝酸钾。
②曲线缓升:物质的溶解度受温度的影响很小
如:氯化钠;③曲线下降:物质的溶解度随温度的升高而减小
如:氢氧化钙。
3、溶解度曲线的意义及应用:①表示同一种物质在不同温度时的溶解度,查找指定温度时物质的溶解度,并根据溶解度判断溶解性。
②表示不同物质在同一温度时的溶解度,可以比较同一温度时,不同物质的溶解度的大小;
③ 两条溶解度曲线的交点,表示在该点所示的温度下,两种物质的溶解度相等。
④比较和确定物质的溶解度受温度影响的程度,并据此确定物质结晶或混合物分离提纯的方法。
⑤表示物质的溶解度随温度的变化情况,比较和确定物质的溶解度受温度影响的程度⑥确定溶液的状态(饱和与不饱和)
A:溶解度曲线上的点表示物质在该点所示温度下的溶 解度,溶液所处的状态是饱和溶液。
B:溶解度曲线下面的面积上的点,表示溶液所处的状态是不饱和状态,依其数据配制的溶液为对应温度时的不饱和溶液。
C:溶解度曲线上面的面积上的点,依其数据配制的溶液为对应温度时的饱和溶液,且该溶质有剩余。
1、如图是A、B两种固体物质的溶解
度曲线,根据该图回答
下列问题:
(1)在 ℃时,
A、B两种物质的溶解度
相等。
(2)溶解度受温度变
化影响大的是 ;
(3)A物质的溶解度随
温度的升高而 (填“增大”、“减少”或“变化不大”)。O溶解度(克)温度( ℃)t1t2t3ABt2A增大课堂练习2、如图是A、B、C三种物质在水中的溶解度曲线,请回答:
(1)M点的含义是_______________________
(2)当温度为t1oC,三种物质溶解度由小到大依次为_______,当温度为t3oC时,溶解度最大的是____.
(3)C可能表示哪种物质:
____________________
A和C两种物质在t2oC时的溶解度相同B少,要使氢氧化钙的不饱和溶液变成饱
和溶液,可采取的措施是( )
(1)升高温度 (2)降低温度
(3)蒸发溶剂后恢复到原温度
(4)通入二氧化碳后过滤
(5)加入足量氢氧化钙
A、(2)(5)
B、(4)(5)
C、(1)(3)(5)
D、(1)(4)(5)C四、气体的溶解度1、概念——该气体在压强为101千帕和一定
温度时,气体溶解在1体积水里达到饱和
状态时的气体体积叫气体的溶解度。例如在0 ℃时,氧气的溶解度为0.049,就是指在0 ℃,氧气压强为101 kPa时,1体积水中最多能溶解0.049体积氧气。气体的溶解度与固体的溶解度比较2、影响气体溶解度的因素(1)压强:气体溶解度随压强的
增大而增大,随压强
减小而减小。(2)温度:气体溶解度随温度升
高而降低。你能举出几例子来说明吗? 2、影响固体物质的溶解度的因素是: 温度学完本课我知道了1、固体的溶解度:在一定温度下,某固态
物质在100克溶剂里达到饱和状态时所溶
解的质量 ,叫做这种物质在这种溶剂里
的溶解度。 3、气体的溶解度:该气体在压强为101千
帕和一定温度时,气体溶解在1体积水
里达到饱和状态时的气体体积叫气体
的溶解度。
4、影响气体物质的溶解度的因素是: 温度、
压强(1)大部分固体物质溶解度随温度升高
而升高。如:KNO3 少数的固体物质的溶解度随温度升高
而变化不大。如:NaCl 5、溶解度曲线 (2)应用溶解度曲线查出某物质在一定温
度时的溶解度;比较不同物质在同一温
度下的溶解度大小。 极少数固体物质的溶解度随温度升高而减小。如:Ca(OH)2....1、 20℃,100克水中达到饱和状态时,食盐溶解36克( )2、 20℃,100克水中达到饱和状态时,食盐可以溶解36克( )3、 20℃,100克水中食盐最多溶解36克( ) 6、 20℃,136克饱和食盐水中,蒸发100克水中后,析
出36克食盐( ) 4、 20℃,100克水中达到饱和状态时,食盐一定溶解
36克( ) 5、 20℃,100克水中溶解食盐,形成饱和溶液质量为
136克( )√√√√√√挑战一下自己吧!!!8、食盐溶解度为36克( )9、20℃时,食盐溶解度为36( )10、20℃时,50克水中最多能溶解18克食盐( )11、20℃时,溶解度实质上是溶质克数( )12、20℃时,溶解度实质上是溶剂克数( )7、 20℃,200克饱和食盐水中,蒸发100克水后,一定
析出36 克食盐( )√√××××14.欲增大硝酸钾在水中的溶解度,适宜的办法是( )
A、增加溶剂 B、升高温度
C、增加硝酸钾固体 D、用玻璃棒搅拌
15.物质的溶解度与( )无关
A、溶质、溶剂的多少 B、温度的高低
C、溶剂的种类 D、溶质的种类
16.20℃时硝酸钾的溶解度是31.6g,下列说法正确的
是( )
A.100g水溶解31.6g 硝酸钾一定饱和
B. 20℃时,100g硝酸钾饱和溶解里含有 31.6g硝酸钾
C. 20℃时,131.6g硝酸钾饱和溶解里含有31.6g硝酸钾
D.此时溶液质量一定是131.6g BAC下节课再见!
回忆并思考实验:把高锰酸钾和碘分别加入一定量的水中。
现象:高锰酸钾_溶于水中,而碘__溶于水。
结论:不同的物质在同种溶剂中溶解能力__。
不能不同实验:把碘分别加入一定量的水中和酒精中。
现象:碘__溶于水中,却__溶于酒精中。
小结:同种物质在不同的溶剂中溶解能力__。不能能不同能实验: 200C时把51.6克硝酸钾放到100克水中,充分搅拌 后仍有20克剩余,给混合物加热到400C时
现象: 剩下的20克又溶解了
结论: 物质的溶解能力和 有关.温度二、固体物质的溶解度1、溶解性
①定义:一种物质在另一种物质里的溶解能力。
②影响因素:溶质和溶剂本身的性质(内因)
温度、压强(外因)
③ 表示方法:溶解度2、溶解度
①定义:在一定温度下,某固态物质
在100克溶剂里达到饱和状态
时所溶解的质量,叫做这种
物质在种溶剂里的溶解度。
②要素 条件:在一定温度下 标准:100克溶剂(一般指水) 状态:溶液是饱和状态 单位:克③涵义例如: NaCl在20 ℃的溶解度为36 g
表示的意义就是:在20 ℃时,100 g水中溶解36 g氯化钠时溶液恰好达到饱和状态。或者说,在20 ℃时,100 g水中最多能
溶解36 g氯化钠。易溶可溶微溶难溶>10g>1g<1g<0.01g3、溶解性和溶解度的关系
0.01克1克10克难溶微溶可溶易溶S 几种固体物质在不同温度时的溶解度(克)从表中你能获取的信息有哪些:温度:在溶质和溶剂一定的情况下,温度是影响固体溶解度的重要因素。
4、影响固体物质的溶解度的因素:
一般规律如下:
①大部分固体物质的溶解度随着温度的升高而增大(如硝酸钾);
②少数固体物质的溶解度受温度变化影响较小(如氯化钠);
③极少数固体物质的溶解度随着温度的升高而减小(如氢氧化钙)。
1、下列关于溶解度的叙述是否正确。
①.100g水中最多能溶解NaCl36g,NaCl的溶解度是36g。
②.20℃时,90g水最多能溶解NaCl32g,20℃时NaCl的溶解度是32g。
③.20℃时,100g水中溶解有32gNaCl,20℃时NaCl的溶解度是32g。
④.20℃时,100g水最多能溶解36gNaCl,20℃时NaCl的溶解度是36g。
思考判断下列说法是否正确(从条件、标准、状态、单位等四个方面去分析)2、20℃时,KNO3的溶解度为31.6g,
这句话的含义是什么?思考3、20℃时,50克水中最多能溶解某物质0.8克,则这种物质属于( )
A难溶物质 B 微溶物质
C 可溶物质 D 易溶物质C4、 20℃时,20克水中最多能溶解5克某物质,则这种物质的溶解度是多少克?解:设这种物质200C时的溶解度为S克,则:溶质 溶剂 溶液5克 20克 25克S克 100克 S+100克即: S=25克思考 下面是几种固体物质在不同温度时的溶解度(g)你能将它们的溶解度在坐标系中画出来吗?溶解度(克)温度(oc)0 10 20 30 40 50 6080
70
60
50
40
30
20
10KNO31、溶解度曲线: 由于固体物质的溶解度随温度变化而变化,随温度一定而一定,这种变化可以用溶解度曲线来表示。我们用纵坐标表示溶解度,横坐标表示温度,绘出固体物质的溶解度随温度变化的曲线,这种曲线叫做溶解度曲线。
三、溶解度曲线 溶解度(克)温度(℃)1601501401301201101009080706050403020102001901801701010090807060504030200硝酸铵硝酸钾硝酸钠氯化铵氯化钠硼酸几种物质的溶解度曲线.a从这些溶解度曲线图你能获取哪些信息?熟石灰的溶解度曲线2、溶解度曲线受温度影响的变化趋势 ①曲线陡升:物质的溶解度随温度升高而增大
如:硝酸钾。
②曲线缓升:物质的溶解度受温度的影响很小
如:氯化钠;③曲线下降:物质的溶解度随温度的升高而减小
如:氢氧化钙。
3、溶解度曲线的意义及应用:①表示同一种物质在不同温度时的溶解度,查找指定温度时物质的溶解度,并根据溶解度判断溶解性。
②表示不同物质在同一温度时的溶解度,可以比较同一温度时,不同物质的溶解度的大小;
③ 两条溶解度曲线的交点,表示在该点所示的温度下,两种物质的溶解度相等。
④比较和确定物质的溶解度受温度影响的程度,并据此确定物质结晶或混合物分离提纯的方法。
⑤表示物质的溶解度随温度的变化情况,比较和确定物质的溶解度受温度影响的程度⑥确定溶液的状态(饱和与不饱和)
A:溶解度曲线上的点表示物质在该点所示温度下的溶 解度,溶液所处的状态是饱和溶液。
B:溶解度曲线下面的面积上的点,表示溶液所处的状态是不饱和状态,依其数据配制的溶液为对应温度时的不饱和溶液。
C:溶解度曲线上面的面积上的点,依其数据配制的溶液为对应温度时的饱和溶液,且该溶质有剩余。
1、如图是A、B两种固体物质的溶解
度曲线,根据该图回答
下列问题:
(1)在 ℃时,
A、B两种物质的溶解度
相等。
(2)溶解度受温度变
化影响大的是 ;
(3)A物质的溶解度随
温度的升高而 (填“增大”、“减少”或“变化不大”)。O溶解度(克)温度( ℃)t1t2t3ABt2A增大课堂练习2、如图是A、B、C三种物质在水中的溶解度曲线,请回答:
(1)M点的含义是_______________________
(2)当温度为t1oC,三种物质溶解度由小到大依次为_______,当温度为t3oC时,溶解度最大的是____.
(3)C可能表示哪种物质:
____________________
A和C两种物质在t2oC时的溶解度相同B
和溶液,可采取的措施是( )
(1)升高温度 (2)降低温度
(3)蒸发溶剂后恢复到原温度
(4)通入二氧化碳后过滤
(5)加入足量氢氧化钙
A、(2)(5)
B、(4)(5)
C、(1)(3)(5)
D、(1)(4)(5)C四、气体的溶解度1、概念——该气体在压强为101千帕和一定
温度时,气体溶解在1体积水里达到饱和
状态时的气体体积叫气体的溶解度。例如在0 ℃时,氧气的溶解度为0.049,就是指在0 ℃,氧气压强为101 kPa时,1体积水中最多能溶解0.049体积氧气。气体的溶解度与固体的溶解度比较2、影响气体溶解度的因素(1)压强:气体溶解度随压强的
增大而增大,随压强
减小而减小。(2)温度:气体溶解度随温度升
高而降低。你能举出几例子来说明吗? 2、影响固体物质的溶解度的因素是: 温度学完本课我知道了1、固体的溶解度:在一定温度下,某固态
物质在100克溶剂里达到饱和状态时所溶
解的质量 ,叫做这种物质在这种溶剂里
的溶解度。 3、气体的溶解度:该气体在压强为101千
帕和一定温度时,气体溶解在1体积水
里达到饱和状态时的气体体积叫气体
的溶解度。
4、影响气体物质的溶解度的因素是: 温度、
压强(1)大部分固体物质溶解度随温度升高
而升高。如:KNO3 少数的固体物质的溶解度随温度升高
而变化不大。如:NaCl 5、溶解度曲线 (2)应用溶解度曲线查出某物质在一定温
度时的溶解度;比较不同物质在同一温
度下的溶解度大小。 极少数固体物质的溶解度随温度升高而减小。如:Ca(OH)2....1、 20℃,100克水中达到饱和状态时,食盐溶解36克( )2、 20℃,100克水中达到饱和状态时,食盐可以溶解36克( )3、 20℃,100克水中食盐最多溶解36克( ) 6、 20℃,136克饱和食盐水中,蒸发100克水中后,析
出36克食盐( ) 4、 20℃,100克水中达到饱和状态时,食盐一定溶解
36克( ) 5、 20℃,100克水中溶解食盐,形成饱和溶液质量为
136克( )√√√√√√挑战一下自己吧!!!8、食盐溶解度为36克( )9、20℃时,食盐溶解度为36( )10、20℃时,50克水中最多能溶解18克食盐( )11、20℃时,溶解度实质上是溶质克数( )12、20℃时,溶解度实质上是溶剂克数( )7、 20℃,200克饱和食盐水中,蒸发100克水后,一定
析出36 克食盐( )√√××××14.欲增大硝酸钾在水中的溶解度,适宜的办法是( )
A、增加溶剂 B、升高温度
C、增加硝酸钾固体 D、用玻璃棒搅拌
15.物质的溶解度与( )无关
A、溶质、溶剂的多少 B、温度的高低
C、溶剂的种类 D、溶质的种类
16.20℃时硝酸钾的溶解度是31.6g,下列说法正确的
是( )
A.100g水溶解31.6g 硝酸钾一定饱和
B. 20℃时,100g硝酸钾饱和溶解里含有 31.6g硝酸钾
C. 20℃时,131.6g硝酸钾饱和溶解里含有31.6g硝酸钾
D.此时溶液质量一定是131.6g BAC下节课再见!
同课章节目录
