质量守恒定律课件
图片预览








文档简介
课件22张PPT。?
无中不能生有,任何存在的东西也不会消灭.看起来万物是死了,但是实则犹生:正如一场春雨落地,霎时失去踪影;可是草木把它吸收,长成花叶果实——依然欣欣向荣.
——德谟克利特质量守恒定律
及相关知识专题复习?实验探究实验用品:盐酸、大理石、托盘天平、烧杯、试管。 实验操作: ①把装有稀盐酸的小试管放到成有大理石的烧杯中。 ②将烧杯放到左盘上,在右盘上加砝码,使之平衡。 ③取下烧杯,将小试管中的稀盐酸倒入烧杯中,使反应发生,并将小试管再次放到小烧杯中。 ④将烧杯再放回托盘天平,观察天平是否平衡。 实验现象: ①稀盐酸与大理石混合后大理石溶解,有大量气泡冒出。 ②再次将烧杯放回托盘天平时,指针向右偏转,天平不再平衡。 实验结论:化学反应前后,物质的总质量变小。该反应不遵守质量守恒定律。质量守恒定律参加反应的
各物质的质
量总 和生成的各物质的质量
总和参加化学反应的各物质的质量总和等于反应后生成的各物质的质量总和。思维点击要准确把握该定律,应注意哪些问题?理解质量守恒定律的定义时要注意: 2.质量守恒定律适用于所有化学反应。3.质量守恒定律的“守恒”指的是质量守恒,其它方面如体积等不一定守恒。
1. “生成的各物质的质量总和”,应当包括生成的各种物质,如沉淀、气体等。
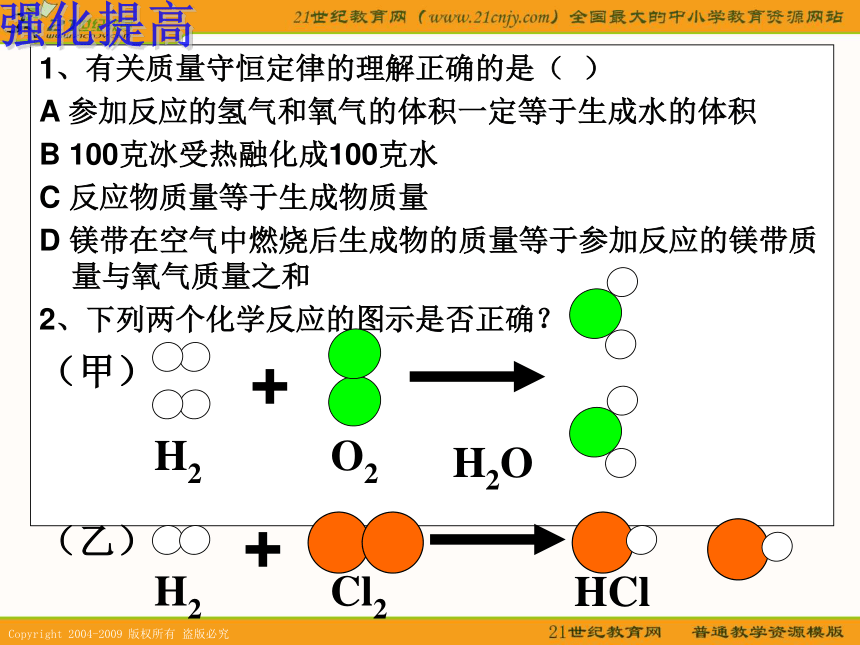
4.“参加”是指发生反应。1、有关质量守恒定律的理解正确的是( )
A 参加反应的氢气和氧气的体积一定等于生成水的体积
B 100克冰受热融化成100克水
C 反应物质量等于生成物质量
D 镁带在空气中燃烧后生成物的质量等于参加反应的镁带质量与氧气质量之和
2、下列两个化学反应的图示是否正确?强化提高HCl化学反应前后动动脑一定不变一定改变可能改变???分子的个数原子的种类
原子的数目
原子的质量
元素的种类
物质质量总和物质的种类
分子的种类点击中考:
1.解释一些化学现象。
质量守恒定律的应用2.利用反应前后元素守恒确定物质组成元素。3.利用反应前后原子的种类和数目守恒推断
物质的化学式或化学计量数。4.根据质量守恒定律进行各物质质量的计算。(1)成语“点石成金”,本意为古代术士的
一种法术,即能使石头变成黄金;现比喻
能化腐朽为神奇。有人说他能把石灰石变
成黄金,请你用化学知识说明石灰石不能
变成黄金的道理。
1.解释化学现象:(2) 生物的呼吸作用表示为: 有机物 + 氧气→二氧化碳 + 水 + 能量。以下关于有机物组成元素推断正确的是( )
A.只含碳元素
B.只含碳元素和氢元素
C.一定含碳、氢和氧元素
D.一定含有碳元素和氢元素,可能含有氧元素
(3)将4.6克某化合物放入氧气中完全燃烧,生成8.8克二氧化碳和5.4克水.问:这种化合物有哪几种元素组成?2.确定物质的元素组成:(4)一氧化氮是大气的主要污染物之一。近几年来又发现生物体内存在少量一氧化氮,它有扩张血管、增强记忆的功能,成为当前生命科学的热点。工业上制得一氧化氮的化学式为:4X + 5O2 =4NO + 6H2O ,则X的化学式为( ) A.N2 B.NO2 C.NH3 D.N2O5
(5)下图是某化学反应的微观模拟图,根据图示判断
参加反应的 和 与反应后生成的 个数
比为 。
3.确定化学式及化学计量数:(6)在化学反应A+2B = 2C+D中,6gA和8gB 恰好完全反应,生成9gD。若反应生成15gC,则参加反应的A的质量为( ) A.18g B.24g C.12g D.16g
(7)一密闭容器中,盛放A.B.C三种物质各30g,经电火花引燃,充分反应后,各物质质量变化如下:
关于此反应,下列不正确的是:( ) A. C物质中所含元素种类是ABD中所有元素种类之和B. 变化后待测的A为5g C. 该变化是分解反应 D. A物质有可能是单质4.简单计算:魔术——冰块燃烧 拿一块冰,放上一小块石头,用火柴在靠近小石头的地方点燃,很快就形成了一团烈火,冰块和石头一起燃烧起来,你想知道为什么吗?其实,那块小石头不是普通的石头,它叫电石,化学名称叫碳化钙(CaC2) ,电石遇水发生剧烈的化学反应,生成氢氧化钙Ca(OH)2和乙炔(C2H2) ,乙炔是一种可燃性气体。请写出有关反应的化学方程式。二、化学方程式2.以客观事实为依据二、化学方程式表示意义赛一赛,看谁最厉害 甲、乙是常见的单质,A、B是常见的化合物,它们的反应:甲+A B+乙(式中各物质的化学计量数和反应条件已略去)。请回答:
(1)反应类型是 。
(2)若甲为金属,且乙的硫酸盐溶液为蓝
色,写出反应的化学方程式 。
(3)若乙为非金属单质,B中含有+3价金属
元素,写出反应的化学方程式 。我思我获通过本堂课学习,收获如何?
让我们一起回顾一遍!表示意义 如图所示是测定蜡烛燃烧时的质量变化装置,天平是物理天平,左托盘上蜡烛的上方罩着吸收器。如果实验时,蜡烛正常燃烧,生成的气体顺利通过吸收器,吸收器的药品只在3min内起吸收作用。
试回答:
(1)本实验中,蜡烛燃烧时,反应物
是 ,生成物是 ,
反应条件是 。
(2)3min内天平是否保持平衡? ,
原因是
(3)3min后会出现什么结果? ,原因是
。
是否符合质量守恒定律? 。蜡烛和氧气二氧化碳和水点燃不平衡生成物中增加了氧元素,并且被吸收器吸收,左盘内物质质量增加天平右盘向下倾斜 3min后吸收器的药物不能再吸收生成物,二氧化碳和水蒸气逸散符合反思
1、命题的用意何在?(所考查的知识点)
2、解题中用了什么方法,有什么规律性东西?
3、所用的是不是最佳方法?有无创 新之处?
4、在解答过程中,自己的思路是否简捷?并与
老师和同学所运用的思维形式、思维规律和
思维方法相比较,及时归纳学习思考问题
“点金术”。
无中不能生有,任何存在的东西也不会消灭.看起来万物是死了,但是实则犹生:正如一场春雨落地,霎时失去踪影;可是草木把它吸收,长成花叶果实——依然欣欣向荣.
——德谟克利特质量守恒定律
及相关知识专题复习?实验探究实验用品:盐酸、大理石、托盘天平、烧杯、试管。 实验操作: ①把装有稀盐酸的小试管放到成有大理石的烧杯中。 ②将烧杯放到左盘上,在右盘上加砝码,使之平衡。 ③取下烧杯,将小试管中的稀盐酸倒入烧杯中,使反应发生,并将小试管再次放到小烧杯中。 ④将烧杯再放回托盘天平,观察天平是否平衡。 实验现象: ①稀盐酸与大理石混合后大理石溶解,有大量气泡冒出。 ②再次将烧杯放回托盘天平时,指针向右偏转,天平不再平衡。 实验结论:化学反应前后,物质的总质量变小。该反应不遵守质量守恒定律。质量守恒定律参加反应的
各物质的质
量总 和生成的各物质的质量
总和参加化学反应的各物质的质量总和等于反应后生成的各物质的质量总和。思维点击要准确把握该定律,应注意哪些问题?理解质量守恒定律的定义时要注意: 2.质量守恒定律适用于所有化学反应。3.质量守恒定律的“守恒”指的是质量守恒,其它方面如体积等不一定守恒。
1. “生成的各物质的质量总和”,应当包括生成的各种物质,如沉淀、气体等。
4.“参加”是指发生反应。1、有关质量守恒定律的理解正确的是( )
A 参加反应的氢气和氧气的体积一定等于生成水的体积
B 100克冰受热融化成100克水
C 反应物质量等于生成物质量
D 镁带在空气中燃烧后生成物的质量等于参加反应的镁带质量与氧气质量之和
2、下列两个化学反应的图示是否正确?强化提高HCl化学反应前后动动脑一定不变一定改变可能改变???分子的个数原子的种类
原子的数目
原子的质量
元素的种类
物质质量总和物质的种类
分子的种类点击中考:
1.解释一些化学现象。
质量守恒定律的应用2.利用反应前后元素守恒确定物质组成元素。3.利用反应前后原子的种类和数目守恒推断
物质的化学式或化学计量数。4.根据质量守恒定律进行各物质质量的计算。(1)成语“点石成金”,本意为古代术士的
一种法术,即能使石头变成黄金;现比喻
能化腐朽为神奇。有人说他能把石灰石变
成黄金,请你用化学知识说明石灰石不能
变成黄金的道理。
1.解释化学现象:(2) 生物的呼吸作用表示为: 有机物 + 氧气→二氧化碳 + 水 + 能量。以下关于有机物组成元素推断正确的是( )
A.只含碳元素
B.只含碳元素和氢元素
C.一定含碳、氢和氧元素
D.一定含有碳元素和氢元素,可能含有氧元素
(3)将4.6克某化合物放入氧气中完全燃烧,生成8.8克二氧化碳和5.4克水.问:这种化合物有哪几种元素组成?2.确定物质的元素组成:(4)一氧化氮是大气的主要污染物之一。近几年来又发现生物体内存在少量一氧化氮,它有扩张血管、增强记忆的功能,成为当前生命科学的热点。工业上制得一氧化氮的化学式为:4X + 5O2 =4NO + 6H2O ,则X的化学式为( ) A.N2 B.NO2 C.NH3 D.N2O5
(5)下图是某化学反应的微观模拟图,根据图示判断
参加反应的 和 与反应后生成的 个数
比为 。
3.确定化学式及化学计量数:(6)在化学反应A+2B = 2C+D中,6gA和8gB 恰好完全反应,生成9gD。若反应生成15gC,则参加反应的A的质量为( ) A.18g B.24g C.12g D.16g
(7)一密闭容器中,盛放A.B.C三种物质各30g,经电火花引燃,充分反应后,各物质质量变化如下:
关于此反应,下列不正确的是:( ) A. C物质中所含元素种类是ABD中所有元素种类之和B. 变化后待测的A为5g C. 该变化是分解反应 D. A物质有可能是单质4.简单计算:魔术——冰块燃烧 拿一块冰,放上一小块石头,用火柴在靠近小石头的地方点燃,很快就形成了一团烈火,冰块和石头一起燃烧起来,你想知道为什么吗?其实,那块小石头不是普通的石头,它叫电石,化学名称叫碳化钙(CaC2) ,电石遇水发生剧烈的化学反应,生成氢氧化钙Ca(OH)2和乙炔(C2H2) ,乙炔是一种可燃性气体。请写出有关反应的化学方程式。二、化学方程式2.以客观事实为依据二、化学方程式表示意义赛一赛,看谁最厉害 甲、乙是常见的单质,A、B是常见的化合物,它们的反应:甲+A B+乙(式中各物质的化学计量数和反应条件已略去)。请回答:
(1)反应类型是 。
(2)若甲为金属,且乙的硫酸盐溶液为蓝
色,写出反应的化学方程式 。
(3)若乙为非金属单质,B中含有+3价金属
元素,写出反应的化学方程式 。我思我获通过本堂课学习,收获如何?
让我们一起回顾一遍!表示意义 如图所示是测定蜡烛燃烧时的质量变化装置,天平是物理天平,左托盘上蜡烛的上方罩着吸收器。如果实验时,蜡烛正常燃烧,生成的气体顺利通过吸收器,吸收器的药品只在3min内起吸收作用。
试回答:
(1)本实验中,蜡烛燃烧时,反应物
是 ,生成物是 ,
反应条件是 。
(2)3min内天平是否保持平衡? ,
原因是
(3)3min后会出现什么结果? ,原因是
。
是否符合质量守恒定律? 。蜡烛和氧气二氧化碳和水点燃不平衡生成物中增加了氧元素,并且被吸收器吸收,左盘内物质质量增加天平右盘向下倾斜 3min后吸收器的药物不能再吸收生成物,二氧化碳和水蒸气逸散符合反思
1、命题的用意何在?(所考查的知识点)
2、解题中用了什么方法,有什么规律性东西?
3、所用的是不是最佳方法?有无创 新之处?
4、在解答过程中,自己的思路是否简捷?并与
老师和同学所运用的思维形式、思维规律和
思维方法相比较,及时归纳学习思考问题
“点金术”。
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
