co2的实验室制法
图片预览





文档简介
课件15张PPT。
CO2的实验室制法 枣庄东方国际学校复习提问1.回忆二氧化碳的化学性质,写出相应的化学方程式。
2.写出已经学过的可以得到二氧化碳气体的化学方程式。
3、实验室制取氧气的两种方法的反应原理是什么?如何
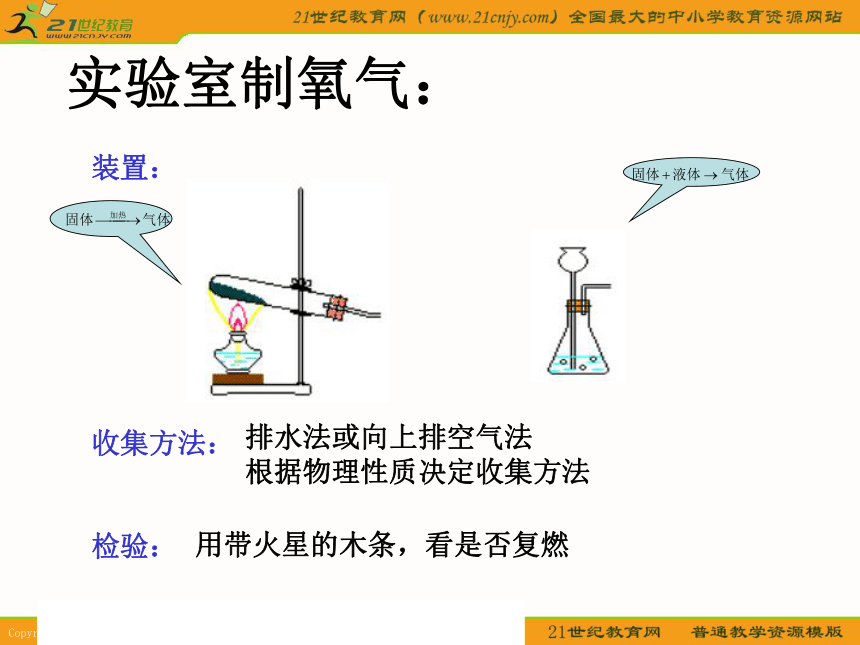
选择装置?怎样收集氧气?怎样检验氧气?思考:在实验室里制取二氧化碳能否利用这些反应呢? 反应原理:实验室里制气体,不能只考虑一个反应能否生成要制的气体,还要考虑其他因素,如反应条件、仪器装置在实验室是否易于实现等。 实验室制氧气:装置:
收集方法:
检验:排水法或向上排空气法
根据物理性质决定收集方法用带火星的木条,看是否复燃在实验室里制取气体要考虑哪些问题? 反应原理
装置的选择
收集方法
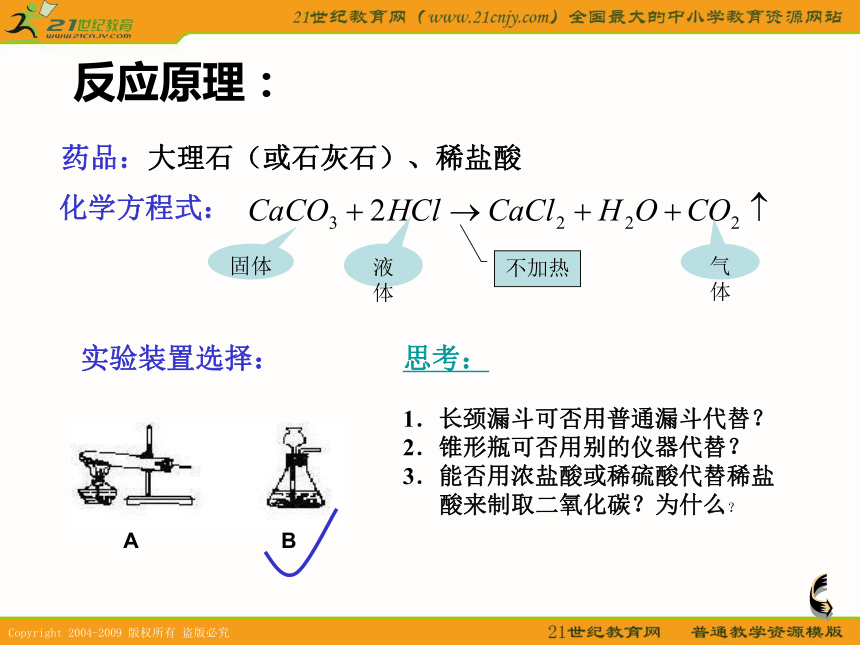
检验方法等CO2的实验室制法 反应原理:药品:大理石(或石灰石)、稀盐酸化学方程式:思考:
1.长颈漏斗可否用普通漏斗代替? 2.锥形瓶可否用别的仪器代替? 3.能否用浓盐酸或稀硫酸代替稀盐
酸来制取二氧化碳?为什么?实验装置:1、不能用普通漏斗代替长颈漏斗,因为普通漏斗颈太短,产生的二氧化碳气体会从漏斗处逸出。长颈漏斗下端管口必须在液面以下才能达到密封的效果。 B2、锥形瓶可以用大试管、广口瓶等玻璃仪器代替。3、浓盐酸具有较强的挥发性,使得收集到的二氧化碳气体中含有氯化
氢气体而不纯,故不能用浓盐酸代替稀盐酸。 补充实验:现象:有气泡产生,但很快停止原因:稀硫酸和碳酸钙发生如下反应:
CaCO3+H2SO4=CaSO4+H2O+CO2↑ 生成的硫酸钙微溶于水,未能溶解的硫酸钙覆盖在碳酸
钙表面,使得反应不能很好进行甚至中止,故不能用稀
硫酸代替稀盐酸。 收集方法:CO2检验方法:验满方法:把CO2通入澄
清石灰水,看
是否变浑浊将燃着的木条放在集气瓶口,如火焰熄灭,则二氧化碳已收满。 实验步骤:1、检验装置的气密性?2、装药品(怎么往锥形瓶中
放大理石? )3、连接装置(顺序?)4、开始反应(加到锥形瓶里的液
体的位置?为什么?)5、收集、检验、验满用块状大理石和粉末状固体碳酸钙分别与
稀盐酸反应,观察实验现象。比较实验:反应物的状态不同对化学反应有什么影响?现象:B中产生气体的速度明显比A快。结论:反应物的状态影响化学反应的速度,粉末
状比块状物质接触面大,微粒间的碰撞几
率增加,所以反应速度快,有时不能方便
的收集气体。1.了解实验室制取气体所需药品及相应的化学反应方程式;
2.根据反应物、生成物的状态及反应条件选择合适的反应装置;
3.根据气体的物理性质(尤其是密度及其在水中的溶解性),选择合适的收集方法及验满方法。 明确实验室制取气体的顺序是:启普发生器:荷兰化学家启普设计的气体发生器使用方法(启普发生器制取氢气)装有固体的部位就是气体发生
的地方,气体在这里导出,液
体在这个部位可进可退。 打开活塞,容器内压强减小,液体从球
形漏斗流入仪器的中间部分与固体接触,放
出氢气;关闭活塞,容器压强增大,使液体
与固体脱离接触,停止制气。工作原理:适用范围:优点:1、可制取大量的气体;
2、可控制反应随时发生、随时停止。根据启普发生器的原理设计几种简易的制取气体装置启普发生器:设计探究实验:问题:在实验室如何制取氢气?资料: 十六世纪末,瑞土化学家巴拉采尔斯把铁放在硫酸中,铁片顿时和硫酸发生激烈的化学反应,放出许多气泡——氢气。现在如果制取少量的氢气,用的金属锌和稀硫酸反应。氢气是无色无味且最轻的气体。 1780年,法国化学家布拉克便把氢气灌入猪的膀胱中,制得了世界上第一个、也是最原始的氢气球,它冉冉地飞向高空。现在,人们就是往橡胶薄膜中灌入氢气,大量制造氢气球。节日里放的彩色气球,便灌着氢气。在气象台,人们差不多每天都要放几个气球,探测高空的风云。氢在空气或氧气中能燃烧,发出淡蓝色的火焰并生成水,因此,它的希腊文原意,便是“水的生成者”。 反应原理
装置的选择
收集方法
检验方法猜测:
步骤:实验室用金属锌和稀硫酸反应制取氢气,
采用排水法或向下排空气法收集,并用
点燃的方法来检验是否是氢气。实验室制取氢气:
3、实验室制取氧气的两种方法的反应原理是什么?如何
选择装置?怎样收集氧气?怎样检验氧气?思考:在实验室里制取二氧化碳能否利用这些反应呢? 反应原理:实验室里制气体,不能只考虑一个反应能否生成要制的气体,还要考虑其他因素,如反应条件、仪器装置在实验室是否易于实现等。 实验室制氧气:装置:
收集方法:
检验:排水法或向上排空气法
根据物理性质决定收集方法用带火星的木条,看是否复燃在实验室里制取气体要考虑哪些问题? 反应原理
装置的选择
收集方法
检验方法等CO2的实验室制法 反应原理:药品:大理石(或石灰石)、稀盐酸化学方程式:思考:
1.长颈漏斗可否用普通漏斗代替? 2.锥形瓶可否用别的仪器代替? 3.能否用浓盐酸或稀硫酸代替稀盐
酸来制取二氧化碳?为什么?实验装置:1、不能用普通漏斗代替长颈漏斗,因为普通漏斗颈太短,产生的二氧化碳气体会从漏斗处逸出。长颈漏斗下端管口必须在液面以下才能达到密封的效果。 B2、锥形瓶可以用大试管、广口瓶等玻璃仪器代替。3、浓盐酸具有较强的挥发性,使得收集到的二氧化碳气体中含有氯化
氢气体而不纯,故不能用浓盐酸代替稀盐酸。 补充实验:现象:有气泡产生,但很快停止原因:稀硫酸和碳酸钙发生如下反应:
CaCO3+H2SO4=CaSO4+H2O+CO2↑ 生成的硫酸钙微溶于水,未能溶解的硫酸钙覆盖在碳酸
钙表面,使得反应不能很好进行甚至中止,故不能用稀
硫酸代替稀盐酸。 收集方法:CO2检验方法:验满方法:把CO2通入澄
清石灰水,看
是否变浑浊将燃着的木条放在集气瓶口,如火焰熄灭,则二氧化碳已收满。 实验步骤:1、检验装置的气密性?2、装药品(怎么往锥形瓶中
放大理石? )3、连接装置(顺序?)4、开始反应(加到锥形瓶里的液
体的位置?为什么?)5、收集、检验、验满用块状大理石和粉末状固体碳酸钙分别与
稀盐酸反应,观察实验现象。比较实验:反应物的状态不同对化学反应有什么影响?现象:B中产生气体的速度明显比A快。结论:反应物的状态影响化学反应的速度,粉末
状比块状物质接触面大,微粒间的碰撞几
率增加,所以反应速度快,有时不能方便
的收集气体。1.了解实验室制取气体所需药品及相应的化学反应方程式;
2.根据反应物、生成物的状态及反应条件选择合适的反应装置;
3.根据气体的物理性质(尤其是密度及其在水中的溶解性),选择合适的收集方法及验满方法。 明确实验室制取气体的顺序是:启普发生器:荷兰化学家启普设计的气体发生器使用方法(启普发生器制取氢气)装有固体的部位就是气体发生
的地方,气体在这里导出,液
体在这个部位可进可退。 打开活塞,容器内压强减小,液体从球
形漏斗流入仪器的中间部分与固体接触,放
出氢气;关闭活塞,容器压强增大,使液体
与固体脱离接触,停止制气。工作原理:适用范围:优点:1、可制取大量的气体;
2、可控制反应随时发生、随时停止。根据启普发生器的原理设计几种简易的制取气体装置启普发生器:设计探究实验:问题:在实验室如何制取氢气?资料: 十六世纪末,瑞土化学家巴拉采尔斯把铁放在硫酸中,铁片顿时和硫酸发生激烈的化学反应,放出许多气泡——氢气。现在如果制取少量的氢气,用的金属锌和稀硫酸反应。氢气是无色无味且最轻的气体。 1780年,法国化学家布拉克便把氢气灌入猪的膀胱中,制得了世界上第一个、也是最原始的氢气球,它冉冉地飞向高空。现在,人们就是往橡胶薄膜中灌入氢气,大量制造氢气球。节日里放的彩色气球,便灌着氢气。在气象台,人们差不多每天都要放几个气球,探测高空的风云。氢在空气或氧气中能燃烧,发出淡蓝色的火焰并生成水,因此,它的希腊文原意,便是“水的生成者”。 反应原理
装置的选择
收集方法
检验方法猜测:
步骤:实验室用金属锌和稀硫酸反应制取氢气,
采用排水法或向下排空气法收集,并用
点燃的方法来检验是否是氢气。实验室制取氢气:
同课章节目录
- 第一单元 步入化学殿堂
- 第一节 化学真奇妙
- 第二节 体验化学探究
- 到实验室去:化学实验基本技能训练(一)
- 第二单元 探秘水世界
- 第一节 运动的水分子
- 第二节 自然界中的水
- 第三节 水分子的变化
- 到实验室去:化学实验基本技能训练(二)
- 第三单元 物质构成的奥秘
- 第一节 原子的构成
- 第二节 元素
- 第三节 物质组成的表示
- 第四单元 我们周围的空气
- 第一节 空气的成分
- 第二节 氧气
- 到实验室去:氧气的实验室制取与性质
- 第五单元 定量研究化学反应
- 第一节 化学反应中的质量守恒
- 第二节 化学反应的表示
- 第三节 化学反应中的有关计算
- 到实验室去:探究燃烧的条件
- 第六单元 燃烧与燃料
- 第一节 燃烧与灭火
- 第二节 化石燃料的利用
- 第三节 大自然中的二氧化碳
- 到实验室去 二氧化碳的实验室制取与性质
