2008年暑期培训材料之九 必修2内容分析与教学建议
文档属性
| 名称 | 2008年暑期培训材料之九 必修2内容分析与教学建议 |

|
|
| 格式 | rar | ||
| 文件大小 | 4.7MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2010-02-26 00:00:00 | ||
图片预览




文档简介
课件44张PPT。《化学2》
教材内容分析与教学建议
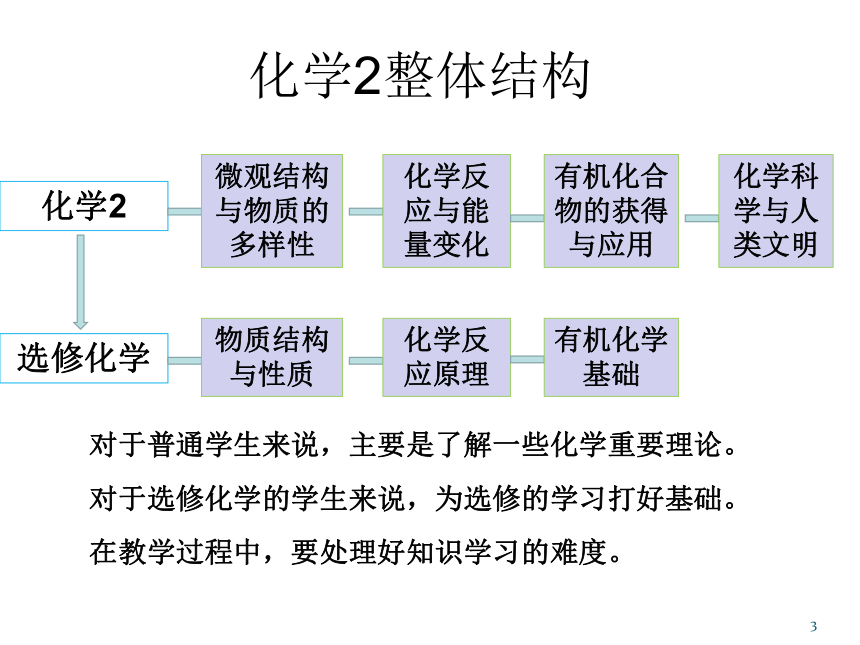
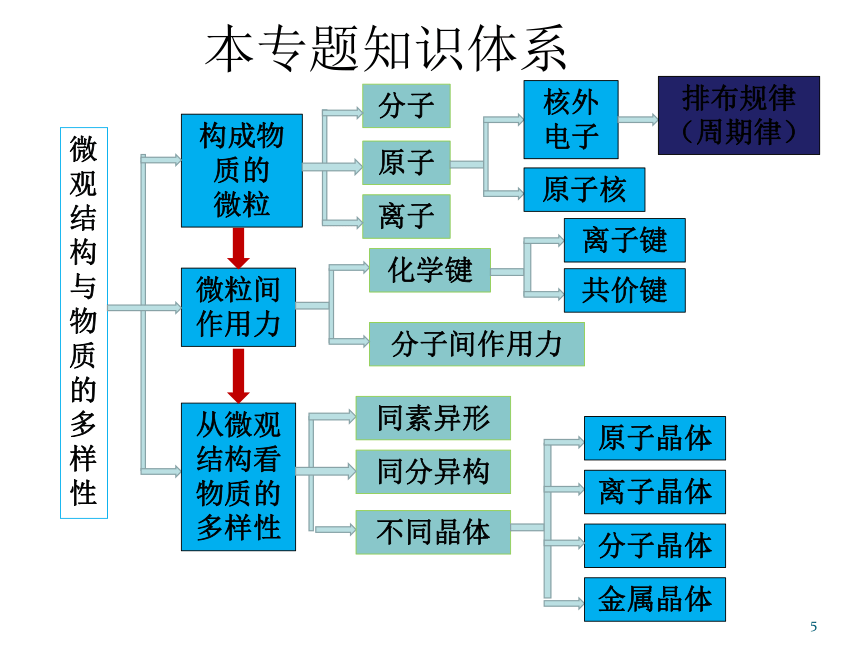
1化学2整体结构1化学2选修化学微观结构与物质的多样性化学反应与能量变化有机化合物的获得与应用化学科学与人类文明物质结构与性质化学反应原理有机化学基础对于普通学生来说,主要是了解一些化学重要理论。对于选修化学的学生来说,为选修的学习打好基础。在教学过程中,要处理好知识学习的难度。专题1 微观结构与物质的多样性1本专题知识体系1微观结构与物质的多样性构成物质的
微粒分子从微观结构看物质的多样性离子原子分子间作用力同素异形微粒间
作用力化学键同分异构原子核核外电子排布规律
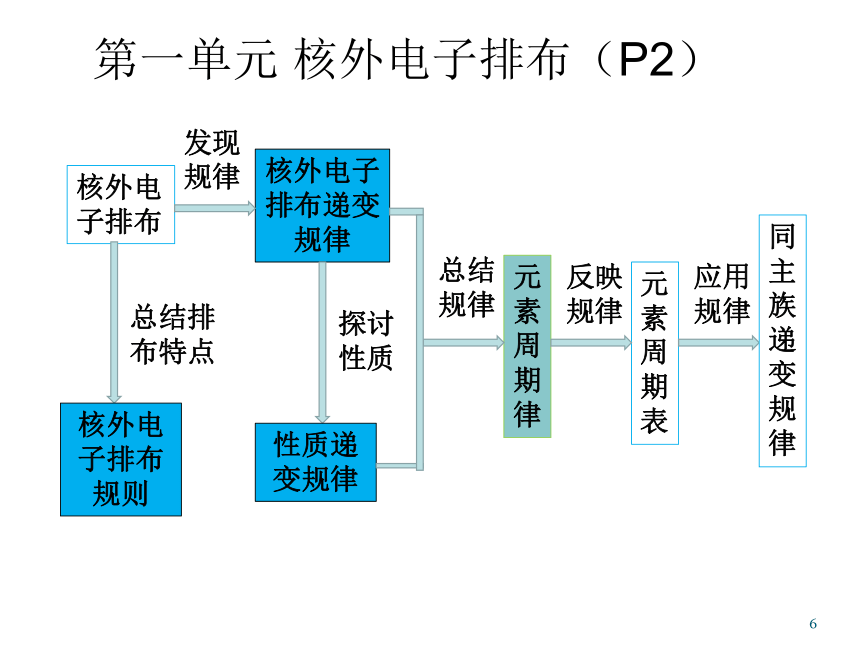
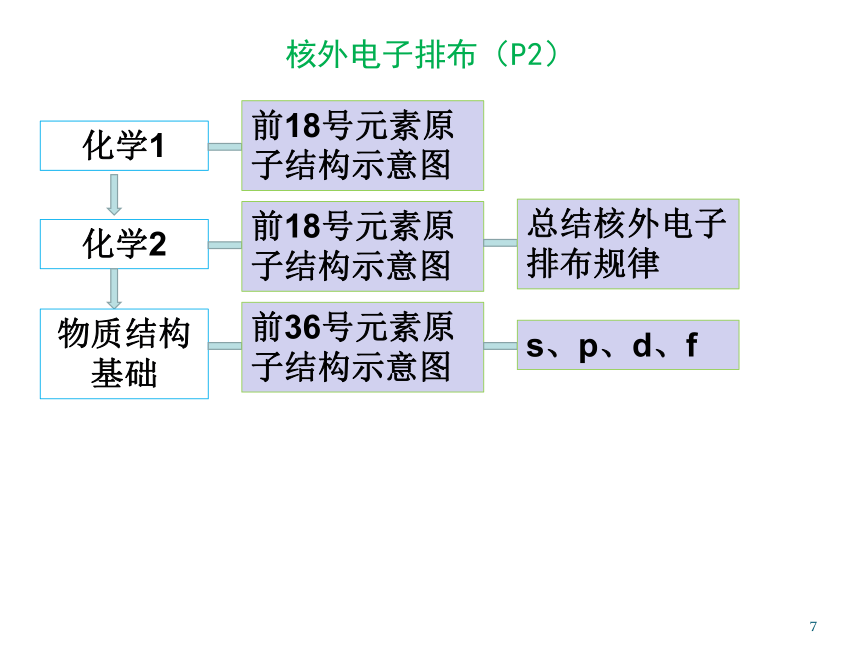
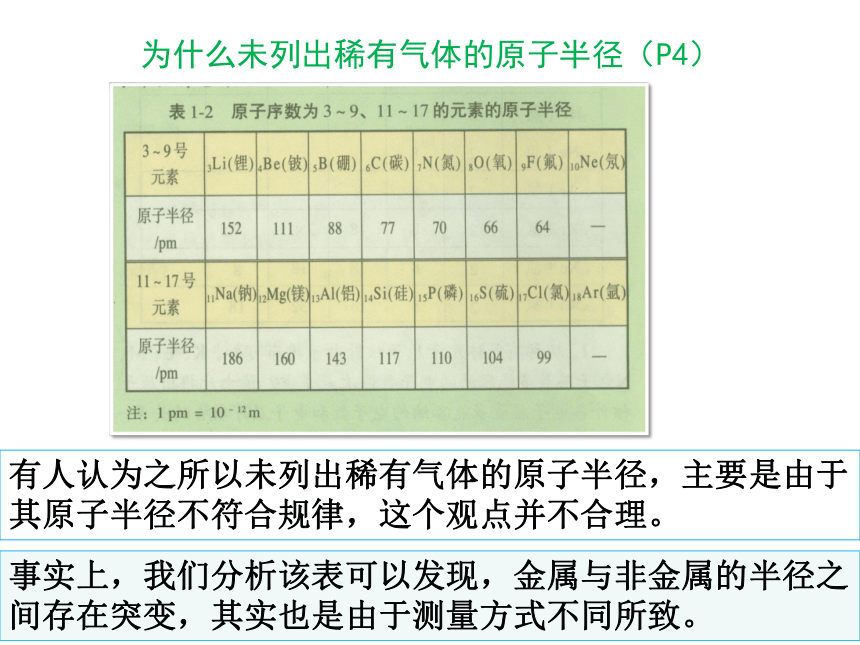
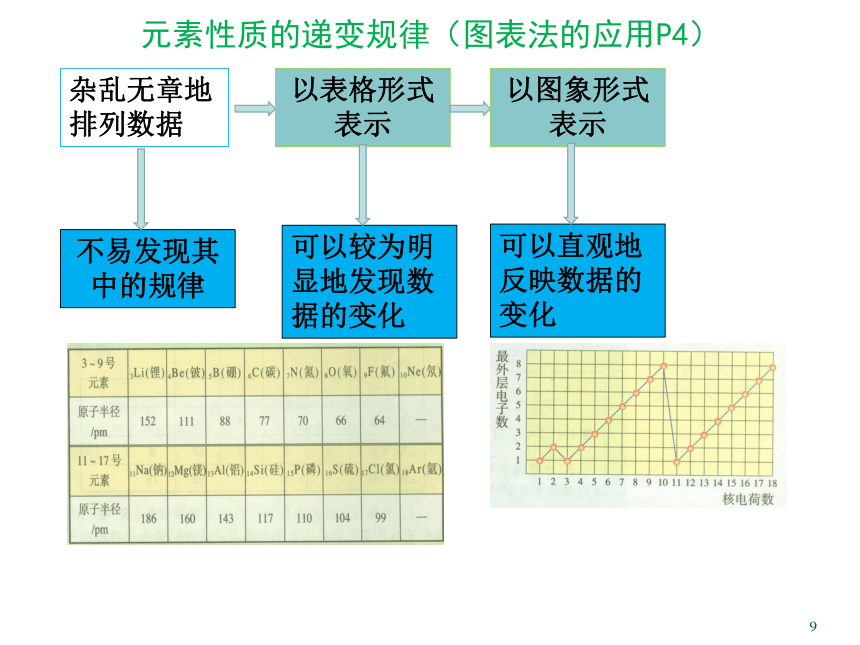
(周期律)离子键共价键不同晶体原子晶体分子晶体离子晶体金属晶体第一单元 核外电子排布(P2)1核外电子排布核外电子排布递变规律元素周期律发现规律总结规律元素周期表核外电子排布规则总结排布特点探讨性质性质递变规律反映规律应用规律同主族递变规律核外电子排布(P2)1化学1化学2物质结构基础前18号元素原子结构示意图前18号元素原子结构示意图前36号元素原子结构示意图总结核外电子排布规律s、p、d、f为什么未列出稀有气体的原子半径(P4)1有人认为之所以未列出稀有气体的原子半径,主要是由于其原子半径不符合规律,这个观点并不合理。事实上,我们分析该表可以发现,金属与非金属的半径之间存在突变,其实也是由于测量方式不同所致。元素性质的递变规律(图表法的应用P4)1杂乱无章地排列数据不易发现其中的规律以表格形式表示可以较为明显地发现数据的变化以图象形式表示可以直观地反映数据的变化金属性与金属活动性(P5)金属性的强弱通常用金属元素气态原子失去电子成为气态阳离子时所需要的能量大小来衡量。
金属的活动性反映金属在水溶液里起氧化反应的难易,它是以金属的标准电极电势为依据的。金属的标准电极电势除了与金属元素原子的电离能有关外,还与金属的升华能、水合能等多种因素有关。
金属性强的元素,一般来说它的活动性也大,但也有不一致的情况。例如,钠的第一电离能比钙的第一电离能要小,因此钠的金属性要比钙强。但是钙在水溶液中形成水合离子的倾向比钠大,即钙的标准电极电势比钠要负,所以钙的金属活动性比钠大。
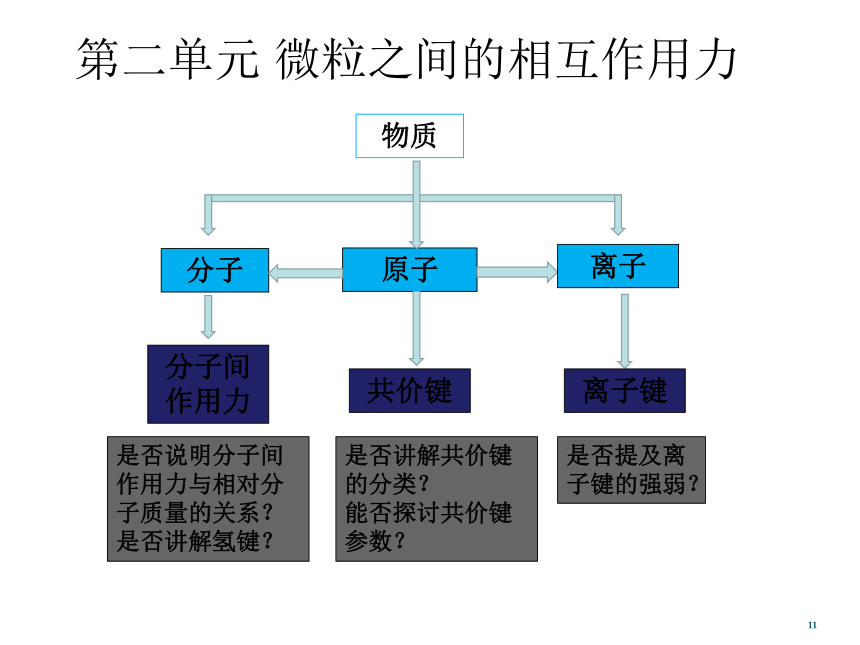
1在教学过程中不必加以区分,但应避免呈现例外情况。第二单元 微粒之间的相互作用力1分子原子分子间作用力离子共价键离子键物质是否说明分子间作用力与相对分子质量的关系?
是否讲解氢键?是否讲解共价键的分类?
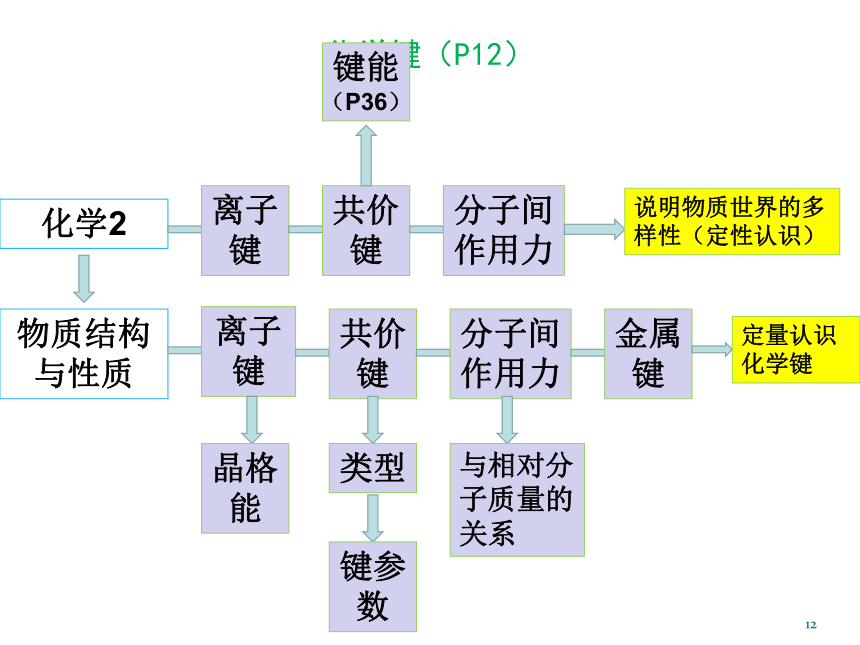
能否探讨共价键参数?是否提及离子键的强弱?化学键(P12)1化学2物质结构与性质离子键离子键共价键分子间作用力说明物质世界的多样性(定性认识)共价键分子间作用力晶格能类型键参数与相对分子质量的关系金属键定量认识化学键键能
(P36)碳原子成键方式多样性与同分异构体(P14)1碳原子
构成物质单键链状从成键
方式角度双键叁键从转接
方式角度环状说明物质的多样性为同分异构打基础第三单元 从微观结构看物质的多样性1从微观结构看物质的多样性同素异形同分异构不同晶体原子晶体分子晶体离子晶体金属晶体结构模型(P18)1金刚石、石墨的性质为什么存在很大差异你知道吗呈现金刚石、石墨、碳纳米管等的结构模型目的:说明结构与性质关系密切呈现图片教学要求:金刚石与石墨之所以性质不同,是因为结构不同所致;金刚石熔点高是因为要破坏共价键,而石墨润滑是破坏分子间作用力。不宜要求学生记忆金刚石与石墨的结构特征。同分异构现象(同分异构现象)1同:分子式学生制作:含有4个碳原子的只含有碳碳单键和碳氢键的物质的结构分析两种结构的相似之处与差异之处同分异构体的概念异:结构同分异构体的判断本部分最大的教学难点在于例证的不足,因为学生尚未系统地学习有机知识,当然也就无法有效地书写同分异构体。故在此部分主要进行判断,书写可以安排在学习有机物时进行。不同类型的晶体(P23)1性质晶体类型结构不同类晶体的物理性质比较化学2物质结构与性质同类别晶体物理性质的比较专题2 化学反应与能量转化1本专题知识体系1化学反应与能量转化化学反应速率表示方法化学反应中的能量简单计算影响因素化学反应中的热量化学反应限度可逆反应化学能与电能转化催化剂浓度化学平衡能源原电池电解池温度特征化学反应速率(P30)1镁、铁与盐酸反应浓度化学反应速率化学反应有快有慢如何表示影响因素温度催化剂(1)可否讲解压强对反应速率的影响?
(2)是否应用碰撞理论进行解释?
(3)P31图2-1设置的目的是什么?化学反应的限度(P32)1化学反应中的热量(P34)1原电池(P40)1以铜锌等简单原电池(锌-硫酸铜)为例,了解原电池的结构特征,理解放电原理,书写简单的电极反应式,并初步了解化学电源与钢铁的电化学腐蚀。电解(P44)1化学1专题2专题4电解熔融氯化钠、氯化镁、氧化铝、电解饱和食盐水电解氯化铜溶液、电解精炼铜(拓展视野)电解熔融氯化钠与电解氯化钠水溶液(资料卡)初中电解水反应原理电解熔融氯化钠、氯化铜溶液、饱和食盐水及电镀太阳能、生物质能和氢能的利用(P47)1太阳能热能热能生物质能光合作用供给人体直接燃烧生物化学转换化学能直接应用热能、电能、化学能光解水氢能来源问题贮存问题专题3 有机化合物的获得与应用1本专题知识体系1有机化合物化石燃料与有机化合物乙烯甲烷苯食品中的有机化合物乙醇糖类
人工合成的有机化合物油脂乙酸蛋白质乙炔烃卤代烃苯酚酯烃的衍生物醛甲烷(P59)1甲烷结构结构式空间构型物质结构与性质有机化学基础物理性质化学性质燃烧反应取代反应实验室制法无乙烯(P61)1主要变化:以石油为原料制取乙烯(工业制法)代替以乙醇为原料(实验室制法,位于《有机化学基础》乙醇脱水实验中)。石油烃类分馏乙烯等小分子烃裂化裂解学生已有基础:蒸馏的基本操作。教学注意点:关于分馏,同学一般仍然认为是逐步升温,然后不同的物质从不同的出口流出。实际上,此过程是在直接在较高温度下(超过350)进行,然后逐步降温,不同沸点的在不同的位置冷凝。乙炔(P64)1(1)为什么将乙炔置于问题解决中?很难纳入正文知识体系中;有利于学生迁移能力及问题解决能力的培养。(2)在教学过程中如何处理?最简单处理:解答“问题解决”。
探究性处理:学生依据结构提出假设,进行实验验证假设,并得出相应结论。
不适宜处理:补充乙炔的实验室制法。苯(P66)1乙醇1化学2与钠反应有机化学基础与氧反应酯化反应与钠反应与卤化氢反应脱水反应酯化反应酸(P71)1特点1:关注乙酸的酸性,体现已有基础的应用作用。学生设计实验:如何验证醋酸属于酸;如何比较醋酸与硫酸、碳酸的酸性强弱。特点2:强化乙醇与乙酸的反应机理(用明显的色彩表示出化学键的变化)。 在选择有关某物质的知识时,强调知识的有用性,强调对学生生活的指导。在教学过程中应关注指导学生生活,关注以知识为载体发展学生能力,而不必强调知识的完整性油脂、糖类、蛋白质的体系编排特点1活动与探究(P75)1第1个实验主要目的是了解糖类的物理性质。第2、3个实验主要是说明葡萄糖的重要特征反应—银镜反应和菲林反应,可以解释是由于其中含有醛基所致,并说明这是醛基的主要性质,但不宜出现反应的化学方程式,也不宜出现葡萄糖的结构。(这些内容在《有机化学基础》中呈现)第4个实验可以设计成探究形式,由学生设计实验方案证明淀粉是否已经发生水解,或是否水解完全。简单有机物的合成(80)1以乙酸乙酯的合成为主要载体,学习化学合成设计的一般方法,并将本章知识网络化。乙烯是一种重要的化工原料,请以乙烯为原料合成乙酸乙酯。(已知乙醛能与氧气反应生成乙酸)合成高分子(P84)1(1)以加聚反应为重点,简单提及缩聚反应,不要求掌握酚醛树脂的合成。(2)可先呈现聚乙烯、聚氯乙烯及聚苯乙烯的结构,引导学生分析其结构单元(链节),并由此推测其单体(不要出现名称)。再分析这些反应的共同点,得出加聚反应的概念。(3)可以比较聚乙烯和聚氯乙烯的特点,分析哪个可用作食品袋,并思考超市不再无偿提供食品袋是否合理,体现对社会问题 关注。专题4 化学科学与人类文明1本专题知识体系1化学科学与人类文明认识物质世界创造新物质物质的制备物质的分离促进科技发展改进新技术催生新技术解决环境问题治理环境污染绿色化学整体特点1(1)进一步认识化学学科在社会可持续发展中的作用,激发学生深入学习化学的兴趣。(2)引导学生在问题解决的过程中复习巩固化学学科的基础知识。(3)帮助学生了解后续各选修化学课程的主要内容,为学生作出选择提供指导。(1)复习常见金属的冶炼方法。(2)了解常见金属的化学性质。(3)能应用氧化还原原理进行分析。1人类对酸碱的认识(P93)1根据味道石蕊试液反应特征电离理论质子理论电子理论经验总结科学概括科学本质学生生活波义耳的著名实验阿伦尼乌斯电离理论阿斯匹林(P97)水杨酸乙酰水杨酸钠缓释阿斯匹林酯化反应乙酰水杨酸中和反应水解反应水解反应酯化反应水解反应谢谢联系电话:021-62232049
手机:13564362935
电子邮箱:zxyecnu@126.com1
教材内容分析与教学建议
1化学2整体结构1化学2选修化学微观结构与物质的多样性化学反应与能量变化有机化合物的获得与应用化学科学与人类文明物质结构与性质化学反应原理有机化学基础对于普通学生来说,主要是了解一些化学重要理论。对于选修化学的学生来说,为选修的学习打好基础。在教学过程中,要处理好知识学习的难度。专题1 微观结构与物质的多样性1本专题知识体系1微观结构与物质的多样性构成物质的
微粒分子从微观结构看物质的多样性离子原子分子间作用力同素异形微粒间
作用力化学键同分异构原子核核外电子排布规律
(周期律)离子键共价键不同晶体原子晶体分子晶体离子晶体金属晶体第一单元 核外电子排布(P2)1核外电子排布核外电子排布递变规律元素周期律发现规律总结规律元素周期表核外电子排布规则总结排布特点探讨性质性质递变规律反映规律应用规律同主族递变规律核外电子排布(P2)1化学1化学2物质结构基础前18号元素原子结构示意图前18号元素原子结构示意图前36号元素原子结构示意图总结核外电子排布规律s、p、d、f为什么未列出稀有气体的原子半径(P4)1有人认为之所以未列出稀有气体的原子半径,主要是由于其原子半径不符合规律,这个观点并不合理。事实上,我们分析该表可以发现,金属与非金属的半径之间存在突变,其实也是由于测量方式不同所致。元素性质的递变规律(图表法的应用P4)1杂乱无章地排列数据不易发现其中的规律以表格形式表示可以较为明显地发现数据的变化以图象形式表示可以直观地反映数据的变化金属性与金属活动性(P5)金属性的强弱通常用金属元素气态原子失去电子成为气态阳离子时所需要的能量大小来衡量。
金属的活动性反映金属在水溶液里起氧化反应的难易,它是以金属的标准电极电势为依据的。金属的标准电极电势除了与金属元素原子的电离能有关外,还与金属的升华能、水合能等多种因素有关。
金属性强的元素,一般来说它的活动性也大,但也有不一致的情况。例如,钠的第一电离能比钙的第一电离能要小,因此钠的金属性要比钙强。但是钙在水溶液中形成水合离子的倾向比钠大,即钙的标准电极电势比钠要负,所以钙的金属活动性比钠大。
1在教学过程中不必加以区分,但应避免呈现例外情况。第二单元 微粒之间的相互作用力1分子原子分子间作用力离子共价键离子键物质是否说明分子间作用力与相对分子质量的关系?
是否讲解氢键?是否讲解共价键的分类?
能否探讨共价键参数?是否提及离子键的强弱?化学键(P12)1化学2物质结构与性质离子键离子键共价键分子间作用力说明物质世界的多样性(定性认识)共价键分子间作用力晶格能类型键参数与相对分子质量的关系金属键定量认识化学键键能
(P36)碳原子成键方式多样性与同分异构体(P14)1碳原子
构成物质单键链状从成键
方式角度双键叁键从转接
方式角度环状说明物质的多样性为同分异构打基础第三单元 从微观结构看物质的多样性1从微观结构看物质的多样性同素异形同分异构不同晶体原子晶体分子晶体离子晶体金属晶体结构模型(P18)1金刚石、石墨的性质为什么存在很大差异你知道吗呈现金刚石、石墨、碳纳米管等的结构模型目的:说明结构与性质关系密切呈现图片教学要求:金刚石与石墨之所以性质不同,是因为结构不同所致;金刚石熔点高是因为要破坏共价键,而石墨润滑是破坏分子间作用力。不宜要求学生记忆金刚石与石墨的结构特征。同分异构现象(同分异构现象)1同:分子式学生制作:含有4个碳原子的只含有碳碳单键和碳氢键的物质的结构分析两种结构的相似之处与差异之处同分异构体的概念异:结构同分异构体的判断本部分最大的教学难点在于例证的不足,因为学生尚未系统地学习有机知识,当然也就无法有效地书写同分异构体。故在此部分主要进行判断,书写可以安排在学习有机物时进行。不同类型的晶体(P23)1性质晶体类型结构不同类晶体的物理性质比较化学2物质结构与性质同类别晶体物理性质的比较专题2 化学反应与能量转化1本专题知识体系1化学反应与能量转化化学反应速率表示方法化学反应中的能量简单计算影响因素化学反应中的热量化学反应限度可逆反应化学能与电能转化催化剂浓度化学平衡能源原电池电解池温度特征化学反应速率(P30)1镁、铁与盐酸反应浓度化学反应速率化学反应有快有慢如何表示影响因素温度催化剂(1)可否讲解压强对反应速率的影响?
(2)是否应用碰撞理论进行解释?
(3)P31图2-1设置的目的是什么?化学反应的限度(P32)1化学反应中的热量(P34)1原电池(P40)1以铜锌等简单原电池(锌-硫酸铜)为例,了解原电池的结构特征,理解放电原理,书写简单的电极反应式,并初步了解化学电源与钢铁的电化学腐蚀。电解(P44)1化学1专题2专题4电解熔融氯化钠、氯化镁、氧化铝、电解饱和食盐水电解氯化铜溶液、电解精炼铜(拓展视野)电解熔融氯化钠与电解氯化钠水溶液(资料卡)初中电解水反应原理电解熔融氯化钠、氯化铜溶液、饱和食盐水及电镀太阳能、生物质能和氢能的利用(P47)1太阳能热能热能生物质能光合作用供给人体直接燃烧生物化学转换化学能直接应用热能、电能、化学能光解水氢能来源问题贮存问题专题3 有机化合物的获得与应用1本专题知识体系1有机化合物化石燃料与有机化合物乙烯甲烷苯食品中的有机化合物乙醇糖类
人工合成的有机化合物油脂乙酸蛋白质乙炔烃卤代烃苯酚酯烃的衍生物醛甲烷(P59)1甲烷结构结构式空间构型物质结构与性质有机化学基础物理性质化学性质燃烧反应取代反应实验室制法无乙烯(P61)1主要变化:以石油为原料制取乙烯(工业制法)代替以乙醇为原料(实验室制法,位于《有机化学基础》乙醇脱水实验中)。石油烃类分馏乙烯等小分子烃裂化裂解学生已有基础:蒸馏的基本操作。教学注意点:关于分馏,同学一般仍然认为是逐步升温,然后不同的物质从不同的出口流出。实际上,此过程是在直接在较高温度下(超过350)进行,然后逐步降温,不同沸点的在不同的位置冷凝。乙炔(P64)1(1)为什么将乙炔置于问题解决中?很难纳入正文知识体系中;有利于学生迁移能力及问题解决能力的培养。(2)在教学过程中如何处理?最简单处理:解答“问题解决”。
探究性处理:学生依据结构提出假设,进行实验验证假设,并得出相应结论。
不适宜处理:补充乙炔的实验室制法。苯(P66)1乙醇1化学2与钠反应有机化学基础与氧反应酯化反应与钠反应与卤化氢反应脱水反应酯化反应酸(P71)1特点1:关注乙酸的酸性,体现已有基础的应用作用。学生设计实验:如何验证醋酸属于酸;如何比较醋酸与硫酸、碳酸的酸性强弱。特点2:强化乙醇与乙酸的反应机理(用明显的色彩表示出化学键的变化)。 在选择有关某物质的知识时,强调知识的有用性,强调对学生生活的指导。在教学过程中应关注指导学生生活,关注以知识为载体发展学生能力,而不必强调知识的完整性油脂、糖类、蛋白质的体系编排特点1活动与探究(P75)1第1个实验主要目的是了解糖类的物理性质。第2、3个实验主要是说明葡萄糖的重要特征反应—银镜反应和菲林反应,可以解释是由于其中含有醛基所致,并说明这是醛基的主要性质,但不宜出现反应的化学方程式,也不宜出现葡萄糖的结构。(这些内容在《有机化学基础》中呈现)第4个实验可以设计成探究形式,由学生设计实验方案证明淀粉是否已经发生水解,或是否水解完全。简单有机物的合成(80)1以乙酸乙酯的合成为主要载体,学习化学合成设计的一般方法,并将本章知识网络化。乙烯是一种重要的化工原料,请以乙烯为原料合成乙酸乙酯。(已知乙醛能与氧气反应生成乙酸)合成高分子(P84)1(1)以加聚反应为重点,简单提及缩聚反应,不要求掌握酚醛树脂的合成。(2)可先呈现聚乙烯、聚氯乙烯及聚苯乙烯的结构,引导学生分析其结构单元(链节),并由此推测其单体(不要出现名称)。再分析这些反应的共同点,得出加聚反应的概念。(3)可以比较聚乙烯和聚氯乙烯的特点,分析哪个可用作食品袋,并思考超市不再无偿提供食品袋是否合理,体现对社会问题 关注。专题4 化学科学与人类文明1本专题知识体系1化学科学与人类文明认识物质世界创造新物质物质的制备物质的分离促进科技发展改进新技术催生新技术解决环境问题治理环境污染绿色化学整体特点1(1)进一步认识化学学科在社会可持续发展中的作用,激发学生深入学习化学的兴趣。(2)引导学生在问题解决的过程中复习巩固化学学科的基础知识。(3)帮助学生了解后续各选修化学课程的主要内容,为学生作出选择提供指导。(1)复习常见金属的冶炼方法。(2)了解常见金属的化学性质。(3)能应用氧化还原原理进行分析。1人类对酸碱的认识(P93)1根据味道石蕊试液反应特征电离理论质子理论电子理论经验总结科学概括科学本质学生生活波义耳的著名实验阿伦尼乌斯电离理论阿斯匹林(P97)水杨酸乙酰水杨酸钠缓释阿斯匹林酯化反应乙酰水杨酸中和反应水解反应水解反应酯化反应水解反应谢谢联系电话:021-62232049
手机:13564362935
电子邮箱:zxyecnu@126.com1
