2010年备考中考化学系列专题第二章 认识空气 保护空气(适合粤教版)
文档属性
| 名称 | 2010年备考中考化学系列专题第二章 认识空气 保护空气(适合粤教版) |
|
|
| 格式 | rar | ||
| 文件大小 | 1.1MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 粤教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2010-03-14 00:00:00 | ||
图片预览




文档简介
登陆21世纪教育 助您教考全无忧
2010年备考中考化学系列专题
第二章 认识空气 保护空气(适合粤教版)(教师版)
【知识网络】
1. 空气 ①氮气占78%
成分(体积分数) ②氧气占21%
③稀有气体占0.94%
④二氧化碳占0.03%
⑤水蒸气和杂质占0.03%
二氧化氮
空气 气态 二氧化硫
主要污染物 一氧化碳
颗粒物
加强大气质量监测
改进燃料结构
污染防治措施 使用清洁能源
积极植树、造林、种草
2构成物质的微粒
概念:保持物质化学性质的最小微粒
分子 体积和质量都很小
特征 分子间有一定的间隔
构 构 分子在不停的运动
成 成 概念:化学变化中的最小微粒
特征:同分子的特征相似
物质 原子 质子(带正电)
构成 得 原子核(带正电) ( http: / / www. )
失 结构 中子(不带电)
构 电 核外电子(带负电)
成 子
形
成 概念:带电的原子或原子团
离子 阳离子
分类
阴离子
【知识梳理】
一、空气的成分
1、认识空气的组成
空气中含量最多的气体是_______,它大约占空气体积的_______,其次是_______,它大约占空气体积的_______,二氧化碳的体积分数只占_______,但作用很大。另外,还有水蒸气和杂质大约占空气体积的_______。
2、空气是一种重要的资源
(1)在工业上通过降温加压的方法,根据氮气、氧气、稀有气体的_______不同,将各种气体分离出来。这一过程发生的是_______变化。
(2)可用于动物呼吸作用的是_____气,液态______可用作制冷剂,_____可被填充在灯泡中,制造各种用途的电光源。
3、关注空气质量.
目前计入空气污染指数的项目暂定为______、______、______、______等。
二、物质的构成
物质由______、______、______构成。分子由______构成。
三、原子的构成
1、原子的结构
原子是由位于原子中心的带______电的原子核和核外带______电的电子构成。原子核是由带______电的______和不带电的______构成。在原子中,质子数______核电荷数______核外电子数。所以整个原子不显电性。
2、原子结构示意图
(1)原子核外电子的能量越高,离核较 ,能量低的离核 ,通常把电子在离核远近不同的区域运动称为 。
(2)原子结构示意图
下图是钠原子的结构示意图,图中小圈表示 ,圈内的数字表示 ,弧线表示 ,弧线上的数字表示 。
(3)离子是__________________,离子也是构成物质的一种粒子。
3、相对原子质量
原子中原子的质量主要集中在______上。电子的质量______,是1个质子质量的______。原子的质量很小,记忆书写都不很方便,所以用相对原子质量来表示原子的质量,相对原子质量就是________________________。
【答案】:
一、空气的成分
1、氮气 78% 氧气 21% 0.03% 0.03%
2、(1)沸点 物理
(2)氧 二氧化碳 氮气
3、二氧化氮 二氧化硫 一氧化碳 可吸入颗粒物
二、物质的构成
分子 原子 离子 原子
三、原子的构成
1、原子的结构
正 负 正 质子 中子 等于 等于
2、原子结构示意图
(1)远 近 分层排布
(2)原子核 质子数 电子层 该电子层上的电子数
(3)带电的原子
3、原子核 很小 1/1836
【要点讲解】
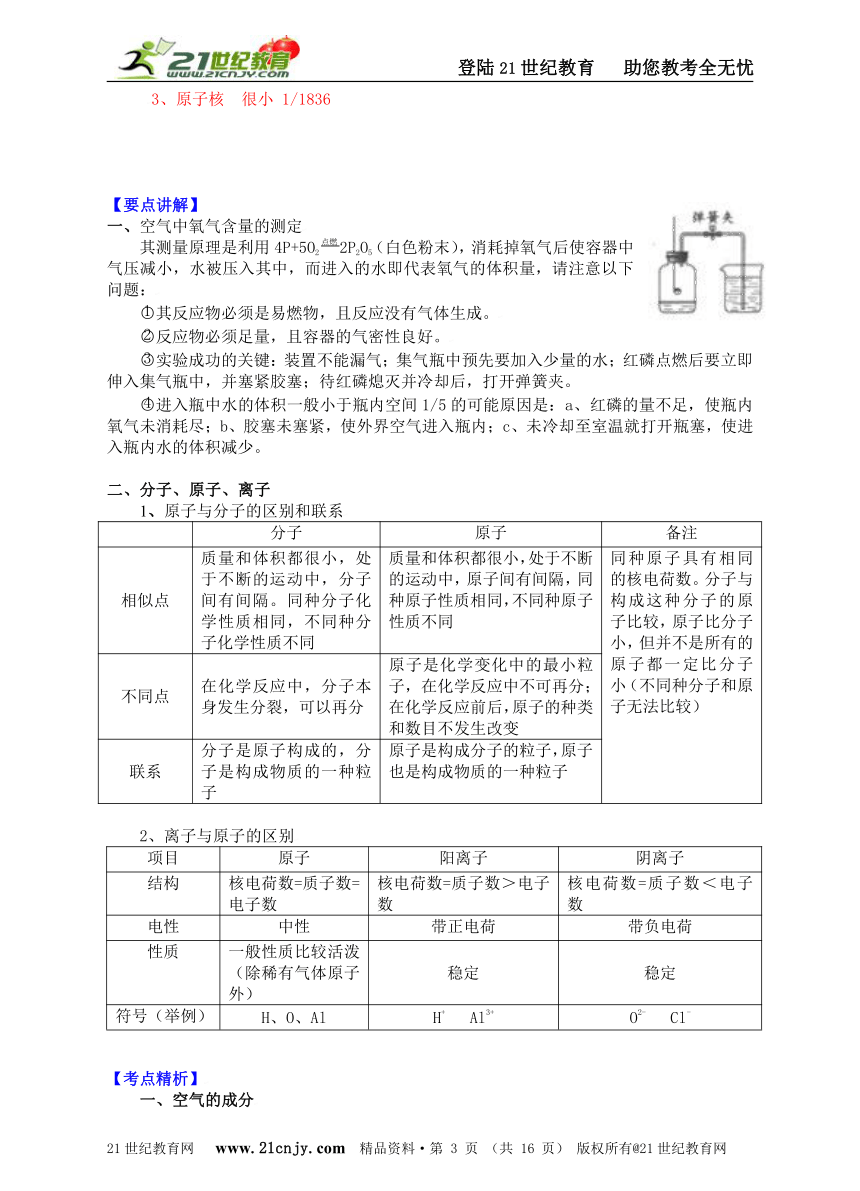
一、空气中氧气含量的测定
其测量原理是利用4P+5O2点燃2P2O5(白色粉末),消耗掉氧气后使容器中气压减小,水被压入其中,而进入的水即代表氧气的体积量,请注意以下问题:
其反应物必须是易燃物,且反应没有气体生成。
反应物必须足量,且容器的气密性良好。
实验成功的关键:装置不能漏气;集气瓶中预先要加入少量的水;红磷点燃后要立即伸入集气瓶中,并塞紧胶塞;待红磷熄灭并冷却后,打开弹簧夹。
进入瓶中水的体积一般小于瓶内空间1/5的可能原因是:a、红磷的量不足,使瓶内氧气未消耗尽;b、胶塞未塞紧,使外界空气进入瓶内;c、未冷却至室温就打开瓶塞,使进入瓶内水的体积减少。
二、分子、原子、离子
1、原子与分子的区别和联系
分子 原子 备注
相似点 质量和体积都很小,处于不断的运动中,分子间有间隔。同种分子化学性质相同,不同种分子化学性质不同 质量和体积都很小,处于不断的运动中,原子间有间隔,同种原子性质相同,不同种原子性质不同 同种原子具有相同的核电荷数。分子与构成这种分子的原子比较,原子比分子小,但并不是所有的原子都一定比分子小(不同种分子和原子无法比较)
不同点 在化学反应中,分子本身发生分裂,可以再分 原子是化学变化中的最小粒子,在化学反应中不可再分;在化学反应前后,原子的种类和数目不发生改变
联系 分子是原子构成的,分子是构成物质的一种粒子 原子是构成分子的粒子,原子也是构成物质的一种粒子
2、离子与原子的区别
项目 原子 阳离子 阴离子
结构 核电荷数=质子数=电子数 核电荷数=质子数>电子数 核电荷数=质子数<电子数
电性 中性 带正电荷 带负电荷
性质 一般性质比较活泼(除稀有气体原子外) 稳定 稳定
符号(举例) H、O、Al H+ Al3+ O2- Cl-
【考点精析】
一、空气的成分
1、命题特点
此考点在历年中考中占分值在2分到4分之间,难度系数在0.8左右,是中考考题中经常考的知识点之一,这一部分的命题思路、内容主要有以下几点:
(1)以考查空气成分为内容的选择题、实验探究题
(2)以空气的污染为为内容的选择题、填空题,其命题主要围绕酸雨、温室效应、臭氧层等内容。
2、方法技巧
(1)空气的成分:按体积汁算,大约是: 氮气78%、氧气21%、稀有气体0.94%、二氧化碳0.03%、其他气体和杂质0.03%。请注意以上各分数不是质量分数,而是体积分数。空气的成分一般来说是比较固定的。
(2)空气成分实验探究:科学家:拉瓦锡、舍勒、普利斯特利
成分研究:怎样证明空气中含有约 21% 体积的O2 (4P+5O2点燃2P2O5)
(3)空气的污染和保护
有害气体(SO2、CO、NO、NO2等)
空气中的有害物质
烟尘(可吸入颗粒物)
空气污染的危害:损害人体健康、影响作物生长、破坏生态平衡,导致全球气候变暖,酸雨和臭氧层破坏等。
保护空气措施:加强大气质量监测,改进燃料结构,使用清洁能源,积极植树、造林、种草等。
城市空气质量日报、预报:空气质量日报的主要内容包括“空气污染指数”、“首要污染物”、“空气质量级别”等;目前计入空气污染指数的项目暂定为:SO2、CO、NO、可吸入颗粒物和臭氧等。空气质量级别有优、良好、轻度污染、中度污染和重度污染等几类。
【例1】(2009·烟台)下列有关空气各成分的说法正确的是( )
A.氧气的化学性质比较活泼,属于可燃物
B.氮气的化学性质不活泼,可用于食品防腐
C.空气质量报告中所列的空气质量级别越大,空气质量越好
D.二氧化碳在空气中含量增多会引起温室效应,属于空气污染物
【答案】B
【解析】氧气能支持燃烧但不能燃烧,空气质量级别越大,空气质量越差,二氧化碳虽然能引起温室效应,但不属于污染物。
【规律小结】
【例2】(2008·北京)如图所示装置可用于测定空气中氧气的含量,实验前在集气瓶内加入少量水,并做上记号。下列说法中,不正确的是 ( )
A、实验时红磷一定过量
B、点燃红磷前先用弹簧夹夹紧乳胶管
C、红磷熄灭后立刻打开弹簧夹
D、最终进入瓶中水的体积约为氧气的体积
【答案】C
【解析】此题是考查有关空气中氧气含量的题,若在红磷熄灭后立即打开弹簧夹,会因集气瓶中的温度过高使水不能完全的被倒吸入集气瓶中,使测量不准确。
【规律小结】空气中氧气含量的测定
其测量原理是利用4P+5O2点燃2P2O5(白色粉末),消耗掉氧气后使容器中气压减小,水被压入其中,而进入的水即代表氧气的体积量,请注意以下问题:
其反应物必须是易燃物,且反应没有气体生成。
反应物必须足量,且容器的气密性良好。
实验成功的关键:装置不能漏气;集气瓶中预先要加入少量的水;红磷点燃后要立即伸入集气瓶中,并塞紧胶塞;待红磷熄灭并冷却后,打开弹簧夹。
进入瓶中水的体积一般小于瓶内空间1/5的可能原因是:a、红磷的量不足,使瓶内氧气未消耗尽;b、胶塞未塞紧,使外界空气进入瓶内;c、未冷却至室温就打开瓶塞,使进入瓶内水的体积减少。
变式训练一
1、(2008·肇庆)2008年北京奥运会若用大型遥控飞艇作广告。为了安全,艇内充入的气体最好是 ( )
A.氢气 B.氧气 C.氦气 D.二氧化碳
2、(2009·兰州)右图所示装置可用于测定空气中氧气的含量,实验前在集气瓶内加入少量水,并做上记号。下列说法中不正确的是( )
A.该实验证明空气中氧气的含量约占1/5
B.实验时红磷一定要过量
C.实验前一定要检验装置的气密性
D.红磷燃烧产生大量的白雾,火焰熄灭后立刻打开弹簧夹
3、(2008·安徽)某校研究性学习小组用右下图装置进行镁条在空气中燃烧的实验,燃烧、冷却后打开止水夹,进入集气瓶中水的体积约占集气瓶体积的70%。
(1)右图所示A仪器的名称是 ,燃烧、冷却后打开止水夹,水能进入集气瓶的原因是
。
(2)如果镁条只和空气中的氧气反应,则进入集气瓶中水的体积最多不超过其容积的 %。现进入集气瓶中水的体积约为其容积的70%,根据空气的组成可推出减少的气体中有氮气。
【发现问题】氮气是怎样减少的呢?
【假设一】氮气与镁条反应而减少。
【假设二】 。
【查阅资料】镁条在氮气中能燃烧,产物为氮化镁(Mg3N2)固体。氮化镁中氮元素的化合价为 。镁条还可以在二氧化碳气体中燃烧生成碳和氧化镁,该反应类型是 。
(3)通过以上探究,你对燃烧的有关知识有了什么新的认识:
(写出一点即可)。
【答案】
1、C 解析:氢气不安全
2、D 解析:应冷却至室温才打开瓶塞
3、(1)烧杯 集气瓶内压强小于大气压
(2)装置可能漏气 -3 置换反应
(3)燃烧不一定需要氧气
二、分子、原子、离子
1、命题特点
此考点在往年中考中所占分值在2分到5分之间,难度系数在0.8左右,是中考常考知识点,其命题的思路、内容有以下几点:
(1)以考查分子、原子的性质为内容的选择题,注重对分子不停的运动。分子间有间隔的考查
(2)以考查原子的结构为内容的选择题、填空题,其注重考查根据粒子结构推断粒子的种类,具体原子或离子的质子数、核电荷数、电子数、相对原子质量的关系等。
(3)给定原子的结构示意图或元素周期表,让学生总结相关规律的开放性试题。
2、方法技巧:
(1)深刻理解分子、原子、离子的概念,理清相互间的关系
分子 原子 离子
不同点 化学变化中,种类发生变化 化学变化中,种类不变 带电微粒
相同点 都是构成物质的微粒,都很小,不停地运动,微粒之间有间隔
联系 分子是由原子构成的,原子得失电子变成离子
(2)分子和原子都能直接构成物质,分子是保持物质化学性质的最小粒子,分子在化学变化中分裂成原子;而在化学变化中原子不能再分,是化学变化中的最小粒子,分子是由原子构成的,但是并不是每个分子都是由2个原子构成的。
(3)加强对原子结构示意图含义的理解,掌握原子核外电子排布的规律。知道原子的最外层电子数决定其元素的化学性质。充分理解相对原子质量的定义,知道相对原子质量≈质子数+中子数。
【例1】(2009·宿迁)下列有关分子、原子、离子说法正确的是( )
A.分子是化学变化中最小的粒子
B.一切原子的原子核都是由质子、中子构成的
C.分子的质量总比原子质量大
D.分子、原子、离子都能直接构成物质
【答案】D
【解析】化学变化中的最小粒子是原子,氢原子中没有中子,分子的质量比构成其原子的质量大,不能理解成分子的质量比原子的质量大,如氢分子的质量小于氧原子的质量。
【规律总结】分子、原子、离子都可以构成物质,金属单质和稀有气体单质是由原子直接构成的,共价化合物和一般气体大都是由分子构成的,离子化合物是由离子构成的。
【例2】 (2008·北京)下图a是两种元素在元素周期表中的信息,下图b是氟原子的原子结构示意图。
(1)图a方框的横线上填的是 ;图b方框横线上的数字是 。
(2)请将“元素”、“原子”、“分子”填入图c适当的圆圈内,从而完成元素、原子、分子与物质之间的正确的关系图。
分子
【答案】(1)Na ;7 ; 元素
原子
【解析】图a中两图相比较知:方框内应是钠元素的元素符号,图b是氟原子的结构示意图,所以放框内的数字应是7,物质是由分子、原子构成的,分子是由原子构成的,物质是有元素组成的。
【规律总结】两种元素在元素周期表中的信息是:方框的左上角是元素序数(即原子的质子数),右上角是元素符号,中间是元素名称,下方是相对原子质量;原子结构示意图中,圆圈内的数字是原子的质子数,弧线表示电子层,弧线上的数字表示该电子层上的电子数;任何物质都是由分子、原子或离子构成的,分子是由原子构成的,原子得失电子变为离子,物质是有元素组成的。
变式训练一
1、(2008·泰安)分子、原子、离子都是构成物质的微粒,下列由原子直接构成的是( )
A.铜 B.氧气 C. 氯化钠 D.二氧化碳
2、(2009·烟台)雄伟壮观的国家大剧院主体建筑表面安装了近2万块钛(Ti)金属板。已知Ti原子核内有22个质子,则下列叙述正确的是( )
A. Ti可以表示一个钛原子 B. Ti核外有26个电子
C. TiO2中含有氧分子 D. CaTiO3属于金属氧化物
3、(2008·厦门)已知溴元素的元素符号为Br,溴原子结构
示意图为(右图)问:
①x的值为_________。
②溴元素的化学性质与下列哪种元素的化学性质相似______(填序号)
A B C
③溴化氢的化学式为_________。
④溴化氢的水溶液是一种酸,该酸的名称是_________。
【答案】
1、A 【解析】金属由原子构成
2、A【解析】B中Ti核外有26个电子错误,应为22个电子和质子数相等,C中TiO2中含有氧分子错误,应为含有氧原子,D中CaTiO3属于金属氧化物错误,不是氧化物,故选A
3 ①35 【解析】2+8+18+7=35
② B 【解析】最外层电子数相等化学性质相似
【感受真题】
一、选择题(每小题3分,共45分)
1、(2009·潍坊)榴莲被誉为“果中之王”。切开榴莲时可闻到特殊香味,这说明( )
A.分子在不断运动 B.分子质量很小
C.分子体积很小 D.分子间有间隔
2、(2009·烟台)下列对一些事实的解释不正确的是( )
事 实 解 释
A 物质的热胀冷缩 分子或原子间的间隔随温度的改变而改变。
B 一氧化碳有可燃性,而二氧化碳不具有可燃性 物质组成元素不同,分子结构也不同
C 0℃时水结成冰,而海水在-1.9℃才会结冰 海水中含有盐,是混合物,其凝固点比水低
D 盐酸和稀硫酸都能使紫色石蕊试液变红色 盐酸和稀硫酸中都含有大量的氢离子
3、(2009·苏州)用分子的相关知识解释下列生活中的现象,其中错误的是( )
A.热胀冷缩,说明分子的大小随温度升降而改娈
B.“酒香不怕巷子深”,说明分子在不停地运动
C.10mL酒精和10mL水混合后,体积小于20mL,说明分子间有空隙
D.湿衣服在夏天比冬天容易晾干,说明分子的运动速率随温度升高而加快
4、(2009·安徽)我国著名化学家徐光宪因在稀土元素等研究领域做出杰出贡献,荣获2008年度“国家最高科学技术奖”。铈(Ce)是一种常见的稀土元素,下列关于铈的说法错误的是( )
A.原子序数是58 B.相对原子质量是140.1
C.质子数为58 D.铈元素是非金属元素
5、(2009·福州)右图是钠元素的原子结构示意图,下列
有关钠原子的叙述不正确的是( )
A.质子数是11 B.最外层电子数为1
C.核外有3个电子层 D.核外电子总数为10
6、(2008·南京)宁宁在学习“化学元素与人体健康”后,查阅到如下资料,请你给下表的“ ”处选择恰当的选项
种类 主要食物来源
钙 奶类、绿色蔬菜、水产品、肉类、豆类
铁 肝脏、瘦肉、蛋、鱼、豆类、芹菜
锌 海产品、瘦肉、肝脏、奶类、豆类、小米
碘 海产品、加碘盐
A、元素 D、分子 C、原子 D、离子
7、(2009·青岛)下图是元素周期表中的一格,依据图中的信息得到的下列认识错误的是( )
A.该元素原子的质子数为14
B.该元素属于非金属元素
C.该元素一个原子的原子核外有14个电子
D.该元素的相对原子质量为28.09
8、(2009·苏州)参考下列物质的微观结构图示,其中由阴,阳离子构成的物质是( )
A.铜 B.干冰 C.氯化钠 D.金刚石
9、(2009·雅安)结构示意图 所表示的粒子是( )
A.原子 B.分子 C. 阴离子 D.阳离子
10、(2009·南京)原子序数为94的钚(Pu)是一种核原料,该元素一种原子的质子数和中子数之和为239,下列关于该原子的说法不正确的是( )
A.中子数为145 B.核外电子数为94
C.质子数为94 D.核电荷数为239
11、(2008·北京)决定元素种类的是( )
A、质子数 B、中子数 C、电子数 D、最外层电子数
12、(2009·重庆)下列物质中属于化合物的是( )
A.二氧化硫 B.空气 C.磷 D.碘盐
13、(2009·青岛)下列常见的物质中,属于纯净物的是( )
A.啤酒 B.食醋 C.加碘食盐 D.蒸馏水
14、(2009·黔东南州)分类学习是化学重要的学习思想,下列物质分类错误的一组是( )
A. H2、O2、N2 B. HCl、H2SO4、NaHSO4学
C. NaOH、KOH、NH3·H2O D. NaCl、NaHCO3、NH4Cl
15、(2009·广州)下列各组各有两种物质,它们的化学式和所属的物质类别都正确的一组是( )
物质1 物质2
名称 化学式 物质类别 名称 化学式 物质类别
A 氮气 N 非金属单质 氧化亚铁 Fe2O2 碱
B 碳酸氢钠 NaHCO3 盐 硝酸 HNO3 酸
C 硫酸钾 K2SO4 盐 五氧化二磷 P2O5 金属氧化物
D 锰 Mm 金属单质 氢氧化镁 Mg(OH)2 碱
二、填空题
16、(6分)(2009·重庆)(1)用数字和化学符号表示:2个氧原子 ,3个钠离子 。
(2)镁的原子结构示意图为 ,Mg原子在化学反应中容
易 (填“得到”或“失去”)2个电子。
17、(8分)(2009·苏州)形态各异的物质可按一定规律分类。现有以下八种物质,请选用各物质名称前的字母序号填涂在答题卡相应位置。
A.盐酸 B.氯化钾 C.氧化铜 D.淀粉
E.五氧化二磷 F.氮气 G.氢氧化钙 H.甲烷
题号 物质分类标准 字母序号 题号 物质分类标准 字母序号
(1) 金属氧化物 (5) 非金属单质
(2) 非金属氧化物 (6) 挥发性酸
(3) 易溶性盐 (7) 最简单的有机物
(4) 微溶性碱 (8) 糖类
18、(10分)(2008·西安)(1)向容积为250ml的细颈玻璃仪器(如下图所示)中加水至虚线处,再滴几滴红墨水,一段时间后,玻璃仪器中的现象是 ,说明 。
(2)继续向玻璃仪器中加酒精至凹液面最低处正好与刻线相切。塞紧玻璃塞,将玻璃仪器中液体倒转摇匀,重复2次。静置一段时间后,玻璃仪器中的现象为 ,说 明 。仪器细颈部分的作用是 。
19、(9分)(2009·眉山)化学是研究物质的结构、性质以及变化规律的科学,研究元素知识是学好化学的基础。下表包含部分元素的相关信息,完成以下填空:
(1)1869年,科学家 发现了元素周期律和元素周期表。
(2)请画出17号元素原子结构示意图 ,该元素在化学反应中比较容易 (填“得到”或“失去”)电子变成离子。
(3)上表中最活泼的金属元素与地壳中含量最多的元素组成的化合物是
(填化学式)。
20、(10分)(2008·江西)下图中的①、②是氟元素、钙元素在元素周期表中的信息,A、B、C、D是四种粒子的结构示意图。
请你回答:
(1)氟元素的相对原子质量为 ,钙元素的原子序数为 ;
(2)X= ;
(3)A、B、C、D属于同种元素的粒子是 (填序号);
(4)A粒子的化学性质与B、C、D中哪一种粒子的化学性质相似 (填序号)。
【答案】
1、A 解析:由于分子不断的运动,才能被人接触闻到
2、B 解析:一氧化碳和二氧化碳都是由碳元素和氧元素组成。
3、A 解析:热胀冷缩是由于分子间的间隔变大引起的,分子的大小是不变的。
4、D 解析:金属元素的名称都有“钅”字旁,铈属于金属元素。
5、D 解析:从结构示意图中可知核外电子总数为2+8+1=11个。
6、A 解析:生活中的物质成分比较复杂,我们通常所说的物质组成都是指物质的元素组成,是通过元素组成来说明其成分或比较其含量的。
7、D 解析:相对原子质量是针对原子而言的,不能理解成元素的相对原子质量。
8、C 解析:铜和金刚石由原子构成,干冰由分子构成。
9、D 解析:原子核外由18个电子,核内由17个质子,所以其带一个单位的负电荷,属于阴离子。
10、D 解析:原子中原子序数=质子数=电子数=核电荷数。
11、A 解析:元素是指具有相同核电荷数(即质子数)的同一类原子的总称。可见一种元素与另一种元素的本质区别是核电荷数或质子数不同,即决定元素种类的是核电荷数或质子数。
12、A 解析:化合物是含有多种元素的纯净物,BD为混合物,C只含有磷元素。
13、D 解析:啤酒中含有二氧化碳和乙醇,食醋中含有乙酸和水,加碘食盐中含有碘和氯化钠。
14、B 解析:HCl和H2SO4属于酸,NaHSO4属于盐
15、B 解析:氮气的化学式为N2; 氧化亚铁的化学式为FeO,属于金属氧化物;P2O5属于非金属氧化物;锰的化学式为Mn。
16、(1)2O 3Na+ (2)失去
解析:镁原子的最外层电子数为2,小于4个,易失去电子形成稳定结构。
17、(1)C (2)E (3)B (4)G (5)F (6)A (7)H (8)D
18、(1)整瓶水变红;分子在不断运动
(2)液面低于刻线;分子间有间隔;便于观察液面变化
解析:分子是在不断运动的,当向水中滴几滴红墨水后,红墨水分子会运动的水分子中,是整瓶水变红;由于分子间有间隔,当两种不同的液体相互混合时,它们的分子相互渗透,彼此充满在分子间隔中,所以其体积会小于两者的体积之和,但这个差值不大,使用细颈仪器会便于观察。
19、(1)门捷列夫 (2) 得到 (3)Na2O(Na2O2)
20、(1)19.00;20 (2)8 (3) B C (4) B
解析:元素周期表中原子最下面部分为其相对原子质量,元素符合前面的数字为原子序数;D中的质子数为18,其原子中核外电子数为18,具有稳定结构,最外层电子数为8;决定元素种类的是核电荷数(即质子数),B和C的质子数都为17,所以为同种元素;元素的化学性质取决于最外层电子数,A的最外层电子数为7与B的最外层电子数相同,所以两种的化学性质相似。
【09中考模拟】
一、选择题
1、(2009·湖南模拟)我们知道,食物较长时间露置在空气中就会变质,这主要是由于空气中含有 ( )
A.氧气 B.氮气 C. 二氧化碳 D. 稀有气体
2、(2009· 镇江模拟)右图为某有机物(C9H10O3)的分子模型,该有机物是一种高效食品防腐剂。下列说法中,不正确的是( )
A.该有机物由3种元素组成
B.该有机物能减缓食品变质
C.该有机物分子中碳、氧原子的个数比为3∶1
D.该有机物中含氧元素的质量分数最小
3、(2009· 北京模拟)右图是测定空气中氧气含量的实验装置。下列叙述不正确的是( )
A.反应后燃烧匙中的红磷完全消失
B.进入瓶中水的体积约为氧气的体积
C.钟罩内气体压强的减小导致水面上升
D.反应结束后需冷却至室温再观察钟罩内的液面高度
4、(2009·厦门模拟)甲醇(化学式:CH3OH)是一种新型电池的燃料,下列关于甲醇的说法不正确的是( )
A.相对分子质量为32 B.其碳、氢、氧三种元素的质量比为3:1:4
C.100g甲醇含氧50g D.一个甲醇分子含有一个氢氧根离子
5、(2009·四川省模拟)把分别充满红棕色NO2气体和无色H2的集气瓶,按照右图A、B两种方式放置,然后把两瓶中间的玻璃片抽走,使两瓶口密合在一起(不用振荡),可观察到A中两瓶气体的颜色很快趋于一致(两气体不反应),而B中需很长时间才能达到同样的效果。不能由此现象直接得出的结论是 ( )
A.分子是不断运动的 B.分子间有间隔
C.氢气的密度比二氧化氮的密度小 D.分子由原子构成
6、(2009·河南模拟) “分子足球”C60之后,科学家又发现另一种“分子足球”N60。一定条件下N60中积累的巨大能量会在一瞬间释放出来,是未来的火箭燃料,N60属于( )
A.金属单质 B.非金属单质 C.化合物 D.混合物
7、(2009·厦门模拟)我国的“神舟六号”载人飞船已发射成功,“嫦娥”探月工程也已正式启动。据科学家预测,月球的土壤中吸附着数百万吨的氦(He—3),其原子核中质子数为2、中子数为1,每百吨氦(He—3)核聚变所释放出的能量相当于目前人类一年消耗的能量。下列关于氦(He—3)元素的说法正确的是( )
A.原子核外电子数为3 B.相对原子质量为2
C.原子结构示意图为 D.原子结构示意图为
8、(2009·上海模拟)某些花岗岩石材中含有放射性元素氡。某种氡原子的质子数为86,中子数为136,这种氡原子的核外电子数为( )
A. 50 B. 86 C. 136 D. 222
9、(2009·枣庄模拟)下列各结构示意图中,能表示阳离子的是 ( )
二、填空题
11、(2009·厦门模拟) “用微粒的眼光看世界”,是我们学习化学的重要思想方法。试根据以下材料,结合你所学知识,简要回答问题:
材料一:微波炉的工作原理是利用微波穿透食物达5cm深,使食物中的水分子产生高频率震动,并摩擦,产生大量的热量,达到运动式加热或烹饪食物的目的。
材料二:一滴水里大约有15万亿亿个水分子,如果10亿人来数一滴水里的水分子, 每人每分钟数100个,日夜不停,需要数3万多年才能完成。
材料三:某同学在课后做如图所示的实验:在一个玻璃容器中加入100mL水,向水中放入一块糖,立即在容器外壁沿液面画一水平线,过一会儿发现糖块溶解,液面比原来水平线降低了。
(1)材料一说明_____________________________;
(2)材料二说明______________________________;
(3)材料三说明______________________________;
12、(2009·厦门模拟)信息1.对于我国环境问题的现状,中国环保局长周生贤毫不掩饰自己的忧虑。他指出:在发达国家上百年时间的工业化过程中分阶段出现的环境问题,现在却在我国集中出现了。目前,我国1/5的城市空气污染严重,1/3的国土面积受到酸雨影响,近1/5的土地面积有不同程度的沙化现象,近1/3的土地面临水土流失,90%以上的天然草原退化,2007年已成为我国节能减排工作关键的一年。
信息2.下表是2007年3月31日我国部分地区的空气质量日报内容:
序号 城市 污染指数 首要污染物 空气污染指数 空气质量级别
① 北京 103 可吸入颗粒物 Ⅲ 轻微污染
② 呼和浩特 500 可吸入颗粒物 Ⅴ 重污染
③ 厦门 72 可吸入颗粒物 Ⅱ 良
④ 深圳 36 无 Ⅰ 优
回答下列问题(友情提醒:选择题可能有多个正确选项)
(1)当日空气质量最好的城市是(填序号)
(2)人类需要洁净的空气。目前我国城市空气质量日报中的污染物不包括( )
A.可吸入颗粒物 B.二氧化碳 C.二氧化氮 D.氮气
(3) 为改善空气质量,北京开展了“为首都多一个蓝天,我们每月少开一天车”的主题活动,下列说法正确的是
A.尾气不会对空气造成污染
B.每月少开一天车不会减少汽车尾气的排放
C.汽车尾气中只含有CO2和H2O
D.“为首都多一个蓝天”是每个市民的职责
(4)SO2气体是空气的主要污染物, 该气体可用氢氧化钙悬浊液吸收,生成难溶于水的亚硫酸钙(CaSO3)和水。请写出该反应的化学方程式
(5) 想一想,请说出厦门空气主要污染物的一个来源
为改善厦门的空气质量,保护蓝色美丽的天空,请提出你的一个建议
【答案】
一、选择题
1、A 解析:食物露置在空气中变质是与氧气反应
2、C 解析:D中该有机物中含氧元素的质量分数最小是错误,氢元素的质量分数最小
3、A 解析:反应后燃烧匙中的红磷完全消失是错误,红磷应有剩余
4、D 解析:D中一个甲醇分子含有一个氢氧根离子是错误,不是氢氧根离子
5、D 解析:不能证明分子由原子构成
6、B 解析:N60属于非金属单质
7、D 解析:氦(He—3)是相对原子质量是3的氦原子,质子数等于电子数为2,故选D
8、B 解析:质子数等于电子数,质子数为86,所以电子数等于86
9、A 解析:质子数大于电子数
二、填空题
11、(1)分子不断运动
(2)分子很小
(3)分子间有间隙
12 (1)④
(2) B D
(3) D
(4)SO2+Ca(OH)2 =======CaSO3+H2O
(5)粉尘 植树
【单元限时训练】
第二章单元检测
一、选择题
1、(2008·自贡)2008年初,一场大范围历史罕见的低温雨雪冰冻袭击了中国南方部分省区市,此次雪灾给我国造成了巨大的经济损失。下列说法正确的是 ( )
A、雪是一种单质 B、冰和雪的主要成分都水
C、当雨雪成为冰冻时,分子的运动就停止了
D、冰雪融化的过程是一种化学变化
2、(2008·北京) 用分子观点解释右图漫画中小女孩的话,正确的是 ( )
A.分子质量小 B.分子间有间隔
C.分子体积小 D.分子在不断运动
3、(2008·揭阳)由我国著名科学家、中国科学院院士张青莲教授主持测定了铟、铱、锑、铕等几种元素的相对原子质量新值,其中他测定核电荷数为63的铕元素的相对原子质量的新值为152。则下列说法正确的是( )
A.铕元素的原子质子数为63 B.铕元素的原子中子数为63
C.铕元素的原子核外电子数为152 D.铕元素的原子的质量为152
4、(2009·青岛)下列常见的物质中,属于纯净物的是( )
A.啤酒 B.食醋 C.加碘食盐 D.蒸馏水
5、(2009·雅安)用分子的观点对下列常见现象的解释中,不正确的是( )
A. 食物腐败——分子本身发生变化
B. 酒精挥发——分子间间隔变大
C. 花香四溢——分子不停地运动
D. 热胀冷缩——分子大小随温度变化而改变
6、(2009·南京)下列粒子结构示意图中,表示原子的是( )
7、(2009·衡阳)右图是元素周期表的一格,下列有关叙述不正确的是( )
A.锰元素的原子序数为25
B.锰元素的相对原子质量为55
C.锰元素的原子核外电子数为25
D.锰元素的原子核内中子数为25
8、(2009·扬州模拟)下列生活事实不能体现分子性质的是( )
9、(2009·成都模拟)如图是氯化氢的形成过程。从微观角度分析,下列说法不正确的是( )
A.物质全部由原子构成
B.化学变化的实质是分子破裂成原子,原子重新组合成新分子
C.化学是从原子、分子角度研究物质的组成、结构、性质及其变化
D.可由构成微粒的结构,研究物质的性质
10、(2009·黄冈)下列有关分子、原子和离子的说法正确的是( )
A.保持氧气化学性质的粒子是氧原子
B.原子的最外层电子数决定元素的种类
C.氯化钠是由离子构成的化合物
11、(2009·北京)右图是元素周期表中钠元素的信息示意图,对图中信息理解不正确的是( )
A.质子数为11 B.元素名称为钠元素
C.元素符号为Na D.核外电子数为22.99
12、(2009·茂名)下列选项中代表离子的是(说明:数字代表质子数,“+”表示原子核所带的电荷,黑点代 表核外电子)( )
13、(2009·济宁)分析钠原子、钠离子的结构示意图得到的以下说法中,错误的是:( )
A.钠原子有三个电子层,钠离子有两个电子层
B.钠原子、钠离子的质子数都为11
C.一个钠原子在化学反应中可失去一个电子,因此,钠元素为+1价
D.钠原子和钠离子不属于同一种元素
14(2008·盐城)下列对分子、原子、离子的认识,正确的是( ) ( http: / / www. )
A、分子是保持物质的最小粒子 B、原子是最小的粒子,不可再分 ( http: / / www. )
C、原子得到或失去电子后形成离子 ( http: / / www. )
D、CO2和CO性质的差异主要是由于分子间的间隔不同 ( http: / / www. )
二、填空题
15、(2009·重庆)(1)用数字和化学符号表示:2个氧原子 ,3个钠离子 。
(2)镁的原子结构示意图为 ,Mg原子在化学反应中容易
(填“得到”或“失去”)2个电子。
16、(2008·自贡)图A是两种元素在元素周期表中的信息,图B是氟原子的原子结构示意图。
(1)图A方框的横线上填的是 ,图B方框的横线上的数字是 。
(2)用化学符号和数字表示:2个氟原子 ,钠离子 。
(3)钠元素属于 (填“金属”或“非金属”)元素。
【答案】
1、 B解析:冰和雪的主要成分都水,属于化合物,分子在任何状态下都不会停止,只是运动会减慢,冰雪融化的过程没有生成新物质是物理变化,故选B
2、D
3、A解析:根据核电荷数=质子数=电子数和质子数+中子数=相对原子质量故选A
4、D
5、D解析:热胀冷缩是分子间间隔变化
6、B解析:原子是质子数=电子数
7、D
8、D
9、A解析:物质不是全部由原子构成,有分子,原子,离子等
10、C
11、D
12、C解析:原子是质子数=电子数,离子是质子数不等于电子数
13、D
14.C
二、填空题
15、(1)2O 3Na+
(2)失去
16、(1)Na 7
(2)2F Na+
(3)金属
14 Si
硅
28.09
2
8
2
+12
+2
1
+2
2
H
H
+
Cl
Cl
Cl
H
Cl
H
2
8
2
+12
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
21世纪教育网 www.21cnjy.com 精品资料·第 1 页 (共 16 页) 版权所有@21世纪教育网
2010年备考中考化学系列专题
第二章 认识空气 保护空气(适合粤教版)(教师版)
【知识网络】
1. 空气 ①氮气占78%
成分(体积分数) ②氧气占21%
③稀有气体占0.94%
④二氧化碳占0.03%
⑤水蒸气和杂质占0.03%
二氧化氮
空气 气态 二氧化硫
主要污染物 一氧化碳
颗粒物
加强大气质量监测
改进燃料结构
污染防治措施 使用清洁能源
积极植树、造林、种草
2构成物质的微粒
概念:保持物质化学性质的最小微粒
分子 体积和质量都很小
特征 分子间有一定的间隔
构 构 分子在不停的运动
成 成 概念:化学变化中的最小微粒
特征:同分子的特征相似
物质 原子 质子(带正电)
构成 得 原子核(带正电) ( http: / / www. )
失 结构 中子(不带电)
构 电 核外电子(带负电)
成 子
形
成 概念:带电的原子或原子团
离子 阳离子
分类
阴离子
【知识梳理】
一、空气的成分
1、认识空气的组成
空气中含量最多的气体是_______,它大约占空气体积的_______,其次是_______,它大约占空气体积的_______,二氧化碳的体积分数只占_______,但作用很大。另外,还有水蒸气和杂质大约占空气体积的_______。
2、空气是一种重要的资源
(1)在工业上通过降温加压的方法,根据氮气、氧气、稀有气体的_______不同,将各种气体分离出来。这一过程发生的是_______变化。
(2)可用于动物呼吸作用的是_____气,液态______可用作制冷剂,_____可被填充在灯泡中,制造各种用途的电光源。
3、关注空气质量.
目前计入空气污染指数的项目暂定为______、______、______、______等。
二、物质的构成
物质由______、______、______构成。分子由______构成。
三、原子的构成
1、原子的结构
原子是由位于原子中心的带______电的原子核和核外带______电的电子构成。原子核是由带______电的______和不带电的______构成。在原子中,质子数______核电荷数______核外电子数。所以整个原子不显电性。
2、原子结构示意图
(1)原子核外电子的能量越高,离核较 ,能量低的离核 ,通常把电子在离核远近不同的区域运动称为 。
(2)原子结构示意图
下图是钠原子的结构示意图,图中小圈表示 ,圈内的数字表示 ,弧线表示 ,弧线上的数字表示 。
(3)离子是__________________,离子也是构成物质的一种粒子。
3、相对原子质量
原子中原子的质量主要集中在______上。电子的质量______,是1个质子质量的______。原子的质量很小,记忆书写都不很方便,所以用相对原子质量来表示原子的质量,相对原子质量就是________________________。
【答案】:
一、空气的成分
1、氮气 78% 氧气 21% 0.03% 0.03%
2、(1)沸点 物理
(2)氧 二氧化碳 氮气
3、二氧化氮 二氧化硫 一氧化碳 可吸入颗粒物
二、物质的构成
分子 原子 离子 原子
三、原子的构成
1、原子的结构
正 负 正 质子 中子 等于 等于
2、原子结构示意图
(1)远 近 分层排布
(2)原子核 质子数 电子层 该电子层上的电子数
(3)带电的原子
3、原子核 很小 1/1836
【要点讲解】
一、空气中氧气含量的测定
其测量原理是利用4P+5O2点燃2P2O5(白色粉末),消耗掉氧气后使容器中气压减小,水被压入其中,而进入的水即代表氧气的体积量,请注意以下问题:
其反应物必须是易燃物,且反应没有气体生成。
反应物必须足量,且容器的气密性良好。
实验成功的关键:装置不能漏气;集气瓶中预先要加入少量的水;红磷点燃后要立即伸入集气瓶中,并塞紧胶塞;待红磷熄灭并冷却后,打开弹簧夹。
进入瓶中水的体积一般小于瓶内空间1/5的可能原因是:a、红磷的量不足,使瓶内氧气未消耗尽;b、胶塞未塞紧,使外界空气进入瓶内;c、未冷却至室温就打开瓶塞,使进入瓶内水的体积减少。
二、分子、原子、离子
1、原子与分子的区别和联系
分子 原子 备注
相似点 质量和体积都很小,处于不断的运动中,分子间有间隔。同种分子化学性质相同,不同种分子化学性质不同 质量和体积都很小,处于不断的运动中,原子间有间隔,同种原子性质相同,不同种原子性质不同 同种原子具有相同的核电荷数。分子与构成这种分子的原子比较,原子比分子小,但并不是所有的原子都一定比分子小(不同种分子和原子无法比较)
不同点 在化学反应中,分子本身发生分裂,可以再分 原子是化学变化中的最小粒子,在化学反应中不可再分;在化学反应前后,原子的种类和数目不发生改变
联系 分子是原子构成的,分子是构成物质的一种粒子 原子是构成分子的粒子,原子也是构成物质的一种粒子
2、离子与原子的区别
项目 原子 阳离子 阴离子
结构 核电荷数=质子数=电子数 核电荷数=质子数>电子数 核电荷数=质子数<电子数
电性 中性 带正电荷 带负电荷
性质 一般性质比较活泼(除稀有气体原子外) 稳定 稳定
符号(举例) H、O、Al H+ Al3+ O2- Cl-
【考点精析】
一、空气的成分
1、命题特点
此考点在历年中考中占分值在2分到4分之间,难度系数在0.8左右,是中考考题中经常考的知识点之一,这一部分的命题思路、内容主要有以下几点:
(1)以考查空气成分为内容的选择题、实验探究题
(2)以空气的污染为为内容的选择题、填空题,其命题主要围绕酸雨、温室效应、臭氧层等内容。
2、方法技巧
(1)空气的成分:按体积汁算,大约是: 氮气78%、氧气21%、稀有气体0.94%、二氧化碳0.03%、其他气体和杂质0.03%。请注意以上各分数不是质量分数,而是体积分数。空气的成分一般来说是比较固定的。
(2)空气成分实验探究:科学家:拉瓦锡、舍勒、普利斯特利
成分研究:怎样证明空气中含有约 21% 体积的O2 (4P+5O2点燃2P2O5)
(3)空气的污染和保护
有害气体(SO2、CO、NO、NO2等)
空气中的有害物质
烟尘(可吸入颗粒物)
空气污染的危害:损害人体健康、影响作物生长、破坏生态平衡,导致全球气候变暖,酸雨和臭氧层破坏等。
保护空气措施:加强大气质量监测,改进燃料结构,使用清洁能源,积极植树、造林、种草等。
城市空气质量日报、预报:空气质量日报的主要内容包括“空气污染指数”、“首要污染物”、“空气质量级别”等;目前计入空气污染指数的项目暂定为:SO2、CO、NO、可吸入颗粒物和臭氧等。空气质量级别有优、良好、轻度污染、中度污染和重度污染等几类。
【例1】(2009·烟台)下列有关空气各成分的说法正确的是( )
A.氧气的化学性质比较活泼,属于可燃物
B.氮气的化学性质不活泼,可用于食品防腐
C.空气质量报告中所列的空气质量级别越大,空气质量越好
D.二氧化碳在空气中含量增多会引起温室效应,属于空气污染物
【答案】B
【解析】氧气能支持燃烧但不能燃烧,空气质量级别越大,空气质量越差,二氧化碳虽然能引起温室效应,但不属于污染物。
【规律小结】
【例2】(2008·北京)如图所示装置可用于测定空气中氧气的含量,实验前在集气瓶内加入少量水,并做上记号。下列说法中,不正确的是 ( )
A、实验时红磷一定过量
B、点燃红磷前先用弹簧夹夹紧乳胶管
C、红磷熄灭后立刻打开弹簧夹
D、最终进入瓶中水的体积约为氧气的体积
【答案】C
【解析】此题是考查有关空气中氧气含量的题,若在红磷熄灭后立即打开弹簧夹,会因集气瓶中的温度过高使水不能完全的被倒吸入集气瓶中,使测量不准确。
【规律小结】空气中氧气含量的测定
其测量原理是利用4P+5O2点燃2P2O5(白色粉末),消耗掉氧气后使容器中气压减小,水被压入其中,而进入的水即代表氧气的体积量,请注意以下问题:
其反应物必须是易燃物,且反应没有气体生成。
反应物必须足量,且容器的气密性良好。
实验成功的关键:装置不能漏气;集气瓶中预先要加入少量的水;红磷点燃后要立即伸入集气瓶中,并塞紧胶塞;待红磷熄灭并冷却后,打开弹簧夹。
进入瓶中水的体积一般小于瓶内空间1/5的可能原因是:a、红磷的量不足,使瓶内氧气未消耗尽;b、胶塞未塞紧,使外界空气进入瓶内;c、未冷却至室温就打开瓶塞,使进入瓶内水的体积减少。
变式训练一
1、(2008·肇庆)2008年北京奥运会若用大型遥控飞艇作广告。为了安全,艇内充入的气体最好是 ( )
A.氢气 B.氧气 C.氦气 D.二氧化碳
2、(2009·兰州)右图所示装置可用于测定空气中氧气的含量,实验前在集气瓶内加入少量水,并做上记号。下列说法中不正确的是( )
A.该实验证明空气中氧气的含量约占1/5
B.实验时红磷一定要过量
C.实验前一定要检验装置的气密性
D.红磷燃烧产生大量的白雾,火焰熄灭后立刻打开弹簧夹
3、(2008·安徽)某校研究性学习小组用右下图装置进行镁条在空气中燃烧的实验,燃烧、冷却后打开止水夹,进入集气瓶中水的体积约占集气瓶体积的70%。
(1)右图所示A仪器的名称是 ,燃烧、冷却后打开止水夹,水能进入集气瓶的原因是
。
(2)如果镁条只和空气中的氧气反应,则进入集气瓶中水的体积最多不超过其容积的 %。现进入集气瓶中水的体积约为其容积的70%,根据空气的组成可推出减少的气体中有氮气。
【发现问题】氮气是怎样减少的呢?
【假设一】氮气与镁条反应而减少。
【假设二】 。
【查阅资料】镁条在氮气中能燃烧,产物为氮化镁(Mg3N2)固体。氮化镁中氮元素的化合价为 。镁条还可以在二氧化碳气体中燃烧生成碳和氧化镁,该反应类型是 。
(3)通过以上探究,你对燃烧的有关知识有了什么新的认识:
(写出一点即可)。
【答案】
1、C 解析:氢气不安全
2、D 解析:应冷却至室温才打开瓶塞
3、(1)烧杯 集气瓶内压强小于大气压
(2)装置可能漏气 -3 置换反应
(3)燃烧不一定需要氧气
二、分子、原子、离子
1、命题特点
此考点在往年中考中所占分值在2分到5分之间,难度系数在0.8左右,是中考常考知识点,其命题的思路、内容有以下几点:
(1)以考查分子、原子的性质为内容的选择题,注重对分子不停的运动。分子间有间隔的考查
(2)以考查原子的结构为内容的选择题、填空题,其注重考查根据粒子结构推断粒子的种类,具体原子或离子的质子数、核电荷数、电子数、相对原子质量的关系等。
(3)给定原子的结构示意图或元素周期表,让学生总结相关规律的开放性试题。
2、方法技巧:
(1)深刻理解分子、原子、离子的概念,理清相互间的关系
分子 原子 离子
不同点 化学变化中,种类发生变化 化学变化中,种类不变 带电微粒
相同点 都是构成物质的微粒,都很小,不停地运动,微粒之间有间隔
联系 分子是由原子构成的,原子得失电子变成离子
(2)分子和原子都能直接构成物质,分子是保持物质化学性质的最小粒子,分子在化学变化中分裂成原子;而在化学变化中原子不能再分,是化学变化中的最小粒子,分子是由原子构成的,但是并不是每个分子都是由2个原子构成的。
(3)加强对原子结构示意图含义的理解,掌握原子核外电子排布的规律。知道原子的最外层电子数决定其元素的化学性质。充分理解相对原子质量的定义,知道相对原子质量≈质子数+中子数。
【例1】(2009·宿迁)下列有关分子、原子、离子说法正确的是( )
A.分子是化学变化中最小的粒子
B.一切原子的原子核都是由质子、中子构成的
C.分子的质量总比原子质量大
D.分子、原子、离子都能直接构成物质
【答案】D
【解析】化学变化中的最小粒子是原子,氢原子中没有中子,分子的质量比构成其原子的质量大,不能理解成分子的质量比原子的质量大,如氢分子的质量小于氧原子的质量。
【规律总结】分子、原子、离子都可以构成物质,金属单质和稀有气体单质是由原子直接构成的,共价化合物和一般气体大都是由分子构成的,离子化合物是由离子构成的。
【例2】 (2008·北京)下图a是两种元素在元素周期表中的信息,下图b是氟原子的原子结构示意图。
(1)图a方框的横线上填的是 ;图b方框横线上的数字是 。
(2)请将“元素”、“原子”、“分子”填入图c适当的圆圈内,从而完成元素、原子、分子与物质之间的正确的关系图。
分子
【答案】(1)Na ;7 ; 元素
原子
【解析】图a中两图相比较知:方框内应是钠元素的元素符号,图b是氟原子的结构示意图,所以放框内的数字应是7,物质是由分子、原子构成的,分子是由原子构成的,物质是有元素组成的。
【规律总结】两种元素在元素周期表中的信息是:方框的左上角是元素序数(即原子的质子数),右上角是元素符号,中间是元素名称,下方是相对原子质量;原子结构示意图中,圆圈内的数字是原子的质子数,弧线表示电子层,弧线上的数字表示该电子层上的电子数;任何物质都是由分子、原子或离子构成的,分子是由原子构成的,原子得失电子变为离子,物质是有元素组成的。
变式训练一
1、(2008·泰安)分子、原子、离子都是构成物质的微粒,下列由原子直接构成的是( )
A.铜 B.氧气 C. 氯化钠 D.二氧化碳
2、(2009·烟台)雄伟壮观的国家大剧院主体建筑表面安装了近2万块钛(Ti)金属板。已知Ti原子核内有22个质子,则下列叙述正确的是( )
A. Ti可以表示一个钛原子 B. Ti核外有26个电子
C. TiO2中含有氧分子 D. CaTiO3属于金属氧化物
3、(2008·厦门)已知溴元素的元素符号为Br,溴原子结构
示意图为(右图)问:
①x的值为_________。
②溴元素的化学性质与下列哪种元素的化学性质相似______(填序号)
A B C
③溴化氢的化学式为_________。
④溴化氢的水溶液是一种酸,该酸的名称是_________。
【答案】
1、A 【解析】金属由原子构成
2、A【解析】B中Ti核外有26个电子错误,应为22个电子和质子数相等,C中TiO2中含有氧分子错误,应为含有氧原子,D中CaTiO3属于金属氧化物错误,不是氧化物,故选A
3 ①35 【解析】2+8+18+7=35
② B 【解析】最外层电子数相等化学性质相似
【感受真题】
一、选择题(每小题3分,共45分)
1、(2009·潍坊)榴莲被誉为“果中之王”。切开榴莲时可闻到特殊香味,这说明( )
A.分子在不断运动 B.分子质量很小
C.分子体积很小 D.分子间有间隔
2、(2009·烟台)下列对一些事实的解释不正确的是( )
事 实 解 释
A 物质的热胀冷缩 分子或原子间的间隔随温度的改变而改变。
B 一氧化碳有可燃性,而二氧化碳不具有可燃性 物质组成元素不同,分子结构也不同
C 0℃时水结成冰,而海水在-1.9℃才会结冰 海水中含有盐,是混合物,其凝固点比水低
D 盐酸和稀硫酸都能使紫色石蕊试液变红色 盐酸和稀硫酸中都含有大量的氢离子
3、(2009·苏州)用分子的相关知识解释下列生活中的现象,其中错误的是( )
A.热胀冷缩,说明分子的大小随温度升降而改娈
B.“酒香不怕巷子深”,说明分子在不停地运动
C.10mL酒精和10mL水混合后,体积小于20mL,说明分子间有空隙
D.湿衣服在夏天比冬天容易晾干,说明分子的运动速率随温度升高而加快
4、(2009·安徽)我国著名化学家徐光宪因在稀土元素等研究领域做出杰出贡献,荣获2008年度“国家最高科学技术奖”。铈(Ce)是一种常见的稀土元素,下列关于铈的说法错误的是( )
A.原子序数是58 B.相对原子质量是140.1
C.质子数为58 D.铈元素是非金属元素
5、(2009·福州)右图是钠元素的原子结构示意图,下列
有关钠原子的叙述不正确的是( )
A.质子数是11 B.最外层电子数为1
C.核外有3个电子层 D.核外电子总数为10
6、(2008·南京)宁宁在学习“化学元素与人体健康”后,查阅到如下资料,请你给下表的“ ”处选择恰当的选项
种类 主要食物来源
钙 奶类、绿色蔬菜、水产品、肉类、豆类
铁 肝脏、瘦肉、蛋、鱼、豆类、芹菜
锌 海产品、瘦肉、肝脏、奶类、豆类、小米
碘 海产品、加碘盐
A、元素 D、分子 C、原子 D、离子
7、(2009·青岛)下图是元素周期表中的一格,依据图中的信息得到的下列认识错误的是( )
A.该元素原子的质子数为14
B.该元素属于非金属元素
C.该元素一个原子的原子核外有14个电子
D.该元素的相对原子质量为28.09
8、(2009·苏州)参考下列物质的微观结构图示,其中由阴,阳离子构成的物质是( )
A.铜 B.干冰 C.氯化钠 D.金刚石
9、(2009·雅安)结构示意图 所表示的粒子是( )
A.原子 B.分子 C. 阴离子 D.阳离子
10、(2009·南京)原子序数为94的钚(Pu)是一种核原料,该元素一种原子的质子数和中子数之和为239,下列关于该原子的说法不正确的是( )
A.中子数为145 B.核外电子数为94
C.质子数为94 D.核电荷数为239
11、(2008·北京)决定元素种类的是( )
A、质子数 B、中子数 C、电子数 D、最外层电子数
12、(2009·重庆)下列物质中属于化合物的是( )
A.二氧化硫 B.空气 C.磷 D.碘盐
13、(2009·青岛)下列常见的物质中,属于纯净物的是( )
A.啤酒 B.食醋 C.加碘食盐 D.蒸馏水
14、(2009·黔东南州)分类学习是化学重要的学习思想,下列物质分类错误的一组是( )
A. H2、O2、N2 B. HCl、H2SO4、NaHSO4学
C. NaOH、KOH、NH3·H2O D. NaCl、NaHCO3、NH4Cl
15、(2009·广州)下列各组各有两种物质,它们的化学式和所属的物质类别都正确的一组是( )
物质1 物质2
名称 化学式 物质类别 名称 化学式 物质类别
A 氮气 N 非金属单质 氧化亚铁 Fe2O2 碱
B 碳酸氢钠 NaHCO3 盐 硝酸 HNO3 酸
C 硫酸钾 K2SO4 盐 五氧化二磷 P2O5 金属氧化物
D 锰 Mm 金属单质 氢氧化镁 Mg(OH)2 碱
二、填空题
16、(6分)(2009·重庆)(1)用数字和化学符号表示:2个氧原子 ,3个钠离子 。
(2)镁的原子结构示意图为 ,Mg原子在化学反应中容
易 (填“得到”或“失去”)2个电子。
17、(8分)(2009·苏州)形态各异的物质可按一定规律分类。现有以下八种物质,请选用各物质名称前的字母序号填涂在答题卡相应位置。
A.盐酸 B.氯化钾 C.氧化铜 D.淀粉
E.五氧化二磷 F.氮气 G.氢氧化钙 H.甲烷
题号 物质分类标准 字母序号 题号 物质分类标准 字母序号
(1) 金属氧化物 (5) 非金属单质
(2) 非金属氧化物 (6) 挥发性酸
(3) 易溶性盐 (7) 最简单的有机物
(4) 微溶性碱 (8) 糖类
18、(10分)(2008·西安)(1)向容积为250ml的细颈玻璃仪器(如下图所示)中加水至虚线处,再滴几滴红墨水,一段时间后,玻璃仪器中的现象是 ,说明 。
(2)继续向玻璃仪器中加酒精至凹液面最低处正好与刻线相切。塞紧玻璃塞,将玻璃仪器中液体倒转摇匀,重复2次。静置一段时间后,玻璃仪器中的现象为 ,说 明 。仪器细颈部分的作用是 。
19、(9分)(2009·眉山)化学是研究物质的结构、性质以及变化规律的科学,研究元素知识是学好化学的基础。下表包含部分元素的相关信息,完成以下填空:
(1)1869年,科学家 发现了元素周期律和元素周期表。
(2)请画出17号元素原子结构示意图 ,该元素在化学反应中比较容易 (填“得到”或“失去”)电子变成离子。
(3)上表中最活泼的金属元素与地壳中含量最多的元素组成的化合物是
(填化学式)。
20、(10分)(2008·江西)下图中的①、②是氟元素、钙元素在元素周期表中的信息,A、B、C、D是四种粒子的结构示意图。
请你回答:
(1)氟元素的相对原子质量为 ,钙元素的原子序数为 ;
(2)X= ;
(3)A、B、C、D属于同种元素的粒子是 (填序号);
(4)A粒子的化学性质与B、C、D中哪一种粒子的化学性质相似 (填序号)。
【答案】
1、A 解析:由于分子不断的运动,才能被人接触闻到
2、B 解析:一氧化碳和二氧化碳都是由碳元素和氧元素组成。
3、A 解析:热胀冷缩是由于分子间的间隔变大引起的,分子的大小是不变的。
4、D 解析:金属元素的名称都有“钅”字旁,铈属于金属元素。
5、D 解析:从结构示意图中可知核外电子总数为2+8+1=11个。
6、A 解析:生活中的物质成分比较复杂,我们通常所说的物质组成都是指物质的元素组成,是通过元素组成来说明其成分或比较其含量的。
7、D 解析:相对原子质量是针对原子而言的,不能理解成元素的相对原子质量。
8、C 解析:铜和金刚石由原子构成,干冰由分子构成。
9、D 解析:原子核外由18个电子,核内由17个质子,所以其带一个单位的负电荷,属于阴离子。
10、D 解析:原子中原子序数=质子数=电子数=核电荷数。
11、A 解析:元素是指具有相同核电荷数(即质子数)的同一类原子的总称。可见一种元素与另一种元素的本质区别是核电荷数或质子数不同,即决定元素种类的是核电荷数或质子数。
12、A 解析:化合物是含有多种元素的纯净物,BD为混合物,C只含有磷元素。
13、D 解析:啤酒中含有二氧化碳和乙醇,食醋中含有乙酸和水,加碘食盐中含有碘和氯化钠。
14、B 解析:HCl和H2SO4属于酸,NaHSO4属于盐
15、B 解析:氮气的化学式为N2; 氧化亚铁的化学式为FeO,属于金属氧化物;P2O5属于非金属氧化物;锰的化学式为Mn。
16、(1)2O 3Na+ (2)失去
解析:镁原子的最外层电子数为2,小于4个,易失去电子形成稳定结构。
17、(1)C (2)E (3)B (4)G (5)F (6)A (7)H (8)D
18、(1)整瓶水变红;分子在不断运动
(2)液面低于刻线;分子间有间隔;便于观察液面变化
解析:分子是在不断运动的,当向水中滴几滴红墨水后,红墨水分子会运动的水分子中,是整瓶水变红;由于分子间有间隔,当两种不同的液体相互混合时,它们的分子相互渗透,彼此充满在分子间隔中,所以其体积会小于两者的体积之和,但这个差值不大,使用细颈仪器会便于观察。
19、(1)门捷列夫 (2) 得到 (3)Na2O(Na2O2)
20、(1)19.00;20 (2)8 (3) B C (4) B
解析:元素周期表中原子最下面部分为其相对原子质量,元素符合前面的数字为原子序数;D中的质子数为18,其原子中核外电子数为18,具有稳定结构,最外层电子数为8;决定元素种类的是核电荷数(即质子数),B和C的质子数都为17,所以为同种元素;元素的化学性质取决于最外层电子数,A的最外层电子数为7与B的最外层电子数相同,所以两种的化学性质相似。
【09中考模拟】
一、选择题
1、(2009·湖南模拟)我们知道,食物较长时间露置在空气中就会变质,这主要是由于空气中含有 ( )
A.氧气 B.氮气 C. 二氧化碳 D. 稀有气体
2、(2009· 镇江模拟)右图为某有机物(C9H10O3)的分子模型,该有机物是一种高效食品防腐剂。下列说法中,不正确的是( )
A.该有机物由3种元素组成
B.该有机物能减缓食品变质
C.该有机物分子中碳、氧原子的个数比为3∶1
D.该有机物中含氧元素的质量分数最小
3、(2009· 北京模拟)右图是测定空气中氧气含量的实验装置。下列叙述不正确的是( )
A.反应后燃烧匙中的红磷完全消失
B.进入瓶中水的体积约为氧气的体积
C.钟罩内气体压强的减小导致水面上升
D.反应结束后需冷却至室温再观察钟罩内的液面高度
4、(2009·厦门模拟)甲醇(化学式:CH3OH)是一种新型电池的燃料,下列关于甲醇的说法不正确的是( )
A.相对分子质量为32 B.其碳、氢、氧三种元素的质量比为3:1:4
C.100g甲醇含氧50g D.一个甲醇分子含有一个氢氧根离子
5、(2009·四川省模拟)把分别充满红棕色NO2气体和无色H2的集气瓶,按照右图A、B两种方式放置,然后把两瓶中间的玻璃片抽走,使两瓶口密合在一起(不用振荡),可观察到A中两瓶气体的颜色很快趋于一致(两气体不反应),而B中需很长时间才能达到同样的效果。不能由此现象直接得出的结论是 ( )
A.分子是不断运动的 B.分子间有间隔
C.氢气的密度比二氧化氮的密度小 D.分子由原子构成
6、(2009·河南模拟) “分子足球”C60之后,科学家又发现另一种“分子足球”N60。一定条件下N60中积累的巨大能量会在一瞬间释放出来,是未来的火箭燃料,N60属于( )
A.金属单质 B.非金属单质 C.化合物 D.混合物
7、(2009·厦门模拟)我国的“神舟六号”载人飞船已发射成功,“嫦娥”探月工程也已正式启动。据科学家预测,月球的土壤中吸附着数百万吨的氦(He—3),其原子核中质子数为2、中子数为1,每百吨氦(He—3)核聚变所释放出的能量相当于目前人类一年消耗的能量。下列关于氦(He—3)元素的说法正确的是( )
A.原子核外电子数为3 B.相对原子质量为2
C.原子结构示意图为 D.原子结构示意图为
8、(2009·上海模拟)某些花岗岩石材中含有放射性元素氡。某种氡原子的质子数为86,中子数为136,这种氡原子的核外电子数为( )
A. 50 B. 86 C. 136 D. 222
9、(2009·枣庄模拟)下列各结构示意图中,能表示阳离子的是 ( )
二、填空题
11、(2009·厦门模拟) “用微粒的眼光看世界”,是我们学习化学的重要思想方法。试根据以下材料,结合你所学知识,简要回答问题:
材料一:微波炉的工作原理是利用微波穿透食物达5cm深,使食物中的水分子产生高频率震动,并摩擦,产生大量的热量,达到运动式加热或烹饪食物的目的。
材料二:一滴水里大约有15万亿亿个水分子,如果10亿人来数一滴水里的水分子, 每人每分钟数100个,日夜不停,需要数3万多年才能完成。
材料三:某同学在课后做如图所示的实验:在一个玻璃容器中加入100mL水,向水中放入一块糖,立即在容器外壁沿液面画一水平线,过一会儿发现糖块溶解,液面比原来水平线降低了。
(1)材料一说明_____________________________;
(2)材料二说明______________________________;
(3)材料三说明______________________________;
12、(2009·厦门模拟)信息1.对于我国环境问题的现状,中国环保局长周生贤毫不掩饰自己的忧虑。他指出:在发达国家上百年时间的工业化过程中分阶段出现的环境问题,现在却在我国集中出现了。目前,我国1/5的城市空气污染严重,1/3的国土面积受到酸雨影响,近1/5的土地面积有不同程度的沙化现象,近1/3的土地面临水土流失,90%以上的天然草原退化,2007年已成为我国节能减排工作关键的一年。
信息2.下表是2007年3月31日我国部分地区的空气质量日报内容:
序号 城市 污染指数 首要污染物 空气污染指数 空气质量级别
① 北京 103 可吸入颗粒物 Ⅲ 轻微污染
② 呼和浩特 500 可吸入颗粒物 Ⅴ 重污染
③ 厦门 72 可吸入颗粒物 Ⅱ 良
④ 深圳 36 无 Ⅰ 优
回答下列问题(友情提醒:选择题可能有多个正确选项)
(1)当日空气质量最好的城市是(填序号)
(2)人类需要洁净的空气。目前我国城市空气质量日报中的污染物不包括( )
A.可吸入颗粒物 B.二氧化碳 C.二氧化氮 D.氮气
(3) 为改善空气质量,北京开展了“为首都多一个蓝天,我们每月少开一天车”的主题活动,下列说法正确的是
A.尾气不会对空气造成污染
B.每月少开一天车不会减少汽车尾气的排放
C.汽车尾气中只含有CO2和H2O
D.“为首都多一个蓝天”是每个市民的职责
(4)SO2气体是空气的主要污染物, 该气体可用氢氧化钙悬浊液吸收,生成难溶于水的亚硫酸钙(CaSO3)和水。请写出该反应的化学方程式
(5) 想一想,请说出厦门空气主要污染物的一个来源
为改善厦门的空气质量,保护蓝色美丽的天空,请提出你的一个建议
【答案】
一、选择题
1、A 解析:食物露置在空气中变质是与氧气反应
2、C 解析:D中该有机物中含氧元素的质量分数最小是错误,氢元素的质量分数最小
3、A 解析:反应后燃烧匙中的红磷完全消失是错误,红磷应有剩余
4、D 解析:D中一个甲醇分子含有一个氢氧根离子是错误,不是氢氧根离子
5、D 解析:不能证明分子由原子构成
6、B 解析:N60属于非金属单质
7、D 解析:氦(He—3)是相对原子质量是3的氦原子,质子数等于电子数为2,故选D
8、B 解析:质子数等于电子数,质子数为86,所以电子数等于86
9、A 解析:质子数大于电子数
二、填空题
11、(1)分子不断运动
(2)分子很小
(3)分子间有间隙
12 (1)④
(2) B D
(3) D
(4)SO2+Ca(OH)2 =======CaSO3+H2O
(5)粉尘 植树
【单元限时训练】
第二章单元检测
一、选择题
1、(2008·自贡)2008年初,一场大范围历史罕见的低温雨雪冰冻袭击了中国南方部分省区市,此次雪灾给我国造成了巨大的经济损失。下列说法正确的是 ( )
A、雪是一种单质 B、冰和雪的主要成分都水
C、当雨雪成为冰冻时,分子的运动就停止了
D、冰雪融化的过程是一种化学变化
2、(2008·北京) 用分子观点解释右图漫画中小女孩的话,正确的是 ( )
A.分子质量小 B.分子间有间隔
C.分子体积小 D.分子在不断运动
3、(2008·揭阳)由我国著名科学家、中国科学院院士张青莲教授主持测定了铟、铱、锑、铕等几种元素的相对原子质量新值,其中他测定核电荷数为63的铕元素的相对原子质量的新值为152。则下列说法正确的是( )
A.铕元素的原子质子数为63 B.铕元素的原子中子数为63
C.铕元素的原子核外电子数为152 D.铕元素的原子的质量为152
4、(2009·青岛)下列常见的物质中,属于纯净物的是( )
A.啤酒 B.食醋 C.加碘食盐 D.蒸馏水
5、(2009·雅安)用分子的观点对下列常见现象的解释中,不正确的是( )
A. 食物腐败——分子本身发生变化
B. 酒精挥发——分子间间隔变大
C. 花香四溢——分子不停地运动
D. 热胀冷缩——分子大小随温度变化而改变
6、(2009·南京)下列粒子结构示意图中,表示原子的是( )
7、(2009·衡阳)右图是元素周期表的一格,下列有关叙述不正确的是( )
A.锰元素的原子序数为25
B.锰元素的相对原子质量为55
C.锰元素的原子核外电子数为25
D.锰元素的原子核内中子数为25
8、(2009·扬州模拟)下列生活事实不能体现分子性质的是( )
9、(2009·成都模拟)如图是氯化氢的形成过程。从微观角度分析,下列说法不正确的是( )
A.物质全部由原子构成
B.化学变化的实质是分子破裂成原子,原子重新组合成新分子
C.化学是从原子、分子角度研究物质的组成、结构、性质及其变化
D.可由构成微粒的结构,研究物质的性质
10、(2009·黄冈)下列有关分子、原子和离子的说法正确的是( )
A.保持氧气化学性质的粒子是氧原子
B.原子的最外层电子数决定元素的种类
C.氯化钠是由离子构成的化合物
11、(2009·北京)右图是元素周期表中钠元素的信息示意图,对图中信息理解不正确的是( )
A.质子数为11 B.元素名称为钠元素
C.元素符号为Na D.核外电子数为22.99
12、(2009·茂名)下列选项中代表离子的是(说明:数字代表质子数,“+”表示原子核所带的电荷,黑点代 表核外电子)( )
13、(2009·济宁)分析钠原子、钠离子的结构示意图得到的以下说法中,错误的是:( )
A.钠原子有三个电子层,钠离子有两个电子层
B.钠原子、钠离子的质子数都为11
C.一个钠原子在化学反应中可失去一个电子,因此,钠元素为+1价
D.钠原子和钠离子不属于同一种元素
14(2008·盐城)下列对分子、原子、离子的认识,正确的是( ) ( http: / / www. )
A、分子是保持物质的最小粒子 B、原子是最小的粒子,不可再分 ( http: / / www. )
C、原子得到或失去电子后形成离子 ( http: / / www. )
D、CO2和CO性质的差异主要是由于分子间的间隔不同 ( http: / / www. )
二、填空题
15、(2009·重庆)(1)用数字和化学符号表示:2个氧原子 ,3个钠离子 。
(2)镁的原子结构示意图为 ,Mg原子在化学反应中容易
(填“得到”或“失去”)2个电子。
16、(2008·自贡)图A是两种元素在元素周期表中的信息,图B是氟原子的原子结构示意图。
(1)图A方框的横线上填的是 ,图B方框的横线上的数字是 。
(2)用化学符号和数字表示:2个氟原子 ,钠离子 。
(3)钠元素属于 (填“金属”或“非金属”)元素。
【答案】
1、 B解析:冰和雪的主要成分都水,属于化合物,分子在任何状态下都不会停止,只是运动会减慢,冰雪融化的过程没有生成新物质是物理变化,故选B
2、D
3、A解析:根据核电荷数=质子数=电子数和质子数+中子数=相对原子质量故选A
4、D
5、D解析:热胀冷缩是分子间间隔变化
6、B解析:原子是质子数=电子数
7、D
8、D
9、A解析:物质不是全部由原子构成,有分子,原子,离子等
10、C
11、D
12、C解析:原子是质子数=电子数,离子是质子数不等于电子数
13、D
14.C
二、填空题
15、(1)2O 3Na+
(2)失去
16、(1)Na 7
(2)2F Na+
(3)金属
14 Si
硅
28.09
2
8
2
+12
+2
1
+2
2
H
H
+
Cl
Cl
Cl
H
Cl
H
2
8
2
+12
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
21世纪教育网 www.21cnjy.com 精品资料·第 1 页 (共 16 页) 版权所有@21世纪教育网
同课章节目录
