常见酸和碱复习
图片预览




文档简介
课件16张PPT。常见的酸和碱执教者:时庄镇第二中学 孔志强1、什么叫酸?电离时生成的阳离子全部是氢离子的化合物叫做酸。2、什么叫碱?电离时生成的阴离子全部是氢氧根离子的化合物叫做碱。思考问题:碱:HCl HNO3 H2SO4NaOH Ca(OH)2HCl HNO3 NaOH H2SO4 Ca(OH)2 酸:复习:常见的酸和碱
3、掌握酸的通性、碱的通性及相关化学
方程式书写。
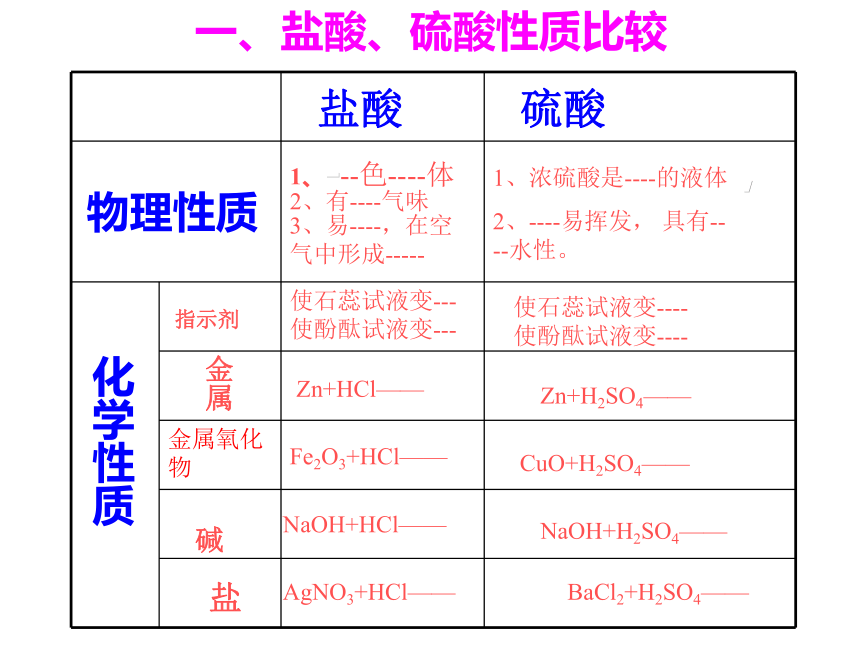
1、掌握盐酸、硫酸的性质。2、掌握氢氧化钠、氢氧化钙的性质。复习目标:一、盐酸、硫酸性质比较盐酸硫酸物理性质 化学性质指示剂金属碱盐Zn+HCl——Zn+H2SO4——Fe2O3+HCl——CuO+H2SO4——NaOH+HCl——NaOH+H2SO4——AgNO3+HCl——BaCl2+H2SO4——总结:酸的通性1、酸溶液与酸碱指示剂的作用:使的紫色石蕊 试液变——色,使无色的酚酞试液——变色。红不2、与金属的反应: 金属+酸——盐+氢气3、与金属氧化物的反应:金属氧化物+酸——盐+水4、与碱的反应:碱 + 酸——盐 + 水5、与某些盐的反应:盐 + 酸——新盐 + 新酸火碱、烧碱、苛性钠消石灰、熟石灰——色——体,——溶于水——色粉末,——溶于水,它的水溶液俗称——使石蕊试液变——色,使酚酞试液变——色蓝红使石蕊试液变——色
使酚酞试液变——色蓝红CO2+NaOH——CO2+Ca(OH)2 ——NaOH+HCl——Ca(OH)2 +HCl——CuSO4+NaOH——Na2CO3+Ca(OH)2——总结:碱的通性蓝红2、与非金属氧化物的反应非金属氧化物+碱——盐+水3、与酸的中和反应碱+酸——盐+水4、与某些盐的反应碱+盐——新碱+新盐
3、掌握酸的通性、碱的通性及相关化学
方程式书写。
1、掌握盐酸、硫酸的性质。2、掌握氢氧化钠、氢氧化钙的性质。复习目标:答案:_____C选择题 2、混有少量水蒸气的下列气体,能用氢氧化钠固体干燥的是( )
A: CO2 B: H2 C: SO2 D: HClB3、下列物质长期露置在空气中,质量会减少的是( )
A:浓盐酸 B:固体烧碱
C:大理石 D:浓硫酸A4、在氯化铁溶液中滴入烧碱溶液,观察到的现象是( )
A:有白色沉淀 B:有红褐色沉淀
C:有气泡冒出 D:有蓝色沉淀产生B5、下列四种物质中,在一定条件下能与其它三种物质发生反应的是( )
A: CuSO4 B:CO2
C:NaOH D:H2SO4C6、下列物质与稀硫酸反应不能产生氢气的是( )
A: 镁 B:银 C:铁 D:铝B7、下列各组物质混合后不产生沉淀和气体,能得到无色溶液的是( )
A:氢氧化钡溶液和稀硫酸
B:氧化铜和稀盐酸
C:大理石和稀盐酸
D:石灰水和稀盐酸D8、把纯水、稀硫酸和氢氧化钠三种无色溶液区别开的最简单的方法是( )
A:滴入酚酞试液 B:滴入石蕊试液
C:滴入氯化钡溶液 D:通入二氧化碳气体B9、下列物质不能和氢氧化钠溶液反应生成盐和水的是( )
A:三氧化硫 B:二氧化碳
C:氧化镁 D:稀硫酸C祝学习进步
心情愉快
3、掌握酸的通性、碱的通性及相关化学
方程式书写。
1、掌握盐酸、硫酸的性质。2、掌握氢氧化钠、氢氧化钙的性质。复习目标:一、盐酸、硫酸性质比较盐酸硫酸物理性质 化学性质指示剂金属碱盐Zn+HCl——Zn+H2SO4——Fe2O3+HCl——CuO+H2SO4——NaOH+HCl——NaOH+H2SO4——AgNO3+HCl——BaCl2+H2SO4——总结:酸的通性1、酸溶液与酸碱指示剂的作用:使的紫色石蕊 试液变——色,使无色的酚酞试液——变色。红不2、与金属的反应: 金属+酸——盐+氢气3、与金属氧化物的反应:金属氧化物+酸——盐+水4、与碱的反应:碱 + 酸——盐 + 水5、与某些盐的反应:盐 + 酸——新盐 + 新酸火碱、烧碱、苛性钠消石灰、熟石灰——色——体,——溶于水——色粉末,——溶于水,它的水溶液俗称——使石蕊试液变——色,使酚酞试液变——色蓝红使石蕊试液变——色
使酚酞试液变——色蓝红CO2+NaOH——CO2+Ca(OH)2 ——NaOH+HCl——Ca(OH)2 +HCl——CuSO4+NaOH——Na2CO3+Ca(OH)2——总结:碱的通性蓝红2、与非金属氧化物的反应非金属氧化物+碱——盐+水3、与酸的中和反应碱+酸——盐+水4、与某些盐的反应碱+盐——新碱+新盐
3、掌握酸的通性、碱的通性及相关化学
方程式书写。
1、掌握盐酸、硫酸的性质。2、掌握氢氧化钠、氢氧化钙的性质。复习目标:答案:_____C选择题 2、混有少量水蒸气的下列气体,能用氢氧化钠固体干燥的是( )
A: CO2 B: H2 C: SO2 D: HClB3、下列物质长期露置在空气中,质量会减少的是( )
A:浓盐酸 B:固体烧碱
C:大理石 D:浓硫酸A4、在氯化铁溶液中滴入烧碱溶液,观察到的现象是( )
A:有白色沉淀 B:有红褐色沉淀
C:有气泡冒出 D:有蓝色沉淀产生B5、下列四种物质中,在一定条件下能与其它三种物质发生反应的是( )
A: CuSO4 B:CO2
C:NaOH D:H2SO4C6、下列物质与稀硫酸反应不能产生氢气的是( )
A: 镁 B:银 C:铁 D:铝B7、下列各组物质混合后不产生沉淀和气体,能得到无色溶液的是( )
A:氢氧化钡溶液和稀硫酸
B:氧化铜和稀盐酸
C:大理石和稀盐酸
D:石灰水和稀盐酸D8、把纯水、稀硫酸和氢氧化钠三种无色溶液区别开的最简单的方法是( )
A:滴入酚酞试液 B:滴入石蕊试液
C:滴入氯化钡溶液 D:通入二氧化碳气体B9、下列物质不能和氢氧化钠溶液反应生成盐和水的是( )
A:三氧化硫 B:二氧化碳
C:氧化镁 D:稀硫酸C祝学习进步
心情愉快
