化学:2.2《分子的立体结构》课件(第一课时)(新人教版选修3)
文档属性
| 名称 | 化学:2.2《分子的立体结构》课件(第一课时)(新人教版选修3) |

|
|
| 格式 | rar | ||
| 文件大小 | 731.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2010-03-31 00:00:00 | ||
图片预览



文档简介
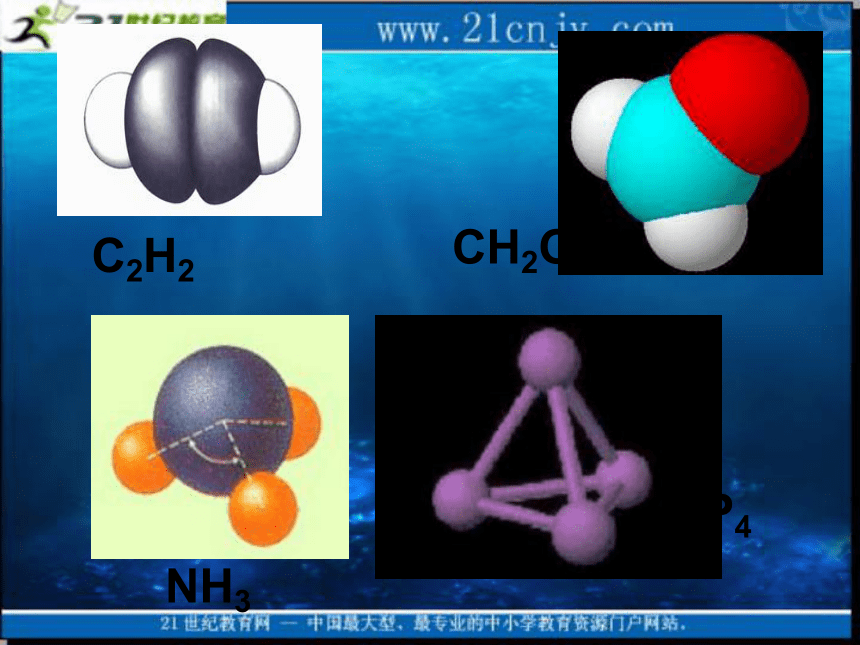
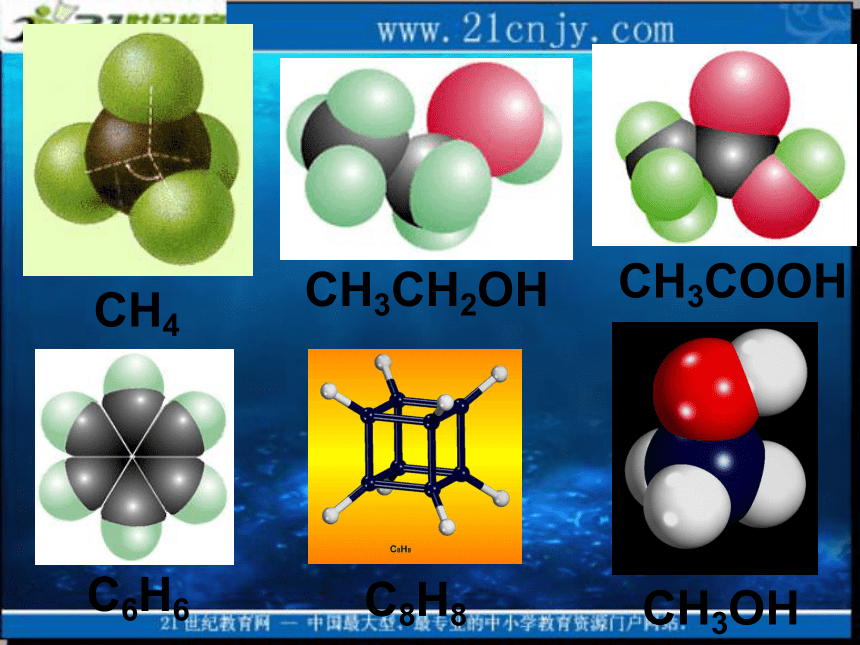
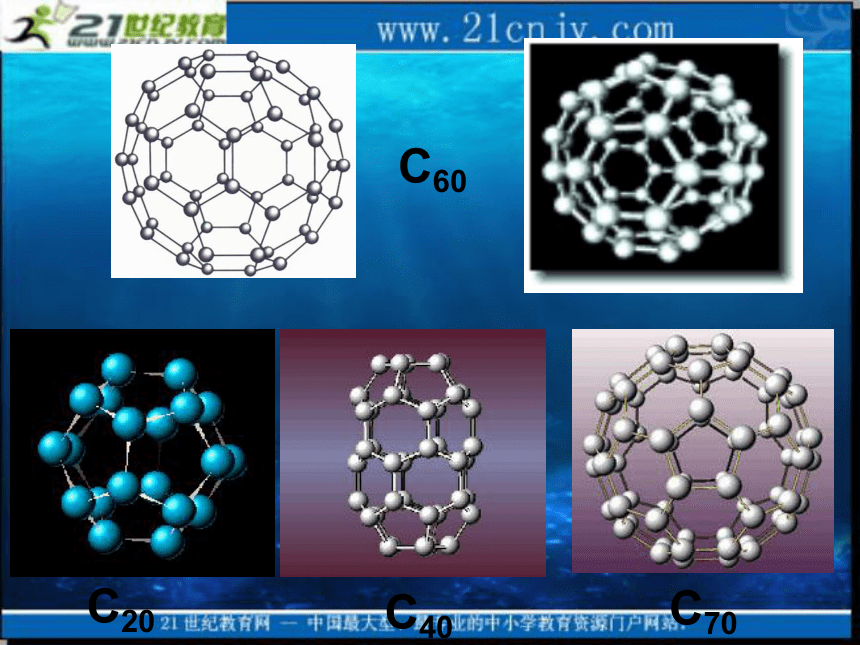
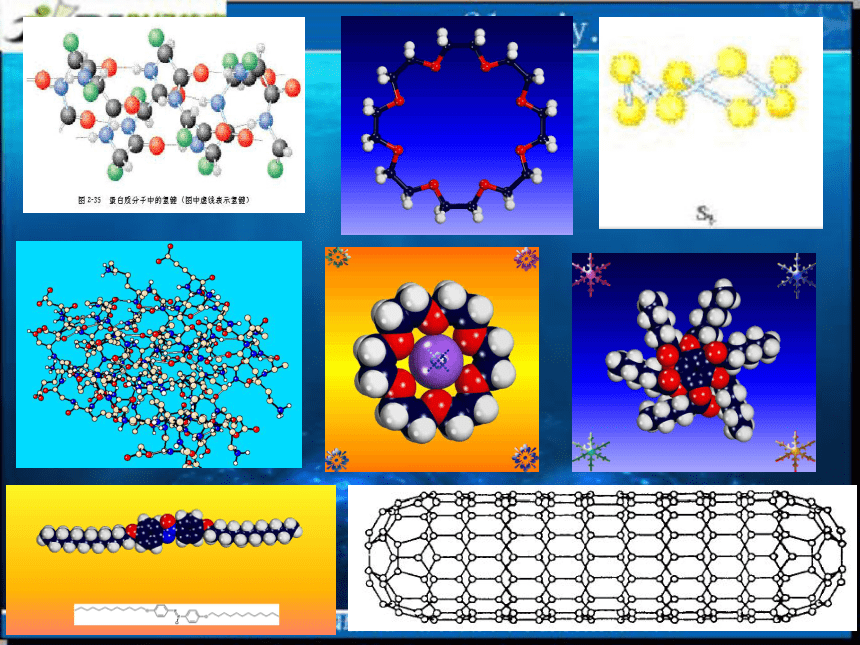
课件18张PPT。分子的立体结构(第一课时)一、形形色色的分子O2HClH2OCO2C2H2NH3CH2OP4CH4CH3CH2OHCH3COOHC6H6C8H8CH3OHC60C20C40C70思考: 同为三原子分子,CO2 和 H2O 分子的空间结构却不同,为什么? 同为四原子分子,CH2O与 NH3 分子的空间结构也不同,为什么?二、价层电子对互斥理论 (VSEPR模型)1、要点:对ABn型的分子或离子,中心原子A价层电子对(包括用于形成共价键的共用电子对和没有成键的孤对电子)之间存在排斥力,将使分子中的原子处于尽可能远的相对位置上,以使彼此之间斥力最小,分子体系能量最低。——预测分子结构的简单理论2、价层电子对互斥模型把分子分成两类:(1)中心原子上的价电子都用于成键 在这类分子中,由于价层电子对之间的相互排斥作用,它们趋向于尽可能的相互远离,成键原子的几何构型总是采取电子对排斥最小的那种结构。它们的立体结构可用中心原子周围的原子数来预测。n = 2直线形CO2、BeCl2n = 3平面三角形CH2O、BF3n = 4正四面体形CH4、CCl4(2)中心原子上有孤对电子的分子 对于这类分子,首先建立四面体模型,每个键占据一个方向(多重键只占据一个方向),孤对电子也要占据中心原子周围的空间,并参与互相排斥H2ONH3V形三角锥形直线形平面三角形正四面体V 形三角锥形小结:价层电子对互斥模型 注:价层电子对互斥模型对少数化合物判断不准,不能适用于过渡金属化合物,除非金属具有全满、半满或全空的d轨道应用反馈:0120100022233444直线形 V 形V 型平面三角形三角锥形四面体正四面体正四面体SO42-04正四面体利用价层电子对互斥理论时,首先要根据原子的最外层电子数,判断中心原子上有没有孤对电子,然后再根据中心原子结合的原子的数目,就可以判断分子的空间构型1、下列物质中,分子的立体结构与
水分子相似的是 ( )
A、CO2 B、H2S
C、PCl3 D、SiCl4B2、下列分子的立体结构,其中属于
直线型分子的是 ( )
A、H2O B、CO2
C、C2H2 D、P4BC3、为了解释和预测分子的空间构型,科
学家在归纳了许多已知的分子空间构型的
基础上,提出了一种十分简单的理论模型
—价层电子对互斥模型。这种模型把分子
分成两类:一类是 ;另一类是是 。BF3和NF3都是四个原子的分 子,BF3的中心原子是 ,NF3的中心原子是 ;BF3分子的立体构型是平面三角形,而NF3分子的立体构型是三角锥形的原因是 。
水分子相似的是 ( )
A、CO2 B、H2S
C、PCl3 D、SiCl4B2、下列分子的立体结构,其中属于
直线型分子的是 ( )
A、H2O B、CO2
C、C2H2 D、P4BC3、为了解释和预测分子的空间构型,科
学家在归纳了许多已知的分子空间构型的
基础上,提出了一种十分简单的理论模型
—价层电子对互斥模型。这种模型把分子
分成两类:一类是 ;另一类是是 。BF3和NF3都是四个原子的分 子,BF3的中心原子是 ,NF3的中心原子是 ;BF3分子的立体构型是平面三角形,而NF3分子的立体构型是三角锥形的原因是 。
