分子间作用力与物质性质
图片预览










文档简介
课件32张PPT。分子间作用力
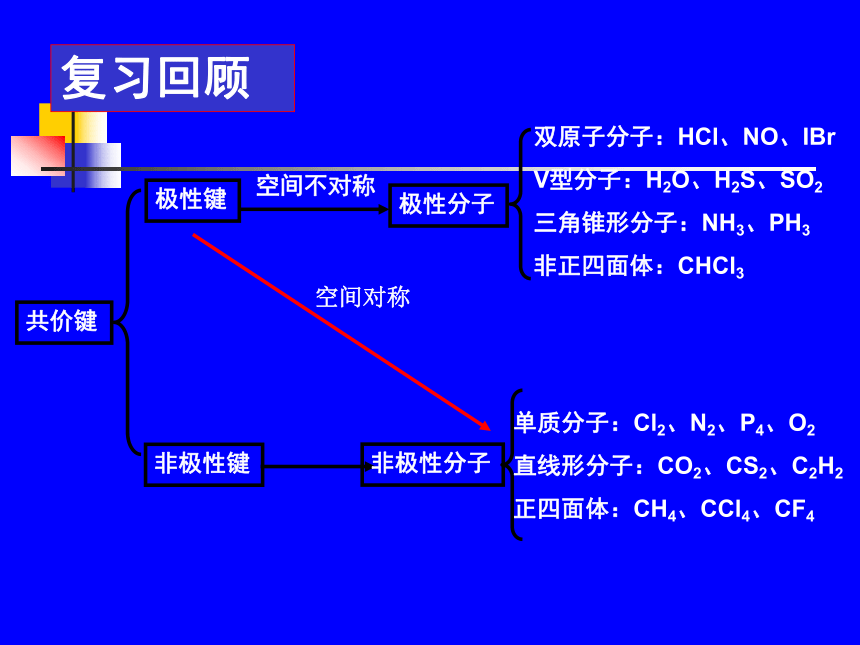
与物质性质共价键极性键非极性键空间不对称极性分子双原子分子:HCl、NO、IBr
V型分子:H2O、H2S、SO2
三角锥形分子:NH3、PH3
非正四面体:CHCl3非极性分子单质分子:Cl2、N2、P4、O2
直线形分子:CO2、CS2、C2H2
正四面体:CH4、CCl4、CF4空间对称复习回顾思考与交流:
判断下列分子中,哪些是极性分子,哪些是非极性分子?
H2、O2、P4、CO2、H2O、CH4、Cl2、HCl、C60、HCN、BF3、CH3Cl、NH3【问题探究一】冰山融化现象是物理变化还是化学变化?冰山融化过程中有没有破坏其中的化学键?那为什么冰山融化过程仍要吸收能量呢? 我们知道:分子内部原子间存在相互作用——化学键,形成或破坏化学键都伴随着能量变化。
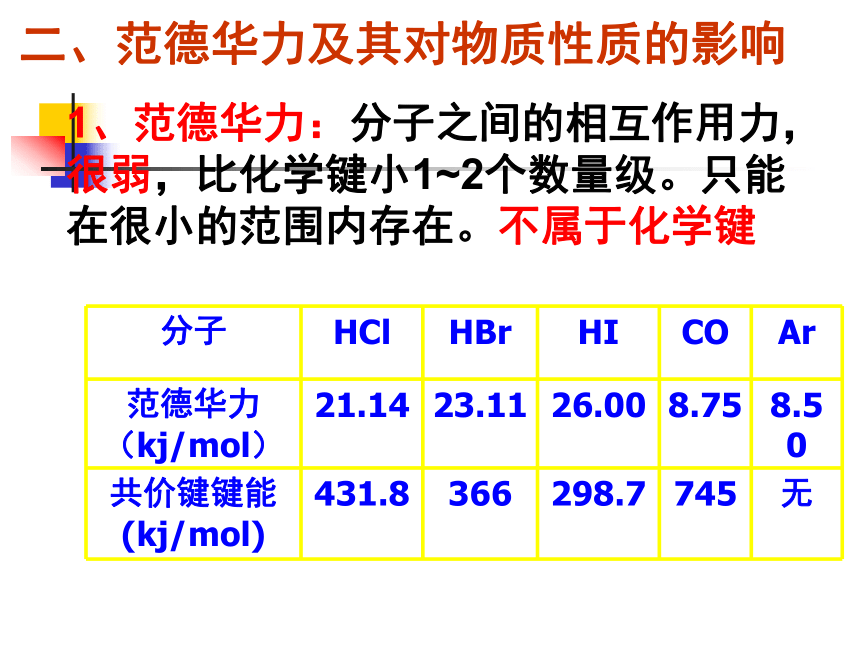
物质三相之间的转化也伴随着能量变化。这说明:分子间也存在着相互作用力。一、分子间作用力 分子间存在着将分子聚集在一起的作用力,这种作用力称为分子间作用力.常见的为范德华力和氢键【问题探究二】范德华力对物质哪些性质有影响?什么是范德华力?范德华力有什么特点?二、范德华力及其对物质性质的影响1、范德华力:分子之间的相互作用力,很弱,比化学键小1~2个数量级。只能在很小的范围内存在。不属于化学键2、范德华力的特点1)广泛存在(由分子构成的物质)2)作用力弱3)主要影响物质的物理性质(熔沸点)4)实质是电性作用,无饱和性和方向性离子键、共价键、金属键、分子间作用力都是微粒间的作用力。下列物质中,只存在一种作用力的是 ( )
A.干冰 B.NaCl C.NaOH
D.I2 E.H2SO4B
下列变化过程只是克服了范德华力的是( )
A、食盐的熔化
B、水的分解
C、碘单质的升华
D、金属钠的熔化C【问题探究三】范德华力如何影响物质的物理性质?卤族元素单质物理性质差异【总结】壁虎为什么能在天花板土爬行自如?这曾是一个困扰科学家一百多年的谜。用电子显微镜可观察到,壁虎的四足覆盖着几十万条纤细的由角蛋白构成的纳米级尺寸的毛。壁虎的足有多大吸力?实验证明,如果在一个分币的面积土布满100万条壁虎足的细毛,可以吊起20kg重的物体。近年来,有人用计算机模拟,证明壁虎的足与墙体之间的作用力在本质上是它的细毛与墙体之间的范德华力。思考?夏天经常见到许多壁虎在墙壁或天花板上爬行,却掉不下来,为什么?比较下列物质的熔沸点的高低
CH4_ CF4 _ CCl4 _ CBr4 _ CI4
H2O_ H2S _ H2Se _ H2Te 1.定义:当氢原子与电负性大的X原子以共价键结合时,它们之间的共用电子对强烈地偏向X,使H几乎成为“裸露”的质子,这样相对显正电性的H与另一分子中相对显负电性的X(或Y)中的孤对电子接近并产生相互作用,这种相互作用称氢键。 四、氢键及其对物质性质的影响实质:静电作用力和一定程度的轨道重叠作用2.表示:氢键可以用X—H…Y表示。X和Y可以是同种原子,也可以是不同种原子,但都是电负性较大、半径极小、具有孤对电子的非金属原子(一般就是N、O、F)。表示式中的实线表示共价键,虚线表示氢键。 3.氢键的键能一般小于40kJ/mol,强度介于化学键和分子间作用力之间.因此氢键不属于化学键,而属于分子间作用力的范畴。 邻羟基苯甲醛(熔点:-7℃)对羟基苯甲醛
(熔点:115-117℃)4.氢键的存在
(1)分子间氢键
(2)分子内氢键4、小结:氢键的特点:(1)作用力比范德华力大,但比化学键小得多
(2)一种特殊的分子间作用力,不是化学键
(3)具有方向性和饱和性
(4)存在范围:分子间或分子内5.氢键对物质性质的影响:
①对物质熔沸点的影响
分子间氢键使物质熔点升高
分子内氢键使物质熔点降低②对物质的溶解性的影响相似相溶──水和甲醇的相互溶解(深蓝色虚线为氢键)③解释一些反常现象:如水结成冰时,为什么体积会膨胀。讨论:尿素、醋酸、硝酸是相对分子质量相近的三种分子,但这三种物质的熔点和沸点相差比较大.尿素常温下是固体,熔点在200℃以上;醋酸的熔点为16.6℃,在温度低于16.6℃时即凝结成冰状的固体;常温下硝酸是一种具有挥发性的液体,熔点为-41.6 ℃.根据上述三种物质熔、沸点差异较大的事实,分析它们可能含有的氢键,画出示意图.下列事实与氢键有关的是 ( )
A.水加热到很高的温度都难以分解
B.水结成冰体积膨胀,密度变小
C.CH4、SiH4、GeH4 、 SnH4的熔点随相对分子质量的增大而升高
D.HF、HCl、HBr、HI的热稳定性依次减弱B固体冰中不存在的作用力是 ( )
A.离子键 B.极性键
C. 氢键 D. 范德华力 A D下列关于范德华力影响物质性质的叙述中,正确的是( )
A.范德华力是决定由分子构成物质熔、沸点高低的唯一因素
B.范德华力与物质的性质没有必然的联系
C.范德华力能够影响物质的化学性质和物理性质
D.范德华力仅是影响物质部分物理性质的一种因素1、比较下列物质的熔、沸点高低,并且说明比较的依据。 (1)金刚石晶体,氯化钠晶体,干冰 (2)CCl4,CF4 ,CBr4 (3)HF , HCl , HI 2、解释氮气分子中含有氮氮叁键,键能很大,为什么熔沸点较低?思考题:范德华力、氢键和共价键的对比
与物质性质共价键极性键非极性键空间不对称极性分子双原子分子:HCl、NO、IBr
V型分子:H2O、H2S、SO2
三角锥形分子:NH3、PH3
非正四面体:CHCl3非极性分子单质分子:Cl2、N2、P4、O2
直线形分子:CO2、CS2、C2H2
正四面体:CH4、CCl4、CF4空间对称复习回顾思考与交流:
判断下列分子中,哪些是极性分子,哪些是非极性分子?
H2、O2、P4、CO2、H2O、CH4、Cl2、HCl、C60、HCN、BF3、CH3Cl、NH3【问题探究一】冰山融化现象是物理变化还是化学变化?冰山融化过程中有没有破坏其中的化学键?那为什么冰山融化过程仍要吸收能量呢? 我们知道:分子内部原子间存在相互作用——化学键,形成或破坏化学键都伴随着能量变化。
物质三相之间的转化也伴随着能量变化。这说明:分子间也存在着相互作用力。一、分子间作用力 分子间存在着将分子聚集在一起的作用力,这种作用力称为分子间作用力.常见的为范德华力和氢键【问题探究二】范德华力对物质哪些性质有影响?什么是范德华力?范德华力有什么特点?二、范德华力及其对物质性质的影响1、范德华力:分子之间的相互作用力,很弱,比化学键小1~2个数量级。只能在很小的范围内存在。不属于化学键2、范德华力的特点1)广泛存在(由分子构成的物质)2)作用力弱3)主要影响物质的物理性质(熔沸点)4)实质是电性作用,无饱和性和方向性离子键、共价键、金属键、分子间作用力都是微粒间的作用力。下列物质中,只存在一种作用力的是 ( )
A.干冰 B.NaCl C.NaOH
D.I2 E.H2SO4B
下列变化过程只是克服了范德华力的是( )
A、食盐的熔化
B、水的分解
C、碘单质的升华
D、金属钠的熔化C【问题探究三】范德华力如何影响物质的物理性质?卤族元素单质物理性质差异【总结】壁虎为什么能在天花板土爬行自如?这曾是一个困扰科学家一百多年的谜。用电子显微镜可观察到,壁虎的四足覆盖着几十万条纤细的由角蛋白构成的纳米级尺寸的毛。壁虎的足有多大吸力?实验证明,如果在一个分币的面积土布满100万条壁虎足的细毛,可以吊起20kg重的物体。近年来,有人用计算机模拟,证明壁虎的足与墙体之间的作用力在本质上是它的细毛与墙体之间的范德华力。思考?夏天经常见到许多壁虎在墙壁或天花板上爬行,却掉不下来,为什么?比较下列物质的熔沸点的高低
CH4_ CF4 _ CCl4 _ CBr4 _ CI4
H2O_ H2S _ H2Se _ H2Te 1.定义:当氢原子与电负性大的X原子以共价键结合时,它们之间的共用电子对强烈地偏向X,使H几乎成为“裸露”的质子,这样相对显正电性的H与另一分子中相对显负电性的X(或Y)中的孤对电子接近并产生相互作用,这种相互作用称氢键。 四、氢键及其对物质性质的影响实质:静电作用力和一定程度的轨道重叠作用2.表示:氢键可以用X—H…Y表示。X和Y可以是同种原子,也可以是不同种原子,但都是电负性较大、半径极小、具有孤对电子的非金属原子(一般就是N、O、F)。表示式中的实线表示共价键,虚线表示氢键。 3.氢键的键能一般小于40kJ/mol,强度介于化学键和分子间作用力之间.因此氢键不属于化学键,而属于分子间作用力的范畴。 邻羟基苯甲醛(熔点:-7℃)对羟基苯甲醛
(熔点:115-117℃)4.氢键的存在
(1)分子间氢键
(2)分子内氢键4、小结:氢键的特点:(1)作用力比范德华力大,但比化学键小得多
(2)一种特殊的分子间作用力,不是化学键
(3)具有方向性和饱和性
(4)存在范围:分子间或分子内5.氢键对物质性质的影响:
①对物质熔沸点的影响
分子间氢键使物质熔点升高
分子内氢键使物质熔点降低②对物质的溶解性的影响相似相溶──水和甲醇的相互溶解(深蓝色虚线为氢键)③解释一些反常现象:如水结成冰时,为什么体积会膨胀。讨论:尿素、醋酸、硝酸是相对分子质量相近的三种分子,但这三种物质的熔点和沸点相差比较大.尿素常温下是固体,熔点在200℃以上;醋酸的熔点为16.6℃,在温度低于16.6℃时即凝结成冰状的固体;常温下硝酸是一种具有挥发性的液体,熔点为-41.6 ℃.根据上述三种物质熔、沸点差异较大的事实,分析它们可能含有的氢键,画出示意图.下列事实与氢键有关的是 ( )
A.水加热到很高的温度都难以分解
B.水结成冰体积膨胀,密度变小
C.CH4、SiH4、GeH4 、 SnH4的熔点随相对分子质量的增大而升高
D.HF、HCl、HBr、HI的热稳定性依次减弱B固体冰中不存在的作用力是 ( )
A.离子键 B.极性键
C. 氢键 D. 范德华力 A D下列关于范德华力影响物质性质的叙述中,正确的是( )
A.范德华力是决定由分子构成物质熔、沸点高低的唯一因素
B.范德华力与物质的性质没有必然的联系
C.范德华力能够影响物质的化学性质和物理性质
D.范德华力仅是影响物质部分物理性质的一种因素1、比较下列物质的熔、沸点高低,并且说明比较的依据。 (1)金刚石晶体,氯化钠晶体,干冰 (2)CCl4,CF4 ,CBr4 (3)HF , HCl , HI 2、解释氮气分子中含有氮氮叁键,键能很大,为什么熔沸点较低?思考题:范德华力、氢键和共价键的对比
