物质的检测(第一课时)
图片预览







文档简介
课件24张PPT。第三单元 物质的检测课题一 物质的检验物质的检测——检测物质的组成元素和结构
(官能团)。——检测某组分(元素)的准确
含量。——测定物质的内部结构。定性检测定量检测结构测定思考与交流P321、试从我们学习过的化学知识及生活常识中,举例说明物质的性质与物质的组成、结构、存在状态等有关。H2O2和H2O,分子组成不同,性质不同;金属和其合金,浓硫酸和稀硫酸,物质成分不同,性质不同;金刚石和石墨,有机物的各种同分异构体,其结构不同,性质不同;另外,物质的性质与其聚集状态也有关系,如溶液和胶体、悬浊液、乳浊液的性质不同。?2、冬季供暖锅炉房备有检测水质软化程度的仪器、试剂,你认为这种检测的目的何在,该检测是属于定性检测还是定量检测。思考与交流P32供暖锅炉用水经常检验水质软化的程度,是为了避免在锅炉中产生较多的水垢,浪费燃料;防止锅炉水垢沉积过多引起锅炉爆炸。需要经常定量检测水中Ca2+、 Mg2+的含量。
?课题一 物质的检验物质检测的原理:
根据物质的性质(物理、化学性质),使被检物质与已知试剂反应,转变为某种已知的物质,或产生某些特殊现象(反应中溶液颜色的改变;沉淀的生成和溶解;气体的生成和气味;火焰的焰色特征等现象),从而确定被检物质的存在。物质检测的一般步骤:
先对试样进行观察,确定其状态、颜色、气味等,然后准备试样。当试样是固体时,一般先取少量试样配成溶液,然后进行检测。在检验配好的溶液中是否含有某种离子时,应每次取少量待测溶液进行检验,不应将检测试剂直接加入到全部待测溶液中。物质检测的核心:
当溶液中有多种离子存在时,应排除离子间的相互干扰(从检验试剂加入顺序或按照性质相近与否将离子逐次分离,再分别逐一检验)。例题:某溶液中含有SO42-和Cl-,请选用合适的试剂和试剂的加入顺序确定这两种离子的存在?
方案:取少量溶液于试管中,先用稀HNO3将溶液酸化,然后滴加Ba(NO3)2溶液至过量,确定SO42-的存在,静置,向上层清液中滴加AgNO3溶液确定Cl-的存在。质谱红外光谱核磁共振波谱物质检测的方法:
1、化学方法:利用特征反应鉴定
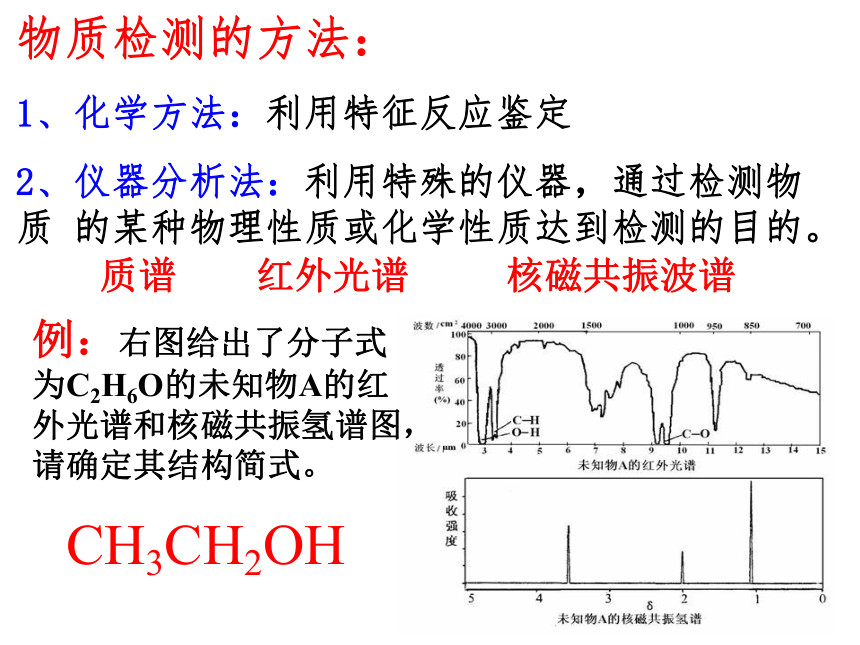
2、仪器分析法:利用特殊的仪器,通过检测物质 的某种物理性质或化学性质达到检测的目的。例:右图给出了分子式为C2H6O的未知物A的红外光谱和核磁共振氢谱图,请确定其结构简式。CH3CH2OH科学探究1、市售胃舒平药片中的辅料为淀粉,试用实验证明。2、有四种白色粉末,已知它们分别是NaCl、BaCl2、Na2CO3和无水CuSO4。试设计实验鉴别它们。科学探究样品1 样品2 样品3 样品4加蒸馏水蓝色溶液无色溶液加稀盐酸有气体产生无气体产生加稀硫酸无沉淀产生NaCl生成白色沉淀BaCl2无机气体的检验(必须掌握)O2:用试管或集气瓶收集气体,将带火星的木条插入试管或集气瓶中;木条复燃H2:点燃,在火焰上方罩一各干燥而冷的小烧杯;淡蓝色火焰,烧杯中有水雾生成NH3:(1)用湿润红色石蕊试纸检验;试纸变蓝。
(2)用玻棒蘸取浓盐酸靠近集气瓶口,打开
玻璃片;有白烟生成CO2:通入澄清石灰水;石灰水变浑浊SO2:(1)通入澄清石灰水;石灰水变浑浊
(2)通入品红溶液;品红褪色H2S:(1)用湿润的醋酸铅试纸或硝酸铅试纸检验;试纸变黑色
(2)通入CuSO4溶液;有黑色沉淀生成CO:通过灼热的氧化铜,反应产物通入澄清石灰水;黑色粉末变成光亮的红色,石灰水变浑浊NO:向待检气体中通入空气;无色气体变红棕色NO2与溴蒸气(红棕色)(1)AgNO3溶液:没有明显现象为NO2;有浅黄色沉淀生成的为溴蒸气
(2)蒸馏水:气体变为无色,溶液也无色的为NO2;气体颜色变浅,溶液呈橙色的为溴蒸气(1)加入盐酸,有无色气体生成,将气体通入品红溶液中,溶液褪色
(2)加入BaCl2溶液,有白色沉淀,再加盐酸,沉淀溶解,生成刺激性气味的气体常见阴离子的检验Cl- :先用硝酸酸化,再加硝酸银溶液;有白色沉淀出现SO42- :先用盐酸酸化,再加BaCl2溶液;有白色沉淀出现SO32-:先加入盐酸,有无色气体生成,将气体通入澄清石灰水中,有白色沉淀出现常见阴离子的检验Br- :先用硝酸酸化,再加硝酸银溶液;有淡黄沉淀出现 I- :先用硝酸酸化,再加硝酸银溶液;有黄色沉淀出现CO32-:(1)滴入紫色石蕊试剂,溶液变红
(2)滴入酚酞试剂,溶液变蓝OH-: S2- :先加入盐酸,有无色气体生成,再用湿润的Pb(AC)2试纸检验,试纸变黑常见阳离子的检验Ag+:加入盐酸有白色沉淀产生,取少量沉淀,加入浓氨水中即溶解,再加稀硝酸,白色沉淀又重新生成。Al3+:加入氨水,有白色絮状沉淀生成。该沉淀能分别溶于氢氧化钠溶液和盐酸,但不溶于氨水NH4+:加入浓NaOH溶液,微热。生成 有刺激性气味的、使湿润的红色石蕊试纸变蓝的气体。Fe3+:1.加入NaOH溶液有红褐色沉淀生成
2.用盐酸酸化,加入KSCN溶液,溶液呈血红色。Na+、K+ :焰色反应Fe2+:1.加入NaOH溶液有白色沉淀生成,迅速变为灰绿色,最终变为红褐色。
2.加入KSCN溶液,无明显现象,再滴加氯水溶液变为血红色。常见阳离子的检验注意:1、对于含有多种不同离子的混合物,若各物质离子间的特征反应互不干扰,则只需取样一次,然后逐级检验。2、对于含有多种不同离子的混合物,若各物质离子间的特征反应有干扰,则需先利用沉淀反应使离子分离,然后分组检验1、在未知液中加入AgNO3溶液有白色沉淀生成,加入稀硝酸后,沉淀部分溶解,有无色无味的气体生成,将气体通人澄清石灰水,石灰水变浑浊,由此判断水溶液中含有( )
A.Cl-,SO42- B.Cl-,NO3- C.Cl-,CO32- D.Cl-,OH-
2、下列各组物质的稀溶液相互反应,无论是前者滴入后者,还是后者滴入前者,反应现象都相同的是( )
A.Ba(OH)2和NaHSO4 B . AlCl3和NaOH C.NaAlO2和H2SO4 D.Na2CO3和HCl
C课堂练习A 3、证明某溶液中只含有Fe2+而不含Fe3+的实验方法是( )
A.先滴加氯水,再滴加KSCN溶液后显红色
B.先滴加KSCN,不显红色,再滴加氯水后显红色
C.滴加NaOH溶液,先产生白色沉淀,后变灰绿,最后呈红褐色
D.只需滴加KSCN溶液
B4、在BaCl2的水溶液中通入SO2末见沉淀,把其分成
两份,向其中一份中A加入NH3,另一份B加入Cl2则
( )
A.只有中A产生沉淀BaSO4 B.只有中产生沉淀
C.都产生沉淀 D.都不产生沉淀 C4、下列各组离子可能大量共存的是( )
A.pH=1的溶液中: Fe2+、Al3+、HCO3-、MnO4-
B.能与金属反应放出氢气的溶液中:K+、SO42-、Cl-、NH4+
C.含有大量OH-的无色溶液中:Na+、Cu2+、AlO2-、SiO32-
D.pH=7的溶液中:Fe3+、Cu2+、Cl-、SO42-
B再见!
(官能团)。——检测某组分(元素)的准确
含量。——测定物质的内部结构。定性检测定量检测结构测定思考与交流P321、试从我们学习过的化学知识及生活常识中,举例说明物质的性质与物质的组成、结构、存在状态等有关。H2O2和H2O,分子组成不同,性质不同;金属和其合金,浓硫酸和稀硫酸,物质成分不同,性质不同;金刚石和石墨,有机物的各种同分异构体,其结构不同,性质不同;另外,物质的性质与其聚集状态也有关系,如溶液和胶体、悬浊液、乳浊液的性质不同。?2、冬季供暖锅炉房备有检测水质软化程度的仪器、试剂,你认为这种检测的目的何在,该检测是属于定性检测还是定量检测。思考与交流P32供暖锅炉用水经常检验水质软化的程度,是为了避免在锅炉中产生较多的水垢,浪费燃料;防止锅炉水垢沉积过多引起锅炉爆炸。需要经常定量检测水中Ca2+、 Mg2+的含量。
?课题一 物质的检验物质检测的原理:
根据物质的性质(物理、化学性质),使被检物质与已知试剂反应,转变为某种已知的物质,或产生某些特殊现象(反应中溶液颜色的改变;沉淀的生成和溶解;气体的生成和气味;火焰的焰色特征等现象),从而确定被检物质的存在。物质检测的一般步骤:
先对试样进行观察,确定其状态、颜色、气味等,然后准备试样。当试样是固体时,一般先取少量试样配成溶液,然后进行检测。在检验配好的溶液中是否含有某种离子时,应每次取少量待测溶液进行检验,不应将检测试剂直接加入到全部待测溶液中。物质检测的核心:
当溶液中有多种离子存在时,应排除离子间的相互干扰(从检验试剂加入顺序或按照性质相近与否将离子逐次分离,再分别逐一检验)。例题:某溶液中含有SO42-和Cl-,请选用合适的试剂和试剂的加入顺序确定这两种离子的存在?
方案:取少量溶液于试管中,先用稀HNO3将溶液酸化,然后滴加Ba(NO3)2溶液至过量,确定SO42-的存在,静置,向上层清液中滴加AgNO3溶液确定Cl-的存在。质谱红外光谱核磁共振波谱物质检测的方法:
1、化学方法:利用特征反应鉴定
2、仪器分析法:利用特殊的仪器,通过检测物质 的某种物理性质或化学性质达到检测的目的。例:右图给出了分子式为C2H6O的未知物A的红外光谱和核磁共振氢谱图,请确定其结构简式。CH3CH2OH科学探究1、市售胃舒平药片中的辅料为淀粉,试用实验证明。2、有四种白色粉末,已知它们分别是NaCl、BaCl2、Na2CO3和无水CuSO4。试设计实验鉴别它们。科学探究样品1 样品2 样品3 样品4加蒸馏水蓝色溶液无色溶液加稀盐酸有气体产生无气体产生加稀硫酸无沉淀产生NaCl生成白色沉淀BaCl2无机气体的检验(必须掌握)O2:用试管或集气瓶收集气体,将带火星的木条插入试管或集气瓶中;木条复燃H2:点燃,在火焰上方罩一各干燥而冷的小烧杯;淡蓝色火焰,烧杯中有水雾生成NH3:(1)用湿润红色石蕊试纸检验;试纸变蓝。
(2)用玻棒蘸取浓盐酸靠近集气瓶口,打开
玻璃片;有白烟生成CO2:通入澄清石灰水;石灰水变浑浊SO2:(1)通入澄清石灰水;石灰水变浑浊
(2)通入品红溶液;品红褪色H2S:(1)用湿润的醋酸铅试纸或硝酸铅试纸检验;试纸变黑色
(2)通入CuSO4溶液;有黑色沉淀生成CO:通过灼热的氧化铜,反应产物通入澄清石灰水;黑色粉末变成光亮的红色,石灰水变浑浊NO:向待检气体中通入空气;无色气体变红棕色NO2与溴蒸气(红棕色)(1)AgNO3溶液:没有明显现象为NO2;有浅黄色沉淀生成的为溴蒸气
(2)蒸馏水:气体变为无色,溶液也无色的为NO2;气体颜色变浅,溶液呈橙色的为溴蒸气(1)加入盐酸,有无色气体生成,将气体通入品红溶液中,溶液褪色
(2)加入BaCl2溶液,有白色沉淀,再加盐酸,沉淀溶解,生成刺激性气味的气体常见阴离子的检验Cl- :先用硝酸酸化,再加硝酸银溶液;有白色沉淀出现SO42- :先用盐酸酸化,再加BaCl2溶液;有白色沉淀出现SO32-:先加入盐酸,有无色气体生成,将气体通入澄清石灰水中,有白色沉淀出现常见阴离子的检验Br- :先用硝酸酸化,再加硝酸银溶液;有淡黄沉淀出现 I- :先用硝酸酸化,再加硝酸银溶液;有黄色沉淀出现CO32-:(1)滴入紫色石蕊试剂,溶液变红
(2)滴入酚酞试剂,溶液变蓝OH-: S2- :先加入盐酸,有无色气体生成,再用湿润的Pb(AC)2试纸检验,试纸变黑常见阳离子的检验Ag+:加入盐酸有白色沉淀产生,取少量沉淀,加入浓氨水中即溶解,再加稀硝酸,白色沉淀又重新生成。Al3+:加入氨水,有白色絮状沉淀生成。该沉淀能分别溶于氢氧化钠溶液和盐酸,但不溶于氨水NH4+:加入浓NaOH溶液,微热。生成 有刺激性气味的、使湿润的红色石蕊试纸变蓝的气体。Fe3+:1.加入NaOH溶液有红褐色沉淀生成
2.用盐酸酸化,加入KSCN溶液,溶液呈血红色。Na+、K+ :焰色反应Fe2+:1.加入NaOH溶液有白色沉淀生成,迅速变为灰绿色,最终变为红褐色。
2.加入KSCN溶液,无明显现象,再滴加氯水溶液变为血红色。常见阳离子的检验注意:1、对于含有多种不同离子的混合物,若各物质离子间的特征反应互不干扰,则只需取样一次,然后逐级检验。2、对于含有多种不同离子的混合物,若各物质离子间的特征反应有干扰,则需先利用沉淀反应使离子分离,然后分组检验1、在未知液中加入AgNO3溶液有白色沉淀生成,加入稀硝酸后,沉淀部分溶解,有无色无味的气体生成,将气体通人澄清石灰水,石灰水变浑浊,由此判断水溶液中含有( )
A.Cl-,SO42- B.Cl-,NO3- C.Cl-,CO32- D.Cl-,OH-
2、下列各组物质的稀溶液相互反应,无论是前者滴入后者,还是后者滴入前者,反应现象都相同的是( )
A.Ba(OH)2和NaHSO4 B . AlCl3和NaOH C.NaAlO2和H2SO4 D.Na2CO3和HCl
C课堂练习A 3、证明某溶液中只含有Fe2+而不含Fe3+的实验方法是( )
A.先滴加氯水,再滴加KSCN溶液后显红色
B.先滴加KSCN,不显红色,再滴加氯水后显红色
C.滴加NaOH溶液,先产生白色沉淀,后变灰绿,最后呈红褐色
D.只需滴加KSCN溶液
B4、在BaCl2的水溶液中通入SO2末见沉淀,把其分成
两份,向其中一份中A加入NH3,另一份B加入Cl2则
( )
A.只有中A产生沉淀BaSO4 B.只有中产生沉淀
C.都产生沉淀 D.都不产生沉淀 C4、下列各组离子可能大量共存的是( )
A.pH=1的溶液中: Fe2+、Al3+、HCO3-、MnO4-
B.能与金属反应放出氢气的溶液中:K+、SO42-、Cl-、NH4+
C.含有大量OH-的无色溶液中:Na+、Cu2+、AlO2-、SiO32-
D.pH=7的溶液中:Fe3+、Cu2+、Cl-、SO42-
B再见!
同课章节目录
- 第一单元 从实验走进化学
- 课题一 实验化学起步
- 实验1-1 蓝瓶子实验
- 课题二 化学实验的绿色追求
- 实验1-2 氯气的生成及其性质的微型实验
- 实验1-3 污水处理--电浮选凝聚法
- 第二单元 物质的获取
- 课题一 物质的分离和提纯
- 实验2-1 纸上层析分离甲基橙和酚酞
- 实验2-2 海水的蒸馏
- 实验2-3 从海带中提取碘
- 课题二 物质的制备
- 实验2-4 硫酸亚铁铵的制备
- 实验2-5 乙酸乙酯的制备及反应条件探究
- 实验2-6 氢氧化铝的制备
- 第三单元 物质的检测
- 课题一 物质的检验
- 实验3-1 几种无机离子的检验
- 实验3-2 几种有机物的检验
- 实验3-3 植物体中某些元素的检验
- 课题二 物质含量的测定
- 实验3-4 酸碱滴定曲线的测绘
- 实验3-5 比色法测定抗贫血药物中铁的含量
- 实验3-6 食醋中总酸量的测定
- 第四单元 研究型实验
- 课题一 物质性质的研究
- 实验4-1 纯净物与混合物性质的比较
- 实验4-2 金属镁、铝、锌化学性质的探究
- 课题二 身边化学问题的探究
- 实验4-3 含氯消毒液性质、作用的探究
- 实验4-4 饮料的研究
