专题2第一单元化学反应速率第1课时
图片预览










文档简介
课件31张PPT。专题2 化学反应速率与化学平衡第一单元 化学反应速率(第一课时:化学反应速率的表示方法)南靖一中 沈建忠课程目标:
1、了解化学反速率的概念和表示方法。
2、通过有关化学反应速率的计算,掌握计算化学反应速率的方法,提高有关化学概念的理解能力。
3、学会根据化学方程式来判断、比较和计算化学反应速率的方法,提高比较化学反应速率及化学反应快慢的能力。
4、初步学会测定化学反应速率两种基本方法。教学重点:
1、化学反应速率的表示方法;
2、化学反应速率的运用。教学引入:
化学反应的快慢可用化学反应速率来衡量。在生产
生活中,我们希望控制化学反应速率:如钢铁生锈
、塑料的老化、食物的腐败、机体的衰老等,我们
希望其速率越慢越好;口腔补牙镶牙材料的固化、
化工产品的生产,我们希望其速率适中;泄漏到海
洋中的石油的分解、废弃有机高分子材料的降解等
我们希望能加快其反应速率。
而不同的化学反应其速率不同,请看下面图片。爆炸牛奶腐坏铁棒生锈溶洞形成很快 较快较慢很慢 定向爆破 火箭发射 煤是古代植物埋藏在地下经历了复杂的变化,经过几亿年的时间,逐渐形成的固体可燃性矿物
大多数石油是由埋藏在地下沉积层中的有机物经过几百万年在75~200摄氏度的温度下形成的 摄于1908年——几百年了我神态安详摄于1968年——这几十年我一下老了? 化学反应速率用单位时间(如每秒、每分、每小时)内反应物浓度的减小或生成物浓度的增大来表示。符号: V1.概念:一、化学反应速率2、表达式:v =?c/?t =?n/V·?t不同的化学反应快慢是不一样的。怎么样来比较和描述不同反应的快慢呢?3、单位:mol/(L·s) 或mol/(L·min)或mol/(L·h) 注:上式中⊿c表示某物质反应前后浓度的改变;
△n表示该物质反应前后物质的量的改变,⊿t表
示反应前后所需的时间;V表示反应的容器体积。也可表示为:
mol·L-1·s-1或mol·L-1·min-1 或mol·L-1·h-1 。注意:
单位中mol/(L·min)与mol/(L·s)的相互转
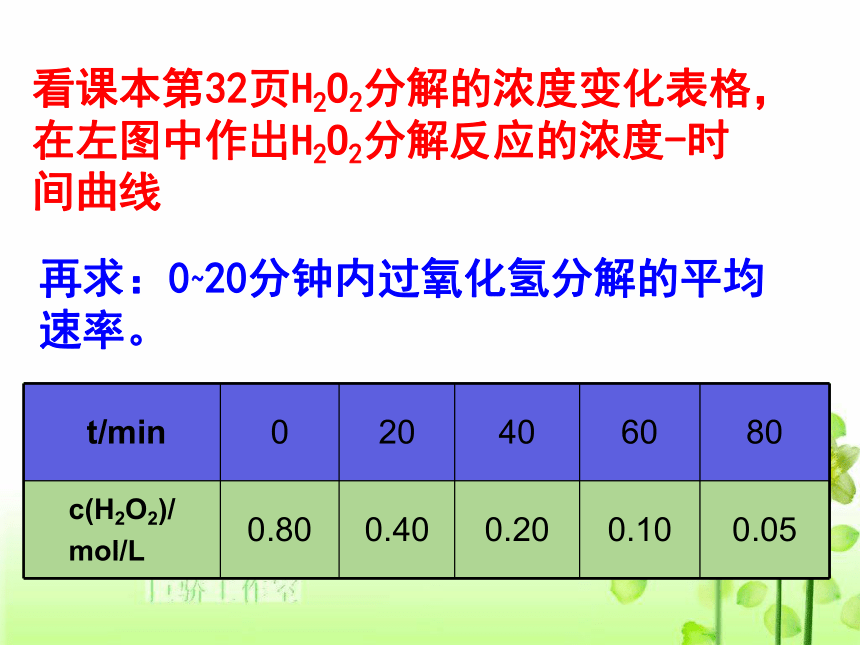
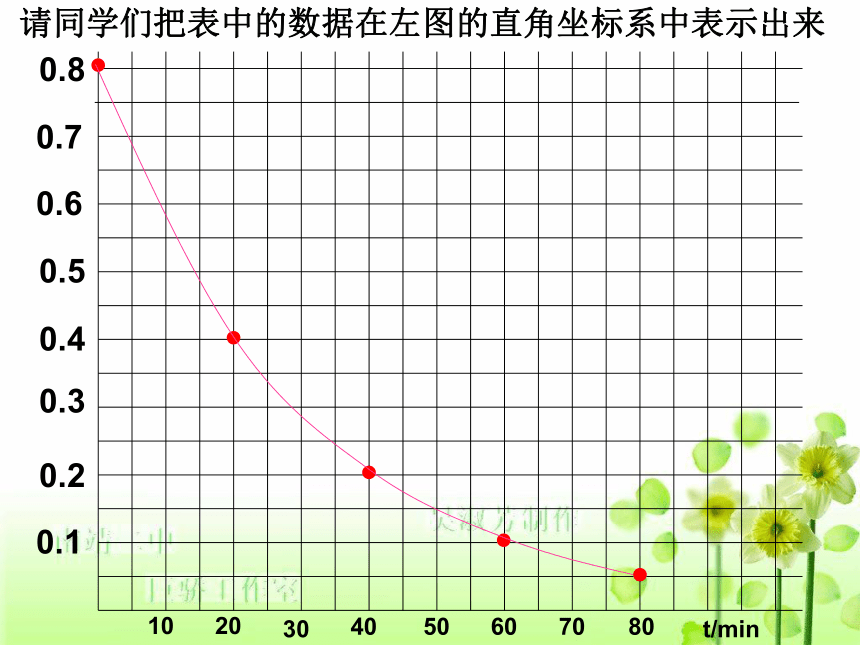
化为:X mol/(L·min)= X/60 mol/(L·s)看课本第32页H2O2分解的浓度变化表格,在左图中作出H2O2分解反应的浓度-时间曲线再求:0~20分钟内过氧化氢分解的平均速率。请同学们把表中的数据在左图的直角坐标系中表示出来H2O2浓度变化量:
0.80mol·L-1-0.40mol·L-1=0.40mol·L-1
时间变化量:20min练习:请计算20~40分钟内该反应的平均速率0.01mol·L-1·min-1请同学们根据图像分别计算任意一个20min间隔中H2O2的分解速率,并思考这些数据给你的启迪?通过计算某段时间内的化学反应速率,可见,在不同的时间内,化学反应的速率可能不同。另外,随着反应的进行,该反应速率越来越慢。我们通常计算的是某时间段内化学反应的平均速率。当Δt非常小时,就是某时刻的即时速率,在该图像上就是某时刻对应的斜率。(2)对于固体或纯液体的反应物,一般情况下其
浓度是常数,通常不用其表示反应速率。4、理解注意:(3)化学反应速率是一段时间内的平均速率而不是瞬时速率,且取正值,且化学反应速率是标量。二、通过有关化学反应速率
的计算来加深对概念的理解。例1:在10L容器中进行如下反应:
A ( g) +B ( g) == 2C( g),
2min后,B由2mol减少到1.2mol,A由1 mol减
少到0.2mol;C由0变为1.6mol。
则:B的速率 mol /(L·min),
A的速率 mol /(L·min),
C的速率 mol /(L·min),
0.040.040.08 1、 同一化学反应,在同一段时间内,可用不
同的反应物或生成物来表示,反应速率数值可
能不同,但表示的意义相同。 习题1、反应4NH3 + 5O2 === 4NO + 6H2O 在5L的密闭容器中进行,30s后,NO的物质的量增加了0.3mol,则此反应的平均速率可表示为:v (NO)=0.3/(5×30)=0.002 mol/(L·s) 2、在同一反应中,用不同的物质表示的化学反应速率数值不一定相等,但其速率之比等于化学方程式中化学计量数之比。即对于在一个容器中的一般反应
aA + bB == cC + dD来说有: VA :VB :VC :VD
== △CA :△CB :△CC :△CD
== △nA :△nB :△nC :△nD
== a :b :c :dP33 交流与讨论0.290.2900.500.2160.650.3320.3750.1660.1880.750.830.4300.5000.5800.1500.1250.1100.0950.0840.250一个化学反应既有反应物又有生成物,表示化学反应速率时,即可用某反应物的浓度变化来表示,还可以用其它反应物或生成物的浓度变化来表示。上述交流与讨论中,该反应的速率即可以用单位时间内N2O5的浓度减少来计算,还可以用单位时间内NO2或O2的浓度增加来表示。请同学们分别用三种物质来表示第3~4分钟内该反应的平均速率。V(N2O5)=0.10mol·L-1·min-1V(NO2)=0.20mol·L-1·min-1V(O2)=0.05mol·L-1·min-1这三个数字都可用于表示第3~4分钟内该反应的平均速率,也就是说,它们表示的化学反应速率是一样快的,但三者有什么关系?结论:同一反应速率可以用不同物质浓度变化表示,其数值之比等于方程式中的化学计量数之比。只要知道用某种物质来表示的化学反应速率数值,就可以换算成用其它物质来表示该反应速率。练习2:在密闭容器中,合成氨反应N2 + 3H2 = 2NH3,开始时N2浓度8mol/L,H2浓度20mol/L,5min后N2浓度变为6mol/L,求该反应的N2、H2、NH3化学反应速率。解:V (N2)== △C/△ t ==(8mol/L -6mol/L)/ 5min ==0.4 mol/(L·min)
V(H2)==1.2mol/(L·min)
V(NH3)==0.8 mol/(L·min)习题3. 已知2SO2+O2=2SO3,若反应速率分别用v(SO2) 、 v(O2) 、 v(SO3)表示,则下列式子正确的是( )
A 、 2v(SO3)=v(O2) B 、v(SO2)=v(O2)=v(SO3)
C 、 1/2v(SO2)=v(O2) D 、v(O2)=2v(SO2)C 例2、反应 A + 3B = 2C + 2D 在四种不同条件下的反应速率为:(1)v(A)=0.3mol/(L·s) (2)v(B)=0.6mol/(L·s) (3)v(C)=0.4mol/(L·s ) (4)v(D)=0.45mol/(L·s),则该反应速率的快慢顺序为—————————————。(1)>(4)>(2)=(3) :当比较用不同物质表示同一反应的反应速
率的相对大小时,在做到两个统一:(1)、统一
的速率单位;(2)、统一用同一种物质表示。3、比较反应速率的大小结论4、根据各物质的反应速率之比写出化学方程式。例3、某温度下,浓度都是1mol/L的两种气体X2和Y2,在密闭容器中反应生成气体Z,经过t min后,测得物质的量浓度分别为:c(X2)=0.4mol/L,c(Y2)=0.8mol/L ,c(Z)=0.4mol/L,则该反应的反应方程式可表示为:3X2 + Y2 === 2Z3X2 + Y2 === 2X3Y 习题4. 对于反应A+3B=2C+2D,下列数据表示不同条件的反应速率,其中反应进行得最快的是( )
v (A) =0.15mol/(L·S) B. v (B) =0.6mol/(L · S)
C. v (C) =1mol/(L · S) D. v (D) =2mol/(L · min)C习题5:根据下图回答:1、反应物是__________.2、2min内A的平均速率是________3、写出化学方程式A、B2.5mol/(L·min)习题6、某温度时,在2L容器中,x、y、z三种物质随时间的变化曲线如图所示。由图中数据分析,该反应的化学方程式是:_______________,反应开始至2min,z的平均速率是 。3x+y=2z0.05mol/(L.min)三、测定化学反应速率的两种基本方法1、有气体生成的反应 通过测定一定条件下反应生成的气体体积,再进行转换和计算出此反应的化学反应速率。2、有颜色变化的反应 用比色的方法测定溶液颜色的深浅,再根据溶液颜色与反应物浓度(或生成物浓度)的关系,换算成反应物(或生成物)在不同反应时刻的浓度,从而计算出此反应的化学反应速率。完成P34页:活动与探究课堂小结化学反应速率概念表示方法:数学表达式、单位理解注意事项化学反应速率的计算化学反应速率大小比较化学反应速率的测定1.在某一化学反应里,反应物A的浓度在10s内从4.0mol/L变成1.0mol/L,在这10s内A的化学反应速率为______________________.2.向4L容器中充入0.7molSO2和0.4molO2,4s末测得剩余SO2是0.3mol,则v(SO2)=_______.v(A)=0.3mol/(L·s)v(SO2)=0.025mol/(L·s)课堂习题3、对于可逆反应N2+3H2 2NH3下列各项所表示的反应速率最快的是
A.V(N2)=0.01mol/(L·S)
B.V(H2)=0.2mol/(L·S)
C.V(H2)=0.6mol/(L·min)
D.V(NH3)=1.2mol/(L·min)B4、某化合物A的蒸气1mol充入0.5L容器中加热分解:2A(g)=B(g)+nC(g),反应到3min时,容器内A的浓度变为0.8mol/L,测得这段时间内,平均速率v(c)=0.6mol/ (L.min),则化学反应方程式中n值为_____, v(B)=_______mol/(L.min)。30.2
1、了解化学反速率的概念和表示方法。
2、通过有关化学反应速率的计算,掌握计算化学反应速率的方法,提高有关化学概念的理解能力。
3、学会根据化学方程式来判断、比较和计算化学反应速率的方法,提高比较化学反应速率及化学反应快慢的能力。
4、初步学会测定化学反应速率两种基本方法。教学重点:
1、化学反应速率的表示方法;
2、化学反应速率的运用。教学引入:
化学反应的快慢可用化学反应速率来衡量。在生产
生活中,我们希望控制化学反应速率:如钢铁生锈
、塑料的老化、食物的腐败、机体的衰老等,我们
希望其速率越慢越好;口腔补牙镶牙材料的固化、
化工产品的生产,我们希望其速率适中;泄漏到海
洋中的石油的分解、废弃有机高分子材料的降解等
我们希望能加快其反应速率。
而不同的化学反应其速率不同,请看下面图片。爆炸牛奶腐坏铁棒生锈溶洞形成很快 较快较慢很慢 定向爆破 火箭发射 煤是古代植物埋藏在地下经历了复杂的变化,经过几亿年的时间,逐渐形成的固体可燃性矿物
大多数石油是由埋藏在地下沉积层中的有机物经过几百万年在75~200摄氏度的温度下形成的 摄于1908年——几百年了我神态安详摄于1968年——这几十年我一下老了? 化学反应速率用单位时间(如每秒、每分、每小时)内反应物浓度的减小或生成物浓度的增大来表示。符号: V1.概念:一、化学反应速率2、表达式:v =?c/?t =?n/V·?t不同的化学反应快慢是不一样的。怎么样来比较和描述不同反应的快慢呢?3、单位:mol/(L·s) 或mol/(L·min)或mol/(L·h) 注:上式中⊿c表示某物质反应前后浓度的改变;
△n表示该物质反应前后物质的量的改变,⊿t表
示反应前后所需的时间;V表示反应的容器体积。也可表示为:
mol·L-1·s-1或mol·L-1·min-1 或mol·L-1·h-1 。注意:
单位中mol/(L·min)与mol/(L·s)的相互转
化为:X mol/(L·min)= X/60 mol/(L·s)看课本第32页H2O2分解的浓度变化表格,在左图中作出H2O2分解反应的浓度-时间曲线再求:0~20分钟内过氧化氢分解的平均速率。请同学们把表中的数据在左图的直角坐标系中表示出来H2O2浓度变化量:
0.80mol·L-1-0.40mol·L-1=0.40mol·L-1
时间变化量:20min练习:请计算20~40分钟内该反应的平均速率0.01mol·L-1·min-1请同学们根据图像分别计算任意一个20min间隔中H2O2的分解速率,并思考这些数据给你的启迪?通过计算某段时间内的化学反应速率,可见,在不同的时间内,化学反应的速率可能不同。另外,随着反应的进行,该反应速率越来越慢。我们通常计算的是某时间段内化学反应的平均速率。当Δt非常小时,就是某时刻的即时速率,在该图像上就是某时刻对应的斜率。(2)对于固体或纯液体的反应物,一般情况下其
浓度是常数,通常不用其表示反应速率。4、理解注意:(3)化学反应速率是一段时间内的平均速率而不是瞬时速率,且取正值,且化学反应速率是标量。二、通过有关化学反应速率
的计算来加深对概念的理解。例1:在10L容器中进行如下反应:
A ( g) +B ( g) == 2C( g),
2min后,B由2mol减少到1.2mol,A由1 mol减
少到0.2mol;C由0变为1.6mol。
则:B的速率 mol /(L·min),
A的速率 mol /(L·min),
C的速率 mol /(L·min),
0.040.040.08 1、 同一化学反应,在同一段时间内,可用不
同的反应物或生成物来表示,反应速率数值可
能不同,但表示的意义相同。 习题1、反应4NH3 + 5O2 === 4NO + 6H2O 在5L的密闭容器中进行,30s后,NO的物质的量增加了0.3mol,则此反应的平均速率可表示为:v (NO)=0.3/(5×30)=0.002 mol/(L·s) 2、在同一反应中,用不同的物质表示的化学反应速率数值不一定相等,但其速率之比等于化学方程式中化学计量数之比。即对于在一个容器中的一般反应
aA + bB == cC + dD来说有: VA :VB :VC :VD
== △CA :△CB :△CC :△CD
== △nA :△nB :△nC :△nD
== a :b :c :dP33 交流与讨论0.290.2900.500.2160.650.3320.3750.1660.1880.750.830.4300.5000.5800.1500.1250.1100.0950.0840.250一个化学反应既有反应物又有生成物,表示化学反应速率时,即可用某反应物的浓度变化来表示,还可以用其它反应物或生成物的浓度变化来表示。上述交流与讨论中,该反应的速率即可以用单位时间内N2O5的浓度减少来计算,还可以用单位时间内NO2或O2的浓度增加来表示。请同学们分别用三种物质来表示第3~4分钟内该反应的平均速率。V(N2O5)=0.10mol·L-1·min-1V(NO2)=0.20mol·L-1·min-1V(O2)=0.05mol·L-1·min-1这三个数字都可用于表示第3~4分钟内该反应的平均速率,也就是说,它们表示的化学反应速率是一样快的,但三者有什么关系?结论:同一反应速率可以用不同物质浓度变化表示,其数值之比等于方程式中的化学计量数之比。只要知道用某种物质来表示的化学反应速率数值,就可以换算成用其它物质来表示该反应速率。练习2:在密闭容器中,合成氨反应N2 + 3H2 = 2NH3,开始时N2浓度8mol/L,H2浓度20mol/L,5min后N2浓度变为6mol/L,求该反应的N2、H2、NH3化学反应速率。解:V (N2)== △C/△ t ==(8mol/L -6mol/L)/ 5min ==0.4 mol/(L·min)
V(H2)==1.2mol/(L·min)
V(NH3)==0.8 mol/(L·min)习题3. 已知2SO2+O2=2SO3,若反应速率分别用v(SO2) 、 v(O2) 、 v(SO3)表示,则下列式子正确的是( )
A 、 2v(SO3)=v(O2) B 、v(SO2)=v(O2)=v(SO3)
C 、 1/2v(SO2)=v(O2) D 、v(O2)=2v(SO2)C 例2、反应 A + 3B = 2C + 2D 在四种不同条件下的反应速率为:(1)v(A)=0.3mol/(L·s) (2)v(B)=0.6mol/(L·s) (3)v(C)=0.4mol/(L·s ) (4)v(D)=0.45mol/(L·s),则该反应速率的快慢顺序为—————————————。(1)>(4)>(2)=(3) :当比较用不同物质表示同一反应的反应速
率的相对大小时,在做到两个统一:(1)、统一
的速率单位;(2)、统一用同一种物质表示。3、比较反应速率的大小结论4、根据各物质的反应速率之比写出化学方程式。例3、某温度下,浓度都是1mol/L的两种气体X2和Y2,在密闭容器中反应生成气体Z,经过t min后,测得物质的量浓度分别为:c(X2)=0.4mol/L,c(Y2)=0.8mol/L ,c(Z)=0.4mol/L,则该反应的反应方程式可表示为:3X2 + Y2 === 2Z3X2 + Y2 === 2X3Y 习题4. 对于反应A+3B=2C+2D,下列数据表示不同条件的反应速率,其中反应进行得最快的是( )
v (A) =0.15mol/(L·S) B. v (B) =0.6mol/(L · S)
C. v (C) =1mol/(L · S) D. v (D) =2mol/(L · min)C习题5:根据下图回答:1、反应物是__________.2、2min内A的平均速率是________3、写出化学方程式A、B2.5mol/(L·min)习题6、某温度时,在2L容器中,x、y、z三种物质随时间的变化曲线如图所示。由图中数据分析,该反应的化学方程式是:_______________,反应开始至2min,z的平均速率是 。3x+y=2z0.05mol/(L.min)三、测定化学反应速率的两种基本方法1、有气体生成的反应 通过测定一定条件下反应生成的气体体积,再进行转换和计算出此反应的化学反应速率。2、有颜色变化的反应 用比色的方法测定溶液颜色的深浅,再根据溶液颜色与反应物浓度(或生成物浓度)的关系,换算成反应物(或生成物)在不同反应时刻的浓度,从而计算出此反应的化学反应速率。完成P34页:活动与探究课堂小结化学反应速率概念表示方法:数学表达式、单位理解注意事项化学反应速率的计算化学反应速率大小比较化学反应速率的测定1.在某一化学反应里,反应物A的浓度在10s内从4.0mol/L变成1.0mol/L,在这10s内A的化学反应速率为______________________.2.向4L容器中充入0.7molSO2和0.4molO2,4s末测得剩余SO2是0.3mol,则v(SO2)=_______.v(A)=0.3mol/(L·s)v(SO2)=0.025mol/(L·s)课堂习题3、对于可逆反应N2+3H2 2NH3下列各项所表示的反应速率最快的是
A.V(N2)=0.01mol/(L·S)
B.V(H2)=0.2mol/(L·S)
C.V(H2)=0.6mol/(L·min)
D.V(NH3)=1.2mol/(L·min)B4、某化合物A的蒸气1mol充入0.5L容器中加热分解:2A(g)=B(g)+nC(g),反应到3min时,容器内A的浓度变为0.8mol/L,测得这段时间内,平均速率v(c)=0.6mol/ (L.min),则化学反应方程式中n值为_____, v(B)=_______mol/(L.min)。30.2
