化学精品课件:化学反应速率与化学平衡复习(2)
文档属性
| 名称 | 化学精品课件:化学反应速率与化学平衡复习(2) |

|
|
| 格式 | rar | ||
| 文件大小 | 164.4KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 其它版本 | ||
| 科目 | 化学 | ||
| 更新时间 | 2010-07-22 00:00:00 | ||
图片预览









文档简介
课件35张PPT。一、化学反应速率和化学平衡 主要知识点 化学反应速度化学平衡化学反应速率是研究在单位时间内
反应物或生成物浓度的变化。 化学平衡是研究反应进行的方向
和反应进行的程度(转化率).化学反应速率、平衡图象分析一 化学反应速度1.反应速率的表示: A(g) + 3B (S) 2C (g) 起始浓度
转化浓度
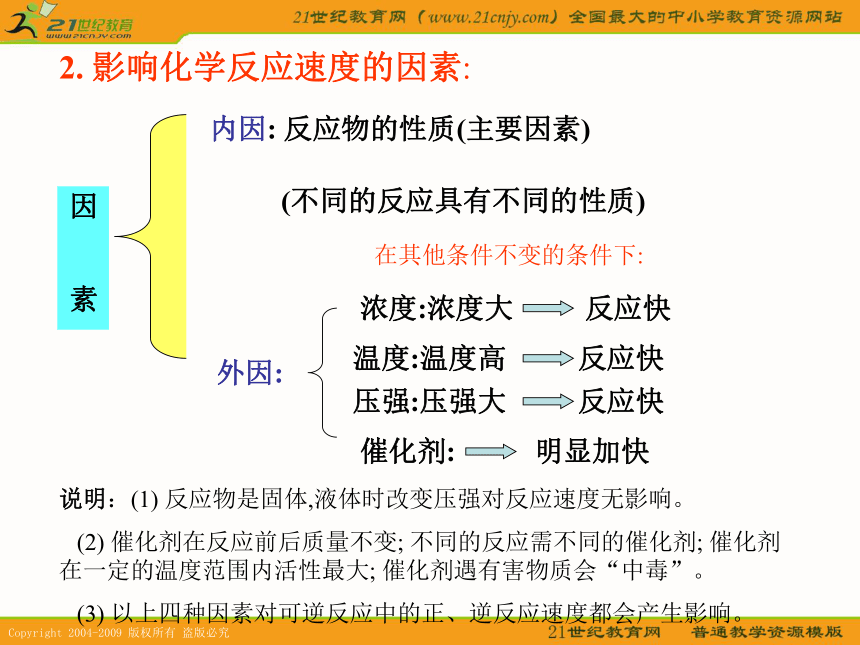
5分钟末的浓度+ 0.5-0.25 ///0.25 ///( mol/L )(mol/L·分) (mol/L·分)VA : VC = 1 : 22. 影响化学反应速度的因素:因 素内因: 反应物的性质(主要因素)(不同的反应具有不同的性质)
外因:温度:温度高 反应快浓度:浓度大 反应快压强:压强大 反应快催化剂: 明显加快在其他条件不变的条件下:说明:(1) 反应物是固体,液体时改变压强对反应速度无影响。
(2) 催化剂在反应前后质量不变; 不同的反应需不同的催化剂; 催化剂 在一定的温度范围内活性最大; 催化剂遇有害物质会“中毒”。
(3) 以上四种因素对可逆反应中的正、逆反应速度都会产生影响。(1)写出 Na2S2O3 溶液和 H2SO4 溶液反应的离子方程式:
DCAB巩固练习:S2O32 - + 2H + → S ↓ + SO2 ↑ + H2O1、化学平衡状态的定义:
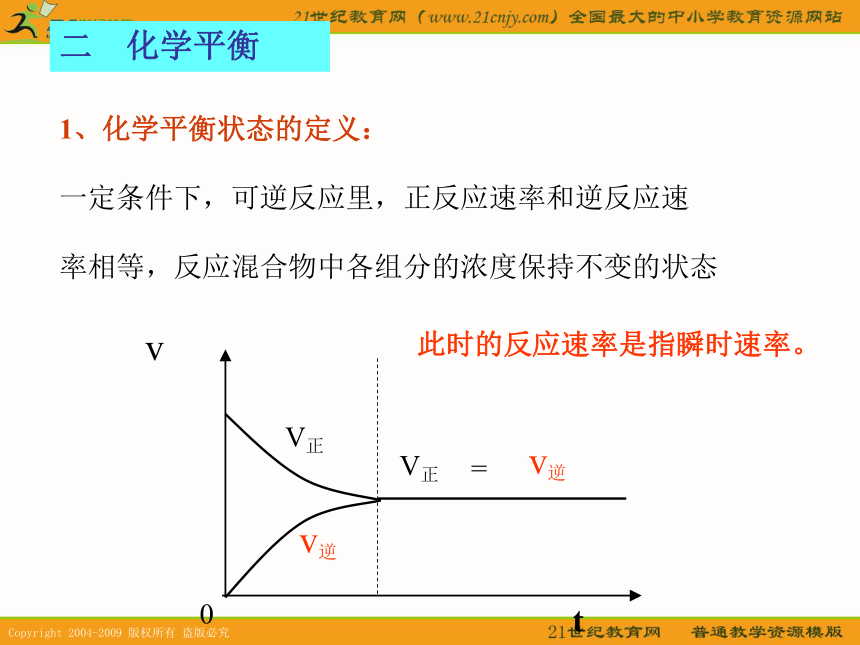
一定条件下,可逆反应里,正反应速率和逆反应速
率相等,反应混合物中各组分的浓度保持不变的状态二 化学平衡此时的反应速率是指瞬时速率。2. 平衡的条件、前提、本质、特点
逆
等
动
定
变——可逆反应(或可逆过程)
——V正 =V逆(不同的平衡对应不同的速率)
——平衡时正逆反应均未停止,只是速率相等
——平衡时,各组分含量保持恒定
——条件改变,平衡移动化学平衡的建立与途径无关。
例如:2SO2+O2 2SO3
在相同的条件下,正向投入2 mol SO2和1molO2或逆向投入
2molSO3,当反应达到平衡时,各物质的平衡含量相等。能够说明 N2 + 3H2 2NH3反应在密闭容器中已达到平衡状态的是 : ①容器内N2、H2、NH3三者共存
②容器内N2、H2、NH3三者浓度相等
③ 容器内N2、H2、NH3的浓度比恰为1:3:2
④t min内生成1molNH3同时消耗0.5molN2
⑤t min内,生成1molN2同时消耗3mol H2
⑥ 某时间内断裂3molH-H键的同时,断裂6molN-H键
⑦容器内质量不随时间的变化而变化
⑧容器内压强不随时间的变化而变化
⑨容器内密度不再发生变化
⑩容器内的平均摩尔质量不再发生变化平衡状态的判断? (⑥ ⑧ ⑩)3、化学平衡常数的应用对于mA(g)+nB(g)? pC(g)+qD(g)
K= 。对于mA(g)+nB(g)? pC(g)+qD(g) K越大,说明平衡体系中生成 ,它的正向反应进行得越 ,转化率越 ;
反之,反应程度就越不 ,转化率越 。
一般情况下K> 时,该反应进行的就比较完全。
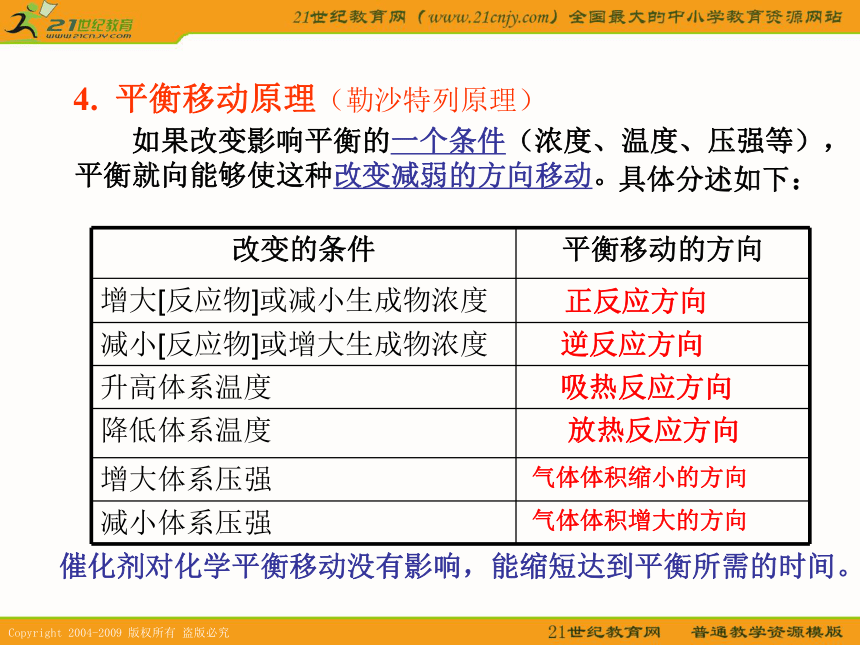
影响化学平衡常数的因素K只受 影响,与其它条件无关4. 平衡移动原理(勒沙特列原理) 如果改变影响平衡的一个条件(浓度、温度、压强等),
平衡就向能够使这种改变减弱的方向移动。具体分述如下:催化剂对化学平衡移动没有影响,能缩短达到平衡所需的时间。 正反应方向逆反应方向吸热反应方向放热反应方向气体体积缩小的方向气体体积增大的方向练习 1练习题 2ACDF练习题 3B二、速率和化学平衡图象1、化学反应速率图象分析(1)看起点和终点分清反应物和生成物,浓度减小的是反应物,浓度增大的是生成物,生成物多数是以原点为起点。看下图:
写反应方程式A + B = C213反应速率之比=反应方程式的系数之比1、化学反应速率图象分析(2). 看变化趋势分清正反应和逆反应; 分清放热反应和吸热反应; 分清“突变”和“渐变”此图表示:增大反应物浓度时,正反应、逆反应的速率变化情况练习: 看图:说出反应起始时是从正反应;还是从逆反应开始?然后是改变什么条件?化学平衡向什么方向移动?练习:看图:说出反应起始时是从正反应;还是从逆反应开始?然后是改变什么条件?化学平衡向什么方向移动?答:逆反应开始。
降温或减压。
平衡向正反应方向移动。时间V练习:看图:说出反应起始时是从正反应;还是从逆反应开始?然后是改变什么条件?化学平衡向什么方向移动?V正V逆V'正V'逆=答:正、逆反应同时开始。
加催化剂或 。
平衡不移动。时间V1、化学反应速率图象分析V正V逆看图:说出反应起始时是从正反应;还是从逆反应开始?化学平衡向什么方向移动?V时间答:逆反应开始。
平衡向正反应方向移动。V正V逆V时间此图合理吗?为什么?时间VV正V逆看图:说出反应起始时是从正反应;还是从逆反应开始?化学平衡向什么方向移动?二.化学平衡图象的解法转化率——压强——温度曲线解法:
作等
温线Tm+n p+q>Q>0等温线二.化学平衡图象的解法Pm+n p+q>Q<0看图技巧:图象中 有三个量时,“定一看二”,再看曲线的变化趋势。等压线二.化学平衡图象的解法Pm+n p+q>Q>0看图技巧:图象中 有三个量时,“定一看二”,再看曲线的变化趋势。等压线物质百分含量——压强——温度曲线物质百分含量——时间曲线看图技巧:先拐先平衡,先平衡则速率快。Q>0转化率——时间曲线看图技巧:先拐先平衡,先平衡则速率快。m+nB. 增大Y的浓度
C. 降低温度
D. 增大体系压强A.D
反应物或生成物浓度的变化。 化学平衡是研究反应进行的方向
和反应进行的程度(转化率).化学反应速率、平衡图象分析一 化学反应速度1.反应速率的表示: A(g) + 3B (S) 2C (g) 起始浓度
转化浓度
5分钟末的浓度+ 0.5-0.25 ///0.25 ///( mol/L )(mol/L·分) (mol/L·分)VA : VC = 1 : 22. 影响化学反应速度的因素:因 素内因: 反应物的性质(主要因素)(不同的反应具有不同的性质)
外因:温度:温度高 反应快浓度:浓度大 反应快压强:压强大 反应快催化剂: 明显加快在其他条件不变的条件下:说明:(1) 反应物是固体,液体时改变压强对反应速度无影响。
(2) 催化剂在反应前后质量不变; 不同的反应需不同的催化剂; 催化剂 在一定的温度范围内活性最大; 催化剂遇有害物质会“中毒”。
(3) 以上四种因素对可逆反应中的正、逆反应速度都会产生影响。(1)写出 Na2S2O3 溶液和 H2SO4 溶液反应的离子方程式:
DCAB巩固练习:S2O32 - + 2H + → S ↓ + SO2 ↑ + H2O1、化学平衡状态的定义:
一定条件下,可逆反应里,正反应速率和逆反应速
率相等,反应混合物中各组分的浓度保持不变的状态二 化学平衡此时的反应速率是指瞬时速率。2. 平衡的条件、前提、本质、特点
逆
等
动
定
变——可逆反应(或可逆过程)
——V正 =V逆(不同的平衡对应不同的速率)
——平衡时正逆反应均未停止,只是速率相等
——平衡时,各组分含量保持恒定
——条件改变,平衡移动化学平衡的建立与途径无关。
例如:2SO2+O2 2SO3
在相同的条件下,正向投入2 mol SO2和1molO2或逆向投入
2molSO3,当反应达到平衡时,各物质的平衡含量相等。能够说明 N2 + 3H2 2NH3反应在密闭容器中已达到平衡状态的是 : ①容器内N2、H2、NH3三者共存
②容器内N2、H2、NH3三者浓度相等
③ 容器内N2、H2、NH3的浓度比恰为1:3:2
④t min内生成1molNH3同时消耗0.5molN2
⑤t min内,生成1molN2同时消耗3mol H2
⑥ 某时间内断裂3molH-H键的同时,断裂6molN-H键
⑦容器内质量不随时间的变化而变化
⑧容器内压强不随时间的变化而变化
⑨容器内密度不再发生变化
⑩容器内的平均摩尔质量不再发生变化平衡状态的判断? (⑥ ⑧ ⑩)3、化学平衡常数的应用对于mA(g)+nB(g)? pC(g)+qD(g)
K= 。对于mA(g)+nB(g)? pC(g)+qD(g) K越大,说明平衡体系中生成 ,它的正向反应进行得越 ,转化率越 ;
反之,反应程度就越不 ,转化率越 。
一般情况下K> 时,该反应进行的就比较完全。
影响化学平衡常数的因素K只受 影响,与其它条件无关4. 平衡移动原理(勒沙特列原理) 如果改变影响平衡的一个条件(浓度、温度、压强等),
平衡就向能够使这种改变减弱的方向移动。具体分述如下:催化剂对化学平衡移动没有影响,能缩短达到平衡所需的时间。 正反应方向逆反应方向吸热反应方向放热反应方向气体体积缩小的方向气体体积增大的方向练习 1练习题 2ACDF练习题 3B二、速率和化学平衡图象1、化学反应速率图象分析(1)看起点和终点分清反应物和生成物,浓度减小的是反应物,浓度增大的是生成物,生成物多数是以原点为起点。看下图:
写反应方程式A + B = C213反应速率之比=反应方程式的系数之比1、化学反应速率图象分析(2). 看变化趋势分清正反应和逆反应; 分清放热反应和吸热反应; 分清“突变”和“渐变”此图表示:增大反应物浓度时,正反应、逆反应的速率变化情况练习: 看图:说出反应起始时是从正反应;还是从逆反应开始?然后是改变什么条件?化学平衡向什么方向移动?练习:看图:说出反应起始时是从正反应;还是从逆反应开始?然后是改变什么条件?化学平衡向什么方向移动?答:逆反应开始。
降温或减压。
平衡向正反应方向移动。时间V练习:看图:说出反应起始时是从正反应;还是从逆反应开始?然后是改变什么条件?化学平衡向什么方向移动?V正V逆V'正V'逆=答:正、逆反应同时开始。
加催化剂或 。
平衡不移动。时间V1、化学反应速率图象分析V正V逆看图:说出反应起始时是从正反应;还是从逆反应开始?化学平衡向什么方向移动?V时间答:逆反应开始。
平衡向正反应方向移动。V正V逆V时间此图合理吗?为什么?时间VV正V逆看图:说出反应起始时是从正反应;还是从逆反应开始?化学平衡向什么方向移动?二.化学平衡图象的解法转化率——压强——温度曲线解法:
作等
温线Tm+n p+q>Q>0等温线二.化学平衡图象的解法Pm+n p+q>Q<0看图技巧:图象中 有三个量时,“定一看二”,再看曲线的变化趋势。等压线二.化学平衡图象的解法Pm+n p+q>Q>0看图技巧:图象中 有三个量时,“定一看二”,再看曲线的变化趋势。等压线物质百分含量——压强——温度曲线物质百分含量——时间曲线看图技巧:先拐先平衡,先平衡则速率快。Q>0转化率——时间曲线看图技巧:先拐先平衡,先平衡则速率快。m+n
C. 降低温度
D. 增大体系压强A.D
同课章节目录
