陕西省延安市实验中学2009-2010学年高一下学期期末考试化学试题(无答案)
文档属性
| 名称 | 陕西省延安市实验中学2009-2010学年高一下学期期末考试化学试题(无答案) |

|
|
| 格式 | rar | ||
| 文件大小 | 107.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2010-07-26 00:00:00 | ||
图片预览


文档简介
延安市实验中学2009—2010学年度第二学期期末考试试题(卷)
高一化学
第Ⅰ卷(共60分)
(考试 时间:100分钟 总分100分)
可能用到的相对原子质量: O:16 H:1 C:12 Mg:24 Al:27 Fe:56
Na:23 S:32 Cl:35.5 Ca:40 Ag:108
第Ⅰ卷(共60分)
一、选择题(本题共20小题,每小题3分,共60分。每小题只有一个选项符合题意)
1.正确掌握化学用语是学好化学的基础。下列化学用语中正确的是 ( )
A.乙烯的结构简式为CH2CH2 B.羟基的电子式:
C.Ca2+的结构示意图为 D .乙醇的分子式:CH3CH2OH
2 .下列过程属于物理变化的是 ( )
A. 由乙烯变为聚乙烯 B.蛋白质盐析 C.O2转变为O3 D.皂化反应
3 . 某有机物的结构为 , 这种有机物不可能具有的性质是 ( )
A.能使酸性KMnO4溶液褪色 B.能发生酯化反应
C.能发生水解反应 D.能跟NaOH溶液反应
4 .下列对有机物结构的叙述中不正确的是 ( )
A.硝基、羟基、氯原子、苯环、甲基都是官能团
B.邻二氯苯不存在同分异构体说明苯分子中6个碳原子之间的键是完全一样的
C.乙烯、苯分子中所有原子共平面
D.CH2Cl2只有一种结构说明甲烷分子是正四面体结构,而不是平面正方形结构
5 . 下列混合物,能用分液漏斗分离的是 ( )21世纪教育网
A. 乙酸乙酯和水 B. 酒精和水 C. 植物油和乙醇 D. 汽油和煤油
6 .下列分子中所有原子都满足最外层为8电子结构的是 ( )
A.BF3 B.H2O
C.SiCl4 D.PCl5
7 .下列关于元素周期表的说法正确的是 ( )
A.能生成碱的金属元素都在ⅠA族
B.元素周期表有18个纵行,分列16个族,即8个主族和8个副族。
C.稀有气体元素原子的最外层电子数均为8
D.原子序数为14的元素位于元素周期表的第3周期ⅣA族
8 .下列叙述中,正确的是 ( )
A.金属阳离子被还原一定得到金属单质?
B.在氧化还原反应中,非金属单质一定是氧化剂?
C.某元素从化合态变为游离态时,该元素一定被还原?
D.含金属元素的离子不一定都是阳离子?
9 .下列结论正确的是 ( )
① 微粒半径:S2->Cl->S>F ② 氢化物的稳定性:HF>HCl>H2S>H2Te
③ 离子的还原性:S2->Cl->Br-> I- ④熔点:SiO2>NaCl>CO2
⑤ 酸性:H2SO4>HClO4>H2SeO4 ⑥碱性强弱:NaOH>Mg(OH)2>Al(OH)3
A.①②④⑥ B.①③④ C.①③ D.⑤⑥
10 .下列各组物质汽化或熔化,所克服的微粒间的作用力,属于同种类型的是 ( )
A.碘单质的升华和金刚石的熔化 B.二氧化硅和氯化钾的熔化
C.氧化铝和冰的熔化 D.乙醇和液氯的汽化
11 .下列说法中,正确的是 ( )
A.离子化合物中一定不含共价键
B.两种元素组成的化合物中一定只含有一种化学健
C.共价化合物中一定不含离子键
D.由于水分子之间存在氢键,所以水分子比较稳定
12 .下列物质只含一种分子的是 ( )
A.聚乙烯 B.分子组成为C4H10的有机物
C.氯仿(CHCl3) D.分子组成为C2H6O的有机物
13 .下列反应中,属于加成反应的是 ( )
A.CH3COOCH2CH3 + H2O CH3CH2OH + CH3COOH
B.CH2=CH2+HClCH3CH2Cl
C.2CH3CH2OH+O22CH3CHO +2H2O
D.
14 .下列关于乙醇和乙酸两种物质的说法不正确的是 ( )
A.都能发生取代反应
B.都能使紫色石蕊试液变红
C.都能发生酯化反应
D.都能和金属钠反应生成H2
15 .能使蛋白质变性的是: ( )
①硫酸钾 ②甲醛 ③硝酸钾 ④硝酸汞 ⑤氯化铵 ⑥氢氧化钠21世纪教育网
A. ②④⑥ B. ①③⑤ C. ①②③ D. ③④⑤ [来源:21世纪教育网]
16 .鉴别下列各组物质的水溶液所选的试剂(括号内)中不正确的是 ( )
A.白酒、食醋(NaHCO3溶液)
B.葡萄糖、福尔马林[新制Cu(OH)2悬浊液]
C.食盐、纯碱(盐酸)
D.淀粉、鸡蛋清(碘水)
17 . 将等质量的铜丝在酒精灯上加热后,分别插入下列物质中,放置片刻,铜丝质量增大的是 ( )
A.硝酸 B.无水乙醇
C.石灰水 D.HCl
18 . 下列有机物发生的反应属于加成反应的是 ( )
A. 乙烯使KMnO4溶液褪色
B. 乙烯水化制乙醇
C. 甲烷和氯气混合,见光
D. 用乙醇、乙酸与浓H2SO4 混合加热
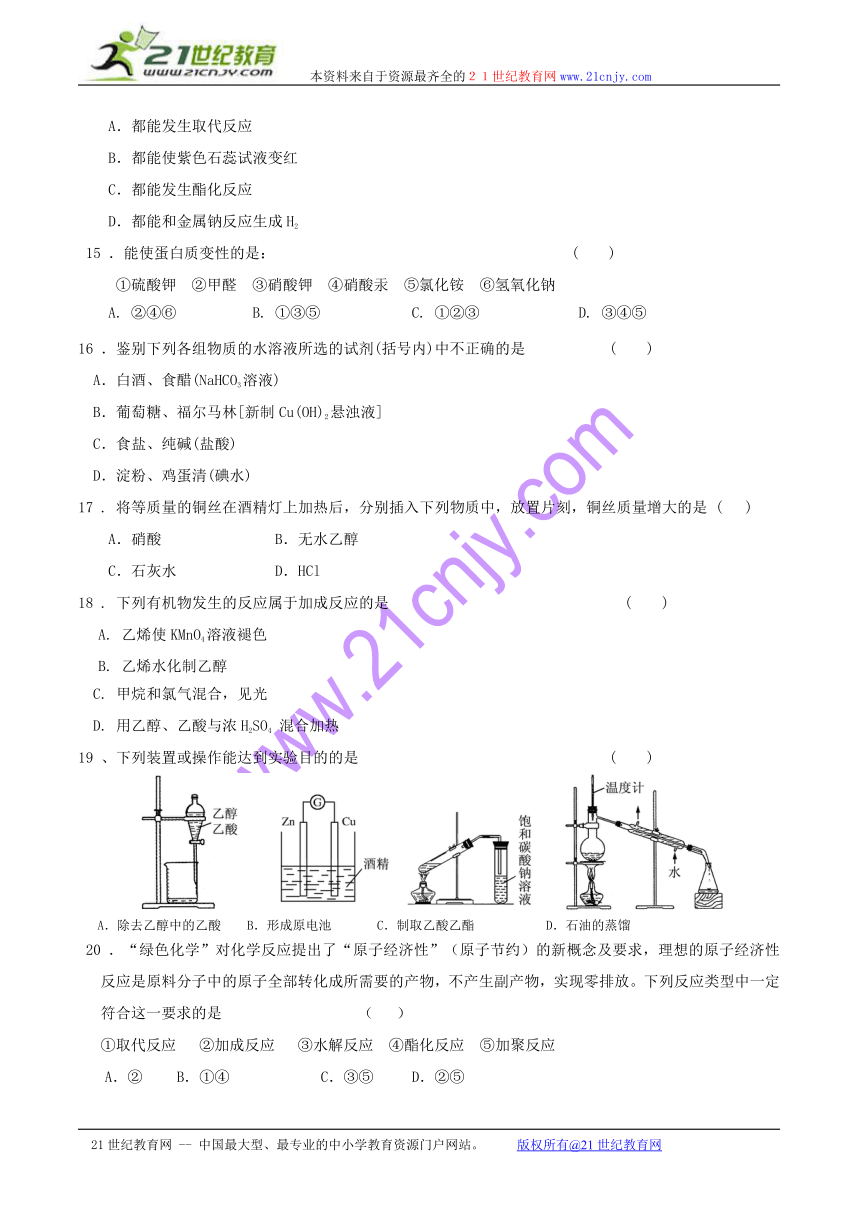
19 、下列装置或操作能达到实验目的的是 ( )
A.除去乙醇中的乙酸 B.形成原电池 C.制取乙酸乙酯 D.石油的蒸馏
20 .“绿色化学”对化学反应提出了“原子经济性”(原子节约)的新概念及要求,理想的原子经济性反应是原料分子中的原子全部转化成所需要的产物,不产生副产物,实现零排放。下列反应类型中一定符合这一要求的是 ( )
①取代反应 ②加成反应 ③水解反应 ④酯化反应 ⑤加聚反应
A.② B.①④ C.③⑤ D.②⑤
延安市实验中学2009—2010学年度第二学期期末考试试题(卷)
高一化学
注意:
卷面书写分:语、英、政、史各占3分,数、理、化、生、地各占2分
评分标准:①书写规范、字体美观、卷面整洁得3分;②书写认真、字体
工整、卷面清洁得2分;③书写较认真、卷面较整齐清洁得1分。
第Ⅱ卷(共40分)
二、填空题
21.(6分)今有两个氢气燃烧生成水的热化学方程式
H2(g) + 1/2O2(g) == H2O(g) △H=a kJ/mol
2H2(g) + O2(g) == 2H2O(l) △H=b kJ/mol
请回答下列问题:(提示:︱b︱表示b的绝对值)
(1)若2 mol H2完全燃烧生成水蒸气,则放出的热量 ︱b︱kJ(填“>”、“<”或“=”)
(2)反应热的关系:2a b(填“>”、“<”或“=”)。
(3)若已知H2(g) + 1/2O2(g) == H2O(g) △H=—242 kJ/mol ,且氧气中1mol O=O键完全断裂时吸收热量496kJ,水蒸气中1mol H—O键形成时放出热量463kJ,则氢气中1mol
H—H键断裂时吸收的热量为
22.(8分)“酒是陈的香”,这是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用下图所示装置制取乙酸乙酯。
回答下列问题:
(1)写出制取乙酸乙酯的化学反应方程式:__________________________
(2)浓硫酸的作用是:①______________;②_____________
(3)插入右边试管的导气管上接有一个球状容器,其作用为________________
(4)将接收液与乙酸乙酯分离的方法是___________________
(5)做此实验时,有时还向作反应容器的试管里加入几块碎瓷片,其目的是____________
23.(14分)A是一种重要的化工原料,A的产量可以用来衡量一个国家的石油化工水平,E是具有果香气味的烃的衍生物。A、B、C、D在一定条件下存在如下转化关系(部分反应条件、产物被省略)。
⑴A→B的反应类型是_______________;
B、D中官能团的名称分别是_______、 ________;
⑵写出反应B→C的化学方程式:_______________________________________。
⑶丁烷是由石蜡油获得A的过程中的中间产物之一,它的一种同分异构体中含有三个甲基,则这种同分异构体的结构简式:
____________________________________________。
⑷人在做过剧烈运动后,有一段时间腿和胳膊感到有酸胀或疼痛的感觉。原因之一是
。已知乳酸分子中含有与B、D中相
同的官能团,且有一个甲基,则乳酸的结构简式是 , 90 g乳酸与足量金属钠完全反应产生的气体在标准状况下的体积是 L
(5) 可用于检验有机物C的试剂是
24.(10分)现有部分短周期元素的性质或原子结构如下表:
元素编号
元素性质或原子结构
T
能形成双原子分子,原子间存在3对共用电子对
X
M层有3个电子
Y21世纪教育网
最外层电子数是最内层电子数2倍,其最高价氧化物是一种固体,用于生产光导纤维
Z
最低负价为—2价,且无最高正价
用化学符号回答以下问题:
(1) 比较:氢化物的稳定性:T Z,最高价氧化物对应水化物的酸性:T Y。(填“>”、“<”或“=”)
(2) 写出T的氢化物的电子式: 。
(3) X的最高价氧化物对应水化物与烧碱反应的离子方程式为:
(4) T、X、Y、Z四种原子的半径由大到小的顺序为: 。
5) 汽车内燃机工作时产生的高温会引起T2和Z2的反应,是导致汽车尾气中含有TZ的原因之一。汽车尾气中还含有CO气体。为避免汽车尾气中的有害气体对大气的污染,给汽车安装尾气净化装置,使尾气中的有害气体成分在催化剂作用下转化为无害气体排出,参
与大气循环。写出此反应的化学方式: 。
高一化学
第Ⅰ卷(共60分)
(考试 时间:100分钟 总分100分)
可能用到的相对原子质量: O:16 H:1 C:12 Mg:24 Al:27 Fe:56
Na:23 S:32 Cl:35.5 Ca:40 Ag:108
第Ⅰ卷(共60分)
一、选择题(本题共20小题,每小题3分,共60分。每小题只有一个选项符合题意)
1.正确掌握化学用语是学好化学的基础。下列化学用语中正确的是 ( )
A.乙烯的结构简式为CH2CH2 B.羟基的电子式:
C.Ca2+的结构示意图为 D .乙醇的分子式:CH3CH2OH
2 .下列过程属于物理变化的是 ( )
A. 由乙烯变为聚乙烯 B.蛋白质盐析 C.O2转变为O3 D.皂化反应
3 . 某有机物的结构为 , 这种有机物不可能具有的性质是 ( )
A.能使酸性KMnO4溶液褪色 B.能发生酯化反应
C.能发生水解反应 D.能跟NaOH溶液反应
4 .下列对有机物结构的叙述中不正确的是 ( )
A.硝基、羟基、氯原子、苯环、甲基都是官能团
B.邻二氯苯不存在同分异构体说明苯分子中6个碳原子之间的键是完全一样的
C.乙烯、苯分子中所有原子共平面
D.CH2Cl2只有一种结构说明甲烷分子是正四面体结构,而不是平面正方形结构
5 . 下列混合物,能用分液漏斗分离的是 ( )21世纪教育网
A. 乙酸乙酯和水 B. 酒精和水 C. 植物油和乙醇 D. 汽油和煤油
6 .下列分子中所有原子都满足最外层为8电子结构的是 ( )
A.BF3 B.H2O
C.SiCl4 D.PCl5
7 .下列关于元素周期表的说法正确的是 ( )
A.能生成碱的金属元素都在ⅠA族
B.元素周期表有18个纵行,分列16个族,即8个主族和8个副族。
C.稀有气体元素原子的最外层电子数均为8
D.原子序数为14的元素位于元素周期表的第3周期ⅣA族
8 .下列叙述中,正确的是 ( )
A.金属阳离子被还原一定得到金属单质?
B.在氧化还原反应中,非金属单质一定是氧化剂?
C.某元素从化合态变为游离态时,该元素一定被还原?
D.含金属元素的离子不一定都是阳离子?
9 .下列结论正确的是 ( )
① 微粒半径:S2->Cl->S>F ② 氢化物的稳定性:HF>HCl>H2S>H2Te
③ 离子的还原性:S2->Cl->Br-> I- ④熔点:SiO2>NaCl>CO2
⑤ 酸性:H2SO4>HClO4>H2SeO4 ⑥碱性强弱:NaOH>Mg(OH)2>Al(OH)3
A.①②④⑥ B.①③④ C.①③ D.⑤⑥
10 .下列各组物质汽化或熔化,所克服的微粒间的作用力,属于同种类型的是 ( )
A.碘单质的升华和金刚石的熔化 B.二氧化硅和氯化钾的熔化
C.氧化铝和冰的熔化 D.乙醇和液氯的汽化
11 .下列说法中,正确的是 ( )
A.离子化合物中一定不含共价键
B.两种元素组成的化合物中一定只含有一种化学健
C.共价化合物中一定不含离子键
D.由于水分子之间存在氢键,所以水分子比较稳定
12 .下列物质只含一种分子的是 ( )
A.聚乙烯 B.分子组成为C4H10的有机物
C.氯仿(CHCl3) D.分子组成为C2H6O的有机物
13 .下列反应中,属于加成反应的是 ( )
A.CH3COOCH2CH3 + H2O CH3CH2OH + CH3COOH
B.CH2=CH2+HClCH3CH2Cl
C.2CH3CH2OH+O22CH3CHO +2H2O
D.
14 .下列关于乙醇和乙酸两种物质的说法不正确的是 ( )
A.都能发生取代反应
B.都能使紫色石蕊试液变红
C.都能发生酯化反应
D.都能和金属钠反应生成H2
15 .能使蛋白质变性的是: ( )
①硫酸钾 ②甲醛 ③硝酸钾 ④硝酸汞 ⑤氯化铵 ⑥氢氧化钠21世纪教育网
A. ②④⑥ B. ①③⑤ C. ①②③ D. ③④⑤ [来源:21世纪教育网]
16 .鉴别下列各组物质的水溶液所选的试剂(括号内)中不正确的是 ( )
A.白酒、食醋(NaHCO3溶液)
B.葡萄糖、福尔马林[新制Cu(OH)2悬浊液]
C.食盐、纯碱(盐酸)
D.淀粉、鸡蛋清(碘水)
17 . 将等质量的铜丝在酒精灯上加热后,分别插入下列物质中,放置片刻,铜丝质量增大的是 ( )
A.硝酸 B.无水乙醇
C.石灰水 D.HCl
18 . 下列有机物发生的反应属于加成反应的是 ( )
A. 乙烯使KMnO4溶液褪色
B. 乙烯水化制乙醇
C. 甲烷和氯气混合,见光
D. 用乙醇、乙酸与浓H2SO4 混合加热
19 、下列装置或操作能达到实验目的的是 ( )
A.除去乙醇中的乙酸 B.形成原电池 C.制取乙酸乙酯 D.石油的蒸馏
20 .“绿色化学”对化学反应提出了“原子经济性”(原子节约)的新概念及要求,理想的原子经济性反应是原料分子中的原子全部转化成所需要的产物,不产生副产物,实现零排放。下列反应类型中一定符合这一要求的是 ( )
①取代反应 ②加成反应 ③水解反应 ④酯化反应 ⑤加聚反应
A.② B.①④ C.③⑤ D.②⑤
延安市实验中学2009—2010学年度第二学期期末考试试题(卷)
高一化学
注意:
卷面书写分:语、英、政、史各占3分,数、理、化、生、地各占2分
评分标准:①书写规范、字体美观、卷面整洁得3分;②书写认真、字体
工整、卷面清洁得2分;③书写较认真、卷面较整齐清洁得1分。
第Ⅱ卷(共40分)
二、填空题
21.(6分)今有两个氢气燃烧生成水的热化学方程式
H2(g) + 1/2O2(g) == H2O(g) △H=a kJ/mol
2H2(g) + O2(g) == 2H2O(l) △H=b kJ/mol
请回答下列问题:(提示:︱b︱表示b的绝对值)
(1)若2 mol H2完全燃烧生成水蒸气,则放出的热量 ︱b︱kJ(填“>”、“<”或“=”)
(2)反应热的关系:2a b(填“>”、“<”或“=”)。
(3)若已知H2(g) + 1/2O2(g) == H2O(g) △H=—242 kJ/mol ,且氧气中1mol O=O键完全断裂时吸收热量496kJ,水蒸气中1mol H—O键形成时放出热量463kJ,则氢气中1mol
H—H键断裂时吸收的热量为
22.(8分)“酒是陈的香”,这是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用下图所示装置制取乙酸乙酯。
回答下列问题:
(1)写出制取乙酸乙酯的化学反应方程式:__________________________
(2)浓硫酸的作用是:①______________;②_____________
(3)插入右边试管的导气管上接有一个球状容器,其作用为________________
(4)将接收液与乙酸乙酯分离的方法是___________________
(5)做此实验时,有时还向作反应容器的试管里加入几块碎瓷片,其目的是____________
23.(14分)A是一种重要的化工原料,A的产量可以用来衡量一个国家的石油化工水平,E是具有果香气味的烃的衍生物。A、B、C、D在一定条件下存在如下转化关系(部分反应条件、产物被省略)。
⑴A→B的反应类型是_______________;
B、D中官能团的名称分别是_______、 ________;
⑵写出反应B→C的化学方程式:_______________________________________。
⑶丁烷是由石蜡油获得A的过程中的中间产物之一,它的一种同分异构体中含有三个甲基,则这种同分异构体的结构简式:
____________________________________________。
⑷人在做过剧烈运动后,有一段时间腿和胳膊感到有酸胀或疼痛的感觉。原因之一是
。已知乳酸分子中含有与B、D中相
同的官能团,且有一个甲基,则乳酸的结构简式是 , 90 g乳酸与足量金属钠完全反应产生的气体在标准状况下的体积是 L
(5) 可用于检验有机物C的试剂是
24.(10分)现有部分短周期元素的性质或原子结构如下表:
元素编号
元素性质或原子结构
T
能形成双原子分子,原子间存在3对共用电子对
X
M层有3个电子
Y21世纪教育网
最外层电子数是最内层电子数2倍,其最高价氧化物是一种固体,用于生产光导纤维
Z
最低负价为—2价,且无最高正价
用化学符号回答以下问题:
(1) 比较:氢化物的稳定性:T Z,最高价氧化物对应水化物的酸性:T Y。(填“>”、“<”或“=”)
(2) 写出T的氢化物的电子式: 。
(3) X的最高价氧化物对应水化物与烧碱反应的离子方程式为:
(4) T、X、Y、Z四种原子的半径由大到小的顺序为: 。
5) 汽车内燃机工作时产生的高温会引起T2和Z2的反应,是导致汽车尾气中含有TZ的原因之一。汽车尾气中还含有CO气体。为避免汽车尾气中的有害气体对大气的污染,给汽车安装尾气净化装置,使尾气中的有害气体成分在催化剂作用下转化为无害气体排出,参
与大气循环。写出此反应的化学方式: 。
同课章节目录
