硫酸硝酸
图片预览






文档简介
课件14张PPT。第四节 硫酸硝酸和氨(一)、物理性质:纯硫酸是一种 无色 油状 液体。常用的浓硫酸质量分数是98.3%,其密度为1.84g/cm3,其物质的量浓度约为18.4mol/L。硫酸是一种高沸点 难挥发的强酸,易溶于水,能以任意比和水混溶。浓硫酸溶于水时会放出大量的热。思考:在稀释浓硫酸时,应该注意哪些地方?思考:现有封闭、体积相等的试剂瓶二个,分别装等体积的浓硫酸和浓盐酸,不用化学方法如何加以鉴别?注意:稀释浓硫酸的时候,要把浓硫酸沿着
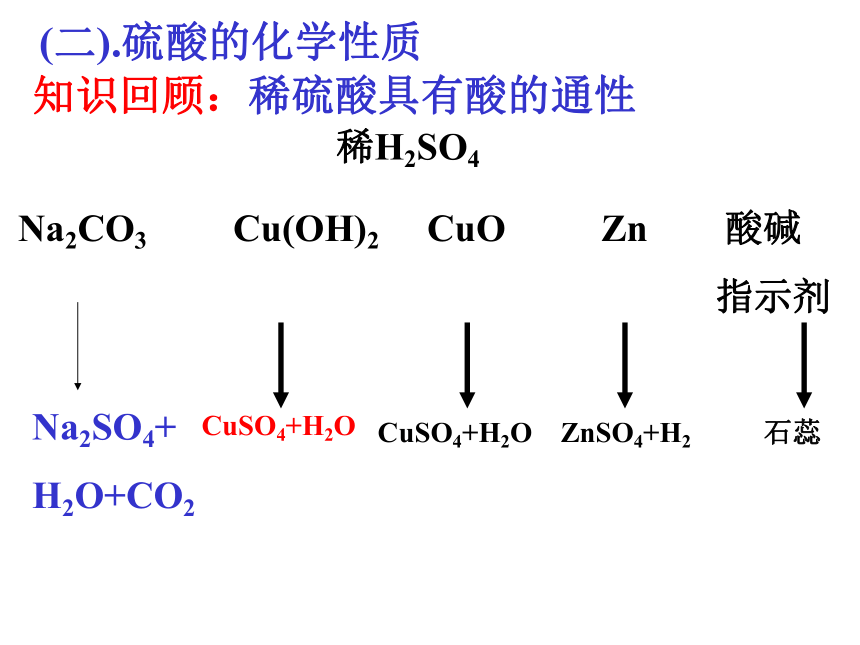
器壁 慢慢地 注入水里,并不断搅拌。知识回顾:稀硫酸具有酸的通性 Na2CO3 Cu(OH)2 CuO Zn 酸碱
指示剂稀H2SO4CuSO4+H2OCuSO4+H2OZnSO4+H2石蕊Na2SO4+
H2O+CO2(二).硫酸的化学性质思考:浓硫酸敞口放置,是怎样变质的?用途:干燥剂(干燥H2 、CO2、N2 、 O2等)1、吸水性2、脱水性:思考:浓硫酸的吸水性与脱水性有什么不同? 浓硫酸的特性浓硫酸能把含氧的有机物中的H和O 原子按照水的组成(2:1)
脱水炭化,放出热,并氧化生成的部分碳,生成CO2和SO2。3、强氧化性:思考:在这个反应中,硫酸起了什么作用?CuO+H2SO4==CuSO4+H2O(1)与金属反应体现氧化性体现酸性思考:浓硫酸在加热时能氧化铜,那么能氧化其他金属吗?浓H2SO4加热:能与大多数金属(Au、Pt除外)反应常温:能与活泼金属反应(注意:不生成H2)常温下, Fe 和Al遇到浓硫酸被钝化
(被氧化成一层致密的氧化膜,
阻止内部金属进一步被氧化。)(2)与非金属反应:问:氧化产物与还原产物的物质的量之比想一想:为什么蔗糖脱水后变得疏松多孔?问:设计一个实验检验反应产生的气体成分?〖巩固练习〗1.如何鉴别失去标签的稀硫酸和浓硫酸?请同学们提出尽可能多的方案 (1)用手掂重量(2)看有无粘性(1)在干净白纸上写字(2)加入到胆矾晶体中……..2、利用浓硫酸的脱水性3、利用浓硫酸的氧化性4、利用浓硫酸的钝化作用(3)利用浓硫酸溶于水放热1 、利用物理性质的区别二、硝酸的性质:1、物理性质:无色,易挥发、有刺激性气味的液体,能以任意比溶于水2、化学性质:(1)酸性(略)(2)氧化性:① 与金属反应(除Au和 Pt外) 反应激烈,产生红棕色气体,
溶液由无色变为绿色。Cu+4HNO3(浓) = Cu(NO3)2+2NO2 +2H2O结论:硝酸具有强的氧化性,能氧化不活泼金属。3Cu+8HNO3(稀) =3Cu(NO3)2+2NO +4H2O 反应较缓慢,产生无色气体,逸至试管口变为红棕色, 溶液由无色变为绿色。注意:Fe 和Al遇到冷的浓硝酸被钝化,被氧化成一层致密的氧化膜,情形跟浓硫酸一样。氧化性:浓硝酸>稀硝酸小结:硝酸与金属或非金属(如碳、硫等)反应时,主要是HNO3中+5价的氮得到电子,被还原成较低价氮的物质,稀硝酸的还原产物一般是NO,浓硝酸的还原产物一般是NO2,而不像盐酸与金属反应那样生成H2 3体积浓盐酸与1体积浓硝酸的混合物叫做王水,它的氧化能力更强,能溶解 金(Au )和 铂(Pt ) 体积比为 3 : 1帮
你
记
忆 硝酸的氧化性强至可以氧化大多数金属,但还是没办法氧化Au和 Pt3、硫酸和硝酸的用途:制化肥、农药、炸药、染料、盐等
器壁 慢慢地 注入水里,并不断搅拌。知识回顾:稀硫酸具有酸的通性 Na2CO3 Cu(OH)2 CuO Zn 酸碱
指示剂稀H2SO4CuSO4+H2OCuSO4+H2OZnSO4+H2石蕊Na2SO4+
H2O+CO2(二).硫酸的化学性质思考:浓硫酸敞口放置,是怎样变质的?用途:干燥剂(干燥H2 、CO2、N2 、 O2等)1、吸水性2、脱水性:思考:浓硫酸的吸水性与脱水性有什么不同? 浓硫酸的特性浓硫酸能把含氧的有机物中的H和O 原子按照水的组成(2:1)
脱水炭化,放出热,并氧化生成的部分碳,生成CO2和SO2。3、强氧化性:思考:在这个反应中,硫酸起了什么作用?CuO+H2SO4==CuSO4+H2O(1)与金属反应体现氧化性体现酸性思考:浓硫酸在加热时能氧化铜,那么能氧化其他金属吗?浓H2SO4加热:能与大多数金属(Au、Pt除外)反应常温:能与活泼金属反应(注意:不生成H2)常温下, Fe 和Al遇到浓硫酸被钝化
(被氧化成一层致密的氧化膜,
阻止内部金属进一步被氧化。)(2)与非金属反应:问:氧化产物与还原产物的物质的量之比想一想:为什么蔗糖脱水后变得疏松多孔?问:设计一个实验检验反应产生的气体成分?〖巩固练习〗1.如何鉴别失去标签的稀硫酸和浓硫酸?请同学们提出尽可能多的方案 (1)用手掂重量(2)看有无粘性(1)在干净白纸上写字(2)加入到胆矾晶体中……..2、利用浓硫酸的脱水性3、利用浓硫酸的氧化性4、利用浓硫酸的钝化作用(3)利用浓硫酸溶于水放热1 、利用物理性质的区别二、硝酸的性质:1、物理性质:无色,易挥发、有刺激性气味的液体,能以任意比溶于水2、化学性质:(1)酸性(略)(2)氧化性:① 与金属反应(除Au和 Pt外) 反应激烈,产生红棕色气体,
溶液由无色变为绿色。Cu+4HNO3(浓) = Cu(NO3)2+2NO2 +2H2O结论:硝酸具有强的氧化性,能氧化不活泼金属。3Cu+8HNO3(稀) =3Cu(NO3)2+2NO +4H2O 反应较缓慢,产生无色气体,逸至试管口变为红棕色, 溶液由无色变为绿色。注意:Fe 和Al遇到冷的浓硝酸被钝化,被氧化成一层致密的氧化膜,情形跟浓硫酸一样。氧化性:浓硝酸>稀硝酸小结:硝酸与金属或非金属(如碳、硫等)反应时,主要是HNO3中+5价的氮得到电子,被还原成较低价氮的物质,稀硝酸的还原产物一般是NO,浓硝酸的还原产物一般是NO2,而不像盐酸与金属反应那样生成H2 3体积浓盐酸与1体积浓硝酸的混合物叫做王水,它的氧化能力更强,能溶解 金(Au )和 铂(Pt ) 体积比为 3 : 1帮
你
记
忆 硝酸的氧化性强至可以氧化大多数金属,但还是没办法氧化Au和 Pt3、硫酸和硝酸的用途:制化肥、农药、炸药、染料、盐等
