2011届高三化学一轮复习精品练习 第4课时 化学实验方案的设计 (含答案)
文档属性
| 名称 | 2011届高三化学一轮复习精品练习 第4课时 化学实验方案的设计 (含答案) |
|
|
| 格式 | rar | ||
| 文件大小 | 213.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2010-08-23 00:00:00 | ||
图片预览


文档简介
本资料来自于资源最齐全的21世纪教育网www.21cnjy.com
2011届高三化学一轮复习精品练习
第4课时 化学实验方案的设计 课时作业
一、选择题(包括8小题。1~6小题只有一个选项符合题意,7~8小题有两个选项符合题意。)1.下列实验方案的设计合理的是( )
A.用过量的氨水除去Al3+溶液中的少量Fe3+
B.用稀硫酸清洗长期存放氯化铁溶液的试剂瓶内壁所附着的不溶物
C.用加热法分离I2和NH4Cl的混合物
D.为了更快得到氢气,可以用纯锌代替粗锌与稀硫酸反应
2.(2009年沈阳模拟)如图所示,夹子开始处于关闭状态,将液体A滴入试管②与气体B充分反应,打开夹子,可发现试管①内的水立刻沸腾了。则液体A和气体B的组合不可能
是下列的( )
A.氢氧化钠溶液、二氧化碳
B.水、氨气
C.氢氧化钠溶液、一氧化氮
D.水、二氧化氮
3.利用下列各组中的物质制备并收集少量相应的气体,能采用如图所示装置的是( )
①浓氨水和固体NaOH制NH3
②大理石和稀盐酸制CO2
③过氧化氢溶液和二氧化锰制O2
④稀硝酸和铜片制NO
⑤浓盐酸和二氧化锰制Cl2
⑥电石和水制乙炔
⑦锌粒和稀H2SO4制H2
⑧乙醇和浓H2SO4制乙稀
A.②③
B.①⑥⑦
C.②⑤⑧
D.①④⑥
4.某氯碱厂利用废铁皮制取净水剂FeCl3,最合理的生产途径是( )
A.Cl2FeCl3FeCl3溶液
B.Cl2HCl盐酸FeCl2溶液FeCl3溶液
C.Cl2FeCl3
D.Cl2HCl盐酸
FeCl3溶液
废铁 Fe2O3
5.(2009年广东五校模拟)在下列实验中,不能达到目的的是( )
A.Fe与Cl2反应生成FeCl3,Fe与S反应生成FeS,确定非金属性:Cl>S
B.用石墨作电极,电解Mg(NO3)2、Cu(NO3)2的混合溶液,确定铜的镁的金属活动性强弱
C.进行H2O和H2S的热分解实验,确定硫和氧两种元素的非金属性强弱
D.测定NaCl和NaF溶液的pH,确定F、Cl两元素非金属性的强弱
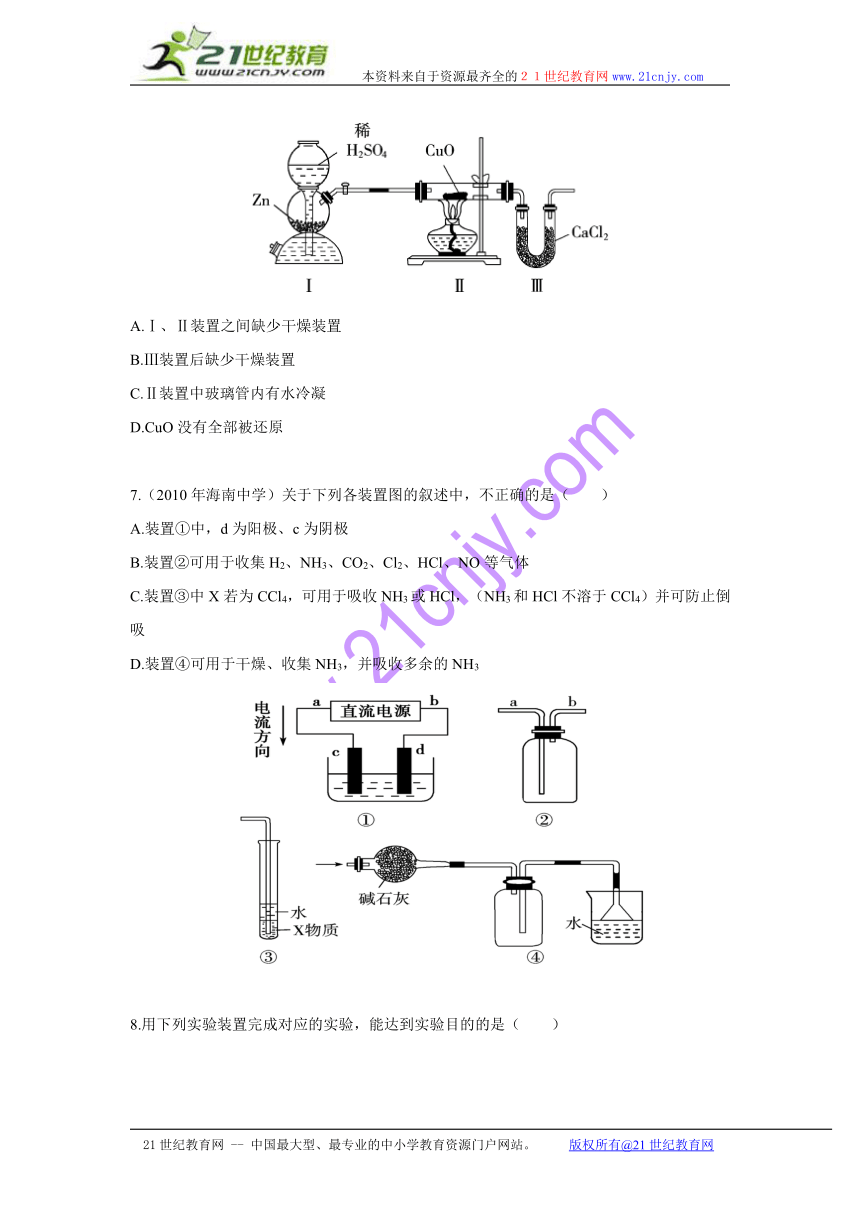
6.(2009年泰安模拟)用如下图装置测定水中氢、氧元素的质量比,其方法是分别测定通氢气前后玻璃管的质量差和U形管的质量差,实验测得?m(H)∶m(O)>1∶8。下列对导致这一结果的原因的分析中,一定错误的是( )
A.Ⅰ、Ⅱ装置之间缺少干燥装置
B.Ⅲ装置后缺少干燥装置
C.Ⅱ装置中玻璃管内有水冷凝
D.CuO没有全部被还原
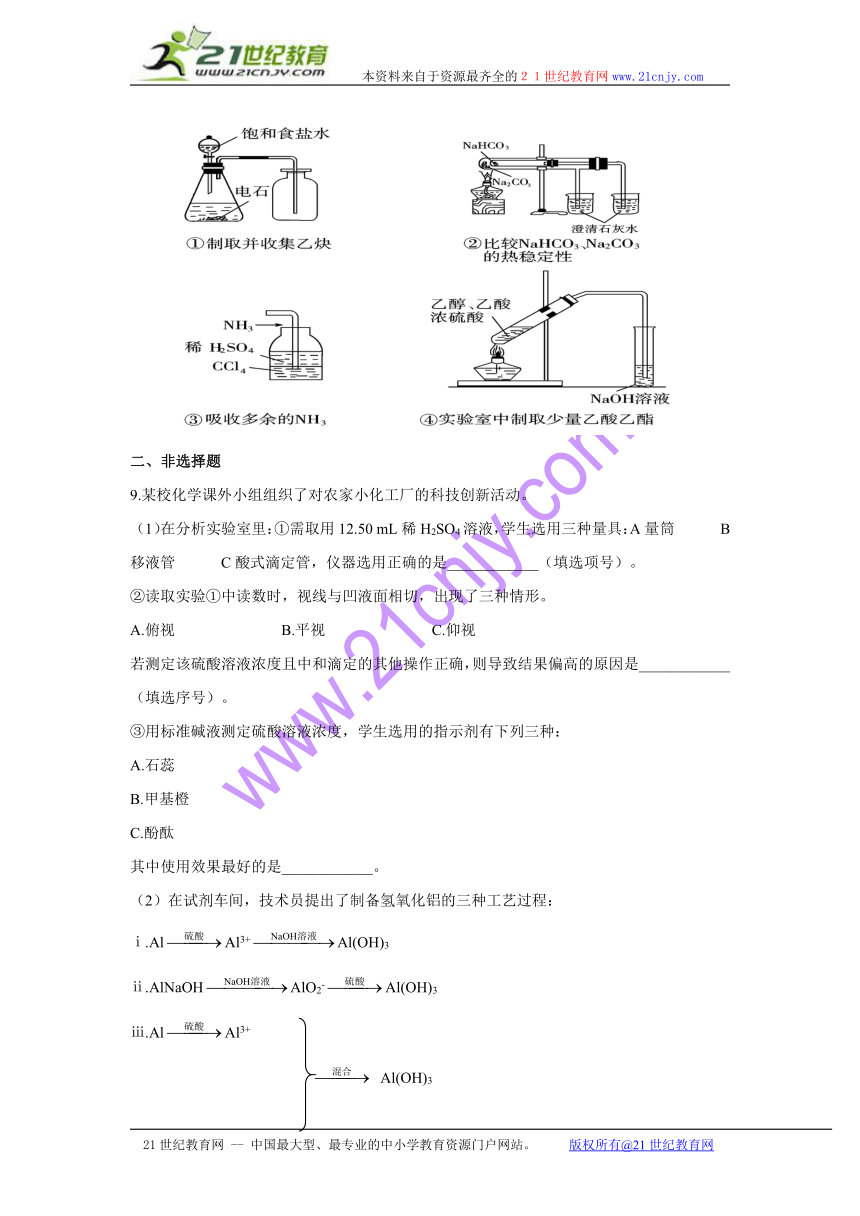
7.(2010年海南中学)关于下列各装置图的叙述中,不正确的是( )
A.装置①中,d为阳极、c为阴极
B.装置②可用于收集H2、NH3、CO2、Cl2、HCl、NO等气体
C.装置③中X若为CCl4,可用于吸收NH3或HCl,(NH3和HCl不溶于CCl4)并可防止倒吸
D.装置④可用于干燥、收集NH3,并吸收多余的NH3
8.用下列实验装置完成对应的实验,能达到实验目的的是( )
二、非选择题
9.某校化学课外小组组织了对农家小化工厂的科技创新活动。
(1)在分析实验室里:①需取用12.50 mL稀H2SO4溶液,学生选用三种量具:A量筒 B移液管 C酸式滴定管,仪器选用正确的是____________(填选项号)。
②读取实验①中读数时,视线与凹液面相切,出现了三种情形。
A.俯视 B.平视 C.仰视
若测定该硫酸溶液浓度且中和滴定的其他操作正确,则导致结果偏高的原因是____________(填选序号)。
③用标准碱液测定硫酸溶液浓度,学生选用的指示剂有下列三种:
A.石蕊
B.甲基橙
C.酚酞
其中使用效果最好的是____________。
(2)在试剂车间,技术员提出了制备氢氧化铝的三种工艺过程:
ⅰ.AlAl3+Al(OH)3
ⅱ.AlNaOHAlO2-Al(OH)3
ⅲ.AlAl3+
Al(OH)3
Al AlO2-
试从成本、环保达标等方面评价,第____________种工艺最优。
(3)根据市场的需求,厂长请学生设计开发胆矾产品的方案。学生们设计了以下三种方案:方案甲:废铜屑 CuSO4溶液CuSO4·5H2O
方案乙:废铜屑CuSO4溶液CuSO4·5H2O
方案丙:废铜屑CuOCuSO4溶液CuSO4·5H2O
则合理可行的方案为____________。
10.(2009年安徽卷)某厂废水中含5.00×10-3mol·L-1的Cr2O72-,其毒性较大。某研究性学习小组为了变废为宝,将废水处理得到磁性材料Cr0.5Fe1.5FeO4(Fe的化合价依次为+3、+2),设计了如下实验流程:
〖FK)〗
(1)第①步反应的离子方程式是____________ 。
(2)第②步中用pH试纸测定溶液pH的操作是:____________ 。
(3)第②步过滤得到的滤渣中主要成分除Cr(OH)3外,还有____________。
(4)欲使1 L该废水中的Cr2O72-完全转化为Cr0.5Fe1.5FeO4,理论上需要加入____________g FeSO4·7H2O。
11.(2009年宁夏卷)碱式碳酸铜可表示为:
xCuCO3·yCu(OH)2·zH2O,测定碱式碳酸铜组成的方法有多种。
(1)现采用氢气还原法,请回答下列问题:
①写出xCuCO3·yCu(OH)2y·zH2O与氢气反应的化学方程式____________ ;
②实验装置用下列所有仪器连接而成,按氢气流方向的连接顺序是(填入仪器接口字母编号):
(a)→( )( )→( )( )→( )( )→( )( )→( )( )→(l)
③称取23.9 g某碱式碳酸铜样品,充分反应后得到12.7 g残留物,生成4.4 g二氧化碳和7.2 g水。该样品的结晶水质量为____________g,化学式为____________;
(2)某同学以氮气代替氢气,并用上述全部或部分仪器来测定碱式碳酸铜的组成,你认识是否可行?请说明理由。____________ 。
12.(2009年启东模拟)铁是日常生活中最常见的金属,某班同学在学习铁的知识时,有下列问题:
问题1:铁为何称为黑色金属?
问题2:CuO在高温下可分解为Cu2O和O2,Fe2O3在高温下可分解为FeO和O2吗?
(1)对于问题1,同学们上网查找,有两种解释:
A.因为在铁表面有黑色的铁的氧化物,所以叫黑色金属
B.因为铁的粉末为黑色,铁的氧化物也均为黑色,所以叫黑色金属
①你认为正确的说法是____________。
②若有一黑色粉末,如何鉴别是铁粉,还是Fe3O4粉末:
____________ 。
③若有一黑色粉末,为铁和四氧化三铁的混合物,如何证明其中有Fe3O4(只要求简述实验方法):____________ 。
(2)对于问题2,同学们准备实验探究,他们设想了两种方法:
A.将三氧化二铁高温灼烧,看灼烧前后颜色是否变化
B.将三氧化二铁高温灼烧,看灼烧前后质量是否变化
①实验中应将Fe2O3放在____________(填仪器名称)中灼烧。
②方法A中,如果高温灼烧后颜色由____________变为____________ ,
说明Fe2O3确实发生了变化。能说明生成的一定为FeO吗?____________(填“能”或“不能”)。理由是____________。
③方法B中,如果发生了预期的反应,固体高温灼烧前后质量比应为____________,但是,实验结果是固体灼烧前后质量比为30∶29,则高温灼烧后生成物是____________。
④比较两种方法,你认为较好的方法是____________。
参考答案:
1.解析:过量氨水与Al3+和Fe3+反应生成Al(OH)3和Fe(OH)3沉淀;加热时I2升华,NH4Cl分解成NH3和HCl,遇冷又生成NH4Cl,故不能分离;粗锌可以形成原电池加快反应。
答案:B
2.解析:如果气体B在液体A中能溶解或反应,使试管②中气体的物质的量减少,整个装置压强减小,就可使水的沸点降低,即在96℃可沸腾。
答案:C
3.解析:该装置的特点是固体与液体不需要加热生成密度比空气大的气体。②、③均满足。①、⑦生成的气体均比空气轻,应向下排空气,⑤、⑧反应均需加热,④、⑥生成的气体均不能用排空气法收集。
答案:A
4.解析:H2和Cl2混合光照发生爆炸;工业采用H2在Cl2中燃烧制取HCl。答案:B
5.解析:B选项中,先析出的金属阳离子氧化性强(Cu2+),对应单质的活动性弱;D选项中,只能判定HCl和HF的酸性强弱。
答案:D
6.解析:?m(H)∶m(O)=。若Ⅰ、Ⅱ装置间缺少干燥装置,则U形管质量差增大,m(H)∶m(O)增大,即大于1∶8;Ⅲ装置后缺少干燥装置也导致U形管质量差增大,使m(H)∶m(O)>1∶8,而Ⅱ装置中玻璃管内有水冷凝,则玻璃管质量差减小,m(H)∶m(O)增大,即大于1∶8,实验结果与CuO是否全部被还原无关。
答案:D
7.解析:①根据电流方向即可得出,电源正极连电解池阳极,A错。②收集比空气轻的气体从a进,比空气重的从b进,NO不能用排空气法。③可以防止倒吸。
答案:AB
8.解析:A项,C2H2密度与空气相近,应用排水集气法收集;B项,直接被加热的不能产生使石灰水变浑浊的气体,间接加热的NaHCO3能产生使石灰水变浑的气体,B正确。C项,NH3不溶于CCl4,从CCl4层逸出后再被H2SO42-吸收,不会引起倒吸;D项,用饱和Na2CO3溶液收集乙酸乙酯,且导管不能伸入液面以下。答案:BC
9.解析:(1)①由已知12.50 mL可知题目要求精确至0.01 mL,只有滴定管符合要求。选C。
②c(H2SO42-)=,c(H2SO42-)偏高必然是V(H2SO42-)偏低所致,选A。
③从变色明显角度来看,用碱滴定酸,最好选用酚酞作指示剂。
(2)制取同样多的Al(OH)3,第ⅲ种方法最节约试剂。
(3)方案甲中,铜与浓H2SO42-反应会生成SO2污染环境,方案乙中,铜与稀H2SO42-不反应。
答案:(1)①C②A③C(2)ⅲ(3)丙
10.解析:(1)Cr2O2-7有较强氧化性,FeSO42-·7H2O中Fe2+有一定的还原性,在酸性介质中发生氧化还原反应,Cr2O72-转化为Cr3+,Fe2+转化为Fe3+。
Cr2O72-+14H++6Fe2+=2Cr3++6Fe3++7H2O
(2)应将试纸放在表面皿上,用玻璃棒蘸取待测液滴在试纸中部,再与标准比色卡对照得出pH。
(3)由题给框图之二可得:Fe2+过量,加NaOH时,产生Cr(OH)3、Fe(OH)3和Fe(OH)2三种沉淀物。
(4)1 L废水中含n(Cr2O72-)=5.00×10-3 mol。
由题意得:Cr2O72-~4Cr0.5Fe1.5FeO42-~10FeSO42-·7H2O,所以理论上n(FeSO42-·7H2O)=10n(Cr2O72-)=0.05 mol。
m(FeSO42-·7H2O)=0.05 mol×278 g·mol-1=13.9 g。
答案:(1)Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O
(2)将一小片pH试纸放在表面皿上,用玻璃棒蘸取少量待测液,点在pH试纸上,再与标准比色卡对照
(3)Fe(OH)3、Fe(OH)2
(4)13.9
11.解析:(1)①与H2反应的化学方程式,利用氧化还原反应原理,把金属Cu还原出来,碳元素变成CO2,氢元素变成水。
②仪器连接时,洗气瓶要“长进短出”,其中水是观察H2生成速率的。
③残留固体一定是Cu,则n(Cu)=12.7/63.5=0.2(mol),根据题意,n(CO2)=n(CuCO3)=4.4/44=0.1(mol),所以,m(CuCO3)=123.5×n(CuCO3)=12.35(g),m[Cu(OH)2]=97.5×[n(Cu)-n(CuCO3)]=9.75(g),m(结晶水)=23.9-12.35-9.75=1.8(g)。该碱式碳酸铜化学式为CuCO3·Cu(OH)2·H2O。
(2)根据xCuCO3·yCu(OH)2·zH2O(x+y)CuO+xCO2↑+(y+z)H2O↑,依据元素守恒和质量守恒,即可得出答案。
答案:(1)①xCuCO3·yCu(OH)2·zH2O+(x+y)H2 (x+y)Cu+xCO2+(x+2y+z)H2O
②a→kj→gf(或hi)→de(或ed)→hi(或gf)→bc(或cb)→l
③1.8CuCO3·Cu(OH)2·H2O
(2)可以
根据反应xCuCO3·yCu(OH)2·zH2O〖FY)〗(x+y)CuO+4CO2↑+(y+z)H2O↑
依据碱式碳酸铜样品、CuO、CO2和H2O质量(或其中任意三个量),即可计算出其组成。
12.(1)①A
②取黑色粉末少许于试管中,加适量稀盐酸或稀硫酸,若有气泡产生则原黑色粉末为铁,或无气泡产生则原粉末为Fe3O42-(其他合理答案亦可)
③用干燥的氢气与黑色粉末加热反应,用无水硫酸铜检测是否有水产生(或用纯净的一氧化碳与黑色粉末加热反应,用澄清石灰水检测是否有二氧化碳产生)(其他合理答案亦可)
(2)①坩埚②红棕色黑色不能也可能为Fe3O42-③10/9Fe3O42-④B
含Cr3+、Fe2+、Fe3+的溶液
含Cr2O72-的酸性废水
21世纪教育网 -- 中国最大型、最专业的中小学教育资源门户网站。 版权所有@21世纪教育网
2011届高三化学一轮复习精品练习
第4课时 化学实验方案的设计 课时作业
一、选择题(包括8小题。1~6小题只有一个选项符合题意,7~8小题有两个选项符合题意。)1.下列实验方案的设计合理的是( )
A.用过量的氨水除去Al3+溶液中的少量Fe3+
B.用稀硫酸清洗长期存放氯化铁溶液的试剂瓶内壁所附着的不溶物
C.用加热法分离I2和NH4Cl的混合物
D.为了更快得到氢气,可以用纯锌代替粗锌与稀硫酸反应
2.(2009年沈阳模拟)如图所示,夹子开始处于关闭状态,将液体A滴入试管②与气体B充分反应,打开夹子,可发现试管①内的水立刻沸腾了。则液体A和气体B的组合不可能
是下列的( )
A.氢氧化钠溶液、二氧化碳
B.水、氨气
C.氢氧化钠溶液、一氧化氮
D.水、二氧化氮
3.利用下列各组中的物质制备并收集少量相应的气体,能采用如图所示装置的是( )
①浓氨水和固体NaOH制NH3
②大理石和稀盐酸制CO2
③过氧化氢溶液和二氧化锰制O2
④稀硝酸和铜片制NO
⑤浓盐酸和二氧化锰制Cl2
⑥电石和水制乙炔
⑦锌粒和稀H2SO4制H2
⑧乙醇和浓H2SO4制乙稀
A.②③
B.①⑥⑦
C.②⑤⑧
D.①④⑥
4.某氯碱厂利用废铁皮制取净水剂FeCl3,最合理的生产途径是( )
A.Cl2FeCl3FeCl3溶液
B.Cl2HCl盐酸FeCl2溶液FeCl3溶液
C.Cl2FeCl3
D.Cl2HCl盐酸
FeCl3溶液
废铁 Fe2O3
5.(2009年广东五校模拟)在下列实验中,不能达到目的的是( )
A.Fe与Cl2反应生成FeCl3,Fe与S反应生成FeS,确定非金属性:Cl>S
B.用石墨作电极,电解Mg(NO3)2、Cu(NO3)2的混合溶液,确定铜的镁的金属活动性强弱
C.进行H2O和H2S的热分解实验,确定硫和氧两种元素的非金属性强弱
D.测定NaCl和NaF溶液的pH,确定F、Cl两元素非金属性的强弱
6.(2009年泰安模拟)用如下图装置测定水中氢、氧元素的质量比,其方法是分别测定通氢气前后玻璃管的质量差和U形管的质量差,实验测得?m(H)∶m(O)>1∶8。下列对导致这一结果的原因的分析中,一定错误的是( )
A.Ⅰ、Ⅱ装置之间缺少干燥装置
B.Ⅲ装置后缺少干燥装置
C.Ⅱ装置中玻璃管内有水冷凝
D.CuO没有全部被还原
7.(2010年海南中学)关于下列各装置图的叙述中,不正确的是( )
A.装置①中,d为阳极、c为阴极
B.装置②可用于收集H2、NH3、CO2、Cl2、HCl、NO等气体
C.装置③中X若为CCl4,可用于吸收NH3或HCl,(NH3和HCl不溶于CCl4)并可防止倒吸
D.装置④可用于干燥、收集NH3,并吸收多余的NH3
8.用下列实验装置完成对应的实验,能达到实验目的的是( )
二、非选择题
9.某校化学课外小组组织了对农家小化工厂的科技创新活动。
(1)在分析实验室里:①需取用12.50 mL稀H2SO4溶液,学生选用三种量具:A量筒 B移液管 C酸式滴定管,仪器选用正确的是____________(填选项号)。
②读取实验①中读数时,视线与凹液面相切,出现了三种情形。
A.俯视 B.平视 C.仰视
若测定该硫酸溶液浓度且中和滴定的其他操作正确,则导致结果偏高的原因是____________(填选序号)。
③用标准碱液测定硫酸溶液浓度,学生选用的指示剂有下列三种:
A.石蕊
B.甲基橙
C.酚酞
其中使用效果最好的是____________。
(2)在试剂车间,技术员提出了制备氢氧化铝的三种工艺过程:
ⅰ.AlAl3+Al(OH)3
ⅱ.AlNaOHAlO2-Al(OH)3
ⅲ.AlAl3+
Al(OH)3
Al AlO2-
试从成本、环保达标等方面评价,第____________种工艺最优。
(3)根据市场的需求,厂长请学生设计开发胆矾产品的方案。学生们设计了以下三种方案:方案甲:废铜屑 CuSO4溶液CuSO4·5H2O
方案乙:废铜屑CuSO4溶液CuSO4·5H2O
方案丙:废铜屑CuOCuSO4溶液CuSO4·5H2O
则合理可行的方案为____________。
10.(2009年安徽卷)某厂废水中含5.00×10-3mol·L-1的Cr2O72-,其毒性较大。某研究性学习小组为了变废为宝,将废水处理得到磁性材料Cr0.5Fe1.5FeO4(Fe的化合价依次为+3、+2),设计了如下实验流程:
〖FK)〗
(1)第①步反应的离子方程式是____________ 。
(2)第②步中用pH试纸测定溶液pH的操作是:____________ 。
(3)第②步过滤得到的滤渣中主要成分除Cr(OH)3外,还有____________。
(4)欲使1 L该废水中的Cr2O72-完全转化为Cr0.5Fe1.5FeO4,理论上需要加入____________g FeSO4·7H2O。
11.(2009年宁夏卷)碱式碳酸铜可表示为:
xCuCO3·yCu(OH)2·zH2O,测定碱式碳酸铜组成的方法有多种。
(1)现采用氢气还原法,请回答下列问题:
①写出xCuCO3·yCu(OH)2y·zH2O与氢气反应的化学方程式____________ ;
②实验装置用下列所有仪器连接而成,按氢气流方向的连接顺序是(填入仪器接口字母编号):
(a)→( )( )→( )( )→( )( )→( )( )→( )( )→(l)
③称取23.9 g某碱式碳酸铜样品,充分反应后得到12.7 g残留物,生成4.4 g二氧化碳和7.2 g水。该样品的结晶水质量为____________g,化学式为____________;
(2)某同学以氮气代替氢气,并用上述全部或部分仪器来测定碱式碳酸铜的组成,你认识是否可行?请说明理由。____________ 。
12.(2009年启东模拟)铁是日常生活中最常见的金属,某班同学在学习铁的知识时,有下列问题:
问题1:铁为何称为黑色金属?
问题2:CuO在高温下可分解为Cu2O和O2,Fe2O3在高温下可分解为FeO和O2吗?
(1)对于问题1,同学们上网查找,有两种解释:
A.因为在铁表面有黑色的铁的氧化物,所以叫黑色金属
B.因为铁的粉末为黑色,铁的氧化物也均为黑色,所以叫黑色金属
①你认为正确的说法是____________。
②若有一黑色粉末,如何鉴别是铁粉,还是Fe3O4粉末:
____________ 。
③若有一黑色粉末,为铁和四氧化三铁的混合物,如何证明其中有Fe3O4(只要求简述实验方法):____________ 。
(2)对于问题2,同学们准备实验探究,他们设想了两种方法:
A.将三氧化二铁高温灼烧,看灼烧前后颜色是否变化
B.将三氧化二铁高温灼烧,看灼烧前后质量是否变化
①实验中应将Fe2O3放在____________(填仪器名称)中灼烧。
②方法A中,如果高温灼烧后颜色由____________变为____________ ,
说明Fe2O3确实发生了变化。能说明生成的一定为FeO吗?____________(填“能”或“不能”)。理由是____________。
③方法B中,如果发生了预期的反应,固体高温灼烧前后质量比应为____________,但是,实验结果是固体灼烧前后质量比为30∶29,则高温灼烧后生成物是____________。
④比较两种方法,你认为较好的方法是____________。
参考答案:
1.解析:过量氨水与Al3+和Fe3+反应生成Al(OH)3和Fe(OH)3沉淀;加热时I2升华,NH4Cl分解成NH3和HCl,遇冷又生成NH4Cl,故不能分离;粗锌可以形成原电池加快反应。
答案:B
2.解析:如果气体B在液体A中能溶解或反应,使试管②中气体的物质的量减少,整个装置压强减小,就可使水的沸点降低,即在96℃可沸腾。
答案:C
3.解析:该装置的特点是固体与液体不需要加热生成密度比空气大的气体。②、③均满足。①、⑦生成的气体均比空气轻,应向下排空气,⑤、⑧反应均需加热,④、⑥生成的气体均不能用排空气法收集。
答案:A
4.解析:H2和Cl2混合光照发生爆炸;工业采用H2在Cl2中燃烧制取HCl。答案:B
5.解析:B选项中,先析出的金属阳离子氧化性强(Cu2+),对应单质的活动性弱;D选项中,只能判定HCl和HF的酸性强弱。
答案:D
6.解析:?m(H)∶m(O)=。若Ⅰ、Ⅱ装置间缺少干燥装置,则U形管质量差增大,m(H)∶m(O)增大,即大于1∶8;Ⅲ装置后缺少干燥装置也导致U形管质量差增大,使m(H)∶m(O)>1∶8,而Ⅱ装置中玻璃管内有水冷凝,则玻璃管质量差减小,m(H)∶m(O)增大,即大于1∶8,实验结果与CuO是否全部被还原无关。
答案:D
7.解析:①根据电流方向即可得出,电源正极连电解池阳极,A错。②收集比空气轻的气体从a进,比空气重的从b进,NO不能用排空气法。③可以防止倒吸。
答案:AB
8.解析:A项,C2H2密度与空气相近,应用排水集气法收集;B项,直接被加热的不能产生使石灰水变浑浊的气体,间接加热的NaHCO3能产生使石灰水变浑的气体,B正确。C项,NH3不溶于CCl4,从CCl4层逸出后再被H2SO42-吸收,不会引起倒吸;D项,用饱和Na2CO3溶液收集乙酸乙酯,且导管不能伸入液面以下。答案:BC
9.解析:(1)①由已知12.50 mL可知题目要求精确至0.01 mL,只有滴定管符合要求。选C。
②c(H2SO42-)=,c(H2SO42-)偏高必然是V(H2SO42-)偏低所致,选A。
③从变色明显角度来看,用碱滴定酸,最好选用酚酞作指示剂。
(2)制取同样多的Al(OH)3,第ⅲ种方法最节约试剂。
(3)方案甲中,铜与浓H2SO42-反应会生成SO2污染环境,方案乙中,铜与稀H2SO42-不反应。
答案:(1)①C②A③C(2)ⅲ(3)丙
10.解析:(1)Cr2O2-7有较强氧化性,FeSO42-·7H2O中Fe2+有一定的还原性,在酸性介质中发生氧化还原反应,Cr2O72-转化为Cr3+,Fe2+转化为Fe3+。
Cr2O72-+14H++6Fe2+=2Cr3++6Fe3++7H2O
(2)应将试纸放在表面皿上,用玻璃棒蘸取待测液滴在试纸中部,再与标准比色卡对照得出pH。
(3)由题给框图之二可得:Fe2+过量,加NaOH时,产生Cr(OH)3、Fe(OH)3和Fe(OH)2三种沉淀物。
(4)1 L废水中含n(Cr2O72-)=5.00×10-3 mol。
由题意得:Cr2O72-~4Cr0.5Fe1.5FeO42-~10FeSO42-·7H2O,所以理论上n(FeSO42-·7H2O)=10n(Cr2O72-)=0.05 mol。
m(FeSO42-·7H2O)=0.05 mol×278 g·mol-1=13.9 g。
答案:(1)Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O
(2)将一小片pH试纸放在表面皿上,用玻璃棒蘸取少量待测液,点在pH试纸上,再与标准比色卡对照
(3)Fe(OH)3、Fe(OH)2
(4)13.9
11.解析:(1)①与H2反应的化学方程式,利用氧化还原反应原理,把金属Cu还原出来,碳元素变成CO2,氢元素变成水。
②仪器连接时,洗气瓶要“长进短出”,其中水是观察H2生成速率的。
③残留固体一定是Cu,则n(Cu)=12.7/63.5=0.2(mol),根据题意,n(CO2)=n(CuCO3)=4.4/44=0.1(mol),所以,m(CuCO3)=123.5×n(CuCO3)=12.35(g),m[Cu(OH)2]=97.5×[n(Cu)-n(CuCO3)]=9.75(g),m(结晶水)=23.9-12.35-9.75=1.8(g)。该碱式碳酸铜化学式为CuCO3·Cu(OH)2·H2O。
(2)根据xCuCO3·yCu(OH)2·zH2O(x+y)CuO+xCO2↑+(y+z)H2O↑,依据元素守恒和质量守恒,即可得出答案。
答案:(1)①xCuCO3·yCu(OH)2·zH2O+(x+y)H2 (x+y)Cu+xCO2+(x+2y+z)H2O
②a→kj→gf(或hi)→de(或ed)→hi(或gf)→bc(或cb)→l
③1.8CuCO3·Cu(OH)2·H2O
(2)可以
根据反应xCuCO3·yCu(OH)2·zH2O〖FY)〗(x+y)CuO+4CO2↑+(y+z)H2O↑
依据碱式碳酸铜样品、CuO、CO2和H2O质量(或其中任意三个量),即可计算出其组成。
12.(1)①A
②取黑色粉末少许于试管中,加适量稀盐酸或稀硫酸,若有气泡产生则原黑色粉末为铁,或无气泡产生则原粉末为Fe3O42-(其他合理答案亦可)
③用干燥的氢气与黑色粉末加热反应,用无水硫酸铜检测是否有水产生(或用纯净的一氧化碳与黑色粉末加热反应,用澄清石灰水检测是否有二氧化碳产生)(其他合理答案亦可)
(2)①坩埚②红棕色黑色不能也可能为Fe3O42-③10/9Fe3O42-④B
含Cr3+、Fe2+、Fe3+的溶液
含Cr2O72-的酸性废水
21世纪教育网 -- 中国最大型、最专业的中小学教育资源门户网站。 版权所有@21世纪教育网
同课章节目录
