金属和金属材料复习学案
图片预览
文档简介
第八单元金属和金属材料
复习学案
教学目标:
形成单元知识框架,并利用所学知识解决实际问题。
教学重、难点:金属活动性的探究及有关化学方程式中杂质问题的计算。
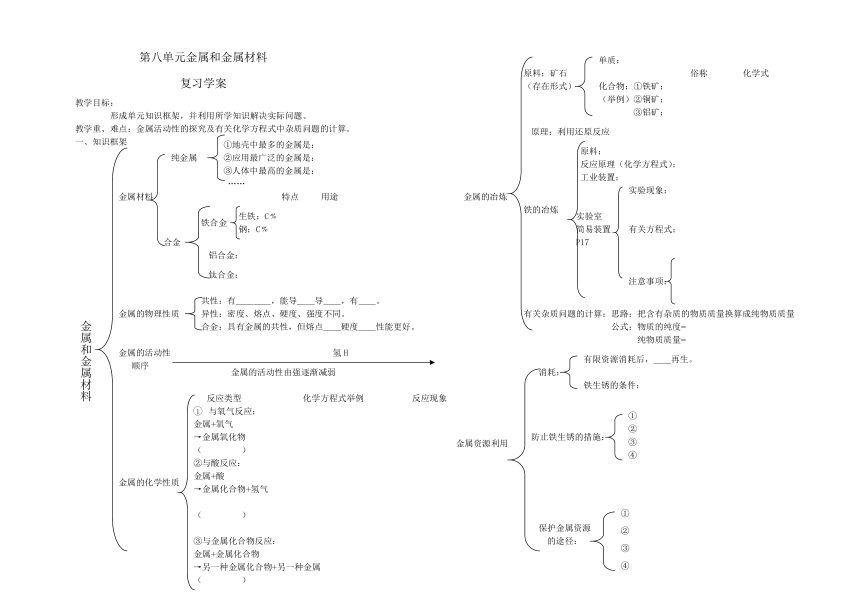
1、 知识框架
二、练习题
1、用元素符号表示下列所用的物质.
涂在保温瓶胆夹层内的银白色金属是__________;包装糖果、香烟的银白色材料是__________;白炽灯泡内的灯丝通常是由__________制成的;温度计中填充的金属是__________.
2、初中化学课学完以后,化学学习兴趣小组对“金属活动性顺序”从内容、规律以及应用等方面进行了总结。请你认真填写下面的空白内容:
(1)金属活动性顺序表:K Ca Na Al Zn Fe Sn Pb (H) Cu Ag Pt Au
(2)金属与酸反应的规律是 。
试举出实际应用的实例(可用化学方程式表示) 。
下列物质可通过相应的金属与稀酸发生反应而得到的是
A.ZnCl2 B.AgCl C.CuCl 2 D.Fe2(SO4)3
(3)金属与盐发生置换反应,必须符合三点①K、Ca、Na三种金属非常活泼,不能把金属直接从其盐溶液中置换出来;②
③ ;
3、金属是一种重要的材料,人类的生活和生产都离不开金属。
⑴ 根据有关的化学知识,你认为金属大规模开发、利用的先后顺序跟下列哪些因素有关 。①地壳中金属元素的含量②金属的导电性③金属的活动性④金属的延展性⑤金属冶炼的难易程度
⑵钢铁的生产和使用是人类文明和社会进步的一个重要标志。请你写出一氧化碳在高温条件下把铁从赤铁矿(主要成分是氧化铁)里还原出来的化学方程式。
⑶每年世界上钢铁的产量很高,但钢铁的锈蚀也给人类带来了巨大的损失。铁在空气中锈蚀,实际上是铁跟 等物质相互作用的结果。
⑷铝的活动性比铁强,但铝在空气中却表现出良好的抗蚀性,其原因是什么?
⑸若将13锌放入100稀硫酸溶液中恰好完全反应,则可生成氢气多少克?参加反应的稀硫酸中溶质的质量分数是多少?
4、下列金属中导电性最好的是( )
A.Cu B.Al C.Fe D.Ag
5、下列叙述正确的是( )
A、不能用铁桶来盛硫酸铜溶液,是因为硫酸铜溶液易溢出,不便于运输
B、钢铁工业上,炼铁的主要设备是高炉
C、氧化碳和氧化铁在高温下反应可生成铁,是因为一氧化碳有毒
D、铜、铁在潮湿的空气中都会生锈
6、在CuCl2和AlCl3的混合溶液中,加入过量的锌粉,充分反应后过滤,留在滤纸上的物质是( )A.Cu B.Cu和Al C.Zn和Cu D.Cu、Al和Zn
7、往AgNO3、Cu(NO3)2、Zn(NO3)2的混合溶液中加入一些铁粉,待反应完成后再过滤,不可能存在的情况是 (A)滤纸上有Ag,滤液中有Ag+、Cu2+、Zn2+、Fe2+
(B)滤纸上有Ag、Cu,滤液中有Ag+、Zn2+、Fe2+
(C)滤纸上有Ag、Cu、Fe,滤液中有Zn2+、Fe2+
(D)滤纸上有Ag、Cu、Fe、Zn,滤液中有Zn2+、Fe2+
8、La(镧)是一种活动性比锌强的金属元素,其氧化物为La2O3,对应的碱La(OH)3。难溶于水,而LaCl3、La(NO3)3都易溶于水。下列各组物质中,不能直接反应制得LaCl3的是
A.La+HCl B.La2O3+HCl
C.La(OH)3+HCl D.BaCl2+La(NO3)3
9、某化学兴趣小组为测定Fe、Cu、Ag三种金属的活动性顺序设计了四种方案,每种方案设计如下,其中你认为不可行的是 [ ]
(A)Cu、Ag、FeSO4溶液(B)Fe、Ag、CuSO4溶液
(C)Fe、Cu、稀盐酸、AgNO3溶液(D)Cu、FeSO4溶液、AgNO3溶液
10、河中化学兴趣小组在A、B、C、D四只
小烧杯中分别放入干燥的细铁丝、浸过食盐水的
细铁丝、浸过清水的细铁丝、完全浸没在食盐水
中的细铁丝,然后装配成四个如右所示的装置中,
每隔一段时间测量导管中水面上升的高度,得到
一组数据如下表:(水柱高度:毫米)
时 间(小时) 0 2 4 8 10
A瓶水柱(干燥的细铁丝) 0 0 0 0 0
B瓶水柱(浸过食盐水的细铁丝) 0 1.2 2.5 4.1 5.8
C瓶水柱(浸过清水的细铁丝) 0 0 05 1.1 2.4
D瓶水柱(浸没在食盐水中的细铁丝) 0 0 0 0 0
上述实验中,铁丝生锈的速率由大到小的排列顺序为________________,铁锈的主要成分是__________,导管中水面上升的原因是___________,影响铁生锈的因素有_____________________________
11、将一块质量为8.5g的铁合金(成分为铁和碳)放入烧杯中,再向烧杯中加入一定量10%稀硫酸,恰好与铁合金中的铁完全反应(碳不溶于稀H2SO4),所得氢气的质量为0.3g。已知含碳量高于2%的铁合金为生铁,含碳量低于2%的铁合金为钢,试根据计算回答:
(1)该铁合金是生铁还是钢?(2)反应后所得溶液中溶质的质量分数是多少?
金属和金属材料
共性:有____,能导__导__,有__。
异性:密度、熔点、硬度、强度不同。
合金:具有金属的共性,但熔点__硬度__性能更好。
金属材料
金属的物理性质
纯金属
金属的活动性
顺序
金属资源利用
金属的化学性质
反应类型 化学方程式举例 反应现象
1 与氧气反应:
金属+氧气
→金属氧化物
( )
②与酸反应:
金属+酸
→金属化合物+氢气
( )
③与金属化合物反应:
金属+金属化合物
→另一种金属化合物+另一种金属
( )
金属的冶炼
氢H
有关杂质问题的计算:思路:把含有杂质的物质质量换算成纯物质质量
公式:物质的纯度=
纯物质质量=
① ② ③ ④
④
①地壳中最多的金属是:
②应用最广泛的金属是:
③人体中最高的金属是:
……
原料:矿石
(存在形式)
原理:利用还原反应
铁的冶炼
金属的活动性由强逐渐减弱
铁合金
生铁:C﹪
钢:C﹪
合金
单质:
俗称 化学式
化合物:①铁矿:
(举例)②铜矿:
③铝矿:
特点 用途
消耗:
① ② ③ ④
④
铝合金:
钛合金:
原料:
反应原理(化学方程式):
工业装置:
实验室
简易装置
P17
实验现象:
有关方程式:
注意事项:
有限资源消耗后,__再生。
铁生锈的条件:
防止铁生锈的措施:
保护金属资源
的途径:
复习学案
教学目标:
形成单元知识框架,并利用所学知识解决实际问题。
教学重、难点:金属活动性的探究及有关化学方程式中杂质问题的计算。
1、 知识框架
二、练习题
1、用元素符号表示下列所用的物质.
涂在保温瓶胆夹层内的银白色金属是__________;包装糖果、香烟的银白色材料是__________;白炽灯泡内的灯丝通常是由__________制成的;温度计中填充的金属是__________.
2、初中化学课学完以后,化学学习兴趣小组对“金属活动性顺序”从内容、规律以及应用等方面进行了总结。请你认真填写下面的空白内容:
(1)金属活动性顺序表:K Ca Na Al Zn Fe Sn Pb (H) Cu Ag Pt Au
(2)金属与酸反应的规律是 。
试举出实际应用的实例(可用化学方程式表示) 。
下列物质可通过相应的金属与稀酸发生反应而得到的是
A.ZnCl2 B.AgCl C.CuCl 2 D.Fe2(SO4)3
(3)金属与盐发生置换反应,必须符合三点①K、Ca、Na三种金属非常活泼,不能把金属直接从其盐溶液中置换出来;②
③ ;
3、金属是一种重要的材料,人类的生活和生产都离不开金属。
⑴ 根据有关的化学知识,你认为金属大规模开发、利用的先后顺序跟下列哪些因素有关 。①地壳中金属元素的含量②金属的导电性③金属的活动性④金属的延展性⑤金属冶炼的难易程度
⑵钢铁的生产和使用是人类文明和社会进步的一个重要标志。请你写出一氧化碳在高温条件下把铁从赤铁矿(主要成分是氧化铁)里还原出来的化学方程式。
⑶每年世界上钢铁的产量很高,但钢铁的锈蚀也给人类带来了巨大的损失。铁在空气中锈蚀,实际上是铁跟 等物质相互作用的结果。
⑷铝的活动性比铁强,但铝在空气中却表现出良好的抗蚀性,其原因是什么?
⑸若将13锌放入100稀硫酸溶液中恰好完全反应,则可生成氢气多少克?参加反应的稀硫酸中溶质的质量分数是多少?
4、下列金属中导电性最好的是( )
A.Cu B.Al C.Fe D.Ag
5、下列叙述正确的是( )
A、不能用铁桶来盛硫酸铜溶液,是因为硫酸铜溶液易溢出,不便于运输
B、钢铁工业上,炼铁的主要设备是高炉
C、氧化碳和氧化铁在高温下反应可生成铁,是因为一氧化碳有毒
D、铜、铁在潮湿的空气中都会生锈
6、在CuCl2和AlCl3的混合溶液中,加入过量的锌粉,充分反应后过滤,留在滤纸上的物质是( )A.Cu B.Cu和Al C.Zn和Cu D.Cu、Al和Zn
7、往AgNO3、Cu(NO3)2、Zn(NO3)2的混合溶液中加入一些铁粉,待反应完成后再过滤,不可能存在的情况是 (A)滤纸上有Ag,滤液中有Ag+、Cu2+、Zn2+、Fe2+
(B)滤纸上有Ag、Cu,滤液中有Ag+、Zn2+、Fe2+
(C)滤纸上有Ag、Cu、Fe,滤液中有Zn2+、Fe2+
(D)滤纸上有Ag、Cu、Fe、Zn,滤液中有Zn2+、Fe2+
8、La(镧)是一种活动性比锌强的金属元素,其氧化物为La2O3,对应的碱La(OH)3。难溶于水,而LaCl3、La(NO3)3都易溶于水。下列各组物质中,不能直接反应制得LaCl3的是
A.La+HCl B.La2O3+HCl
C.La(OH)3+HCl D.BaCl2+La(NO3)3
9、某化学兴趣小组为测定Fe、Cu、Ag三种金属的活动性顺序设计了四种方案,每种方案设计如下,其中你认为不可行的是 [ ]
(A)Cu、Ag、FeSO4溶液(B)Fe、Ag、CuSO4溶液
(C)Fe、Cu、稀盐酸、AgNO3溶液(D)Cu、FeSO4溶液、AgNO3溶液
10、河中化学兴趣小组在A、B、C、D四只
小烧杯中分别放入干燥的细铁丝、浸过食盐水的
细铁丝、浸过清水的细铁丝、完全浸没在食盐水
中的细铁丝,然后装配成四个如右所示的装置中,
每隔一段时间测量导管中水面上升的高度,得到
一组数据如下表:(水柱高度:毫米)
时 间(小时) 0 2 4 8 10
A瓶水柱(干燥的细铁丝) 0 0 0 0 0
B瓶水柱(浸过食盐水的细铁丝) 0 1.2 2.5 4.1 5.8
C瓶水柱(浸过清水的细铁丝) 0 0 05 1.1 2.4
D瓶水柱(浸没在食盐水中的细铁丝) 0 0 0 0 0
上述实验中,铁丝生锈的速率由大到小的排列顺序为________________,铁锈的主要成分是__________,导管中水面上升的原因是___________,影响铁生锈的因素有_____________________________
11、将一块质量为8.5g的铁合金(成分为铁和碳)放入烧杯中,再向烧杯中加入一定量10%稀硫酸,恰好与铁合金中的铁完全反应(碳不溶于稀H2SO4),所得氢气的质量为0.3g。已知含碳量高于2%的铁合金为生铁,含碳量低于2%的铁合金为钢,试根据计算回答:
(1)该铁合金是生铁还是钢?(2)反应后所得溶液中溶质的质量分数是多少?
金属和金属材料
共性:有____,能导__导__,有__。
异性:密度、熔点、硬度、强度不同。
合金:具有金属的共性,但熔点__硬度__性能更好。
金属材料
金属的物理性质
纯金属
金属的活动性
顺序
金属资源利用
金属的化学性质
反应类型 化学方程式举例 反应现象
1 与氧气反应:
金属+氧气
→金属氧化物
( )
②与酸反应:
金属+酸
→金属化合物+氢气
( )
③与金属化合物反应:
金属+金属化合物
→另一种金属化合物+另一种金属
( )
金属的冶炼
氢H
有关杂质问题的计算:思路:把含有杂质的物质质量换算成纯物质质量
公式:物质的纯度=
纯物质质量=
① ② ③ ④
④
①地壳中最多的金属是:
②应用最广泛的金属是:
③人体中最高的金属是:
……
原料:矿石
(存在形式)
原理:利用还原反应
铁的冶炼
金属的活动性由强逐渐减弱
铁合金
生铁:C﹪
钢:C﹪
合金
单质:
俗称 化学式
化合物:①铁矿:
(举例)②铜矿:
③铝矿:
特点 用途
消耗:
① ② ③ ④
④
铝合金:
钛合金:
原料:
反应原理(化学方程式):
工业装置:
实验室
简易装置
P17
实验现象:
有关方程式:
注意事项:
有限资源消耗后,__再生。
铁生锈的条件:
防止铁生锈的措施:
保护金属资源
的途径:
同课章节目录
