原子核外电子排布
图片预览


文档简介
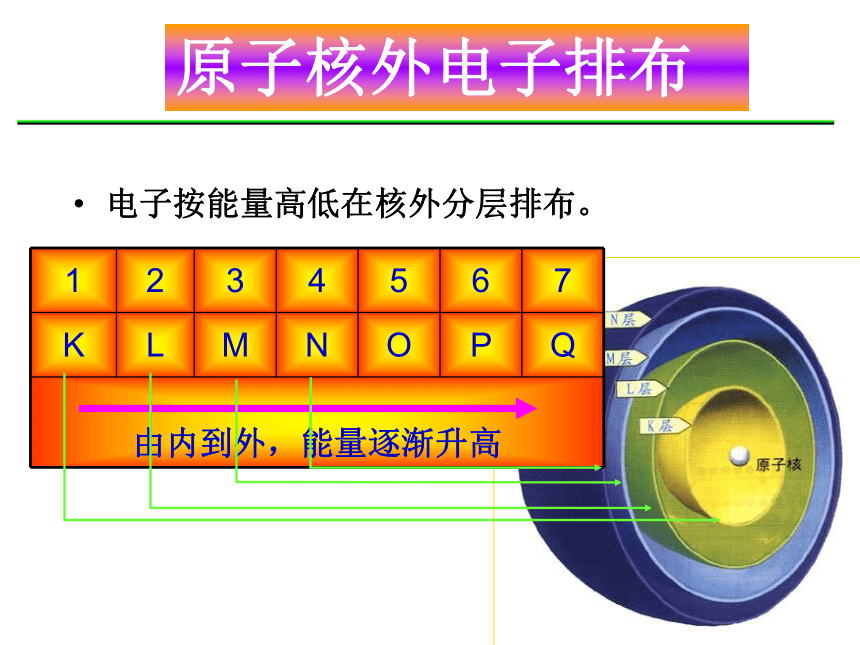
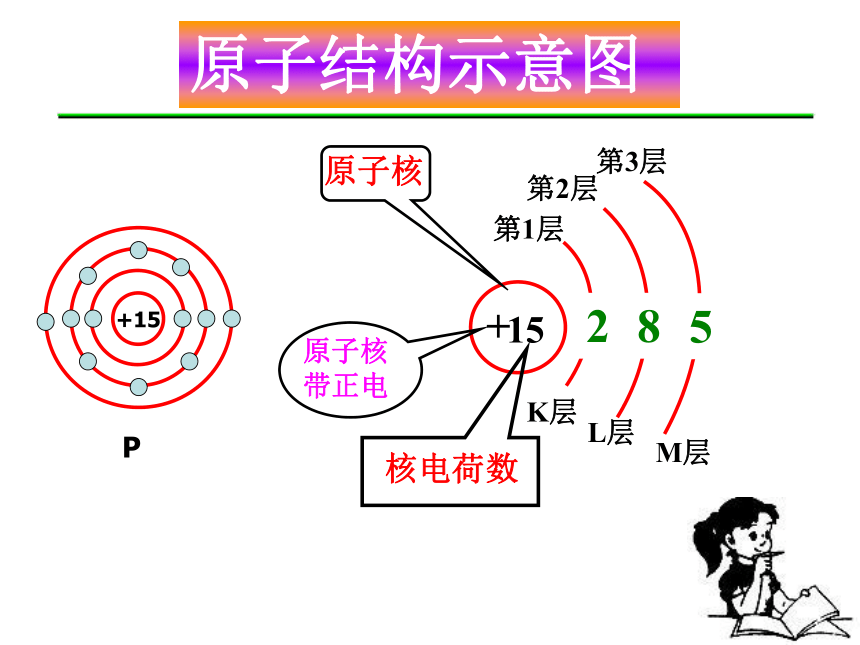
课件14张PPT。电子按能量高低在核外分层排布。原子核外电子排布+15第1层第2层第3层K层L层M层285原子核原子核带正电核电荷数原子结构示意图从前18号元素的原子结构示意图
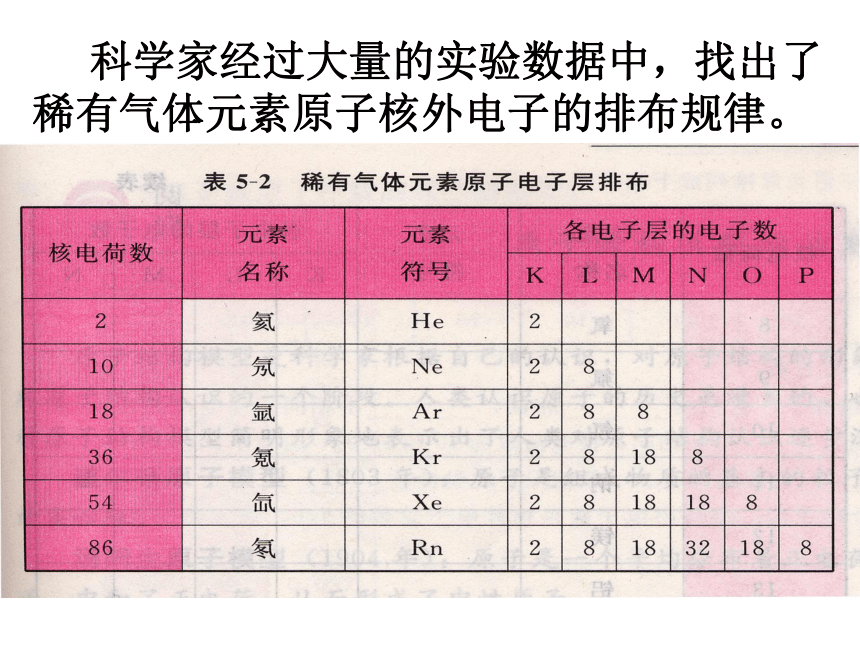
中你能发现原子核外电子排布有些什么规律 科学家经过大量的实验数据中,找出了稀有气体元素原子核外电子的排布规律。①?能量最低原理:先排K层,排满K层后再排L层……②每个电子层最多只能容纳2n2个电子。③ 最外层最多只能容纳 8个电子
次外层最多只能容纳18个电子
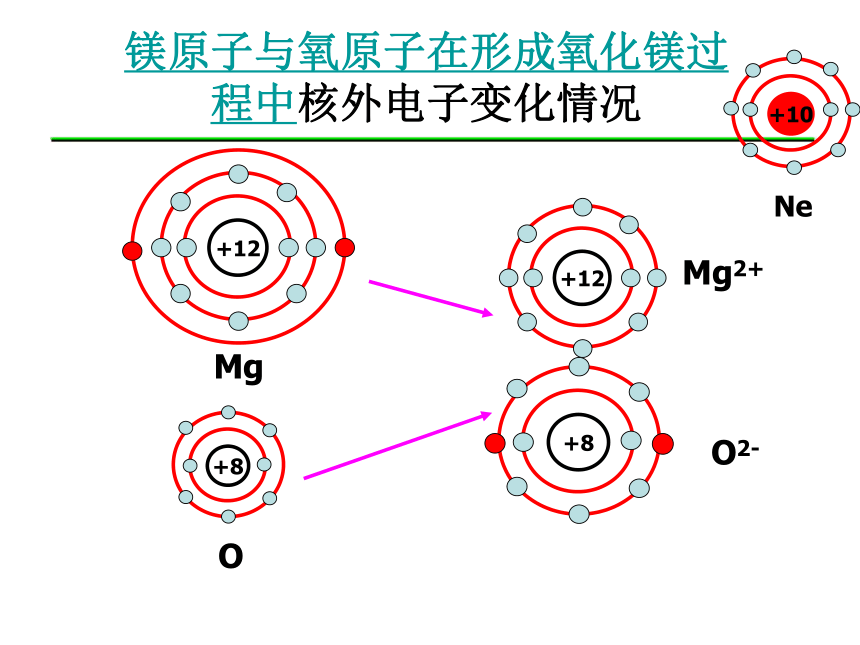
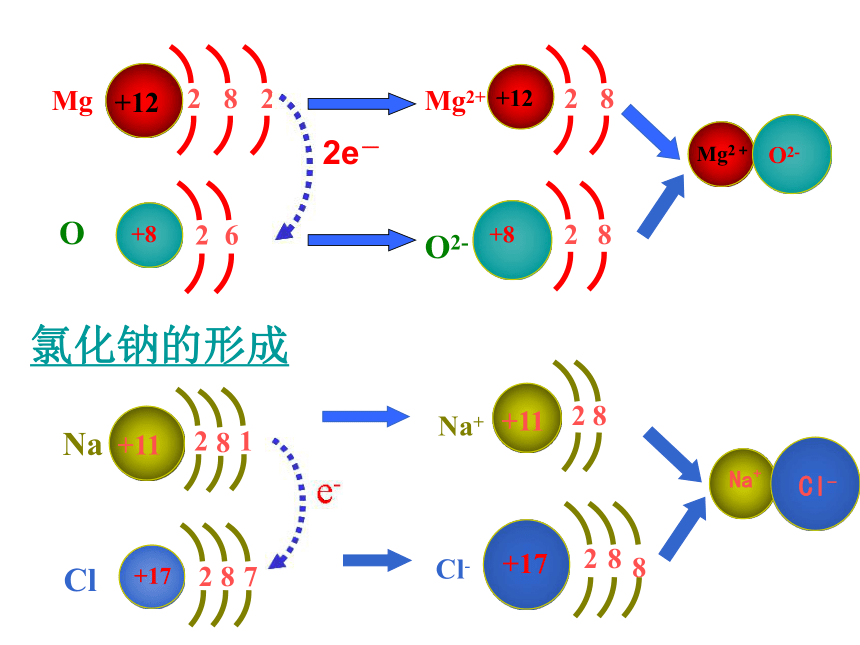
倒数第三层最多只能容纳32个电子注意:多条规律必须同时兼顾。 原子核外电子排布规律镁原子与氧原子在形成氧化镁过程中核外电子变化情况2e- 从氧化镁与氯化钠的形成过程中,你能得出什么结论?结论:
1、活泼金属与活泼非金属反应时,_______容易失去电子,而___________容易得到电子;使最外层达到“__个电子的稳定结构”。3、元素的化合价与其在反应中得失电子的数目有一定的关系。2、在化学反应过程中,_______不发生变化,____________________会发生变化。活泼金属活泼非金属8原子核原子的最外层电子数现在有四种原子 Na O Mg Cl
哪些原子能够通过电子得失的方式结合,
生成较稳定的化合物?(请写出生成物的化学式,Na2O2除外)+1 1 失1e-+2 2失2e--2 6 得2e--1 7得1e- Na2O 、MgO 、 NaCl、MgCl2化合价、最外层电子数、得失电子数目有什么关系?1.活泼金属元素易 电子形成稳定的电子层
结构
正化合价的数值=
= 2.活泼非金属元素易 电子形成稳定的电子
层结构
最低负化合价的绝对值=
=失得最外层电子数失去电子数8-最外层电子数得到电子的数目化合价、最外层电子数、得失电子数目关系课堂总结1、原子结构示意图
2、原子核外电子排布规律
①?能量最低原理
②每个电子层最多只能容纳2n2个电子。
③ 最外层最多只能容纳 8个电子
次外层最多只能容纳18个电子
倒数第三层最多只能容纳32个电子
3、化合价、最外层电子数、得失电子数的关系原子核外电子排布 正化合价的数值=最外层电子数=失去电子数
负化合价的绝对值=8-最外层电子数=得到电子数课堂检测1、钠、镁、铝等活泼金属与活泼非金属反应时最容易 ,在化合物中常显的化合价分别是_____________。氧、氟、氯等活泼非金属与活泼金属反应时容易 ,在化合物中常显的化合价是______________。
2、写出镁分别跟氮、硫等元素形成的化合物的化学式是_________________。失去电子+1,+2,+3-2,-1,-1得到电子Mg 3N2 MgS
中你能发现原子核外电子排布有些什么规律 科学家经过大量的实验数据中,找出了稀有气体元素原子核外电子的排布规律。①?能量最低原理:先排K层,排满K层后再排L层……②每个电子层最多只能容纳2n2个电子。③ 最外层最多只能容纳 8个电子
次外层最多只能容纳18个电子
倒数第三层最多只能容纳32个电子注意:多条规律必须同时兼顾。 原子核外电子排布规律镁原子与氧原子在形成氧化镁过程中核外电子变化情况2e- 从氧化镁与氯化钠的形成过程中,你能得出什么结论?结论:
1、活泼金属与活泼非金属反应时,_______容易失去电子,而___________容易得到电子;使最外层达到“__个电子的稳定结构”。3、元素的化合价与其在反应中得失电子的数目有一定的关系。2、在化学反应过程中,_______不发生变化,____________________会发生变化。活泼金属活泼非金属8原子核原子的最外层电子数现在有四种原子 Na O Mg Cl
哪些原子能够通过电子得失的方式结合,
生成较稳定的化合物?(请写出生成物的化学式,Na2O2除外)+1 1 失1e-+2 2失2e--2 6 得2e--1 7得1e- Na2O 、MgO 、 NaCl、MgCl2化合价、最外层电子数、得失电子数目有什么关系?1.活泼金属元素易 电子形成稳定的电子层
结构
正化合价的数值=
= 2.活泼非金属元素易 电子形成稳定的电子
层结构
最低负化合价的绝对值=
=失得最外层电子数失去电子数8-最外层电子数得到电子的数目化合价、最外层电子数、得失电子数目关系课堂总结1、原子结构示意图
2、原子核外电子排布规律
①?能量最低原理
②每个电子层最多只能容纳2n2个电子。
③ 最外层最多只能容纳 8个电子
次外层最多只能容纳18个电子
倒数第三层最多只能容纳32个电子
3、化合价、最外层电子数、得失电子数的关系原子核外电子排布 正化合价的数值=最外层电子数=失去电子数
负化合价的绝对值=8-最外层电子数=得到电子数课堂检测1、钠、镁、铝等活泼金属与活泼非金属反应时最容易 ,在化合物中常显的化合价分别是_____________。氧、氟、氯等活泼非金属与活泼金属反应时容易 ,在化合物中常显的化合价是______________。
2、写出镁分别跟氮、硫等元素形成的化合物的化学式是_________________。失去电子+1,+2,+3-2,-1,-1得到电子Mg 3N2 MgS
